Síndrome del bebé azul
El síndrome del bebé azul puede referirse a afecciones que causan cianosis o color azul de la piel en los bebés como resultado de niveles bajos de oxígeno en la sangre. Este término se ha aplicado tradicionalmente a la cianosis como resultado de:
- Enfermedad cardíaca cianotica, que es una categoría de defecto cardíaco congénito que resulta en bajos niveles de oxígeno en la sangre. Esto puede ser causado por el flujo sanguíneo reducido a los pulmones o la mezcla de sangre oxigenada y desoxigenada.
- Methemoglobinemia, que es una enfermedad definida por altos niveles de methemoglobina en la sangre. El aumento de los niveles de methemoglobina evita que el oxígeno se libere en los tejidos y resulta en hipoxemia.
Aunque estas son las causas más comunes de la cyanosis, hay otros factores potenciales que pueden causar un tinte azul a la piel del bebé o las membranas mucosas. Estos factores incluyen las diferencias de hipoventilación, perfusión o ventilación en los pulmones y la mala salida cardíaca de sangre oxigenada, entre otros. El síndrome del bebé azul o la cyanosis ocurre cuando la cantidad absoluta de hemoglobina desoxigenada 3g/d L que normalmente se refleja con un O2 saturación del 85 %.
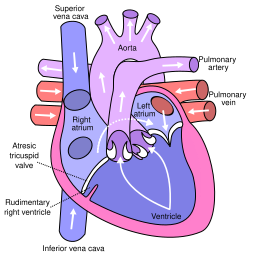
Ambas afecciones causan cianosis o una coloración azulada de la piel o las membranas mucosas. Normalmente, la sangre oxigenada aparece roja y la sangre desoxigenada tiene una apariencia más azul. En los bebés con niveles bajos de oxígeno o mezcla de sangre oxigenada y desoxigenada, la sangre puede tener un color azul o morado, provocando cianosis.
Signos y síntomas
El principal signo del síndrome del bebé azul es la cianosis. Dependiendo de la causa subyacente de la cianosis, los síntomas adicionales pueden ser:
- No prosperar
- Lethargy
- Nasal flar
- Latido cardíaco rápido
- Tasa respiratoria rápida
- Incautaciones
- Falta de aliento
Causas
El síndrome del bebé azul se ha atribuido a enfermedades cardíacas congénitas cianóticas y a la metahemoglobinemia; sin embargo, existen causas adicionales que podrían provocar que un bebé se vuelva cianótico, como:
- Obstrucción de las vías respiratorias
- Reducción de la perfusión de sangre
- Control desordenado de la respiración (ex: ortografías cianóticas, convulsiones)
- Trastornos pulmonares/pulmonares (ex: hipertensión pulmonar, fibrosis quística)
- Síndrome de emergencia respiratoria
Mecanismo
Enfermedad cardíaca cianótica
Tipos específicos de defectos cardíacos congénitos que hacen que la sangre pase directamente del lado derecho del corazón al lado izquierdo provocan cianosis. En estos defectos, parte de la sangre que se bombea al cuerpo no ha sido oxigenada por los pulmones y, por lo tanto, aparecerá más azul. Los bebés con este tipo de defectos cardíacos pueden tener un tinte azulado constante en la piel o pueden tener episodios temporales de cianosis. El grado de cianosis depende de la cantidad de sangre desoxigenada que se mezcla con sangre oxigenada antes de ser bombeada al cuerpo.
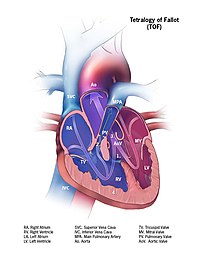
Las afecciones cardíacas en las que hay una disminución del flujo sanguíneo a los pulmones, como la tetralogía de Fallot o la atresia de la válvula pulmonar, provocan que la sangre se oxigene menos. También existen afecciones cardíacas como la transposición de las grandes arterias o tronco arterioso, que resulta en un aumento general del flujo sanguíneo a los pulmones pero con un flujo limitado de sangre oxigenada al resto del cuerpo. Las condiciones en las que hay un flujo sanguíneo deficiente a la circulación sistémica, como la coartación de la aorta, sugieren que el cuerpo no recibe la sangre oxigenada que necesita, con la consiguiente cianosis.
Los cinco defectos cardíacos cianóticos más comunes que pueden provocar el síndrome del bebé azul incluyen los siguientes:
Methemoglobinemia

La metahemoglobinemia puede ser adquirida o congénita. Ocurre cuando el hierro de la hemoglobina se oxida de Fe2+ a Fe3+, lo que provoca una mala unión del oxígeno. Además, el oxígeno que ya está unido se adhiere más estrechamente a la hemoglobina debido a una mayor afinidad, lo que resulta en un menor suministro de oxígeno. Un nivel de metahemoglobina> 1,5 g/dL provoca cianosis. La causa congénita más común es una deficiencia de la enzima citocromo b5 reductasa, que reduce la metahemoglobina en la sangre.
Sin embargo, en los bebés la causa más común de metahemoglobinemia se adquiere mediante la ingestión de nitratos (NO−3) a través de agua de pozo o alimentos. Nitritos (NO−2) producidos por la reducción microbiana del nitrato (directamente en el agua de bebida, o tras la ingestión del lactante, en su aparato digestivo) son oxidantes más potentes que los nitratos y son el agente químico realmente responsable de la oxidación del Fe2+ en Fe3+ en el tetrapirrol hemo de la hemoglobina. Los bebés menores de 4 meses corren un mayor riesgo dado que beben más agua por peso corporal, tienen una actividad NADH-citocromo b5 reductasa más baja y tienen un nivel más alto de hemoglobina fetal que se convierte más fácilmente en metahemoglobina. Además, los bebés corren un mayor riesgo después de un episodio de gastroenteritis debido a la producción de nitritos por parte de las bacterias. Las fuentes de nitrato pueden incluir fertilizantes utilizados en tierras agrícolas, vertederos de desechos o letrinas de pozo. Por ejemplo, los niveles de nitrato están sujetos a monitoreo para cumplir con los estándares de calidad del agua potable en los Estados Unidos y otros países. El vínculo entre el síndrome del bebé azul y los nitratos en el agua potable es ampliamente aceptado, pero a partir de 2006 algunos estudios indicaron que otros contaminantes o fuentes dietéticas de nitratos también podrían desempeñar un papel en el síndrome.
Diagnóstico
Al diagnosticar el síndrome del bebé azul, es importante realizar una historia clínica y un examen físico completos. Al obtener los antecedentes, es importante determinar el momento de aparición de los síntomas y preguntar sobre los factores de riesgo/exposiciones, como los antecedentes prenatales o el acceso a agua de pozo.

En el examen físico es importante visualizar dónde está presente la cianosis para diferenciar entre cianosis periférica y central. La cianosis central suele ser visible como una decoloración azulada en todo el cuerpo y las membranas mucosas. Por el contrario, la cianosis periférica suele tener una coloración azulada en las extremidades. La cianosis se puede observar en los bebés alrededor de los labios, la lengua y el área sublingual, donde la piel es más delgada. Además, es importante observar al bebé en busca de signos de dificultad respiratoria, visualizados como aleteo nasal, retracciones subcostales, etc. El examen debe incluir una evaluación respiratoria y cardíaca.
Una de las herramientas clave en el diagnóstico es un oxímetro de pulso para determinar la saturación de oxígeno. Si bien la cianosis grave puede notarse fácilmente, una saturación de oxígeno tan baja como el 80 % provoca sólo una cianosis clínica leve que es difícil de ver. Además, es útil una gasometría arterial; por ejemplo, en el caso de metahemoglobinemia, se puede esperar que la PO2 sea normal incluso con una saturación de oxígeno baja. Los estudios adicionales incluyen un hemograma completo, glucosa en sangre, hemocultivo, radiografía de tórax y una ecocardiografía.
Los bebés con cianosis debido a una cardiopatía congénita generalmente presentan síntomas horas o días después del nacimiento. Además de la cianosis, a menudo muestran signos de taquipnea (respiración rápida), soplo cardíaco y disminución de los pulsos periféricos. Si se sospecha una enfermedad cardíaca congénita en un recién nacido, es probable que los médicos realicen varias pruebas para evaluar el corazón, incluidas una radiografía de tórax, un ecocardiograma y un electrocardiograma. En la tetralogía de Fallot, los episodios en los que los bebés se vuelven cianóticos se denominan ataques de tet y suelen ocurrir durante la alimentación o el llanto. Cuando son mayores, los niños pueden ponerse en cuclillas para sentir alivio, ya que esto aumenta la resistencia vascular sistémica, lo que hace que más sangre vaya hacia los pulmones, lo que resulta en una mayor oxigenación.
Los bebés con cianosis debido a metahemoglobinemia también suelen presentar cianosis en el período neonatal, pero la oximetría de pulso puede estar falsamente elevada y no siempre revela una saturación baja de oxígeno en la sangre. Se puede utilizar un CO-oxímetro para detectar niveles de metahemoglobina en la sangre si se sospecha metahemoglobinemia, al ver la diferencia entre la saturación de oxígeno en una gasometría arterial y la medición en un cooxímetro. Además, se puede obtener un nivel directo de metahemoglobina.
Prevención/Detección
A partir del 22 de mayo de 2007, la Agencia de Protección Ambiental de los Estados Unidos ha establecido un nivel máximo de contaminante de 10 mg/L para nitrato y 1 mg/L para nitrito en el agua potable debido a los posibles efectos nocivos en los bebés.
Se ha desarrollado una herramienta de detección para detectar defectos cardíacos críticos, que se refieren a lesiones cardíacas que requieren cirugía o intervención en el primer año de vida. Se deben realizar pruebas de detección de defectos cardíacos congénitos críticos en todos los recién nacidos después de 24 horas o poco antes del alta. La saturación de oxígeno se mide en la mano derecha y en cualquiera de los pies.
Una prueba de detección se considera positiva si:
- saturación de oxígeno se realizó un 90 % en cualquier extremidad,
- Saturación de oxígeno 90-94 % en ambas extremidades en 3 mediciones separadas por una hora cada una,
- diferencia de saturación de oxígeno 3 % entre ambas extremidades en 3 mediciones separadas por una hora cada una.
Gestión
El tratamiento para el síndrome del bebé azul dependerá de la causa subyacente.
Al evaluar a un paciente para detectar cianosis o dificultad respiratoria, se deben controlar los signos vitales, especialmente la frecuencia cardíaca y la saturación de oxígeno del paciente. Es beneficioso tener establecido un acceso vascular. En los recién nacidos, el oxímetro de pulso generalmente se coloca en la mano derecha para determinar la oxigenación preductal, refiriéndose a la oxigenación antes del conducto arterioso (conexión entre la aorta y la arteria pulmonar). Esto proporciona el nivel de oxigenación que reciben el corazón y el cerebro. Tradicionalmente, el oxígeno suplementario se administra de manera progresiva, comenzando con oxígeno de flujo libre, progresando a ventilación con presión positiva o presión positiva continua en las vías respiratorias y terminando con intubación mecánica. El objetivo de saturación de oxígeno está entre el 85 y el 95 %. Si un bebé requiere oxígeno suplementario durante un tiempo prolongado, se debe calentar y humidificar para evitar la pérdida de calor.
Enfermedad cardíaca cianótica
Algunos bebés que nacen con enfermedad cardíaca cianótica son tratados con prostaglandina E1 después del nacimiento para mantener abierto el conducto arterioso y permitir que se bombee más sangre oxigenada al cuerpo. Muchos también reciben oxigenoterapia para aumentar el porcentaje de oxígeno en la sangre. La mayoría de estos bebés requerirán cirugía durante la infancia para corregir su defecto cardíaco estructural.
Metahemoglobinemia grave
El tratamiento de primera línea para la metahemoglobinemia grave es el azul de metileno, un medicamento que reducirá la metahemoglobina en la sangre. Esto es posible porque el azul de metileno oxida el NADPH, que a su vez puede convertir la metahemoglobina nuevamente en hemoglobina.
Epidemiología
De todos los bebés que nacen con defectos cardíacos congénitos, alrededor del 25 % tienen cianosis como resultado. La tetralogía de Fallot es el defecto cardíaco cianótico más común.
La metahemoglobinemia se considera poco común, y la metahemoglobinemia adquirida se encuentra más que la forma congénita.
Resultados
En el caso de los defectos cardíacos que causan cianosis, alrededor del 75 % de los bebés sobreviven hasta el año de edad y el 69 % sobrevive hasta los 18 años. Estas personas tienen un mayor riesgo de sufrir retraso en el desarrollo, insuficiencia cardíaca o trastornos del ritmo cardíaco.
La metahemoglobinemia responde bien al tratamiento, su pronóstico está asociado con el nivel de metahemoglobinemia y el grado de daño a órganos terminales que puede causar. La muerte puede ocurrir cuando los niveles alcanzan el 70%.
Historia
La primera operación exitosa para tratar el síndrome del bebé azul causado por la tetralogía de Fallot ocurrió en la Universidad Johns Hopkins en 1944. A través de una colaboración entre la cardióloga pediátrica Helen Taussig, el cirujano Alfred Blalock y la técnica quirúrgica Vivien Thomas, Blalock-Thomas-Taussig se creó la derivación. El Dr. Taussig había reconocido que los niños con tetralogía de Fallot que también tenían un conducto arterioso permeable (CAP) generalmente vivían más tiempo, por lo que el trío intentó crear el mismo efecto que un CAP uniendo la arteria subclavia a la arteria pulmonar, aliviando al niño. #39;cianosis. La operación se publicó en el Journal of the American Medical Association en 1945 y tuvo un impacto en el manejo de los bebés azules en todo el mundo.
Anna era el nombre de la perra que fue la primera sobreviviente de la cirugía, considerada en ese momento un procedimiento experimental. Anna sobrevivió al primer bypass pulmonar después de haber sido operada dos veces. La segunda operación fue necesaria para sustituir los puntos originales por unos flexibles. Después de su éxito con Anna, Blalock y Thomas tuvieron el coraje de realizar la primera cirugía a corazón abierto a Eileen Saxon en 1944. En 1950, la historia de Anna se llevó al cine y la película se proyectó en varias escuelas. y otros grupos.
Contenido relacionado
Ley de Fick
Presión oncótica
Memoria explícita
Sociología médica
Memoria implícita