Reacción de Shapiro
La reacción de Shapiro o descomposición de tosilhidrazona es una reacción orgánica en la que una cetona o un aldehído se convierte en un alqueno a través de una hidrazona intermedia en presencia de 2 equivalentes de organolitio. reactivo. La reacción fue descubierta por Robert H. Shapiro en 1967. La reacción de Shapiro se utilizó en la síntesis total de Nicolaou Taxol. Esta reacción es muy similar a la reacción de Bamford-Stevens, que también implica la descomposición básica de tosil hidrazonas.

Mecanismo de reacción
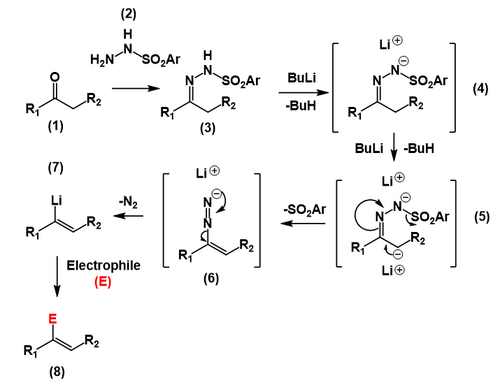
En un preludio de la reacción de Shapiro real, una cetona o un aldehído (1) se hace reaccionar con p-toluenosulfonilhidrazida(2) para formar un p -toluenosulfonilhidrazona (o tosilhidrazona) que es una hidrazona (3). Dos equivalentes de una base fuerte, como el n-butillitio, extraen el protón de la hidrazona (4) seguido del protón α, menos ácido, al carbono de la hidrazona (5), formando una carbanión. Luego, el carbanión sufre una reacción de eliminación que produce un doble enlace carbono-carbono y expulsa el anión tosil, formando un anión diazonio (6). Este anión diazonio luego se pierde como nitrógeno molecular dando como resultado una especie de vinil litio (7), que luego puede reaccionar con varios electrófilos, incluida la simple neutralización con agua o un ácido (8).
Alcance
La posición del alqueno en el producto está controlada por el sitio de desprotonación de la base de organolitio. En general, el sitio cinéticamente favorecido y menos sustituido de las tosilhidrazonas diferencialmente sustituidas se desprotona selectivamente, lo que conduce al intermedio de vinilitio menos sustituido. Aunque existen muchas reacciones secundarias para el grupo funcional vinilitio, en la reacción de Shapiro en particular se agrega agua, lo que resulta en la protonación del alqueno. Otras reacciones de compuestos de vinilitio incluyen reacciones de alquilación con, por ejemplo, haluros de alquilo.

Es importante destacar que la reacción de Shapiro no se puede utilizar para sintetizar 1-litioalquenos (y los derivados funcionalizados resultantes), ya que las sulfonilhidrazonas derivadas de aldehídos se someten a la adición exclusiva de la base de organolitio al carbono del doble enlace C-N.
Reacción catalítica de Shapiro
Las reacciones tradicionales de Shapiro requieren cantidades estequiométricas (a veces en exceso) de base para generar los reactivos de alquenil litio. Para combatir este problema, Yamamoto y sus compañeros desarrollaron una ruta estereoselectiva y regioselectiva eficiente hacia los alquenos utilizando una combinación de cetona fenilaziridinilhidrazonas como equivalentes de arenosulfonilhidrazona con una cantidad catalítica de amidas de litio. La fenilaziridinilhidrazona requerida se preparó a partir de la condensación de undecan-6-ona con 1-amino-2-fenilaziridina. El tratamiento de la fenilaziridinilhidrazona con 0,3 equivalentes de LDA en éter dio como resultado el alqueno que se muestra a continuación con una relación cis:trans de 99,4:0,6. La relación se determinó mediante análisis GLC capilar después de la conversión a los epóxidos correspondientes con mCPBA. La carga de catalizador se puede reducir a 0,05 equivalentes en el caso de una reacción a escala de 30 mmol.
La alta estereoselectividad se obtiene mediante la abstracción preferencial del hidrógeno de α-metileno sintetizado en la fenilaziridina, y también se explica por la quelación interna del intermediario litiado.

Una reacción combinada Shapiro-Suzuki in situ
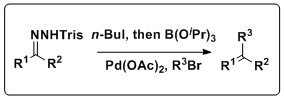
La reacción de Shapiro también se puede combinar con la reacción de Suzuki para producir una variedad de productos de olefina. Keay y sus compañeros de trabajo han desarrollado una metodología que combina estas reacciones en un proceso de un solo recipiente que no requiere el aislamiento del ácido borónico, un inconveniente del acoplamiento tradicional de Suzuki. Esta reacción tiene un amplio alcance y tolera una gran cantidad de trisilhidrazonas y haluros de arilo, así como varios disolventes y fuentes de Pd.
Una aplicación de la reacción de Shapiro en síntesis total
La reacción de Shapiro se ha utilizado para generar olefinas y productos naturales complejos. K. Mori y sus compañeros de trabajo querían determinar la configuración absoluta del grupo de fitocassanos de una clase de productos naturales llamados fitoalexinas. Esto se logró preparando la (–)-fitocassana D natural a partir de la cetona (R)-Wieland-Miescher. En el camino hacia (–)-fitocasano D, se sometió una cetona tricíclica a las condiciones de la reacción de Shapiro para producir el producto alqueno cíclico.

Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar
Ley de las proporciones múltiples
Anilina