Reacción de deshidratación
En química, una reacción de deshidratación es una reacción química que implica la pérdida de agua de la molécula o ion que reacciona. Las reacciones de deshidratación son procesos comunes, lo contrario de una reacción de hidratación.
Reacciones de deshidratación en química orgánica.
Esterificación
El ejemplo clásico de una reacción de deshidratación es la esterificación de Fischer, que consiste en tratar un ácido carboxílico con un alcohol para dar un éster:RCO2H + R′OH ⇌ RCO2R ′ + H2O
A menudo, estas reacciones requieren la presencia de un agente deshidratante, es decir, una sustancia que reaccione con el agua.
Eterificación
Dos monosacáridos, como la glucosa y la fructosa, se pueden unir (para formar sacarosa) mediante síntesis por deshidratación. La nueva molécula, que consta de dos monosacáridos, se denomina disacárido.
Formación de nitrilo
Los nitrilos a menudo se preparan por deshidratación de amidas primarias.RC(O)NH 2 → RCN + H 2 O
Formación de cetenos
El ceteno se produce calentando ácido acético y atrapando el producto:CH 3 CO 2 H → CH 2 =C=O + H 2 O
Formación de alquenos
Los alquenos se pueden obtener a partir de alcoholes por deshidratación. Esta conversión, entre otras, es una reacción clave en la conversión de biomasa en combustibles líquidos. La conversión de etanol a eteno es un ejemplo fundamental: CH 3 CH 2 OH → H 2 C=CH 2 + H 2 O
La reacción es lenta en ausencia de catalizadores ácidos como el ácido sulfúrico y ciertas zeolitas.
Algunos alcoholes son propensos a la deshidratación. Los 3-hidroxilcarbonilos, llamados aldoles, liberan agua al permanecer a temperatura ambiente:RC(O)CH2CH (OH)R' → RC(O)CH=CHR ' + H2O
En el reordenamiento del benceno del dienol, la deshidratación conduce a la aromatización.
A menudo, la reacción se induce deshidratando reactivos. Por ejemplo, el 2-metil-ciclohexan-1-ol se deshidrata a 1-metilciclohexeno en presencia de sulfurano de Martin, que reacciona irreversiblemente con el agua.
La doble deshidratación se ilustra mediante la conversión de glicerol en acroleína: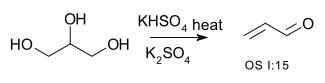
Reacciones de deshidratación en química inorgánica
La formación del enlace pirofosfato es una deshidratación importante relevante para la bioenergética.
Varios materiales de construcción son producidos por deshidratación. El yeso de París se produce por deshidratación del yeso en un horno:{displaystyle {ce {CaSO4.2H2O +}}}


El polvo seco resultante está listo para mezclarse con agua para formar una pasta dura pero manejable que se endurece.
Contenido relacionado
Valencia (química)
Principio de Aufbau
Óxido de aluminio