Fenazina
Fenazina es un compuesto orgánico con la fórmula (C6H4)2N 2. Es una pirazina anulada con dibenzo y la sustancia madre de muchos colorantes, como el rojo de toluileno, las indulinas y las safraninas (y las eurhodinas estrechamente relacionadas). La fenazina cristaliza en agujas amarillas, que son poco solubles en alcohol. El ácido sulfúrico lo disuelve formando una solución de color rojo intenso.
Síntesis
Clásicamente, las fenazinas se preparan mediante la reacción de nitrobenceno y anilina en la reacción de Wohl-Aue. Otros métodos incluyen:
- pirolisis de la sal de bario de azobenzoato
- oxidación de anilina con óxido de plomo
- oxidación de la dihidrofenazina, que se prepara mediante la calefacción de pirocatequina con o-fenilediamina.
- oxidación de orto-aminodifenilamina con peróxido de plomo.
Derivados
- Las fenazinas más complejas, como las naftophenazinas, nafthazinas y nafthotolazinas, pueden ser preparadas mediante la condensación de ortodiaminas con ortoquinones o por la oxidación de una ortodiamina en presencia de α-naphthol, y por la descomposición de orto-anilido-acido-(tolutera)
- Si se utilizan alquil o aryl-ortho-diaminas, se obtienen bases de azonio. Las azinas son en su mayoría amarillas en color, destilan sin cambios y son estables para oxidantes. Agregan los iodidos alquiles fácilmente, formando sales de azonio alquil, formando anhídrido también teniendo lugar entre estos hidroxilogrupos. Se disuelve en ácido sulfúrico concentrado con una fluorescencia verde-amarillenta.
- Las rodaminas, que están estrechamente relacionadas con las ftalinas, se forman por la condensación de los metaaminofenoles alquilos con anhídrido fálico en presencia de ácido sulfúrico. Sus sales son tintes rojos finos. Por la entrada de los grupos amino o hidroxilo en la molécula se forman disestuffs. Los derivados monoamino o eurhodinas se obtienen cuando las arylmonaminas se condensan con compuestos ortoamino azo; mediante la condensación de diclometida quinona o anilina paranitrosodimetilo con monaminas que contienen una posición para libre, o por oxidación ortohidroxidiaminodipbenylaminas. Son sólidos rojos amarillentos, que se comportan como bases débiles, sus sales sometidas a disociación hidrolítica en solución acuosa. Cuando se calienta con ácido clorhídrico concentrado el grupo amino es reemplazado por el grupo hidroxil y se producen los eurhodols fenólicos.
Aminofenazina

Muchas aminofenazinas son colorantes destacados. Dos de los primeros colorantes sintéticos son las aminofenazinas, entre ellas la indulina y la nigrosina.
La diaminofenazina simétrica es la sustancia madre del importante colorante rojo neutro (dimetildiaminotolufenazina). Se obtiene por oxidación de ortofenilendiamina con cloruro férrico.
En un proceso relacionado, la oxidación de una mezcla fría de paraaminodimetilanilina y meta-toluilendiamina da azul de toluileno. Esta indamina se forma como producto intermedio y pasa al rojo cuando se hierve; y también por oxidación de dimetilparafenilendiatnina con metatoluilendiamina. Cristaliza en agujas de color rojo anaranjado y su solución alcohólica presenta una fuerte fluorescencia. Tiñe la seda y el algodón mordido de un fino escarlata. Se le conoce comercialmente como rojo neutro. Para las sales de fenazonio, consulte safranina. La benzo[c]cinolina es un isómero de la fenacina, con la que guarda la misma relación que el fenantreno con el antraceno.
Productos naturales
Las fuentes biológicas conocidas de compuestos de fenazina son en su mayoría de naturaleza bacteriana. Algunos de los géneros que se sabe que producen fenazinas incluyen Pseudomonas spp., Streptomyces spp. y Pantoea agglomerans. Estos productos naturales de fenazina se han implicado en la virulencia y la aptitud competitiva de los organismos productores. Por ejemplo, la fenazina piocianina producida por Pseudomonas aeruginosa contribuye a su capacidad para colonizar los pulmones de pacientes con fibrosis quística. De manera similar, el ácido fenazina-1-carboxílico, producido por varias Pseudomonas, aumenta la supervivencia en ambientes del suelo y se ha demostrado que es esencial para la actividad de control biológico de ciertas cepas.
Mientras que las fenazinas bacterianas participan principalmente en los metabolismos secundarios, la metanofenazina en arqueas metanogénicas (metanógenos) participa en los metabolismos primarios y son importantes portadores de electrones. La metanofenazina actúa como equivalente funcional de las menaquinonas y ubiquinonas en otros organismos. La metanofenazina es la única fenazina conocida de origen no bacteriano y también es la única fenazina que participa en el metabolismo primario.
Biosíntesis
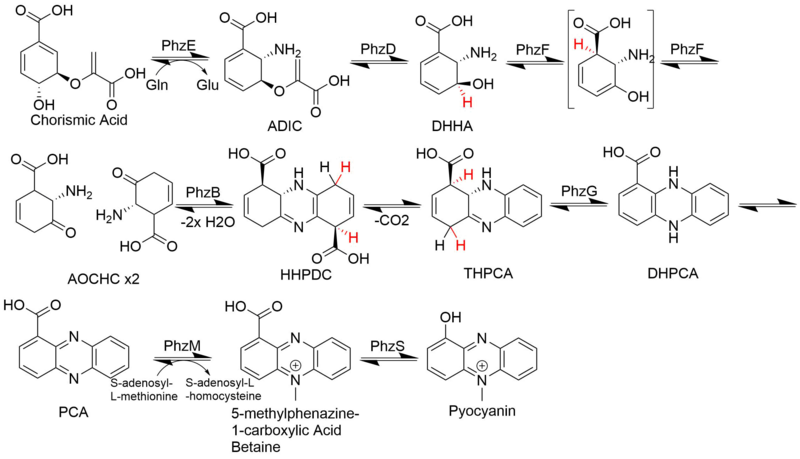
La biosíntesis de fenazina se bifurca en la vía del ácido shikímico en un punto posterior al ácido corísmico. Luego, dos moléculas de este intermediario derivado del corismato se juntan de forma diagonalmente simétrica para formar la estructura básica de fenazina. Luego, las modificaciones secuenciales conducen a una variedad de fenazina con diferentes actividades biológicas. Un ejemplo de alcaloides fenazínicos son la piocianina, el ácido safénico y las esmeraldinas.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar
Ley de las proporciones múltiples
Anilina