Densidad relativa
‹Ver Tfd›
Densidad relativa, o gravedad específica, es la relación entre la densidad (masa de una unidad de volumen) de una sustancia y la densidad de un material de referencia determinado. La gravedad específica de los líquidos casi siempre se mide con respecto al agua en su punto más denso (a 4 °C o 39,2 °F); para gases, la referencia es el aire a temperatura ambiente (20 °C o 68 °F). El término "densidad relativa" (a menudo abreviado r.d. o RD) suele preferirse en el uso científico, mientras que el término "gravedad específica" es obsoleto.
Si la densidad relativa de una sustancia es menor que 1, entonces es menos densa que la referencia; si es mayor que 1, entonces es más denso que la referencia. Si la densidad relativa es exactamente 1, entonces las densidades son iguales; es decir, volúmenes iguales de las dos sustancias tienen la misma masa. Si el material de referencia es agua, entonces una sustancia con una densidad relativa (o gravedad específica) inferior a 1 flotará en el agua. Por ejemplo, un cubo de hielo, con una densidad relativa de alrededor de 0,91, flotará. Una sustancia con una densidad relativa mayor que 1 se hundirá.
La temperatura y la presión deben especificarse tanto para la muestra como para la referencia. La presión es casi siempre de 1 atm (101,325 kPa). Donde no lo es, es más habitual especificar la densidad directamente. Las temperaturas tanto para la muestra como para la referencia varían de una industria a otra. En la práctica cervecera británica, la gravedad específica, como se especificó anteriormente, se multiplica por 1000. La gravedad específica se usa comúnmente en la industria como un medio simple para obtener información sobre la concentración de soluciones de varios materiales como salmueras, peso de mosto (jarabes, jugos, mieles, mosto, mosto, etc.) y ácidos.
Cálculo básico
Densidad relativaRD{displaystyle RD.) o gravedad específica (SG{displaystyle SG) es una cantidad sin dimensiones, ya que es la proporción de densidades o pesos
El material de referencia se puede indicar utilizando subscriptos: RDsubstance/reference{displaystyle RD_{mathrm {sustancia/referencia}} que significa "la densidad relativa sustancia con respecto a referencia". Si la referencia no se declara explícitamente, normalmente se supone que es agua a 4 °C (o, más precisamente, 3.98 °C, que es la temperatura a la que el agua alcanza su densidad máxima). En unidades SI, la densidad del agua es (aproximadamente) 1000 kg/m3 o 1 g/cm3, lo que hace que los cálculos relativos de densidad sean particularmente convenientes: la densidad del objeto sólo necesita ser dividida por 1000 o 1, dependiendo de las unidades.
La densidad relativa de los gases suele medirse con respecto al aire seco a una temperatura de 20 °C y una presión absoluta de 101,325 kPa, que tiene una densidad de 1,205 kg/m3. La densidad relativa con respecto al aire se puede obtener por
Aquellos con SG mayor que 1 son más densos que el agua y, sin tener en cuenta los efectos de la tensión superficial, se hundirán en ella. Los que tienen una SG inferior a 1 son menos densos que el agua y flotarán sobre ella. En el trabajo científico, la relación entre masa y volumen suele expresarse directamente en términos de la densidad (masa por unidad de volumen) de la sustancia en estudio. Es en la industria donde la gravedad específica encuentra una amplia aplicación, a menudo por razones históricas.
La verdadera gravedad específica de un líquido se puede expresar matemáticamente como:
La gravedad específica aparente es simplemente la relación de los pesos de volúmenes iguales de muestra y agua en el aire:
Se puede demostrar que la verdadera gravedad específica se puede calcular a partir de diferentes propiedades:
Donde g es la aceleración local debido a la gravedad, V es el volumen de la muestra y del agua (lo mismo para ambos), ***muestra es la densidad de la muestra, ***H2O es la densidad del agua, WV representa un peso obtenido en vacío, msample{displaystyle {Mathit {m}_{mathrm} {Sample} es la masa de la muestra y mH2O{displaystyle {Mathit {m}_{mathrm} {H_{2}O}es la masa de un volumen igual de agua.
La densidad del agua varía con la temperatura y la presión al igual que la densidad de la muestra. Por lo que es necesario especificar las temperaturas y presiones a las que se determinaron las densidades o pesos. Casi siempre ocurre que las mediciones se realizan a 1 atmósfera nominal (101,325 kPa ± variaciones de patrones climáticos cambiantes). Pero como la gravedad específica generalmente se refiere a soluciones acuosas altamente incompresibles u otras sustancias incompresibles (como los productos del petróleo), las variaciones en la densidad causadas por la presión generalmente se ignoran al menos cuando se mide la gravedad específica aparente. Para cálculos de gravedad específica verdaderos (in vacuo), se debe considerar la presión del aire (ver a continuación). Las temperaturas se especifican mediante la notación (Ts/Tr), con Ts que representa la temperatura a la que se determinó la densidad de la muestra y Tr la temperatura a la que se determina la densidad de referencia (agua). está especificado. Por ejemplo, SG (20 °C/4 °C) se entendería que la densidad de la muestra se determinó a 20 °C y la del agua a 4 °C. Teniendo en cuenta diferentes temperaturas de muestra y de referencia, notamos que, mientras SGH2O = 1.000000 (20 °C/20 °C), también es el caso que SGH2O = 0.998203⁄0.999840 = 0.998363 (20 °C/4 °C). Aquí, la temperatura se especifica utilizando la escala ITS-90 actual y las densidades utilizadas aquí y en el resto de este artículo se basan en esa escala. En la escala IPTS-68 anterior, las densidades a 20 °C y 4 °C son 0,9982071 y 0.9999720 respectivamente, lo que da como resultado un valor SG (20 °C/4 °C) para el agua de 0.9982343.
Como el uso principal de las mediciones de gravedad específica en la industria es la determinación de las concentraciones de sustancias en soluciones acuosas y como éstas se encuentran en tablas de SG versus concentración, es extremadamente importante que el analista ingrese la tabla con la forma correcta de Gravedad específica. Por ejemplo, en la industria cervecera, la tabla Plato enumera la concentración de sacarosa por peso frente a la verdadera SG, y originalmente (20 °C/4 °C), es decir, se basaba en mediciones de la densidad de las soluciones de sacarosa hechas a temperatura de laboratorio (20 °C) pero referenciada a la densidad del agua a 4 °C, que está muy cerca de la temperatura a la que el agua tiene su máxima densidad, ρH2O igual a 999,972 kg/m3 en unidades SI (0,999972 g/cm3 en unidades cgs o 62,43 lb/cu ft en las unidades habituales de Estados Unidos). La tabla ASBC que se usa actualmente en América del Norte, aunque se deriva de la tabla Plato original, es para mediciones de gravedad específica aparente a (20 °C/20 °C) en la escala IPTS-68 donde la densidad del agua es 0.9982071 g/cm3. En las industrias del azúcar, refrescos, miel, jugos de frutas y afines, la concentración de sacarosa en peso se toma de una tabla elaborada por A. Brix, que utiliza SG (17,5 °C/17,5 °C). Como ejemplo final, las unidades SG británicas se basan en temperaturas de referencia y de muestra de 60 °F y, por lo tanto, son (15,56 °C/15,56 °C).
Dada la gravedad específica de una sustancia, su densidad real se puede calcular reorganizando la fórmula anterior:
Ocasionalmente, se especifica una sustancia de referencia que no sea agua (por ejemplo, aire), en cuyo caso la gravedad específica significa densidad relativa a esa referencia.
Dependencia de la temperatura
- Vea Densidad para una tabla de las densidades de agua medidas a diferentes temperaturas.
La densidad de las sustancias varía con la temperatura y la presión, por lo que es necesario especificar las temperaturas y presiones a las que se determinaron las densidades o masas. Casi siempre ocurre que las mediciones se realizan a 1 atmósfera nominal (101,325 kPa sin tener en cuenta las variaciones causadas por los patrones climáticos cambiantes), pero como la densidad relativa generalmente se refiere a soluciones acuosas altamente incompresibles u otras sustancias incompresibles (como los productos del petróleo) variaciones en la densidad causadas por la presión generalmente se desprecian al menos cuando se mide la densidad relativa aparente. Para verdaderos (in vacuo) cálculos de densidad relativa, se debe considerar la presión del aire (ver más abajo). Las temperaturas se especifican mediante la notación (Ts/Tr) con Ts que representa la temperatura a la que se determinó la densidad de la muestra y Tr la temperatura a la que se determina la densidad de referencia (agua) especificado. Por ejemplo, SG (20 °C/4 °C) se entendería que la densidad de la muestra se determinó a 20 °C y la del agua a 4 °C. Teniendo en cuenta diferentes temperaturas de muestra y de referencia, notamos que mientras SGH2O = 1.000000 (20 °C/20 °C) también ocurre que RDH2O = 0.998203/0,998840 = 0,998363 (20 °C/4 °C). Aquí la temperatura se especifica utilizando la escala ITS-90 actual y las densidades utilizadas aquí y en el resto de este artículo se basan en esa escala. En la escala IPTS-68 anterior, las densidades a 20 °C y 4 °C son, respectivamente, 0,9982071 y 0,9999720, lo que da como resultado un valor de RD (20 °C/4 °C) para el agua de 0,9982343.
Las temperaturas de los dos materiales pueden indicarse explícitamente en los símbolos de densidad; Por ejemplo:
- densidad relativa: 8.1520 °C
4 °C; o gravedad específica: 2.43215
0
donde el superíndice indica la temperatura a la que se mide la densidad del material y el subíndice indica la temperatura de la sustancia de referencia con la que se compara.
Usos
La densidad relativa también puede ayudar a cuantificar la flotabilidad de una sustancia en un fluido o gas, o determinar la densidad de una sustancia desconocida a partir de la densidad conocida de otra. Los geólogos y mineralogistas suelen utilizar la densidad relativa para ayudar a determinar el contenido mineral de una roca u otra muestra. Los gemólogos lo utilizan como ayuda en la identificación de piedras preciosas. Se prefiere el agua como referencia porque las mediciones son fáciles de realizar en el campo (consulte a continuación ejemplos de métodos de medición).
Como el uso principal de las mediciones de densidad relativa en la industria es la determinación de las concentraciones de sustancias en soluciones acuosas y estas se encuentran en tablas de RD frente a concentración, es extremadamente importante que el analista ingrese la tabla con la forma correcta de densidad relativa. Por ejemplo, en la industria cervecera, la tabla Plato, que enumera la concentración de sacarosa por masa frente a la RD verdadera, era originalmente (20 °C/4 °C) que se basa en mediciones de la densidad de soluciones de sacarosa hechas a temperatura de laboratorio (20 °C), pero se hace referencia a la densidad del agua a 4 °C, que está muy cerca de la temperatura a la que el agua tiene su densidad máxima de ρ(H
2O) igual a 0,999972 g/cm3 (o 62,43 lb·ft−3). La tabla ASBC que se usa actualmente en América del Norte, si bien se deriva de la tabla Plato original, es para mediciones de densidad relativa aparente a (20 °C/20 °C) en la escala IPTS-68 donde la densidad del agua es 0,9982071 g/ cm3. En las industrias del azúcar, refrescos, miel, jugos de frutas y afines, la concentración de sacarosa en masa se toma de este trabajo que utiliza SG (17,5 °C/17,5 °C). Como ejemplo final, las unidades RD británicas se basan en temperaturas de referencia y de muestra de 60 °F y, por lo tanto, son (15,56 °C/15,56 °C).
Medición
La densidad relativa se puede calcular directamente midiendo la densidad de una muestra y dividiéndola por la densidad (conocida) de la sustancia de referencia. La densidad de la muestra es simplemente su masa dividida por su volumen. Aunque la masa es fácil de medir, el volumen de una muestra de forma irregular puede ser más difícil de determinar. Un método es colocar la muestra en un cilindro graduado lleno de agua y leer cuánta agua desplaza. Alternativamente, el recipiente se puede llenar hasta el borde, sumergir la muestra y medir el volumen de desbordamiento. La tensión superficial del agua puede evitar que se desborde una cantidad significativa de agua, lo que es especialmente problemático para muestras pequeñas. Por esta razón, es deseable utilizar un recipiente de agua con una boca lo más pequeña posible.
Para cada sustancia, la densidad, ρ, viene dada por
Cuando se dividen estas densidades, las referencias a la constante de resorte, la gravedad y el área transversal simplemente se cancelan, dejando
Pesaje hidrostático
La densidad relativa se mide más fácilmente y quizás con mayor precisión sin medir el volumen. Usando una báscula de resorte, la muestra se pesa primero en el aire y luego en el agua. La densidad relativa (con respecto al agua) se puede calcular usando la siguiente fórmula:
- Waire es el peso de la muestra en el aire (medido en newtons, fuerza de libras o alguna otra unidad de fuerza)
- Wagua es el peso de la muestra en el agua (medida en las mismas unidades).
Esta técnica no se puede utilizar fácilmente para medir densidades relativas inferiores a uno, porque la muestra flotará. Wagua se convierte en una cantidad negativa, que representa la fuerza necesaria para mantener la muestra bajo el agua.
Otro método práctico utiliza tres medidas. La muestra se pesa en seco. Luego se pesa un recipiente lleno hasta el borde con agua, y se vuelve a pesar con la muestra sumergida, después de que el agua desplazada se haya desbordado y se haya eliminado. Restar la última lectura de la suma de las dos primeras lecturas da el peso del agua desplazada. El resultado de la densidad relativa es el peso de la muestra seca dividido por el del agua desplazada. Este método permite el uso de básculas que no pueden manejar una muestra suspendida. También se puede manipular una muestra menos densa que el agua, pero hay que sujetarla y tener en cuenta el error que introduce el material de fijación.
Hidrómetro
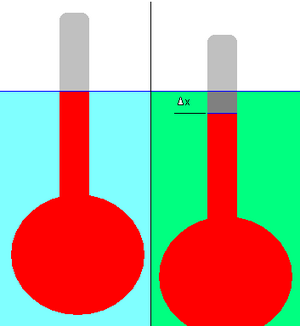
La densidad relativa de un líquido se puede medir con un hidrómetro. Este consiste en un bulbo unido a un tallo de área de sección transversal constante, como se muestra en el diagrama adyacente.
Primero, se hace flotar el hidrómetro en el líquido de referencia (que se muestra en azul claro) y se marca el desplazamiento (el nivel del líquido en el tallo) (línea azul). La referencia podría ser cualquier líquido, pero en la práctica suele ser agua.
Luego, el hidrómetro se hace flotar en un líquido de densidad desconocida (que se muestra en verde). Se anota el cambio en el desplazamiento, Δx. En el ejemplo representado, el hidrómetro ha caído ligeramente en el líquido verde; por lo tanto, su densidad es menor que la del líquido de referencia. Es necesario que el hidrómetro flote en ambos líquidos.
La aplicación de principios físicos simples permite calcular la densidad relativa del líquido desconocido a partir del cambio de desplazamiento. (En la práctica, el tallo del hidrómetro está premarcado con graduaciones para facilitar esta medición).
En la explicación que sigue,
- ***ref es la densidad conocida (masa por volumen de unidad) del líquido de referencia (agua típica).
- ***nuevo es la densidad desconocida del líquido nuevo (verde).
- RDnuevo/ref es la densidad relativa del nuevo líquido con respecto a la referencia.
- V es el volumen de referencia líquido desplazado, es decir, el volumen rojo en el diagrama.
- m es la masa de todo el hidrometro.
- g es la constante gravitacional local.
- Δx es el cambio en el desplazamiento. De acuerdo con la forma en que se gradúan los hidrometros, Δx es aquí tomado como negativo si la línea de desplazamiento se eleva en el tallo del hidrometro, y positivo si cae. En el ejemplo representado, Δx es negativo.
- A es el área transversal del eje.
Dado que el hidrómetro flotante está en equilibrio estático, la fuerza gravitatoria hacia abajo que actúa sobre él debe equilibrar exactamente la fuerza de flotación hacia arriba. La fuerza gravitacional que actúa sobre el hidrómetro es simplemente su peso, mg. Según el principio de flotabilidad de Arquímedes, la fuerza de flotación que actúa sobre el hidrómetro es igual al peso del líquido desplazado. Este peso es igual a la masa de líquido desplazado multiplicada por g, que en el caso del líquido de referencia es ρrefVg . Haciendo estos iguales, tenemos
o simplemente
m=*** *** refV.{displaystyle m=rho _{mathrm {ref}V.} | ()1) |
Exactamente la misma ecuación se aplica cuando el hidrómetro está flotando en el líquido que se está midiendo, excepto que el nuevo volumen es V − A Δx (ver nota anterior sobre el signo de Δx). De este modo,
m=*** *** new()V− − AΔ Δ x).{displaystyle m=rho _{mathrm {new}(V-ADelta x).} | ()2) |
Combinando (1) y (2) se obtiene
RDnew/ref=*** *** new*** *** ref=VV− − AΔ Δ x.{displaystyle RD_{mathrm {new/ref}={frac {rho _{mathrm {new} ¿Qué? }={frac {V}{V-ADelta # | ()3) |
Pero de (1) tenemos V = m/ρref. Sustituyendo en (3) da
RDnew/ref=11− − AΔ Δ xm*** *** ref.{displaystyle RD_{mathrm {new/ref}={frac {1}{1-{frac} {ADelta x} {m}rho _{mathrm {ref} }}} | ()4) |
Esta ecuación permite calcular la densidad relativa a partir del cambio de desplazamiento, la densidad conocida del líquido de referencia y las propiedades conocidas del hidrómetro. Si Δx es pequeño, entonces, como una aproximación de primer orden de la ecuación de la serie geométrica (4) se puede escribir como:
Esto muestra que, para Δx pequeños, los cambios en el desplazamiento son aproximadamente proporcionales a los cambios en la densidad relativa.
Picnómetro
Un picnómetro (del griego: πυκνός (puknos) que significa "denso"), también llamado picnómetro o botella de gravedad específica, es un dispositivo utilizado para determinar la densidad de un líquido. Un picnómetro generalmente está hecho de vidrio, con un tapón de vidrio esmerilado ajustado al cuerpo con un tubo capilar a través de él, de modo que las burbujas de aire puedan escapar del aparato. Este dispositivo permite medir con precisión la densidad de un líquido por referencia a un fluido de trabajo apropiado, como agua o mercurio, utilizando una balanza analítica.
Si el matraz se pesa vacío, lleno de agua y lleno de un líquido cuya densidad relativa se desea, la densidad relativa del líquido se puede calcular fácilmente. La densidad de partículas de un polvo, al que no se puede aplicar el método habitual de pesaje, también se puede determinar con un picnómetro. El polvo se agrega al picnómetro, que luego se pesa, dando el peso de la muestra de polvo. Luego se llena el picnómetro con un líquido de densidad conocida, en el cual el polvo es completamente insoluble. Entonces se puede determinar el peso del líquido desplazado y, por lo tanto, la densidad relativa del polvo.
Un picnómetro de gas, la manifestación basada en gas de un picnómetro, compara el cambio de presión causado por un cambio medido en un volumen cerrado que contiene una referencia (generalmente una esfera de acero de volumen conocido) con el cambio de presión causado por el muestra en las mismas condiciones. La diferencia en el cambio de presión representa el volumen de la muestra en comparación con la esfera de referencia, y generalmente se usa para partículas sólidas que pueden disolverse en el medio líquido del diseño del picnómetro descrito anteriormente, o para materiales porosos en los que el líquido no entraría. penetrar completamente.
Cuando un picnómetro se llena hasta un volumen específico, pero no necesariamente conocido con precisión, V y se coloca sobre una balanza, ejercerá una fuerza
Si a esto le restamos la fuerza medida sobre la botella vacía (o taramos la balanza antes de hacer la medida del agua) obtenemos.
Esto se denomina densidad relativa aparente, denotada por el subíndice A, porque es lo que obtendríamos si tomáramos la relación de pesajes netos en el aire de una balanza analítica o usáramos un hidrómetro (el el vástago desplaza el aire). Tenga en cuenta que el resultado no depende de la calibración de la balanza. El único requisito es que se lea linealmente con fuerza. RDA tampoco depende del volumen real del picnómetro.
Más manipulación y finalmente sustitución de RDV, la verdadera densidad relativa (se usa el subíndice V porque a menudo se lo denomina densidad relativa in vacuo), para ρs/ρw da la relación entre la densidad relativa aparente y la verdadera:
En el caso habitual tendremos pesos medidos y queremos la densidad relativa verdadera. Esto se encuentra de
Dado que la densidad del aire seco a 101,325 kPa a 20 °C es 0,001205 g/cm3 y la del agua es 0,998203 g/cm3 vemos que la La diferencia entre las densidades relativas verdadera y aparente para una sustancia con densidad relativa (20 °C/20 °C) de alrededor de 1,100 sería 0,000120. Cuando la densidad relativa de la muestra es cercana a la del agua (por ejemplo, soluciones diluidas de etanol), la corrección es aún menor.
El picnómetro se utiliza en la norma ISO: ISO 1183-1:2004, ISO 1014–1985 y norma ASTM: ASTM D854.
Tipos
- Gay-Lussac, con forma de pera, con tapón perforado, ajustado, capacidad 1, 2, 5, 10, 25, 50 y 100 mL
- as above, with ground-in thermometer, adjusted, side tube with cap
- Hubbard, para betún y aceites pesados de crudo, tipo cilíndrico, ASTM D 70, 24 mL
- arriba, tipo cónico, ASTM D 115 y D 234, 25 mL
- Bota, con chaqueta de vacío y termómetro, capacidad 5, 10, 25 y 50 mL
Densímetros digitales
Instrumentos basados en presión hidrostática: esta tecnología se basa en el principio de Pascal, que establece que la diferencia de presión entre dos puntos dentro de una columna vertical de fluido depende de la distancia vertical entre los dos puntos, la densidad del fluido y la fuerza gravitacional. Esta tecnología se usa a menudo para aplicaciones de medición de tanques como un medio conveniente para medir el nivel de líquido y la densidad.
Transductores de Elemento Vibrante: Este tipo de instrumento requiere que un elemento vibratorio sea puesto en contacto con el fluido de interés. La frecuencia de resonancia del elemento se mide y se relaciona con la densidad del fluido mediante una caracterización que depende del diseño del elemento. En los laboratorios modernos, las mediciones precisas de la densidad relativa se realizan utilizando medidores de tubo en U oscilantes. Estos son capaces de medir de 5 a 6 lugares más allá del punto decimal y se utilizan en las industrias cervecera, destiladora, farmacéutica, petrolera y otras. Los instrumentos miden la masa real de fluido contenido en un volumen fijo a temperaturas entre 0 y 80 °C, pero como están basados en un microprocesador, pueden calcular la densidad relativa aparente o verdadera y contienen tablas que las relacionan con las concentraciones de ácidos comunes, soluciones de azúcar, etc..
Transductor ultrasónico: las ondas ultrasónicas pasan desde una fuente, a través del fluido de interés, y hacia un detector que mide la espectroscopia acústica de las ondas. Las propiedades del fluido, como la densidad y la viscosidad, se pueden inferir del espectro.
Medidor basado en radiación: la radiación pasa desde una fuente, a través del fluido de interés y hacia un detector de centelleo o contador. A medida que aumenta la densidad del fluido, la radiación detectada "cuenta" va a disminuir. La fuente suele ser el isótopo radiactivo cesio-137, con una vida media de unos 30 años. Una ventaja clave de esta tecnología es que no es necesario que el instrumento esté en contacto con el fluido; por lo general, la fuente y el detector se montan en el exterior de los tanques o las tuberías.
Transductor de fuerza de flotación: la fuerza de flotación que produce un flotador en un líquido homogéneo es igual al peso del líquido que es desplazado por el flotador. Dado que la fuerza de flotabilidad es lineal con respecto a la densidad del líquido dentro del cual se sumerge el flotador, la medida de la fuerza de flotación da una medida de la densidad del líquido. Una unidad disponible en el mercado afirma que el instrumento es capaz de medir la densidad relativa con una precisión de ± 0,005 unidades RD. El cabezal de la sonda sumergible contiene un sistema de resorte-flotador caracterizado matemáticamente. Cuando la cabeza se sumerge verticalmente en el líquido, el flotador se mueve verticalmente y la posición del flotador controla la posición de un imán permanente cuyo desplazamiento es detectado por una matriz concéntrica de sensores de desplazamiento lineal de efecto Hall. Las señales de salida de los sensores se mezclan en un módulo electrónico dedicado que proporciona un voltaje de salida único cuya magnitud es una medida lineal directa de la cantidad a medir.
La densidad relativa en mecánica de suelos
La densidad relativa DR{displaystyle D_{mathrm {R} una medida de la actual relación de vacío en relación con las raciones máximas y mínimas de vacío, y el control efectivo del estrés aplicado el comportamiento mecánico del suelo sin cohesión. La densidad relativa se define por
Ejemplos
| Material | Gravedad específica |
|---|---|
| Balsa madera | 0.2 |
| Madera de roble | 0,75 |
| Ethanol | 0,78 |
| Aceite de oliva | 0.91 |
| Agua | 1 |
| Ironwood | 1,5 |
| Gráfico | 1.9–2.3 |
| Sal | 2.17 |
| Aluminio | 2.7 |
| Cement | 3.15 |
| Iron | 7.87 |
| Copper | 8.96 |
| Lead | 11.35 |
| Mercurio | 13.56 |
| uranio empobrecido | 19.1 |
| Oro | 19.3 |
| Osmium | 22.59 |
(Las muestras pueden variar y estas cifras son aproximadas). Las sustancias con una densidad relativa de 1 tienen flotabilidad neutra, aquellas con RD mayor que uno son más densas que el agua, y por lo tanto (ignorando los efectos de la tensión superficial) se hundirán en ella, y aquellas con una RD menor que uno son menos densas que el agua. y así flotará.
Ejemplo:
El gas helio tiene una densidad de 0,164 g/L; es 0,139 veces más denso que el aire, que tiene una densidad de 1,18 g/L.
- Urine normalmente tiene una gravedad específica entre 1.003 y 1.030. La prueba de diagnóstico de gravedad específica Urine se utiliza para evaluar la capacidad de concentración renal para evaluar el sistema urinario. La baja concentración puede indicar diabetes insipidus, mientras que la alta concentración puede indicar albuminuria o glicosuria.
- La sangre normalmente tiene una gravedad específica de aproximadamente 1.060.
- La prueba Vodka 80° (40% v/v) tiene una gravedad específica de 0.9498.
Contenido relacionado
Konstantin Tsiolkovski
Significado geometrico
Sam Loyd