Xilanasa
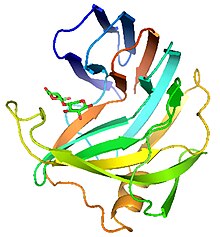
Endo-1,4-β-xilanasa (EC 3.2.1.8, nombre sistemático 4-β-D-xilano xilanohidrolasa) pertenece a una clase de enzimas que degradan el polisacárido lineal xilano en xilosa, descomponiendo así la hemicelulosa, uno de los componentes principales de las paredes celulares de las plantas:
- Endohidrolisis de (1→4)-β-D-vílosidic links in xylans
La xilanasa desempeña un papel importante en los microorganismos que prosperan en fuentes vegetales para la degradación de la materia vegetal en nutrientes utilizables. Las xilanasas son producidas por hongos, bacterias, levaduras, algas marinas, protozoos, caracoles, crustáceos, insectos, semillas, etc.; Los mamíferos no producen xilanasas. Sin embargo, la principal fuente comercial de xilanasas son los hongos filamentosos.
Historia
Décadas de 1970 y 1980: las primeras investigaciones sobre xilanasas comenzaron a mediados de la década de 1970 en el Departamento de Enzimología Química de la Universidad Estatal de Moscú. Los estudios se centraron en comprender el mecanismo, la cinética y las interacciones sinérgicas de las xilanasas y otras carbohidrasas en la conversión enzimática de celulosa y biomasa vegetal. Las aplicaciones comerciales de la xilanasa incluyen el blanqueo sin cloro de la pulpa de madera antes del proceso de fabricación de papel y el aumento de la digestibilidad. de ensilaje (en este aspecto, también se utiliza para compostaje fermentativo).
Hoy en día, la xilanasa continúa siendo un foco de investigación científica, con estudios que profundizan en las propiedades estructurales y funcionales de la enzima para optimizar su uso en diversos procesos biotecnológicos. Sus aplicaciones abarcan las industrias de bebidas y panadería, la producción de papel e incluso los aditivos para piensos avícolas, lo que demuestra el amplio impacto de la enzima tanto en la industria como en la economía.
Clasificación
Las xilanasas se han clasificado al menos de tres maneras: según el peso molecular y el punto isoeléctrico, la estructura cristalina y las propiedades cinéticas, o la especificidad del sustrato y el perfil del producto. El sistema favorable para la clasificación de xilanasas se basa en la estructura primaria y la comparación de los dominios catalíticos. Según la base de datos CAZy (http://www.cazy.orgki>), las xilanasas (EC3.2.1.8) están relacionadas con las familias de glucósidos hidrolasas (GH) 5, 7, 8, 9, 10, 11, 12, 16. , 26, 30, 43, 44, 51 y 62. Entre ellas, las xilanasas en GH 10 y 11 son las dos familias que se han estudiado a fondo.
La familia GH 10 está compuesta por endo-1,4-β-xilanasas y endo-1,3-β-xilanasas (EC 3.2.1.32). Los miembros de esta familia también son capaces de hidrolizar los aril β-glucósidos de xilobiosa y xilotriosa en el enlace aglicónico. Además, estas enzimas son muy activas en xilooligosacáridos cortos, lo que indica pequeños sitios de unión al sustrato. La familia 11 está compuesta únicamente por xilanasas (EC 3.2.1.8), lo que lleva a su consideración como "verdaderas xilanasas", ya que son exclusivamente activas sobre sustratos que contienen d-xilosa. Entre todas las xilanasas, las endoxilanasas son las más importantes debido a su participación directa en la escisión de los enlaces glicosídicos y en la liberación de xilooligosacáridos cortos. Aunque varias especies de Bacillus secretan altos niveles de xilanasa extracelular, los hongos filamentosos secretan altas cantidades de xilanasa extracelular, que a menudo acompaña a las enzimas celulolíticas, por ejemplo, como en especies de Trichoderma, Penicillium y Aspergillus.
Las xilanasas fungales son producidas por una variedad de hongos, incluidas especies de Aspergillus, Trichoderma y Penicillium. Estos hongos son conocidos por su capacidad para secretar grandes cantidades de xilanasa, que pueden usarse para tratar la pulpa de Kraft, mejorando su brillo y delignificación. Aspergillus niger, por ejemplo, es un productor prolífico de xilanasa y se ha utilizado en varios estudios para optimizar la degradación de los desechos de biomasa. Las especies de Trichoderma también son notables por su producción de xilanasa, a menudo utilizadas en combinación con otras especies fúngicas para lograr una descomposición de biomasa eficiente
Las xilanas bacterianas son producidas por bacterias mesofílicas y termofílicas, incluyendo géneros como Bacillus, Streptomyces y Clostridium. Estas bacterias pueden producir xilanases que funcionan a una amplia gama de temperaturas, lo que es beneficioso para diversos procesos industriales. Por ejemplo, las especies de Bacillus se han utilizado en el pienso animal para reducir la viscosidad de la digestión y mejorar la absorción de nutrientes. Streptomyces, un actinomycete, es otro productor significativo de xylanases, con especies como Streptomyces olivaceoviridis E-86 siendo estudiado para su capacidad de degradar sustratos xylan de manera eficiente.
Las actinomicetos xilanasas, particularmente de las especies Streptomyces y Thermomonospora, son conocidas por su robustez y estabilidad, lo que las hace adecuadas para aplicaciones industriales donde prevalecen condiciones duras. El actinomiceto Thermomonospora fusca, por ejemplo, produce xilanasas termoestables que se han estudiado por su potencial en sistemas de cultivo continuo. Las especies de Streptomyces no sólo producen xilanasas sino que también exhiben un amplio espectro de actividades antifúngicas, que pueden ser beneficiosas en entornos agrícolas.
Propiedades
Temperatura óptima
Las xilanasas se pueden clasificar según su temperatura óptima de actividad. Las xilanasas mesófilas funcionan eficientemente a temperaturas moderadas, normalmente entre 40 y 50 °C, lo que las hace adecuadas para procesos que ocurren a temperatura ambiente o cerca de ella. Por otro lado, las xilanasas termófilas exhiben una actividad óptima a temperaturas más altas, por encima de 60°C, lo que resulta ventajoso para procesos industriales que requieren altas temperaturas, ya que estas enzimas son más estables y pueden mantener la actividad en estas condiciones. Por ejemplo, un estudio demostró que una secuencia C-terminal rica en prolina en las xilanasas ruminales GH10 amplía el rango de temperatura óptimo, mejorando su utilidad en procesos que requieren temperaturas operativas más altas.
PH óptimo
La actividad de las xilanasas también depende en gran medida del pH del medio ambiente. La mayoría de las xilanasas tienen un pH óptimo en el rango de ácido a neutro (pH 4-7). Sin embargo, se han identificado xilanasas alcalinas, que tienen un pH óptimo superior a 8, y son particularmente útiles en industrias que operan en condiciones alcalinas. Se han realizado esfuerzos de ingeniería para cambiar el pH óptimo de las xilanasas GH11 hacia valores más alcalinos, ampliando su aplicabilidad en diversos entornos industriales.
Especificidad del sustrato
Las xilanasas varían en su especificidad hacia diferentes sustratos y sustituyentes de xilano. Esta especificidad es crucial para la descomposición eficiente del xilano en sus azúcares constituyentes. Por ejemplo, un estudio sobre una clase de xilanasas derivadas de escarabajos de cuernos largos reveló especificidades de sustrato únicas, destacando la diversidad entre las xilanasas en su enfoque de la hidrólisis de xilano. Comprender y manipular esta especificidad puede conducir a una degradación más eficiente de tipos específicos de biomasa.
Mecanismo catalítico
El mecanismo catalítico de las xilanasas implica dos residuos de glutamato conservados en el sitio activo que facilitan un mecanismo de retención o de inversión para escindir los enlaces β-1,4-xilosídicos en el xilano. En el mecanismo de retención, un glutamato actúa como nucleófilo, formando un intermediario glicosil-enzima covalente, mientras que el otro actúa como un catalizador ácido/base. En el mecanismo de inversión, los dos glutamatos actúan como ácido y base generales, facilitando un ataque nucleofílico directo por parte de una molécula de agua. Los estudios estructurales y la mutagénesis dirigida al sitio han proporcionado información sobre las funciones de los residuos del sitio activo en el reconocimiento, la unión y la catálisis del sustrato.
Producción de xilanasa
La producción de xilanasa implica varios pasos, desde la fermentación microbiana utilizando varios sustratos hasta la extracción, purificación y formulación de la enzima para aplicaciones específicas. Este proceso se puede clasificar en términos generales en cuatro etapas principales: fermentación en estado sólido (SSF), fermentación sumergida (SmF), extracción y purificación, y formulación para aplicaciones específicas.
Fermentación en estado sólido para la producción de xilanasa
La fermentación en estado sólido (SSF) es un proceso en el que los microorganismos crecen en materiales sólidos en ausencia o casi ausencia de agua libre. Este método es particularmente adecuado para hongos, como las especies Penicillium y Aspergillus, que son prolíficos productores de xilanasa. SSF imita el hábitat natural de estos hongos, lo que les permite producir altos rendimientos de enzimas. Los residuos agrícolas como el salvado de trigo, la paja de arroz y las mazorcas de maíz se utilizan comúnmente como sustratos debido a su alto contenido de celulosa y hemicelulosa, que sirven como fuente de carbono para el crecimiento microbiano. Por ejemplo, Penicillium crustosum ha demostrado una notable producción de xilanasa utilizando biomasa de jacinto de agua pretratada en SSF, lo que destaca el potencial de utilizar desechos agrícolas para la producción de enzimas.
Fermentación sumergida para producción de xilanasa
La fermentación sumergida (SmF) implica el cultivo de microorganismos en un medio nutritivo líquido en condiciones controladas. Este método se usa ampliamente para la producción de xilanasa bacteriana, incluidas especies de Bacillus y Streptomyces, debido a la facilidad para controlar los parámetros de fermentación como el pH, la temperatura y la aireación. SmF se caracteriza por tasas de crecimiento microbiano más rápidas y tiempos de fermentación más cortos en comparación con SSF. Un estudio sobre Trichoderma harzianum demostró una producción eficiente de xilanasa en SmF optimizando las condiciones de cultivo, lo que demuestra la eficacia del método para producir xilanasas termoestables adecuadas para aplicaciones industriales.
Extracción y producción de xilanasa
Después de la fermentación, es necesario extraer y purificar la xilanasa del medio de cultivo. El proceso de extracción a menudo implica el uso de sistemas acuosos de dos fases (ATPS) o técnicas de filtración por membrana para separar la enzima de otros componentes celulares. Los pasos de purificación pueden incluir métodos de ultrafiltración, cromatografía o precipitación para lograr el nivel de pureza deseado. Por ejemplo, se ha utilizado un ATPS a base de polietilenglicol y citrato de sodio para extraer xilanasa con alta eficiencia y factor de purificación.
Formulación de xilanasa para aplicación específica
El paso final del proceso de producción es la formulación de la xilanasa purificada para aplicaciones industriales específicas. Esto implica estabilizar la enzima en una forma adecuada, como líquido, polvo o gránulos, y puede incluir la adición de estabilizadores u otros aditivos para mejorar la vida útil y la actividad en las condiciones de aplicación. La formulación depende del uso previsto de la xilanasa, ya sea para la industria de la pulpa y el papel, la producción de biocombustibles, aplicaciones de alimentos y piensos o el procesamiento textil.
Aplicaciones industriales
La versatilidad de las xilanasas ha llevado a su uso extensivo en las industrias de pulpa y papel, alimentos, piensos, biocombustibles y textiles, entre otras.
Industria de celulosa y papel
Tradicionalmente, el proceso de blanqueo en la producción de papel implica el uso de productos químicos agresivos como el cloro y el peróxido de hidrógeno, que pueden tener efectos perjudiciales para el medio ambiente. Sin embargo, la introducción de xilanasas como agente bioblanqueador ha revolucionado este proceso. Al degradar selectivamente el componente xilano de la pulpa, las xilanasas facilitan la eliminación de la lignina, reduciendo así la cantidad de productos químicos necesarios para el blanqueo. Esto no sólo minimiza el impacto ambiental sino que también mejora la calidad general y el brillo de la pulpa.
Industria alimentaria
En la industria alimentaria, las xilanasas han encontrado numerosas aplicaciones, especialmente en el sector de la panificación. Se ha demostrado que la adición de xilanasas a la masa de pan mejora sus propiedades de manipulación, textura y vida útil. Al hidrolizar el xilano presente en la masa, las xilanasas ayudan en la redistribución del agua, lo que mejora la estabilidad de la masa y reduce la pegajosidad. Además, la liberación de xilooligosacáridos durante el proceso de horneado puede contribuir a la formación de un color y sabor de corteza deseables. Las xilanasas también se emplean en el procesamiento de frutas y verduras, donde ayudan a clarificar jugos y vinos al reducir la viscosidad y mejorar la calidad general del producto final.
Industria de alimentación animal
La presencia de polisacáridos no almidones, como xylan, en pienso animal puede conducir a una disminución de la digestibilidad de nutrientes y a una mayor viscosidad del pienso, que puede afectar negativamente el rendimiento animal. Se ha encontrado la incorporación de xilanases en piensos animales para aliviar estos problemas rompiendo el componente xylan, mejorando así la absorción de nutrientes y reduciendo la viscosidad del alimento. Esto, a su vez, conduce a una mejor eficiencia de conversión de piensos y a un mayor crecimiento animal.
Industria de biocombustibles
La producción de bioetanol y otros biocombustibles a partir de biomasa lignocelulósica requiere la sacarificación eficiente de la biomasa en azúcares fermentables. Las xilanasas desempeñan un papel crucial en este proceso al hidrolizar el componente xilano de la fracción de hemicelulosa, aumentando así la accesibilidad de la celulosa para la posterior hidrólisis enzimática. Se ha demostrado que la acción sinérgica de las xilanasas con otras enzimas, como las celulasas, mejora significativamente el rendimiento general de azúcares fermentables, haciendo que el proceso de producción de biocombustibles sea más viable económicamente.
Industria textil
Las xilanasas han encontrado aplicaciones en el procesamiento de fibras vegetales, como el lino y el ramio. Estas fibras suelen contener una cantidad importante de hemicelulosa, que puede interferir con los procesos de teñido y acabado. El tratamiento de estas fibras con xilanasas ayuda a eliminar el componente hemicelulósico, lo que mejora las propiedades de la fibra, como mayor suavidad, brillo y absorción de tinte. Además, el uso de xilanasas reduce la necesidad de tratamientos químicos agresivos, lo que hace que el procesamiento textil sea más ecológico.
Las diversas aplicaciones de las xilanasas en diversas industrias las han convertido en una herramienta invaluable en biotecnología. Desde mejorar la eficiencia y la sostenibilidad de la industria de la pulpa y el papel hasta mejorar el valor nutricional de los piensos y facilitar la producción de biocombustibles, las xilanasas han demostrado su inmenso potencial. A medida que la demanda de procesos sostenibles y respetuosos con el medio ambiente continúa creciendo, se espera que el uso de xilanasas se expanda aún más, impulsando la innovación y los avances en diversos sectores industriales.
Aparte de su uso en la industria de la pulpa y el papel, las xilanasas también se utilizan como aditivos alimentarios para las aves de corral; en harina de trigo para mejorar el manejo de la masa y la calidad de los productos horneados [2]; para la extracción de café, aceites vegetales y almidón; en la mejora de las propiedades nutricionales de los ensilajes agrícolas y los piensos a base de cereales; y en combinación con pectinasa y celulasa para clarificar jugos de frutas y desgomar fuentes de fibra vegetal como lino, cáñamo, yute y ramio. Se encuentra disponible una buena cantidad de literatura científica sobre las características clave de las enzimas xilanasas en biotecnología, desde su detección en fuentes microbianas hasta métodos de producción, caracterización, purificación y aplicaciones en el sector comercial. Para algunas aplicaciones de xilanasa se requiere una alta resiliencia al calentamiento, lo que se puede lograr mediante la selección de enzimas microbianas adecuadas o mediante la ciclación de los extremos mediante la reacción SpyTag/SpyCatcher.
Además, la xilanasa es el ingrediente clave en los acondicionadores de masa s500 y us500 fabricados por Puratos
En el futuro, la xilanasa podrá utilizarse para la producción de biocombustibles a partir de material vegetal inutilizable.
Condición óptima de almacenamiento
El almacenamiento adecuado de las preparaciones de xilanasa es esencial para mantener su actividad y estabilidad, así como para prevenir posibles peligros asociados con la degradación o contaminación de la enzima. Las condiciones óptimas de almacenamiento de xilanasas pueden variar según la formulación enzimática específica y las recomendaciones del fabricante.
En general, las xilanasas deben almacenarse en un lugar fresco y seco, alejado de la luz solar directa y de fuentes de calor. La temperatura de almacenamiento recomendada para la mayoría de las preparaciones de xilanasa está entre 4°C y 25°C. Algunas formulaciones pueden requerir refrigeración para mantener su actividad y estabilidad durante períodos prolongados.
También es fundamental garantizar que las preparaciones de xilanasa se almacenen en recipientes herméticamente cerrados para evitar la absorción de humedad y la contaminación. La exposición a la humedad puede provocar la degradación de las enzimas y la pérdida de actividad, así como el crecimiento de microorganismos que pueden suponer riesgos para la salud.
La vida útil de las preparaciones de xilanasa puede variar según la formulación específica y las condiciones de almacenamiento. Los fabricantes suelen proporcionar información sobre la vida útil esperada de sus productos, que puede variar desde varios meses hasta algunos años. Es importante seguir las pautas del fabricante y utilizar la preparación enzimática antes de su fecha de vencimiento para garantizar un rendimiento y una seguridad óptimos.
Peligros potenciales
Una de las principales preocupaciones al trabajar con xilanasas es la posibilidad de que se produzcan reacciones alérgicas en personas sensibles. Al igual que otras enzimas y proteínas, las xilanasas pueden provocar reacciones alérgicas por inhalación o contacto con la piel. Los síntomas de una reacción alérgica pueden incluir dificultades respiratorias, como asma o rinitis, así como irritación de la piel o dermatitis. En casos raros, pueden producirse reacciones alérgicas graves, como anafilaxia.
Para minimizar el riesgo de reacciones alérgicas, se deben implementar medidas de protección y manipulación adecuadas cuando se trabaja con preparaciones de xilanasa. Esto incluye el uso de equipo de protección personal (EPP) adecuado, como guantes, gafas de seguridad y protección respiratoria, especialmente al manipular formas de la enzima en polvo o aerosoles. Además, se deben implementar medidas adecuadas de ventilación y control del polvo para reducir el riesgo de exposición por inhalación.
Si bien las xilanasas generalmente se consideran seguras y no tóxicas, es esencial ser consciente de los peligros potenciales asociados con su uso, particularmente el riesgo de reacciones alérgicas en personas sensibles. Se deben seguir medidas de protección y manipulación adecuadas, incluido el uso de EPP apropiado y ventilación adecuada, para minimizar estos riesgos. Además, el almacenamiento adecuado de las preparaciones de xilanasa, en un lugar fresco y seco y en recipientes herméticamente cerrados, es crucial para mantener su actividad, estabilidad y seguridad. Siguiendo estas pautas y las recomendaciones del fabricante, el uso industrial de las xilanasas se podrá realizar de forma segura y eficaz.
Sinónimos
Endo-(1→4)-β-xilano 4-xilanohidrolasa, endo-1,4-xilanasa, endo-1,4-β-xilanasa, β-1,4-xilanasa, endo-1,4- β-D-xilanasa, 1,4-β-xilan xilanohidrolasa, β-xilanasa, β-1,4-xilan xilanohidrolasa, β-D-xilanasa
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar