Vancomicina
La vancomicina es un medicamento antibiótico glicopéptido que se utiliza para tratar una serie de infecciones bacterianas. Se recomienda por vía intravenosa como tratamiento para infecciones complicadas de la piel, infecciones del torrente sanguíneo, endocarditis, infecciones de huesos y articulaciones y meningitis causadas por Staphylococcus aureus resistente a la meticilina. Se pueden medir los niveles en sangre para determinar la dosis correcta. La vancomicina también se toma por vía oral como tratamiento para la colitis grave por Clostridium difficile. Cuando se toma por vía oral se absorbe mal.
Los efectos secundarios comunes incluyen dolor en el área de la inyección y reacciones alérgicas. Ocasionalmente, se presenta pérdida de la audición, presión arterial baja o supresión de la médula ósea. La seguridad en el embarazo no está clara, pero no se ha encontrado evidencia de daño, y es probable que sea seguro para su uso durante la lactancia. Es un tipo de antibiótico glicopéptido y funciona bloqueando la construcción de una pared celular.
La vancomicina se aprobó para uso médico en los Estados Unidos en 1958. Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud. La Organización Mundial de la Salud clasifica la vancomicina como de importancia crítica para la medicina humana. Está disponible como medicamento genérico. La vancomicina es producida por la bacteria del suelo Amycolatopsis orientalis.
Usos médicos
La vancomicina está indicada para el tratamiento de infecciones graves y potencialmente mortales por bacterias grampositivas que no responden a otros antibióticos.
La aparición cada vez mayor de enterococos resistentes a la vancomicina ha resultado en el desarrollo de pautas para su uso por parte del Comité Asesor de Prácticas de Control de Infecciones Hospitalarias de los Centros para el Control de Enfermedades. Estas pautas restringen el uso de vancomicina a estas indicaciones:
- Tratamiento de infecciones graves causadas por organismos susceptibles resistentes a penicilinas (resistente a la methicilina S. aureus (MRSA) and multidrug-resistant S. epidermidis (MRSE)) o en individuos con alergia grave a penicilinas
- Tratamiento de la colitis pseudomembrana causada por C. difficile; en particular, en casos de recaída o donde la infección no responde al tratamiento metronidazol (para esta indicación, la vancomicina se administra oralmente, en lugar de por su ruta intravenosa típica)
- Para el tratamiento de infecciones causadas por microorganismos grampositivos en pacientes con alergias graves a antimicrobianos beta-lactam.
- Profilaxis antibacteriana para la endocarditis siguiendo ciertos procedimientos en individuos penicilina-hipersen sensibles a alto riesgo
- Profilaxis quirúrgica para procedimientos principales que implican implantar prótesis en instituciones con una alta tasa de MRSA o MRSE
- Temprano en tratamiento como antibiótico empírico para posible infección de MRSA mientras espera la identificación cultural del organismo infectante
- Halting the progression of primary sclerosing cholangitis and preventing signs; vancomycin does not cure the patient and success is limited
- Tratamiento de la endoftalmitis por inyección intravitreal para la cobertura bacteriana grampositiva. Sin embargo, no se recomienda utilizar para prevenir la afección debido al riesgo de efectos secundarios.
Espectro de susceptibilidad
La vancomicina se considera un medicamento de último recurso para el tratamiento de la sepsis y las infecciones de las vías respiratorias inferiores, la piel y los huesos causadas por bacterias grampositivas. Los datos de susceptibilidad a la concentración inhibitoria mínima para algunas bacterias médicamente significativas son:
- S. aureus: 0.25 μg/mL a 4.0 μg/m L
- S. aureus (resistente a la metilina o MRSA): 1 μg/mL a 138 μg/m L
- S. epidermidis: ≤0.12 μg/mL a 6.25 μg/m L
Efectos secundarios
Los niveles séricos de vancomicina pueden controlarse en un esfuerzo por reducir los efectos secundarios, aunque se ha cuestionado el valor de dicho control. Por lo general, se controlan los niveles máximos y mínimos y, con fines de investigación, a veces también se utiliza el área bajo la curva de concentración. La toxicidad se controla mejor observando los valores mínimos.
Las reacciones adversas al medicamento comunes (≥1 % de los pacientes) asociadas con la vancomicina IV incluyen: dolor local, que puede ser intenso, y tromboflebitis.
El daño a los riñones (nefrotoxicidad) y al oído (ototoxicidad) fueron efectos secundarios de las primeras versiones impuras de la vancomicina, y fueron prominentes en los ensayos clínicos realizados a mediados de la década de 1950. Ensayos posteriores que utilizaron formas más puras de vancomicina encontraron que la nefrotoxicidad es un efecto adverso poco frecuente (0,1% a 1% de los pacientes), pero esto se acentúa en presencia de aminoglucósidos.
Los efectos adversos raros (<0,1 % de los pacientes) incluyen: anafilaxia, necrólisis epidérmica tóxica, eritema multiforme, síndrome del hombre rojo, superinfección, trombocitopenia, neutropenia, leucopenia, tinnitus, mareos u ototoxicidad y síndrome DRESS.
La vancomicina puede inducir anticuerpos reactivos contra las plaquetas en el paciente, lo que lleva a una trombocitopenia severa y sangrado con hemorragias petequiales floridas, equimosis y púrpura húmeda.
Históricamente, la vancomicina se ha considerado un fármaco nefrotóxico y ototóxico, según numerosos informes de casos en la literatura médica luego de la aprobación inicial de la FDA en 1958. Sin embargo, a medida que el uso de vancomicina aumentó con la propagación de MRSA a partir de la década de 1970, se reevaluaron los riesgos de toxicidad. Con la eliminación de las impurezas presentes en las formulaciones anteriores del fármaco y con la introducción del control terapéutico del fármaco, se ha reducido el riesgo de toxicidad grave.
Nefrotoxicidad
El grado de nefrotoxicidad de la vancomicina sigue siendo controvertido. En la década de 1980, la vancomicina con una pureza > El 90 % estaba disponible y la toxicidad renal definida por un aumento de la creatinina sérica de al menos 0,5 mg/dl se produjo en solo alrededor del 5 % de los pacientes. Sin embargo, las pautas de dosificación desde la década de 1980 hasta 2008 recomendaban concentraciones mínimas de vancomicina entre 5 y 15 μg/ml. La preocupación por los fracasos del tratamiento hizo que se recomendaran dosis más altas (mínimas de 15 a 20 μg/ml) para infecciones graves, y aumentaron las tasas de lesión renal aguda (IRA) atribuibles a la vancomicina.
Es importante destacar que el riesgo de AKI aumenta con la administración conjunta de otras nefrotoxinas conocidas, en particular, los aminoglucósidos. Además, el tipo de infecciones tratadas con vancomicina también puede causar LRA y la sepsis es la causa más común de LRA en pacientes críticos. Finalmente, los estudios en humanos son principalmente estudios de asociaciones donde la causa del DRA suele ser multifacético.
Los estudios en animales han demostrado que las dosis más altas y la mayor duración de la exposición a la vancomicina se correlacionan con un mayor daño histopatológico y elevaciones en los biomarcadores urinarios de LRA. como molécula de daño renal-1 (KIM-1), clusterina y osteopontina (OPN), y en humanos, proteína de unión al factor de crecimiento similar a la insulina 7 (IGFBP7) como parte de la prueba nephrocheck.
Los mecanismos que subyacen a la patogenia de la nefrotoxicidad por vancomicina son multifactoriales, pero incluyen nefritis intersticial, lesión tubular debida al estrés oxidativo y formación de cilindros.
Ototoxicidad
Los intentos de establecer las tasas de ototoxicidad inducida por vancomicina son aún más difíciles debido a la escasez de pruebas de calidad. El consenso actual es que los casos claramente relacionados de ototoxicidad por vancomicina son raros. La asociación entre los niveles séricos de vancomicina y la ototoxicidad también es incierta. Si bien se han notificado casos de ototoxicidad en pacientes cuyo nivel sérico de vancomicina excedía los 80 µg/mL, también se han notificado casos en pacientes con niveles terapéuticos. Por lo tanto, si el seguimiento del fármaco terapéutico de la vancomicina con el fin de mantener el estado "terapéutico" los niveles prevendrán la ototoxicidad también sigue sin probarse.
Interacciones con otras nefrotoxinas
Otra área de controversia e incertidumbre se refiere a la cuestión de si la vancomicina aumenta la toxicidad de otras nefrotoxinas y, de ser así, en qué medida. Los estudios clínicos han arrojado resultados variables, pero los modelos animales indican que probablemente se produce un aumento del efecto nefrotóxico cuando se agrega vancomicina a nefrotoxinas como los aminoglucósidos. Sin embargo, no se ha establecido una relación dosis-o nivel sérico-efecto.
Consideraciones de dosificación
La dosis parenteral recomendada en adultos es de 500 mg iv cada 6 horas o 1000 mg cada 12 horas, con modificaciones para lograr un rango terapéutico según sea necesario. La dosis oral recomendada en el tratamiento de enterocolitis pseudomembranosa inducida por antibióticos es de 125 a 500 mg cada 6 horas durante 7 a 10 días.
Administración intravenosa versus oral
La vancomicina debe administrarse por vía intravenosa (IV) para la terapia sistémica, ya que no se absorbe en el intestino. Es una molécula hidrofílica grande que se reparte mal a través de la mucosa gastrointestinal. Debido a su corta vida media, a menudo se inyecta dos veces al día.
La única indicación aprobada para el tratamiento con vancomicina oral es el tratamiento de la colitis pseudomembranosa, donde debe administrarse por vía oral para llegar al sitio de la infección en el colon. Tras la administración oral, la concentración fecal de vancomicina es de alrededor de 500 µg/mL (las cepas sensibles de C. difficile tienen una concentración inhibidora media de ≤2 µg/mL)
La vancomicina inhalada también se ha utilizado (fuera de etiqueta), a través de un nebulizador, para el tratamiento de diversas infecciones de las vías respiratorias superiores e inferiores.
Hay un debate en curso sobre si la vancomicina debe administrarse a través de una vía central o periférica. Según una revisión de 2014, los catéteres de línea media son una opción segura para la administración.
Reacción de enrojecimiento por vancomicina (también conocida como "síndrome del hombre rojo")
Se recomienda administrar vancomicina en una solución diluida lentamente, durante al menos 60 min (velocidad máxima de 10 mg/min para dosis >500 mg) debido a la alta incidencia de dolor y tromboflebitis y para evitar una reacción a la infusión conocida como reacción de lavado con vancomicina. Este fenómeno a menudo se ha denominado clínicamente "síndrome del hombre rojo". La reacción generalmente aparece dentro de los 4 a 10 min después del comienzo o poco después de completar una infusión y se caracteriza por enrojecimiento y/o erupción eritematosa que afecta la cara, el cuello y la parte superior del torso, atribuida a la liberación de histamina de la mastocitos Estos hallazgos se deben a la interacción de la vancomicina con MRGPRX2, un GPCR que media en la desgranulación de mastocitos independiente de IgE. Con menos frecuencia, también pueden ocurrir hipotensión y angioedema. Los síntomas pueden tratarse o prevenirse con antihistamínicos, incluida la difenhidramina, y es menos probable que ocurran con una infusión lenta.
Monitorización de fármacos terapéuticos
Es necesario monitorear el nivel plasmático de vancomicina debido a la distribución biexponencial, la hidrofilicidad intermedia y el potencial de ototoxicidad y nefrotoxicidad del fármaco, especialmente en poblaciones con función renal deficiente y/o mayor propensión a infecciones bacterianas. Se considera que la actividad de la vancomicina depende del tiempo; es decir, la actividad antimicrobiana depende de la duración en que la concentración sérica del fármaco exceda la concentración inhibitoria mínima del organismo objetivo. Por lo tanto, no se ha demostrado que los niveles séricos máximos se correlacionen con la eficacia o la toxicidad; de hecho, el control de la concentración es innecesario en la mayoría de los casos. Las circunstancias en las que se justifica la monitorización terapéutica del fármaco incluyen: pacientes que reciben tratamiento concomitante con aminoglucósidos, pacientes con (potencialmente) parámetros farmacocinéticos alterados, pacientes en hemodiálisis, pacientes que reciben dosis altas o tratamiento prolongado y pacientes con insuficiencia renal. En tales casos, se miden las concentraciones mínimas.
Los rangos objetivo para las concentraciones séricas de vancomicina han cambiado a lo largo de los años. Los primeros autores sugirieron niveles máximos de 30 a 40 mg/L y niveles mínimos de 5 a 10 mg/L, pero las recomendaciones actuales son que no es necesario medir los niveles máximos y que pueden ser apropiados niveles mínimos de 10 a 15 mg/L o de 15 a 20 mg/L, según la naturaleza de la infección y las necesidades específicas del paciente. El uso de concentraciones medidas de vancomicina para calcular las dosis optimiza la terapia en pacientes con depuración renal aumentada.
Biosíntesis
La vancomicina es producida por la bacteria del suelo Amycolatopsis orientalis.
La biosíntesis de vancomicina se produce principalmente a través de tres síntesis de proteínas no ribosómicas (NRPS): VpsA, VpsB y VpsC. Las enzimas determinan la secuencia de aminoácidos durante su ensamblaje a través de sus 7 módulos. Antes de ensamblar la vancomicina a través de NRPS, primero se sintetizan los aminoácidos no proteinogénicos. La L-tirosina se modifica para convertirse en los residuos de β-hidroxitirosina (β-HT) y 4-hidroxifenilglicina (4-Hpg). El anillo de 3,5 dihidroxifenilglicina (3,5-DPG) se deriva del acetato.
La síntesis de péptidos no ribosómicos ocurre a través de distintos módulos que pueden cargar y extender la proteína en un aminoácido por módulo a través de la formación de enlaces amida en los sitios de contacto de los dominios de activación. Cada módulo consta típicamente de un dominio de adenilación (A), un dominio de proteína transportadora de péptidos (PCP) y un dominio de condensación (C). En el dominio A, el aminoácido específico se activa convirtiéndolo en un complejo enzimático de adenilato de aminoacil unido a un cofactor de 4'fosfopanteteína mediante tioesterificación. Luego, el complejo se transfiere al dominio PCP con la expulsión de AMP. El dominio PCP utiliza el grupo prostético 4'-fosfopanteteína adjunto para cargar la cadena peptídica en crecimiento y sus precursores. La organización de los módulos necesarios para biosintetizar Vancomicina se muestra en la Figura 1. En la biosíntesis de Vancomicina, están presentes dominios de modificación adicionales, como el dominio de epimerización (E), que isomeriza el aminoácido de una estereoquímica a otra, y una tioesterasa El dominio (TE) se utiliza como catalizador para la ciclación y liberación de la molécula a través de una escisión de tioesterasa.
Un conjunto de enzimas NRPS (péptido sintasa VpsA, VpsB y VpsC) son responsables de ensamblar el heptapéptido. (Figura 2). Códigos VpsA para los módulos 1, 2 y 3. Códigos VpsB para los módulos 4, 5 y 6, y códigos VpsC para el módulo 7. La aglicona de vancomicina contiene 4 D-aminoácidos, aunque los NRPS solo contienen 3 dominios de epimerización. Se desconoce el origen de D-Leu en el residuo 1. Las tres síntesis de péptidos se ubican al comienzo de la región del genoma bacteriano vinculada con la biosíntesis de antibióticos y abarcan 27 kb.
La β-hidroxitirosina (β-HT) se sintetiza antes de incorporarla al esqueleto del heptapéptido. La L-tirosina se activa y se carga en el NRPS VpsD, se hidroxila por OxyD y se libera por la tioesterasa Vhp. Actualmente no se ha determinado el momento de la cloración por la halogenasa VhaA durante la biosíntesis, pero se propone que ocurra antes del ensamblaje completo del heptapéptido.
Después de sintetizar la molécula de heptapéptido lineal, la vancomicina tiene que sufrir más modificaciones, como el entrecruzamiento oxidativo y la glicosilación, en trans por distintas enzimas, denominadas enzimas de adaptación, para volverse biológicamente activa (Figura 3). Para convertir el heptapéptido lineal en vancomicina glicosilada reticulada, se requieren seis enzimas. Las enzimas OxyA, OxyB, OxyC y OxyD son enzimas del citocromo P450. OxyB cataliza el entrecruzamiento oxidativo entre los residuos 4 y 6, OxyA entre los residuos 2 y 4 y OxyC entre los residuos 5 y 7. Este entrecruzamiento se produce mientras el heptapéptido está unido covalentemente al dominio PCP del 7º módulo NRPS. Estos P450 son reclutados por el dominio X presente en el módulo 7th NRPS, que es exclusivo de la biosíntesis de antibióticos glicopéptidos. El heptapéptido entrecruzado luego se libera por la acción del dominio TE, y la metiltransferasa Vmt luego N-metila el residuo de leucina terminal. Luego, GtfE se une a la D-glucosa con el oxígeno fenólico del residuo 4, seguido de la adición de vancosamina catalizada por GtfD.
Algunas de las glicosiltransferasas capaces de glicosilar la vancomicina y los péptidos no ribosómicos relacionados muestran una permisividad notable y se han empleado para generar bibliotecas de análogos glicosilados diferencialmente a través de un proceso conocido como glicoaleatorización.
Síntesis total
Tanto la aglicona de vancomicina como la molécula completa de vancomicina han sido objetivos alcanzados con éxito por la síntesis total. El objetivo fue alcanzado por primera vez por David Evans en octubre de 1998, KC Nicolaou en diciembre de 1998, Dale Boger en 1999, y recientemente Dale Boger lo sintetizó de manera más selectiva en 2020.
Farmacología y química
La vancomicina es un péptido no ribosómico glicosilado tricíclico ramificado producido por la especie Actinomycetota Amycolatopsis orientalis (anteriormente denominada Nocardia orientalis).
La vancomicina exhibe atropisomerismo: tiene múltiples rotámeros químicamente distintos debido a la restricción rotacional de algunos de los enlaces. La forma presente en el fármaco es el confórmero termodinámicamente más estable.
Mecanismo de acción
La vancomicina actúa inhibiendo la síntesis adecuada de la pared celular en bacterias Gram-positivas. Debido al diferente mecanismo por el cual las bacterias Gram-negativas producen sus paredes celulares y a los diversos factores relacionados con la penetración en la membrana externa de los organismos Gram-negativos, la vancomicina no es activa contra ellos (excepto algunas especies no gonocócicas de Neisseria).
La gran molécula hidrófila es capaz de formar interacciones de enlaces de hidrógeno con los restos terminales D-alanil-D-alanina de los péptidos NAM/NAG. En circunstancias normales, esta es una interacción de cinco puntos. Esta unión de la vancomicina a la D-Ala-D-Ala impide la síntesis en la pared celular de los polímeros largos del ácido N-acetilmurámico (NAM) y N-acetilglucosamina (NAG) que forman las hebras de la columna vertebral de la pared celular bacteriana, y evita que los polímeros de la columna vertebral que logran formarse se entrecrucen entre sí.
Cultivo de tejidos vegetales
La vancomicina es uno de los pocos antibióticos utilizados en el cultivo de tejidos vegetales para eliminar la infección por bacterias Gram-positivas. Tiene una toxicidad relativamente baja para las plantas.
Resistencia a los antibióticos
Resistencia intrínseca
Algunas bacterias Gram-positivas son intrínsecamente resistentes a la vancomicina: las especies Leuconostoc y Pediococcus, pero estos organismos rara vez causan enfermedades en humanos. La mayoría de las especies de Lactobacillus también son intrínsecamente resistentes a la vancomicina, con la excepción de L. acidophilus y L. delbrueckii, que son sensibles. Otras bacterias Gram-positivas con resistencia intrínseca a la vancomicina incluyen Erysipelothrix rhusiopathiae, Weissella confusa y Clostridium innocuum.
La mayoría de las bacterias gramnegativas son intrínsecamente resistentes a la vancomicina porque sus membranas externas son impermeables a las moléculas grandes de glucopéptidos (con la excepción de algunas especies de Neisseria no gonocócicas).
Resistencia adquirida
La evolución de la resistencia microbiana a la vancomicina es un problema creciente, en particular, dentro de los centros de salud como los hospitales. Si bien existen alternativas más nuevas a la vancomicina, como linezolid (2000) y daptomicina (2003), el uso generalizado de vancomicina hace que la resistencia al fármaco sea una preocupación importante, especialmente para pacientes individuales si las infecciones resistentes no se identifican rápidamente y el paciente continúa con el tratamiento ineficaz. tratamiento. Los enterococos resistentes a la vancomicina surgieron en 1986. La resistencia a la vancomicina evolucionó en organismos patógenos más comunes durante las décadas de 1990 y 2000, incluido el S. aureus intermedio a la vancomicina (VISA) y el S. aureus resistente a la vancomicina (VRSA). El uso agrícola de avoparcina, otro antibiótico glicopeptídico similar, puede haber contribuido a la evolución de organismos resistentes a la vancomicina.
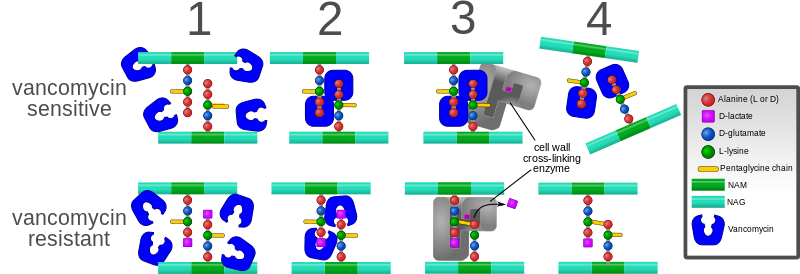
Un mecanismo de resistencia a la vancomicina implica la alteración de los residuos de aminoácidos terminales de las subunidades peptídicas NAM/NAG, en condiciones normales, D-alanil-D -alanina, a la que se une la vancomicina. La variación de D-alanil-D-lactato da como resultado la pérdida de una interacción de enlace de hidrógeno (4, en lugar de 5 para D- alanil-D-alanina) posible entre la vancomicina y el péptido. Esta pérdida de solo un punto de interacción da como resultado una disminución de 1000 veces en la afinidad. La variación D-alanil-D-serina provoca una pérdida de afinidad seis veces mayor entre la vancomicina y el péptido, probablemente debido a un impedimento estérico.
En los enterococos, esta modificación parece deberse a la expresión de una enzima que altera el residuo terminal. Hasta la fecha se han caracterizado tres variantes principales de resistencia entre Enterococcus faecium resistente y E. Poblaciones de faecalis:
- VanA - resistencia enterococal a la vancomicina y teicoplanina; inducible sobre la exposición a estos agentes
- VanB - resistencia enterococal de menor nivel; inducible por vancomycina, pero las cepas pueden permanecer susceptibles a teicoplanina
- VanC - menos importante clínicamente; enterococci resistente sólo a la vancomicina; resistencia constitutiva
Se probó una variante de la vancomicina que se une a la variación del ácido D-láctico resistente en las paredes celulares bacterianas resistentes a la vancomicina y también se une bien al objetivo original (bacterias sensibles a la vancomicina).
"Recuperado" vancomicina
En 2020, un equipo del Hospital Universitario de Heidelberg (Alemania) recuperó el poder antibacteriano de la vancomicina modificando la molécula con un oligopéptido catiónico. El oligopéptido consta de seis unidades de arginina en la posición VN. En comparación con la vancomicina no modificada, la actividad contra las bacterias resistentes a la vancomicina podría potenciarse en un factor de 1.000. Este fármaco aún se encuentra en desarrollo preclínico. Por lo tanto, una posible aprobación llevará varios años más.
Historia
La vancomicina fue aislada por primera vez en 1953 por Edmund Kornfeld (trabajando en Eli Lilly) de una bacteria en una muestra de suelo recolectada en las selvas del interior de Borneo por un misionero, el reverendo William M. Bouw (1918–2006). El organismo que lo produjo finalmente se denominó Amycolatopsis orientalis. La indicación original de la vancomicina era para el tratamiento de Staphylococcus aureus resistente a la penicilina.
El compuesto inicialmente se llamó compuesto 05865, pero finalmente se le dio el nombre genérico de vancomicina, derivado del término "vencer". Una ventaja que se hizo evidente rápidamente fue que los estafilococos no desarrollaron una resistencia significativa, a pesar de los pases en serie en medios de cultivo que contenían vancomicina. El rápido desarrollo de la resistencia a la penicilina por parte de los estafilococos condujo a que la Administración de Alimentos y Medicamentos (FDA) acelerara su aprobación. En 1958, Eli Lilly comercializó por primera vez el clorhidrato de vancomicina con el nombre comercial Vancocin.
La vancomicina nunca se convirtió en el tratamiento de primera línea para S. aureus por varias razones:
- Posee escasa biodisponibilidad oral, por lo que debe administrarse por vía intravenosa para la mayoría de las infecciones.
- β-Lactamase-resistant semisynthetic penicillins such as methicillin (and its successors, nafcillin and cloxacillin) were subsequently developed, which have better activity against non-MRSA staphylococci.
- Los primeros ensayos utilizaron formas tempranas e impuros de la droga ("Lodo Mississippi"), que se encontraron como tóxicos para el oído interno y para los riñones; estos hallazgos llevaron a que la vancomicina se relegara a la posición de un medicamento de último recurso.
En 2004, Eli Lilly otorgó la licencia de Vancocin a ViroPharma en los EE. UU., Flynn Pharma en el Reino Unido y Aspen Pharmacare en Australia. La patente había expirado a principios de la década de 1980 y la FDA autorizó la venta de varias versiones genéricas en los EE. UU., incluso de los fabricantes Bioniche Pharma, Baxter Healthcare, Sandoz, Akorn-Strides y Hospira.
Contenido relacionado
Criostasis (hidratos de clatrato)
Neurofisiología clínica
Eduardo Jenner