Transcripción primaria

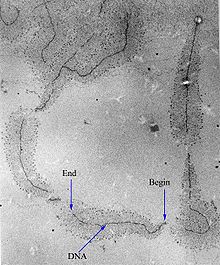
Una transcripción primaria es el producto de ácido ribonucleico (ARN) monocatenario sintetizado mediante la transcripción de ADN y procesado para producir diversos productos de ARN maduro, como ARNm, ARNt y ARNr. Las transcripciones primarias designadas como ARNm se modifican en preparación para la traducción. Por ejemplo, un ARNm precursor (pre-ARNm) es un tipo de transcripción primaria que se convierte en un ARN mensajero (ARNm) después del procesamiento.
Pre-mRNA se sintetiza a partir de una plantilla de ADN en el núcleo celular por transcripción. Pre-mRNA comprende la mayor parte de ARN nuclear heterogénea ()hnRNA). Una vez que el pre-mRNA ha sido procesado por completo, se denomina "RNA Mensajero maduro", o simplemente "RNA más joven". El término hnRNA se utiliza a menudo como sinónimo de pre-mRNA, aunque, en el sentido estricto, hnRNA puede incluir transcripciones nucleares de ARN que no terminan como mRNA citoplasmático.
Hay varios pasos que contribuyen a la producción de transcripciones primarias. Todos estos pasos implican una serie de interacciones para iniciar y completar la transcripción del ADN en el núcleo de eucariotas. Ciertos factores desempeñan funciones clave en la activación e inhibición de la transcripción, donde regulan la producción de transcripción primaria. La transcripción produce transcripciones primarias que son modificadas por varios procesos. Estos procesos incluyen el gorro de 5', 3'-polyadenylation, y el aguijón alternativo. En particular, el riego alternativo contribuye directamente a la diversidad de mRNA que se encuentra en las células. Las modificaciones de las transcripciones primarias se han estudiado en investigación buscando mayor conocimiento del papel y la importancia de estas transcripciones. Estudios experimentales basados en cambios moleculares a las transcripciones primarias y los procesos antes y después de la transcripción han llevado a una mayor comprensión de las enfermedades que implican transcripciones primarias.
Producción
Los pasos que contribuyen a la producción de transcripciones primarias implican una serie de interacciones moleculares que inician la transcripción del ADN dentro del núcleo de una célula. Según las necesidades de una célula determinada, ciertas secuencias de ADN se transcriben para producir una variedad de productos de ARN que se traducirán en proteínas funcionales para uso celular. Para iniciar el proceso de transcripción en el núcleo de una célula, se desenrollan las dobles hélices del ADN y se rompen los enlaces de hidrógeno que conectan los ácidos nucleicos compatibles del ADN para producir dos hebras individuales de ADN desconectadas. Una hebra del molde de ADN se utiliza para la transcripción del ARNm del transcrito primario monocatenario. Esta cadena de ADN está unida por una ARN polimerasa en la región promotora del ADN.
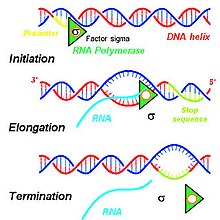
En los eucariotas, se producen tres tipos de ARN (ARNr, ARNt y ARNm) en función de la actividad de tres ARN polimerasas distintas, mientras que, en los procariotas, solo existe una ARN polimerasa para crear todo tipo de moléculas de ARN. La ARN polimerasa II de eucariotas transcribe la transcripción primaria, una transcripción destinada a ser procesada en ARNm, a partir de la plantilla de ADN antisentido en la región 5' a 3' dirección, y este transcrito primario recién sintetizado es complementario a la cadena antisentido de ADN. La ARN polimerasa II construye la transcripción primaria utilizando un conjunto de cuatro residuos de ribonucleósido monofosfato específicos (monofosfato de adenosina (AMP), monofosfato de citidina (CMP), monofosfato de guanosina (GMP) y monofosfato de uridina (UMP)) que se agregan continuamente al 3'. 39; grupo hidroxilo en el 3' extremo del ARNm en crecimiento.
Los estudios de transcripciones primarias producidas por la ARN polimerasa II revelan que una transcripción primaria promedio tiene una longitud de 7000 nucleótidos, y algunas crecen hasta 20 000 nucleótidos de longitud. La inclusión de secuencias de exones e intrones dentro de los transcritos primarios explica la diferencia de tamaño entre los transcritos primarios más grandes y los ARNm maduros más pequeños listos para la traducción en proteínas.
Reglamento
Varios factores contribuyen a la activación e inhibición de la transcripción y, por lo tanto, regulan la producción de transcripciones primarias a partir de una plantilla de ADN determinada.
Laactivación de la actividad de la ARN polimerasa para producir transcripciones primarias a menudo está controlada por secuencias de ADN llamadas potenciadores. Los factores de transcripción, proteínas que se unen a elementos del ADN para activar o reprimir la transcripción, se unen a potenciadores y reclutan enzimas que alteran los componentes del nucleosoma, lo que hace que el ADN sea más o menos accesible a la ARN polimerasa. Las combinaciones únicas de factores de transcripción activadores o inhibidores que se unen a regiones de ADN potenciadoras determinan si el gen con el que interactúa el potenciador se activa o no para la transcripción. La activación de la transcripción depende de si el complejo de elongación de la transcripción, que a su vez consta de una variedad de factores de transcripción, puede inducir a la ARN polimerasa a disociarse del complejo mediador que conecta una región potenciadora con el promotor.

inhibición de la actividad de la ARN polimerasa también puede regularse mediante secuencias de ADN llamadas silenciadores. Al igual que los potenciadores, los silenciadores pueden ubicarse en lugares más arriba o más abajo de los genes que regulan. Estas secuencias de ADN se unen a factores que contribuyen a la desestabilización del complejo de iniciación necesario para activar la ARN polimerasa y, por tanto, inhiben la transcripción.
La modificación de histonas por factores de transcripción es otro factor regulador clave para la transcripción por la ARN polimerasa. En general, los factores que conducen a la acetilación de histonas activan la transcripción, mientras que los factores que conducen a la desacetilación de histonas inhiben la transcripción. La acetilación de histonas induce repulsión entre componentes negativos dentro de los nucleosomas, permitiendo el acceso de la ARN polimerasa. La desacetilación de histonas estabiliza los nucleosomas fuertemente enrollados, inhibiendo el acceso de la ARN polimerasa. Además de los patrones de acetilación de las histonas, los patrones de metilación en las regiones promotoras del ADN pueden regular el acceso de la ARN polimerasa a una plantilla determinada. La ARN polimerasa a menudo es incapaz de sintetizar una transcripción primaria si la región promotora del gen objetivo contiene citosinas metiladas específicas (residuos que dificultan la unión de factores activadores de la transcripción y reclutan otras enzimas para estabilizar una estructura de nucleosoma estrechamente unida, excluyendo el acceso al ARN). polimerasa y previniendo la producción de transcripciones primarias.
Bucles R
Los bucles R se forman durante la transcripción. Un bucle R es una estructura de ácido nucleico de tres cadenas que contiene una región híbrida de ADN-ARN y un ADN monocatenario sin plantilla asociado. Las regiones de ADN transcritas activamente a menudo forman bucles R que son vulnerables al daño del ADN. Los intrones reducen la formación de bucles R y el daño al ADN en genes de levadura altamente expresados.
Tratamiento del ARN
La transcripción, una fase altamente regulada en la expresión genética, produce transcripciones primarias. Sin embargo, la transcripción es sólo el primer paso al que deben seguir muchas modificaciones que produzcan formas funcionales de ARN. Dicho de otra manera, los transcritos primarios recién sintetizados se modifican de varias maneras para convertirlos a sus formas funcionales maduras para producir diferentes proteínas y ARN, como ARNm, ARNt y ARNr.
Procesamiento
El proceso básico de modificación de la transcripción primaria es similar para el ARNt y el ARNr tanto en células eucariotas como procarióticas. Por otro lado, el procesamiento primario de la transcripción varía en los ARNm de células procarióticas y eucariotas. Por ejemplo, algunos ARNm de bacterias procarióticas sirven como plantillas para la síntesis de proteínas al mismo tiempo que se producen mediante transcripción. Alternativamente, el pre-ARNm de células eucariotas sufre una amplia gama de modificaciones antes de su transporte desde el núcleo al citoplasma donde se traducen sus formas maduras. Estas modificaciones son responsables de los diferentes tipos de mensajes codificados que conducen a la traducción de varios tipos de productos. Además, el procesamiento primario de la transcripción proporciona un control de la expresión génica, así como un mecanismo regulador de las tasas de degradación de los ARNm. El procesamiento de pre-ARNm en células eucariotas incluye 5' tapado, 3' poliadenilación y empalme alternativo.
5' capping
Poco después de que se inicia la transcripción en eucariotas, un pre-ARNm 5' El extremo se modifica mediante la adición de una cápsula de 7-metilguanosina, también conocida como cápsula de 5' gorra. El 5' La modificación de la limitación se inicia añadiendo un GTP al 5' nucleótido terminal del pre-ARNm en orientación inversa seguido de la adición de grupos metilo al residuo G. 5' La protección es esencial para la producción de ARNm funcionales desde el 5' cap es responsable de alinear el ARNm con el ribosoma durante la traducción.
Polyadenylation
En eucariotas, la poliadenilación modifica aún más los pre-ARNm durante los cuales se agrega una estructura llamada cola poli-A. Las señales de poliadenilación, que incluyen varios elementos de la secuencia de ARN, son detectadas por un grupo de proteínas que señalan la adición de la cola poli-A (aproximadamente 200 nucleótidos de longitud). La reacción de poliadenilación proporciona una señal para el final de la transcripción y esta reacción finaliza aproximadamente unos cientos de nucleótidos aguas abajo de la ubicación de la cola poli-A.
Empalme alternativo
Los pre-ARNm eucariotas tienen sus intrones separados por espliceosomas formados por pequeñas ribonucleoproteínas nucleares.
En células eucariotas complejas, un transcrito primario es capaz de preparar grandes cantidades de ARNm maduros debido al empalme alternativo. El empalme alternativo está regulado de modo que cada ARNm maduro pueda codificar una multiplicidad de proteínas.

El efecto de la germinación alternativa en la expresión génica se puede ver en los eucariotas complejos que tienen un número fijo de genes en su genoma pero producen un número mucho mayor de diferentes productos génicos. La mayoría de las transcripciones de premRNA eucariotas contienen múltiples intrones y exones. Las diversas combinaciones posibles de 5' y 3' piojos en un pre-mRNA pueden llevar a diferentes escisión y combinación de exones mientras que los intrones se eliminan del mRNA maduro. Así, se generan varios tipos de ARNM maduras. El espolvoreo alternativo tiene lugar en un gran complejo de proteínas llamado el espolvoroso. El aguijón alternativo es crucial para la regulación específica del tejido y el desarrollo en la expresión del gen. El aguijón alternativo puede verse afectado por diversos factores, incluyendo mutaciones como la translocación cromosómica.
En procariotas, el empalme se realiza mediante escisión autocatalítica o mediante escisión endolítica. Las escisiones autocatalíticas, en las que no intervienen proteínas, suelen reservarse para secciones que codifican ARNr, mientras que la escisión endolítica corresponde a precursores de ARNt.
Experimentos
Un estudio realizado por Cindy L. Wills y Bruce J. Dolnick del Departamento de Terapéutica Experimental del Roswell Park Comprehensive Cancer Center (entonces conocido como Roswell Park Memorial Institute) en Buffalo, Nueva York y del Programa de Biología Celular y Molecular. en la Universidad de Wisconsin en Madison, Wisconsin, se logró comprender los procesos celulares que involucran transcripciones primarias. Los investigadores querían comprender si el 5-fluorouracilo (FUra), un fármaco conocido por su uso en el tratamiento del cáncer, inhibe o desactiva el procesamiento del pre-ARNm de la dihidrofolato reductasa (DHFR) y/o la estabilidad del ARNm nuclear en células KB resistentes al metotrexato. La exposición prolongada a FUra no tuvo ningún efecto sobre el nivel de pre-ARNm de DHFR que contiene ciertos intrones, que son secciones de pre-ARNm que generalmente se eliminan de la secuencia como parte del procesamiento. Sin embargo, los niveles de ARNm de DHFR total disminuyeron dos veces en las células expuestas a FUra 1,0 μM. No hubo cambios significativos en la vida media, que se refiere al tiempo que tarda el 50% del ARNm en descomponerse, del ARNm o pre-ARNm total de DHFR observado en células expuestas a FUra. Y los experimentos de etiquetado de ARN nuclear/citoplasmático demostraron que la tasa de cambio del ARN de DHFR nuclear a ARNm de DHFR citoplasmático disminuyó en las células tratadas con FUra. Estos resultados proporcionan evidencia adicional de que FUra puede ayudar en el procesamiento de precursores de ARNm y/o afectar la estabilidad del ARNm de DHFR nuclear.
Judith Lengyel y Sheldon Penman, del departamento de Biología del Instituto Tecnológico de Massachusetts (MIT) en Cambridge, Massachusetts, escribieron un artículo sobre un tipo de transcripción primaria implicada en los genes de dos dípteros, o insectos que tienen dos alas: Drosophila y Aedes. El artículo describe cómo los investigadores observaron las transcripciones primarias de hnRNA, o básicamente pre-mRNA, en los dos tipos de insectos. El tamaño de las transcripciones de hnRNA y la fracción de hnRNA que se convierte en mRNA en líneas celulares, o grupos de células derivadas de una sola célula de lo que se esté estudiando, de Drosophila melanogaster y Aedes albopictus. fueron comparados. Ambos insectos son dípteros, pero Aedes tiene un genoma más grande que Drosophila. Esto significa que Aedes tiene más ADN, lo que significa más genes. La línea Aedes produce hnRNA más grande que la línea Drosophila, aunque las dos líneas celulares crecieron en condiciones similares y produjeron ARNm maduro o procesado del mismo tamaño y complejidad de secuencia. Estos datos sugieren que el tamaño del hnRNA aumenta al aumentar el tamaño del genoma, lo que obviamente lo demuestra Aedes.
Ivo Melcak, Stepanka Melcakova, Vojtech Kopsky, Jaromıra Vecerova e Ivan Raska del departamento de Biología Celular del Instituto de Medicina Experimental de la Academia de Ciencias de la República Checa en Praga estudiaron las influencias de las motas nucleares en el pre-ARNm.. Las motas nucleares (moteas) son parte de los núcleos de las células y están enriquecidas con factores de empalme conocidos por su participación en el procesamiento del ARNm. Se ha demostrado que las motas nucleares sirven a genes activos vecinos como lugares de almacenamiento de estos factores de empalme. En este estudio, los investigadores demostraron que, en las células HeLa que derivan de células de una persona que tenía cáncer de cuello uterino y que han demostrado ser útiles para los experimentos, el primer grupo de espliceosomas en el pre-ARNm proviene de estas motas. Los investigadores utilizaron microinyecciones de pre-ARNm de adenovirus mutantes y que aceptan espliceosomas con unión diferencial de factor de empalme para formar diferentes grupos y luego siguieron los sitios en los que estaban muy presentes. Los pre-ARNm que aceptan empalmesomas se dirigieron rápidamente a las motas, pero se descubrió que la orientación dependía de la temperatura. Las secuencias del tracto de polipirimidina en el ARNm promueven la construcción de grupos de espliceosoma y son necesarias para la orientación, pero, por sí solas, no fueron suficientes. Las secuencias flanqueantes aguas abajo fueron particularmente importantes para apuntar a los pre-ARNm mutantes en las motas. En experimentos de apoyo, el comportamiento de las motas se siguió después de la microinyección de desoxioligoribonucleótidos antisentido (secuencias de ADN o ARN complementarias a una secuencia específica) y, en este caso, secuencias específicas de ARNsn. Los snRNA también son conocidos por ayudar en el procesamiento del pre-ARNm. En estas condiciones, se formaron grupos de espliceosoma en pre-ARNm endógenos. Los investigadores concluyeron que los grupos de espliceosoma en el pre-ARNm microinyectado se forman dentro de las motas. La focalización del pre-ARNm y la acumulación en las motas es el resultado de la carga de factores de empalme en el pre-ARNm, y los grupos de espliceosoma dieron lugar al patrón moteado observado.
Enfermedades relacionadas
La investigación también ha llevado a un mayor conocimiento sobre ciertas enfermedades relacionadas con cambios en las transcripciones primarias. Un estudio involucró receptores de estrógeno y empalme diferencial. El artículo titulado "Empalme alternativo del transcrito primario alfa del receptor de estrógeno humano: mecanismos de omisión de exones" por Paola Ferro, Alessandra Forlani, Marco Muselli y Ulrich Pfeffer del laboratorio de Oncología Molecular del Instituto Nacional de Investigación del Cáncer en Génova, Italia, explica que 1785 nucleótidos de la región del ADN que codifica el receptor de estrógeno alfa (ER-alfa) se distribuyen en una región que contiene más de 300.000 nucleótidos en la transcripción primaria. El corte y empalme de este pre-ARNm conduce frecuentemente a variantes o tipos diferentes de ARNm que carecen de uno o más exones o regiones necesarios para codificar proteínas. Estas variantes se han asociado con la progresión del cáncer de mama. En el ciclo de vida de los retrovirus, el ADN proviral se incorpora en la transcripción del ADN de la célula que se está infectando. Dado que los retrovirus necesitan cambiar su pre-ARNm en ADN para que este ADN pueda integrarse en el ADN del huésped al que afecta, la formación de esa plantilla de ADN es un paso vital para la replicación de los retrovirus. El tipo de célula, la diferenciación o el cambio de estado de la célula y el estado fisiológico de la célula dan como resultado un cambio significativo en la disponibilidad y actividad de ciertos factores necesarios para la transcripción. Estas variables crean una amplia gama de expresión de genes virales. Por ejemplo, las células de cultivo de tejidos que producen activamente viriones infecciosos de los virus de la leucemia aviar o murina (ASLV o MLV) contienen niveles tan altos de ARN viral que entre 5 y 10% del ARNm de una célula puede ser de origen viral. Esto muestra que los transcritos primarios producidos por estos retrovirus no siempre siguen el camino normal hacia la producción de proteínas y se convierten nuevamente en ADN para multiplicarse y expandirse.
Contenido relacionado
Ley de Fick
Híbrido (biología)
Evolución divergente