Sólido

El estado Sólido es uno de los cuatro estados fundamentales de la materia (los otros son líquido, gas y plasma). Las moléculas de un sólido están muy juntas y contienen la menor cantidad de energía cinética. Un sólido se caracteriza por la rigidez estructural y la resistencia a una fuerza aplicada a la superficie. A diferencia de un líquido, un objeto sólido no fluye para tomar la forma de su recipiente, ni se expande para llenar todo el volumen disponible como un gas. Los átomos en un sólido están unidos entre sí, ya sea en una red geométrica regular (sólidos cristalinos, que incluyen metales y hielo ordinario) o irregularmente (un sólido amorfo como el vidrio de una ventana común). Los sólidos no se pueden comprimir con poca presión, mientras que los gases se pueden comprimir con poca presión porque las moléculas de un gas están flojas.
La rama de la física que se ocupa de los sólidos se denomina física del estado sólido y es la rama principal de la física de la materia condensada (que también incluye los líquidos). La ciencia de los materiales se ocupa principalmente de las propiedades físicas y químicas de los sólidos. La química del estado sólido se ocupa especialmente de la síntesis de nuevos materiales, así como de la ciencia de la identificación y la composición química.
Descripción microscópica
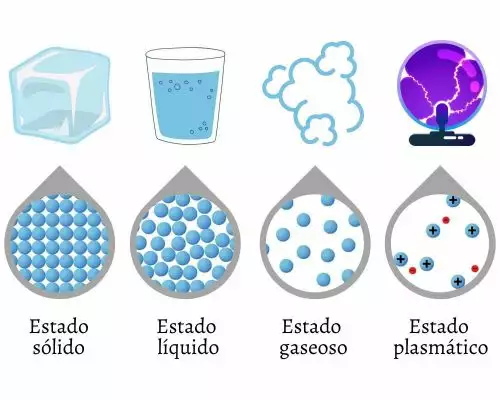
Los átomos, moléculas o iones que componen los sólidos pueden estar dispuestos en un patrón repetitivo ordenado o irregular. Los materiales cuyos componentes están dispuestos en un patrón regular se conocen como cristales. En algunos casos, el pedido regular puede continuar sin interrupciones a gran escala, por ejemplo, diamantes, donde cada diamante es un solo cristal. Los objetos sólidos que son lo suficientemente grandes para verlos y manipularlos rara vez están compuestos de un solo cristal, sino que están hechos de una gran cantidad de cristales simples, conocidos como cristalitos, cuyo tamaño puede variar desde unos pocos nanómetros hasta varios metros. Tales materiales se llaman policristalinos. Casi todos los metales comunes y muchas cerámicas son policristalinos.
En otros materiales, no existe un orden de largo alcance en la posición de los átomos. Estos sólidos se conocen como sólidos amorfos; los ejemplos incluyen poliestireno y vidrio.
Que un sólido sea cristalino o amorfo depende del material involucrado y de las condiciones en las que se formó. Los sólidos que se forman por enfriamiento lento tenderán a ser cristalinos, mientras que los sólidos que se congelan rápidamente tienen más probabilidades de ser amorfos. Asimismo, la estructura cristalina específica que adopta un sólido cristalino depende del material involucrado y de cómo se formó.
Si bien muchos objetos comunes, como un cubito de hielo o una moneda, son químicamente idénticos, muchos otros materiales comunes comprenden varias sustancias diferentes empaquetadas. Por ejemplo, una roca típica es un agregado de varios minerales y mineraloides diferentes, sin una composición química específica. La madera es un material orgánico natural que consiste principalmente en fibras de celulosa incrustadas en una matriz de lignina orgánica. En la ciencia de los materiales, se pueden diseñar compuestos de más de un material constituyente para que tengan las propiedades deseadas.
Clases de sólidos

Las fuerzas entre los átomos en un sólido pueden tomar una variedad de formas. Por ejemplo, un cristal de cloruro de sodio (sal común) se compone de sodio iónico y cloro, que se mantienen unidos por enlaces iónicos. En el diamante o el silicio, los átomos comparten electrones y forman enlaces covalentes. En los metales, los electrones se comparten en enlaces metálicos. Algunos sólidos, en particular la mayoría de los compuestos orgánicos, se mantienen unidos por fuerzas de van der Waals resultantes de la polarización de la nube de carga electrónica en cada molécula. Las diferencias entre los tipos de sólidos resultan de las diferencias entre sus enlaces.
Metales
Los metales suelen ser fuertes, densos y buenos conductores tanto de la electricidad como del calor. La mayor parte de los elementos de la tabla periódica, los que se encuentran a la izquierda de una línea diagonal trazada desde el boro hasta el polonio, son metales. Las mezclas de dos o más elementos en las que el componente principal es un metal se conocen como aleaciones.
La gente ha estado usando metales para una variedad de propósitos desde tiempos prehistóricos. La resistencia y fiabilidad de los metales ha llevado a su uso generalizado en la construcción de edificios y otras estructuras, así como en la mayoría de los vehículos, muchos electrodomésticos y herramientas, tuberías, señales de tráfico y vías férreas. El hierro y el aluminio son los dos metales estructurales más utilizados. También son los metales más abundantes en la corteza terrestre. El hierro se usa más comúnmente en forma de una aleación, el acero, que contiene hasta un 2,1 % de carbono, lo que lo hace mucho más duro que el hierro puro.
Debido a que los metales son buenos conductores de la electricidad, son valiosos en aparatos eléctricos y para transportar una corriente eléctrica a largas distancias con poca pérdida o disipación de energía. Por lo tanto, las redes de energía eléctrica se basan en cables de metal para distribuir la electricidad. Los sistemas eléctricos domésticos, por ejemplo, están cableados con cobre por sus buenas propiedades conductoras y su fácil maquinabilidad. La alta conductividad térmica de la mayoría de los metales también los hace útiles para utensilios de cocina.
El estudio de los elementos metálicos y sus aleaciones constituye una parte importante de los campos de la química del estado sólido, la física, la ciencia de los materiales y la ingeniería.
Los sólidos metálicos se mantienen unidos por una alta densidad de electrones deslocalizados compartidos, conocidos como "enlaces metálicos". En un metal, los átomos pierden fácilmente sus electrones más externos ("valencia"), formando iones positivos. Los electrones libres se distribuyen por todo el sólido, que se mantiene unido firmemente por las interacciones electrostáticas entre los iones y la nube de electrones. La gran cantidad de electrones libres da a los metales sus altos valores de conductividad eléctrica y térmica. Los electrones libres también evitan la transmisión de la luz visible, lo que hace que los metales se vuelvan opacos, brillantes y lustrosos.
Los modelos más avanzados de las propiedades de los metales consideran el efecto de los núcleos de iones positivos en los electrones deslocalizados. Como la mayoría de los metales tienen una estructura cristalina, esos iones generalmente se organizan en una red periódica. Matemáticamente, el potencial de los núcleos de iones puede tratarse mediante varios modelos, siendo el más simple el modelo de electrones casi libres.
Minerales
Los minerales son sólidos naturales formados a través de varios procesos geológicos bajo altas presiones. Para ser clasificado como un verdadero mineral, una sustancia debe tener una estructura cristalina con propiedades físicas uniformes en todas partes. Los minerales varían en composición desde elementos puros y sales simples hasta silicatos muy complejos con miles de formas conocidas. En contraste, una muestra de roca es un agregado aleatorio de minerales y/o mineraloides, y no tiene una composición química específica. La gran mayoría de las rocas de la corteza terrestre consisten en cuarzo (SiO 2 cristalino), feldespato, mica, clorita, caolín, calcita, epidota, olivino, augita, hornblenda, magnetita, hematita, limonita y algunos otros minerales. Algunos minerales, como el cuarzo, la mica o el feldespato, son comunes, mientras que otros solo se han encontrado en algunos lugares del mundo. El grupo más grande de minerales, con mucho, es el de los silicatos (la mayoría de las rocas son ≥95 % de silicatos), que se componen principalmente de silicio y oxígeno, con la adición de iones de aluminio, magnesio, hierro, calcio y otros metales.
Cerámica
Los sólidos cerámicos están compuestos por compuestos inorgánicos, generalmente óxidos de elementos químicos. Son químicamente inertes y, a menudo, son capaces de resistir la erosión química que se produce en un entorno ácido o cáustico. La cerámica generalmente puede soportar altas temperaturas que van desde 1000 a 1600 °C (1800 a 3000 °F). Las excepciones incluyen materiales inorgánicos sin óxido, como nitruros, boruros y carburos.
Las materias primas cerámicas tradicionales incluyen minerales de arcilla como la caolinita, los materiales más recientes incluyen óxido de aluminio (alúmina). Los materiales cerámicos modernos, que se clasifican como cerámicas avanzadas, incluyen el carburo de silicio y el carburo de tungsteno. Ambos son valorados por su resistencia a la abrasión y, por lo tanto, encuentran uso en aplicaciones tales como las placas de desgaste de los equipos de trituración en las operaciones mineras.
La mayoría de los materiales cerámicos, como la alúmina y sus compuestos, se forman a partir de polvos finos, lo que produce una microestructura policristalina de grano fino que está llena de centros de dispersión de luz comparables a la longitud de onda de la luz visible. Por lo tanto, generalmente son materiales opacos, a diferencia de los materiales transparentes. Sin embargo, la tecnología reciente a nanoescala (por ejemplo, sol-gel) ha hecho posible la producción de cerámicas transparentes policristalinas, como alúmina transparente y compuestos de alúmina para aplicaciones como láseres de alta potencia. La cerámica avanzada también se utiliza en las industrias médica, eléctrica y electrónica.
La ingeniería cerámica es la ciencia y la tecnología de la creación de materiales, piezas y dispositivos cerámicos de estado sólido. Esto se hace por la acción del calor o, a temperaturas más bajas, usando reacciones de precipitación de soluciones químicas. El término incluye la purificación de materias primas, el estudio y producción de los compuestos químicos en cuestión, su formación en componentes y el estudio de su estructura, composición y propiedades.
Mecánicamente hablando, los materiales cerámicos son frágiles, duros, fuertes a la compresión y débiles al cizallamiento y la tensión. Los materiales quebradizos pueden exhibir una resistencia a la tracción significativa al soportar una carga estática. La tenacidad indica cuánta energía puede absorber un material antes de la falla mecánica, mientras que la tenacidad a la fractura (indicada como K Ic ) describe la capacidad de un material con fallas microestructurales inherentes para resistir la fractura a través del crecimiento y la propagación de grietas. Si un material tiene un gran valor de tenacidad a la fractura, los principios básicos de la mecánica de la fractura sugieren que lo más probable es que sufra una fractura dúctil. La fractura por fragilidad es muy característica de la mayoría de los materiales cerámicos y de vitrocerámica que normalmente exhiben valores bajos (e inconsistentes) de K Ic .
Como ejemplo de las aplicaciones de la cerámica, la dureza extrema de la zirconia se utiliza en la fabricación de hojas de cuchillos, así como en otras herramientas de corte industriales. Las cerámicas como la alúmina, el carburo de boro y el carburo de silicio se han utilizado en chalecos antibalas para repeler el fuego de rifles de gran calibre. Las piezas de nitruro de silicio se utilizan en rodamientos de bolas de cerámica, donde su alta dureza los hace resistentes al desgaste. En general, las cerámicas también son químicamente resistentes y se pueden usar en ambientes húmedos donde los cojinetes de acero serían susceptibles a la oxidación (u herrumbre).
Como otro ejemplo de aplicaciones cerámicas, a principios de la década de 1980, Toyota investigó la producción de un motor cerámico adiabático con una temperatura de funcionamiento de más de 6000 °F (3300 °C). Los motores cerámicos no requieren un sistema de refrigeración y, por lo tanto, permiten una importante reducción de peso y, por lo tanto, una mayor eficiencia de combustible. En un motor metálico convencional, gran parte de la energía liberada del combustible debe disiparse como calor residual para evitar la fusión de las partes metálicas. También se trabaja en el desarrollo de piezas cerámicas para motores de turbinas de gas. Los motores de turbina hechos con cerámica podrían operar de manera más eficiente, dando a los aviones un mayor alcance y carga útil para una cantidad determinada de combustible. Sin embargo, tales motores no están en producción porque la fabricación de piezas cerámicas con la suficiente precisión y durabilidad es difícil y costosa.
Vitrocerámica
Los materiales vitrocerámicos comparten muchas propiedades tanto con los vidrios no cristalinos como con las cerámicas cristalinas. Se forman como un vidrio y luego se cristalizan parcialmente mediante tratamiento térmico, produciendo fases tanto amorfas como cristalinas, de modo que los granos cristalinos se incrustan dentro de una fase intergranular no cristalina.
La vitrocerámica se utiliza para fabricar utensilios de cocina (originalmente conocidos por la marca CorningWare) y estufas que tienen una alta resistencia al choque térmico y una permeabilidad extremadamente baja a los líquidos. El coeficiente negativo de expansión térmica de la fase cerámica cristalina se puede equilibrar con el coeficiente positivo de la fase vítrea. En cierto punto (~70% cristalino) la vitrocerámica tiene un coeficiente neto de expansión térmica cercano a cero. Este tipo de vitrocerámica presenta excelentes propiedades mecánicas y puede soportar cambios de temperatura repetidos y rápidos de hasta 1000 °C.
La cerámica de vidrio también puede ocurrir naturalmente cuando un rayo cae sobre los granos cristalinos (por ejemplo, cuarzo) que se encuentran en la arena de la playa. En este caso, el calor extremo e inmediato del rayo (~2500 °C) crea estructuras ramificadas huecas parecidas a raíces llamadas fulgurita a través de la fusión.
Sólidos orgánicos
La química orgánica estudia la estructura, las propiedades, la composición, las reacciones y la preparación por síntesis (u otros medios) de compuestos químicos de carbono e hidrógeno, que pueden contener otros elementos como el nitrógeno, el oxígeno y los halógenos: flúor, cloro, bromo y yodo. Algunos compuestos orgánicos también pueden contener los elementos fósforo o azufre. Los ejemplos de sólidos orgánicos incluyen madera, cera de parafina, naftaleno y una amplia variedad de polímeros y plásticos.
Madera
La madera es un material orgánico natural que consiste principalmente en fibras de celulosa incrustadas en una matriz de lignina. En cuanto a las propiedades mecánicas, las fibras son fuertes en tensión y la matriz de lignina resiste la compresión. Por lo tanto, la madera ha sido un material de construcción importante desde que los humanos comenzaron a construir refugios y usar botes. La madera que se utilizará para trabajos de construcción se conoce comúnmente como madera aserrada o madera . En la construcción, la madera no solo es un material estructural, sino que también se utiliza para formar el molde del hormigón.
Los materiales a base de madera también se utilizan ampliamente para embalaje (por ejemplo, cartón) y papel, ambos creados a partir de la pulpa refinada. Los procesos de fabricación de pulpa química utilizan una combinación de productos químicos alcalinos (kraft) o ácidos (sulfitos) a alta temperatura para romper los enlaces químicos de la lignina antes de quemarla.
Polímeros
Una propiedad importante del carbono en la química orgánica es que puede formar ciertos compuestos, cuyas moléculas individuales son capaces de unirse entre sí, formando así una cadena o una red. El proceso se denomina polimerización y las cadenas o redes de polímeros, mientras que el compuesto fuente es un monómero. Existen dos grupos principales de polímeros: los fabricados artificialmente se conocen como polímeros industriales o polímeros sintéticos (plásticos) y los que se producen de forma natural como biopolímeros.
Los monómeros pueden tener varios sustituyentes químicos, o grupos funcionales, que pueden afectar las propiedades químicas de los compuestos orgánicos, como la solubilidad y la reactividad química, así como las propiedades físicas, como la dureza, la densidad, la resistencia mecánica o a la tracción, la resistencia a la abrasión, el calor. resistencia, transparencia, color, etc. En las proteínas, estas diferencias dan al polímero la capacidad de adoptar una conformación biológicamente activa con preferencia a otras (ver autoensamblaje).
La gente ha estado usando polímeros orgánicos naturales durante siglos en forma de ceras y goma laca, que se clasifica como un polímero termoplástico. Un polímero vegetal llamado celulosa proporcionaba la resistencia a la tracción de las fibras y cuerdas naturales, y a principios del siglo XIX el caucho natural era de uso generalizado. Los polímeros son las materias primas (las resinas) que se utilizan para fabricar lo que comúnmente se denominan plásticos. Los plásticos son el producto final, creado después de que uno o más polímeros o aditivos se hayan agregado a una resina durante el procesamiento, que luego se moldea en una forma final. Los polímeros que han existido y que actualmente tienen un uso generalizado incluyen polietileno a base de carbono, polipropileno, cloruro de polivinilo, poliestireno, nailon, poliésteres, acrílicos, poliuretano y policarbonatos, y siliconas a base de silicio. Los plásticos se clasifican generalmente como "
Materiales compuestos
Los materiales compuestos contienen dos o más fases macroscópicas, una de las cuales suele ser cerámica. Por ejemplo, una matriz continua y una fase dispersa de partículas o fibras cerámicas.
Las aplicaciones de los materiales compuestos van desde elementos estructurales como el hormigón reforzado con acero hasta las baldosas térmicamente aislantes que desempeñan un papel clave e integral en el sistema de protección térmica del transbordador espacial de la NASA, que se utiliza para proteger la superficie del transbordador del calor de la re -entrada en la atmosfera terrestre. Un ejemplo es el Carbono-Carbono Reforzado (RCC), el material gris claro que resiste temperaturas de reingreso de hasta 1510 °C (2750 °F) y protege la tapa de la nariz y los bordes de ataque de las alas del transbordador espacial. RCC es un material compuesto laminado hecho de tela de rayón de grafito e impregnado con una resina fenólica. Tras el curado a alta temperatura en autoclave, el laminado se piroliza para convertir la resina en carbón, se impregna con alcohol furfural en cámara de vacío, y curado/pirolizado para convertir el alcohol furfural en carbono. Para proporcionar resistencia a la oxidación para la capacidad de reutilización, las capas exteriores del RCC se convierten en carburo de silicio.
Se pueden ver ejemplos domésticos de materiales compuestos en las carcasas "plásticas" de televisores, teléfonos móviles, etc. Estas cubiertas de plástico suelen ser un material compuesto formado por una matriz termoplástica como el acrilonitrilo butadieno estireno (ABS) en el que se ha agregado tiza de carbonato de calcio, talco, fibras de vidrio o fibras de carbono para aumentar la resistencia, el volumen o la dispersión electrostática. Estas adiciones pueden denominarse fibras de refuerzo o dispersantes, según su propósito.
Así, el material de la matriz rodea y soporta los materiales de refuerzo manteniendo sus posiciones relativas. Los refuerzos imparten sus propiedades mecánicas y físicas especiales para mejorar las propiedades de la matriz. Un sinergismo produce propiedades materiales que no están disponibles a partir de los materiales constituyentes individuales, mientras que la amplia variedad de materiales de matriz y de refuerzo brinda al diseñador la opción de una combinación óptima.
Semiconductores
Los semiconductores son materiales que tienen una resistividad (y conductividad) eléctrica entre la de los conductores metálicos y la de los aislantes no metálicos. Se pueden encontrar en la tabla periódica moviéndose en diagonal hacia abajo a la derecha del boro. Separan los conductores eléctricos (o metales, a la izquierda) de los aislantes (a la derecha).
Los dispositivos fabricados con materiales semiconductores son la base de la electrónica moderna, incluidas las radios, las computadoras, los teléfonos, etc. Los dispositivos semiconductores incluyen el transistor, las células solares, los diodos y los circuitos integrados. Los paneles solares fotovoltaicos son grandes dispositivos semiconductores que convierten directamente la luz en energía eléctrica.
En un conductor metálico, la corriente es transportada por el flujo de electrones", pero en los semiconductores, la corriente puede ser transportada por electrones o por los "agujeros" cargados positivamente en la estructura de la banda electrónica del material. Los materiales semiconductores comunes incluyen silicio, germanio y arseniuro de galio.
Nanomateriales
Muchos sólidos tradicionales exhiben diferentes propiedades cuando se encogen a tamaños nanométricos. Por ejemplo, las nanopartículas generalmente de oro amarillo y silicio gris son de color rojo; las nanopartículas de oro se derriten a temperaturas mucho más bajas (~300 °C para un tamaño de 2,5 nm) que las placas de oro (1064 °C); y los nanocables metálicos son mucho más fuertes que los metales a granel correspondientes.La alta área superficial de las nanopartículas las hace extremadamente atractivas para ciertas aplicaciones en el campo de la energía. Por ejemplo, los metales de platino pueden proporcionar mejoras como catalizadores de combustible para automóviles, así como celdas de combustible de membrana de intercambio de protones (PEM). Además, los óxidos cerámicos (o cermets) de lantano, cerio, manganeso y níquel ahora se están desarrollando como celdas de combustible de óxido sólido (SOFC). Se están aplicando nanopartículas de litio, titanato de litio y tantalio en baterías de iones de litio. Se ha demostrado que las nanopartículas de silicio amplían drásticamente la capacidad de almacenamiento de las baterías de iones de litio durante el ciclo de expansión/contracción. Los nanocables de silicio ciclan sin una degradación significativa y presentan el potencial para su uso en baterías con tiempos de almacenamiento muy ampliados. Las nanopartículas de silicio también se están utilizando en nuevas formas de células de energía solar. La deposición de una película delgada de puntos cuánticos de silicio en el sustrato de silicio policristalino de una celda fotovoltaica (solar) aumenta la salida de voltaje hasta en un 60 % mediante la fluorescencia de la luz entrante antes de la captura. Una vez más, el área de superficie de las nanopartículas (y películas delgadas) juega un papel fundamental en la maximización de la cantidad de radiación absorbida.
Biomateriales
Muchos materiales naturales (o biológicos) son compuestos complejos con propiedades mecánicas notables. Estas estructuras complejas, que han surgido a partir de cientos de millones de años de evolución, están inspirando a los científicos de materiales en el diseño de nuevos materiales. Sus características definitorias incluyen jerarquía estructural, multifuncionalidad y capacidad de autorreparación. La autoorganización es también una característica fundamental de muchos materiales biológicos y la forma en que se ensamblan las estructuras desde el nivel molecular hacia arriba. Así, el autoensamblaje se perfila como una nueva estrategia en la síntesis química de biomateriales de alto rendimiento.
Propiedades físicas
Las propiedades físicas de los elementos y compuestos que brindan evidencia concluyente de la composición química incluyen olor, color, volumen, densidad (masa por unidad de volumen), punto de fusión, punto de ebullición, capacidad calorífica, forma física y forma a temperatura ambiente (sólido, líquido o gas). ; cristales cúbicos, trigonales, etc.), dureza, porosidad, índice de refracción y muchos otros. En esta sección se analizan algunas propiedades físicas de los materiales en estado sólido.
Mecánico
Las propiedades mecánicas de los materiales describen características tales como su resistencia y resistencia a la deformación. Por ejemplo, las vigas de acero se utilizan en la construcción debido a su alta resistencia, lo que significa que no se rompen ni se doblan significativamente bajo la carga aplicada.
Las propiedades mecánicas incluyen elasticidad y plasticidad, resistencia a la tracción, resistencia a la compresión, resistencia al corte, tenacidad a la fractura, ductilidad (bajo contenido de materiales quebradizos) y dureza de indentación. La mecánica de sólidos es el estudio del comportamiento de la materia sólida bajo acciones externas como fuerzas externas y cambios de temperatura.
Un sólido no exhibe flujo macroscópico, como lo hacen los fluidos. Cualquier grado de desviación de su forma original se denomina deformación. La proporción de deformación con respecto al tamaño original se denomina deformación. Si la tensión aplicada es suficientemente baja, casi todos los materiales sólidos se comportan de tal forma que la deformación es directamente proporcional a la tensión (ley de Hooke). El coeficiente de la proporción se denomina módulo de elasticidad o módulo de Young. Esta región de deformación se conoce como región linealmente elástica. Tres modelos pueden describir cómo responde un sólido a una tensión aplicada:
- Elasticidad: cuando se elimina una tensión aplicada, el material vuelve a su estado sin deformar.
- Viscoelasticidad: estos son materiales que se comportan elásticamente, pero también tienen amortiguación. Cuando se elimina la tensión aplicada, se debe realizar trabajo contra los efectos de amortiguación y se convierte en calor dentro del material. Esto da como resultado un bucle de histéresis en la curva de tensión-deformación. Esto implica que la respuesta mecánica tiene una dependencia del tiempo.
- Plasticidad: los materiales que se comportan elásticamente generalmente lo hacen cuando la tensión aplicada es menor que un valor de rendimiento. Cuando la tensión es mayor que la tensión de fluencia, el material se comporta plásticamente y no vuelve a su estado anterior. Es decir, se produce una deformación plástica irreversible (o flujo viscoso) después de la fluencia que es permanente.
Muchos materiales se vuelven más débiles a altas temperaturas. Los materiales que conservan su resistencia a altas temperaturas, llamados materiales refractarios, son útiles para muchos propósitos. Por ejemplo, las vitrocerámicas se han vuelto extremadamente útiles para cocinar en la encimera, ya que exhiben excelentes propiedades mecánicas y pueden soportar cambios de temperatura repetidos y rápidos de hasta 1000 °C. En la industria aeroespacial, los materiales de alto rendimiento utilizados en el diseño de exteriores de aeronaves y/o naves espaciales deben tener una alta resistencia al choque térmico. Por lo tanto, las fibras sintéticas hiladas a partir de polímeros orgánicos y los materiales compuestos de polímero/cerámica/metal y los polímeros reforzados con fibras ahora se están diseñando con este propósito en mente.
Térmico
Debido a que los sólidos tienen energía térmica, sus átomos vibran alrededor de posiciones medias fijas dentro de la red ordenada (o desordenada). El espectro de vibraciones de la red en una red cristalina o vítrea proporciona la base para la teoría cinética de los sólidos. Este movimiento ocurre a nivel atómico y, por lo tanto, no puede observarse ni detectarse sin un equipo altamente especializado, como el que se usa en espectroscopia.
Las propiedades térmicas de los sólidos incluyen la conductividad térmica, que es la propiedad de un material que indica su capacidad para conducir el calor. Los sólidos también tienen una capacidad calorífica específica, que es la capacidad de un material para almacenar energía en forma de calor (o vibraciones de red térmica).
Eléctrico
Las propiedades eléctricas incluyen conductividad, resistencia, impedancia y capacitancia. Los conductores eléctricos como los metales y las aleaciones se contrastan con los aislantes eléctricos como los vidrios y las cerámicas. Los semiconductores se comportan en algún punto intermedio. Mientras que la conductividad en los metales es causada por electrones, tanto los electrones como los huecos contribuyen a la corriente en los semiconductores. Alternativamente, los iones soportan la corriente eléctrica en los conductores iónicos.
Muchos materiales también exhiben superconductividad a bajas temperaturas; incluyen elementos metálicos como el estaño y el aluminio, varias aleaciones metálicas, algunos semiconductores fuertemente dopados y ciertas cerámicas. La resistividad eléctrica de la mayoría de los conductores eléctricos (metálicos) generalmente disminuye gradualmente a medida que baja la temperatura, pero sigue siendo finita. En un superconductor, sin embargo, la resistencia cae abruptamente a cero cuando el material se enfría por debajo de su temperatura crítica. Una corriente eléctrica que fluye en un bucle de cable superconductor puede persistir indefinidamente sin fuente de energía.
Un dieléctrico, o aislante eléctrico, es una sustancia que es altamente resistente al flujo de corriente eléctrica. Un dieléctrico, como el plástico, tiende a concentrar un campo eléctrico aplicado dentro de sí mismo, cuya propiedad se utiliza en los condensadores. Un condensador es un dispositivo eléctrico que puede almacenar energía en el campo eléctrico entre un par de conductores estrechamente espaciados (llamados "placas"). Cuando se aplica voltaje al capacitor, se acumulan cargas eléctricas de igual magnitud, pero de polaridad opuesta, en cada placa. Los condensadores se utilizan en circuitos eléctricos como dispositivos de almacenamiento de energía, así como en filtros electrónicos para diferenciar entre señales de alta y baja frecuencia.
Electromecánica
La piezoelectricidad es la capacidad de los cristales para generar un voltaje en respuesta a una tensión mecánica aplicada. El efecto piezoeléctrico es reversible porque los cristales piezoeléctricos, cuando se someten a un voltaje aplicado externamente, pueden cambiar de forma en una pequeña cantidad. Los materiales poliméricos como el caucho, la lana, el cabello, la fibra de madera y la seda a menudo se comportan como electretos. Por ejemplo, el polímero fluoruro de polivinilideno (PVDF) exhibe una respuesta piezoeléctrica varias veces mayor que el cuarzo piezoeléctrico tradicional (SiO 2 cristalino ). La deformación (~0,1 %) se presta a aplicaciones técnicas útiles como fuentes de alto voltaje, altavoces, láseres, así como sensores y/o transductores químicos, biológicos y acústico-ópticos.
Óptico
Los materiales pueden transmitir (por ejemplo, el vidrio) o reflejar (por ejemplo, los metales) la luz visible.
Los materiales generalmente se dividen en tres categorías: transparentes, translúcidos u opacos.
Materiales transparentes Permiten que los rayos de luz los atraviesen por completo. Ejemplos: agua pura, vidrio limpio. Los materiales translúcidos permiten que los rayos de luz los atraviesen parcialmente. Ejemplos: agua impura, aceite, ventana contaminada. Los materiales opacos no dejan pasar la luz a través de ellos. Ejemplos: madera, hierro, plástico.
Muchos materiales transmitirán algunas longitudes de onda mientras bloquean otras. Por ejemplo, el vidrio de una ventana es transparente a la luz visible, pero mucho menos a la mayoría de las frecuencias de luz ultravioleta que causan quemaduras solares. Esta propiedad se utiliza para filtros ópticos selectivos de frecuencia, que pueden alterar el color de la luz incidente.
Para algunos propósitos, las propiedades ópticas y mecánicas de un material pueden ser de interés. Por ejemplo, los sensores de un misil guiado por infrarrojos ("buscador de calor") deben estar protegidos por una cubierta que sea transparente a la radiación infrarroja. El material de elección actual para las cúpulas de misiles guiados por infrarrojos de alta velocidad es el zafiro monocristalino. La transmisión óptica del zafiro en realidad no se extiende para cubrir todo el rango del infrarrojo medio (3–5 µm), pero comienza a disminuir en longitudes de onda superiores a aproximadamente 4,5 µm a temperatura ambiente. Si bien la resistencia del zafiro es mejor que la de otros materiales de domo infrarrojo de rango medio disponibles a temperatura ambiente, se debilita por encima de los 600 °C. Existe una compensación de larga data entre el paso de banda óptico y la durabilidad mecánica;
La transmisión de ondas de luz guiada involucra el campo de la fibra óptica y la capacidad de ciertos lentes para transmitir, simultáneamente y con baja pérdida de intensidad, un rango de frecuencias (guías de ondas ópticas multimodo) con poca interferencia entre ellas. Las guías de ondas ópticas se utilizan como componentes en circuitos ópticos integrados o como medio de transmisión en sistemas de comunicación óptica.
Optoelectrónico
Una celda solar o celda fotovoltaica es un dispositivo que convierte la energía luminosa en energía eléctrica. Básicamente, el dispositivo debe cumplir solo dos funciones: fotogeneración de portadores de carga (electrones y huecos) en un material absorbente de luz, y separación de los portadores de carga en un contacto conductor que transmitirá la electricidad (en pocas palabras, portador de electrones). apagado a través de un contacto de metal en un circuito externo). Esta conversión se denomina efecto fotoeléctrico, y el campo de investigación relacionado con las células solares se conoce como fotovoltaica.
Las células solares tienen muchas aplicaciones. Se han utilizado durante mucho tiempo en situaciones en las que la energía eléctrica de la red no está disponible, como en sistemas de energía de áreas remotas, satélites en órbita terrestre y sondas espaciales, calculadoras portátiles, relojes de pulsera, radioteléfonos remotos y aplicaciones de bombeo de agua. Más recientemente, se empiezan a utilizar en montajes de módulos solares (matrices fotovoltaicas) conectados a la red eléctrica a través de un inversor, que no actúa como único suministro sino como fuente adicional de electricidad.
Todas las celdas solares requieren un material absorbente de luz contenido dentro de la estructura de la celda para absorber fotones y generar electrones a través del efecto fotovoltaico. Los materiales utilizados en las celdas solares suelen tener la propiedad de absorber preferentemente las longitudes de onda de la luz solar que llegan a la superficie terrestre. Algunas células solares también están optimizadas para la absorción de luz más allá de la atmósfera terrestre.
Contenido relacionado
Julio (unidad)
Ley de Fick
Pascal (unidad)
Newton (unidad)
Trabajo (física)