Siliciuro
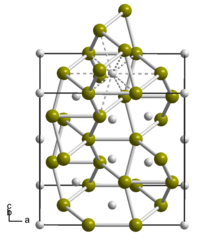
Un siliciuro es un tipo de compuesto químico que combina silicio y un elemento normalmente más electropositivo.
El silicio es más electropositivo que el carbono. En términos de sus propiedades físicas, los siliciuros están estructuralmente más cerca de los boruros que de los carburos. Sin embargo, debido a las diferencias de tamaño, los siliciuros no son isoestructurales con los boruros y los carburos.
Los enlaces en los siliciuros varían desde estructuras conductoras similares a metales hasta covalentes o iónicos. Se han descrito siliciuros de todos los metales que no son de transición, excepto el berilio. Los siliciuros se utilizan en interconexiones.
Estructura
Los átomos de silicio en los siliciuros pueden tener muchas organizaciones posibles:
- átomos de silicio aislados: eléctricamente conductivo (o semiconductor) CrSi, MnSi, FeSi, CoSi, Cu5Si, (V,Cr,Mn)3Si, Fe3Si, Mn3Si, Mg2(Si,Ge,Sn,Pb), (Ca,Ru,Ce,Rh,Ir,Ni)2Si
- Si2 pares: U3Si2, silcidas de hafnio y torio
- Si4 tetrahedra: KSi, RbSi, CsSi
- Sin cadenas: USi, (Ti, Zr, Hf, Th, Ce, Pu)Si, CaSi, SrSi, YSi
- Planar hexagonal graphite-like Si capas: β-USi2, silcidas de otros lanthanoids y actinoides
- Hexagonal corrugado Si capas: CaSi2
- Abierto tridimensional Si esqueletos: SrSi2, ThSi2, α-USi2
Preparación y reactividad
La mayoría de los siliciuros se producen por combinación directa de los elementos.
Un siliciuro preparado mediante un proceso de autoalineación se llama salicida. Este es un proceso en el que los contactos de siliciuro se forman sólo en aquellas áreas en las que el metal depositado (que después del recocido se convierte en un componente metálico del siliciuro) está en contacto directo con el silicio, por lo tanto, el proceso es autoalineado. Se implementa comúnmente en procesos MOS/CMOS para contactos óhmicos de la fuente, el drenaje y la compuerta poli-Si.
Metales alcalinos y alcalinotérreos
Siliciuros de los grupos 1 y 2, p. Na2Si y Ca2Si reaccionan con agua, produciendo hidrógeno y/o silanos.
El siliciuro de magnesio reacciona con el ácido clorhídrico para dar silano:
- Mg2Si + 4 HCl → SiH4 + 2 MgCl2
Los siliciuros del grupo 1 son aún más reactivos. Por ejemplo, el siliciuro de sodio, Na2Si, reacciona rápidamente con agua para producir silicato de sodio, Na2SiO3 y gas hidrógeno. El siliciuro de rubidio es pirofórico y se enciende en contacto con el aire.
Metales de transición y otros elementos
Los siliciuros de metales de transición suelen ser inertes a las soluciones acuosas. Al rojo vivo, reaccionan con hidróxido de potasio, flúor y cloro. El mercurio, el talio, el bismuto y el plomo son inmiscibles con el silicio líquido.
Aplicaciones
Las películas delgadas de siliciuro tienen aplicaciones en microelectrónica debido a su gran contenido de silicio, alta conductividad eléctrica, estabilidad a altas temperaturas y resistencia a la corrosión.
Lista (incompleta)
- Silicida de níquel, NiSi
- Silcida de sodio, NaSi
- Silicidio de magnesio, Mg2Si
- Silcida platino, PtSi (en realidad el platino es más electronegativo que el silicio)
- Silicida de titanio, TiSi2
- Silcida de tungsteno, WSi2
- Molybdenum disilicide, MoSi2
- Silicidio de neoptunio, NpSi2
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar