Reducción de clemmensen
reducción de Clemmensen es una reacción química descrita como una reducción de cetonas o aldehídos a alcanos utilizando amalgama de zinc y ácido clorhídrico concentrado (HCl). Esta reacción lleva el nombre de Erik Christian Clemmensen, un químico danés-estadounidense.

Las condiciones de reducción Clemmensen son particularmente eficaces para reducir las cetonas aryl-alkyl, como las que se forman en una acilación Friedel-Crafts. La secuencia de dos pasos de la acilación Friedel-Crafts seguida por la reducción Clemmensen constituye una estrategia clásica para la alquilación primaria de las arenes.
Mecanismo
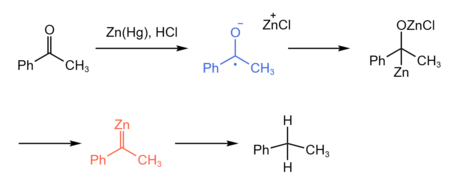
A pesar de que la reacción se descubrió por primera vez en 1914, el mecanismo de la reducción de Clemmensen sigue siendo oscuro. Debido a la naturaleza heterogénea de la reacción, los estudios mecanicistas son difíciles y sólo se han divulgado unos pocos estudios. Las propuestas mecanicistas generalmente invocan intermedios de organozinc, que a veces incluyen carbenoides de zinc, ya sea como especies discretas o como fragmentos orgánicos unidos a la superficie del metal de zinc. Brewster propuso la posibilidad de que la reducción se produjera en la superficie del metal. Dependiendo de la constitución del compuesto carbonílico o de la acidez de la reacción, se puede formar un enlace carbono-metal u oxígeno-metal después de que el compuesto se adhiere a la superficie del metal. Además, Vedeja propuso un mecanismo que implica la formación de un anión radical y un carbenoide de zinc, seguido de la reducción a alcano (como se muestra arriba). Sin embargo, no se cree que el alcohol y el carbanión sean intermediarios, ya que la exposición del alcohol a las condiciones de Clemmensen rara vez produce el producto alcano.
Aplicación
Los compuestos de hidrocarburos altamente simétricos han atraído mucho interés debido a su hermosa estructura y sus posibles aplicaciones, pero los desafíos en la síntesis persisten. Suzuki y cols. dibarrelano sintetizado, un tipo de compuesto hidrocarbonado, mediante reducción de Clemmensen. Plantearon la hipótesis de que el alcohol secundario experimentó una reacción SN1, formando un cloruro. Luego, una cantidad excesiva de zinc redujo el cloruro. Es importante destacar que la reacción redujo eficazmente las dos cetonas, el alcohol y el grupo metoxicarbonilo, evitando al mismo tiempo cualquier subproducto, lo que dio como resultado un producto con un alto rendimiento (61%).

La reducción de Clemmensen no es particularmente eficaz con cetonas alifatas o cíclicas. Una condición modificada, que implica polvo de zinc activado en una disolución anhídrida de cloruro de hidrógeno en éter de dietil o anhídrido acético, resulta en una reducción más efectiva. La reducción modificada de Clemmensen permite la desoxigenación selectiva de cetonas en moléculas que contienen grupos estables como cyano, amido, acetoxy y carboalkoxy. Yamamura et al. efectivamente reducido cholestane-3-uno a cholestane utilizando la condición Clemmensen modificada y dio el producto en alto rendimiento (~76%).

Problemas y enfoques alternativos
Para realizar la reducción de Clemmensen, el sustrato debe ser tolerante a las condiciones fuertemente ácidas de la reacción (37% HCl). Hay varias alternativas disponibles. La reducción de Wolff-Kishner puede reducir sustratos sensibles a los ácidos que son estables a bases fuertes. Para sustratos estables a la hidrogenólisis en presencia de níquel Raney, está disponible un método de reducción Mozingo de dos pasos más suave.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar