Progesterona
La progesterona (P4) es una hormona sexual endógena esteroide y progestágeno implicada en el ciclo menstrual, el embarazo y la embriogénesis de los seres humanos y otras especies. Pertenece a un grupo de hormonas esteroides llamadas progestágenos y es el principal progestágeno del organismo. La progesterona tiene una variedad de funciones importantes en el cuerpo. También es un intermediario metabólico crucial en la producción de otros esteroides endógenos, incluidas las hormonas sexuales y los corticosteroides, y desempeña un papel importante en la función cerebral como neuroesteroide.
Además de su papel como hormona natural, la progesterona también se usa como medicamento, como en combinación con estrógeno para la anticoncepción, para reducir el riesgo de cáncer de útero o de cuello uterino, en la terapia de reemplazo hormonal y en la terapia hormonal feminizante.. Se prescribió por primera vez en 1934.
Actividad biológica
La progesterona es el progestágeno más importante del cuerpo. Como potente agonista del receptor nuclear de progesterona (nPR) (con una afinidad de KD = 1 nM), los efectos resultantes sobre la transcripción ribosomal desempeñan un papel importante en la regulación de la reproducción femenina. Además, la progesterona es un agonista de los receptores de progesterona de membrana (mPR) descubiertos más recientemente, cuya expresión tiene efectos de regulación en la función de reproducción (maduración de ovocitos, trabajo de parto y motilidad de espermatozoides) y cáncer, aunque se requiere investigación adicional para definir mejor la papeles También funciona como un ligando del PGRMC1 (componente 1 de la membrana del receptor de progesterona) que afecta la progresión del tumor, la regulación metabólica y el control de la viabilidad de las células nerviosas. Además, también se sabe que la progesterona es un antagonista del receptor sigma σ1, un modulador alostérico negativo de los receptores nicotínicos de acetilcolina y un potente antagonista del receptor de mineralocorticoides (MR). La progesterona previene la activación del MR al unirse a este receptor con una afinidad que supera incluso la de la aldosterona y los glucocorticoides como el cortisol y la corticosterona, y produce efectos antimineralocorticoides, como la natriuresis, a concentraciones fisiológicas. Además, la progesterona se une y se comporta como un agonista parcial del receptor de glucocorticoides (GR), aunque con una potencia muy baja (EC50 >100 veces menor en relación con el cortisol).
La progesterona, a través de sus metabolitos neuroesteroides activos como la 5α-dihidroprogesterona y la alopregnanolona, actúa indirectamente como un modulador alostérico positivo del receptor GABAA.
La progesterona y algunos de sus metabolitos, como la 5β-dihidroprogesterona, son agonistas del receptor X de pregnano (PXR), aunque débilmente (EC50 >10 μM). De acuerdo, la progesterona induce varias enzimas del citocromo P450 hepático, como CYP3A4, especialmente durante el embarazo cuando las concentraciones son mucho más altas de lo habitual. Se ha encontrado que las mujeres perimenopáusicas tienen una mayor actividad de CYP3A4 en relación con los hombres y las mujeres posmenopáusicas, y se ha inferido que esto puede deberse a los niveles más altos de progesterona presentes en las mujeres perimenopáusicas.
La progesterona modula la actividad de los canales Ca2+ dependientes de voltaje CatSper (canales catiónicos del esperma). Dado que los óvulos liberan progesterona, los espermatozoides pueden usar la progesterona como señal de orientación para nadar hacia los óvulos (quimiotaxis). Como resultado, se ha sugerido que las sustancias que bloquean el sitio de unión de la progesterona en los canales CatSper podrían usarse potencialmente en la anticoncepción masculina.
Función biológica
Interacciones hormonales
La progesterona tiene una serie de efectos fisiológicos que se amplifican en presencia de estrógenos. Los estrógenos a través de los receptores de estrógeno (ER) inducen o regulan al alza la expresión del PR. Un ejemplo de esto es el tejido mamario, donde los estrógenos permiten que la progesterona medie en el desarrollo lobuloalveolar.
Los niveles elevados de progesterona reducen de forma potente la actividad de retención de sodio de la aldosterona, lo que provoca natriuresis y una reducción del volumen de líquido extracelular. La supresión de la progesterona, por otro lado, se asocia a un aumento temporal de la retención de sodio (disminución de la natriuresis, con aumento del volumen de líquido extracelular) debido al aumento compensatorio de la producción de aldosterona, que combate el bloqueo del receptor de mineralocorticoides por parte del previamente elevado. nivel de progesterona.
Sistema reproductor
La progesterona tiene efectos clave a través de señales no genómicas en los espermatozoides humanos a medida que migran a través del tracto femenino antes de que ocurra la fertilización, aunque los receptores todavía no se han identificado. La caracterización detallada de los eventos que ocurren en los espermatozoides en respuesta a la progesterona ha aclarado ciertos eventos que incluyen cambios transitorios y mantenidos de calcio intracelular, oscilaciones lentas de calcio, que ahora se cree que posiblemente regulan la motilidad. Es producido por los ovarios. También se ha demostrado que la progesterona tiene efectos sobre los espermatozoides del pulpo.
La progesterona a veces se denomina la "hormona del embarazo" y tiene muchas funciones relacionadas con el desarrollo del feto:
- La progesterona convierte el endometrio en su escenario secreto para preparar el útero para la implantación. Al mismo tiempo la progesterona afecta el epitelio vaginal y el moco cervical, lo que la hace gruesa e impenetrable al esperma. La progesterona es anti-mitógena en células epiteliales endometriales, y como tal, mitiga los efectos trópicos del estrógeno. Si el embarazo no ocurre, los niveles de progesterona disminuirán, lo que conducirá a la menstruación. El sangrado menstrual normal es progesterona-retirada. Si no se produce ovulación y el cuerpo luteum no se desarrolla, los niveles de progesterona pueden ser bajos, lo que conduce a sangrado uterino disfuncional anovulatorio.
- Durante la implantación y gestación, la progesterona parece disminuir la respuesta inmune materna para permitir la aceptación del embarazo.
- La progesterona disminuye la contractilidad del músculo liso uterino. Este efecto contribuye a la prevención del trabajo prematuro.
- Una caída en los niveles de progesterona es posiblemente un paso que facilita el inicio del trabajo.
- Además, la progesterona inhibe la lactancia durante el embarazo. La caída en los niveles de progesterona después de la entrega es uno de los desencadenantes para la producción de leche.
El feto metaboliza la progesterona placentaria en la producción de esteroides suprarrenales.
Senos
Desarrollo lobuloalveolar
La progesterona juega un papel importante en el desarrollo de los senos en las mujeres. Junto con la prolactina, interviene en la maduración lobuloalveolar de las glándulas mamarias durante el embarazo para permitir la producción de leche y, por lo tanto, la lactancia y el amamantamiento de las crías después del parto. El estrógeno induce la expresión de PR en el tejido mamario y, por lo tanto, la progesterona depende del estrógeno para mediar en el desarrollo lobuloalveolar. Se ha encontrado que RANKL es un mediador crítico aguas abajo de la maduración lobuloalveolar inducida por progesterona. Los ratones knockout para RANKL muestran un fenotipo mamario casi idéntico al de los ratones knockout para PR, incluido el desarrollo ductal mamario normal pero el fracaso total del desarrollo de las estructuras lobuloalveolares.
Desarrollo ductal
Aunque en mucha menor medida que el estrógeno, que es el principal mediador del desarrollo ductal mamario (a través del ERα), la progesterona también puede estar involucrada en el desarrollo ductal de las glándulas mamarias hasta cierto punto. Los ratones knockout para PR o los ratones tratados con el antagonista de PR mifepristona muestran un desarrollo ductal mamario retrasado aunque por lo demás normal en la pubertad. Además, los ratones modificados para tener sobreexpresión de PRA muestran hiperplasia ductal y la progesterona induce el crecimiento ductal en la glándula mamaria del ratón. La progesterona media el desarrollo ductal principalmente a través de la inducción de la expresión de anfiregulina, el mismo factor de crecimiento cuya expresión induce principalmente el estrógeno para mediar el desarrollo ductal. Estos hallazgos en animales sugieren que, aunque no es esencial para el desarrollo ductal mamario completo, la progesterona parece jugar un papel potenciador o acelerador en el desarrollo ductal mamario mediado por estrógenos.
Riesgo de cáncer de mama
La progesterona también parece estar involucrada en la fisiopatología del cáncer de mama, aunque su papel, y si es un promotor o un inhibidor del riesgo de cáncer de mama, no se ha dilucidado por completo. Se ha descubierto que la mayoría de las progestinas, o progestágenos sintéticos, como el acetato de medroxiprogesterona, aumentan el riesgo de cáncer de mama en mujeres posmenopáusicas en combinación con estrógeno como componente de la terapia hormonal menopáusica. La combinación de progesterona oral natural o la progestina didrogesterona atípica con estrógeno se ha asociado con un menor riesgo de cáncer de mama que las progestinas más estrógeno. Sin embargo, esto puede ser simplemente un artefacto de los bajos niveles de progesterona producidos con la progesterona oral. Se necesita más investigación sobre el papel de la progesterona en el cáncer de mama.
Salud de la piel
El receptor de estrógeno, así como el receptor de progesterona, se han detectado en la piel, incluso en queratinocitos y fibroblastos. En la menopausia y posteriormente, la disminución de los niveles de hormonas sexuales femeninas da como resultado atrofia, adelgazamiento y aumento de las arrugas de la piel y una reducción de la elasticidad, firmeza y fuerza de la piel. Estos cambios en la piel constituyen una aceleración del envejecimiento de la piel y son el resultado de la disminución del contenido de colágeno, irregularidades en la morfología de las células epidérmicas de la piel, disminución de la sustancia fundamental entre las fibras de la piel y reducción de los capilares y el flujo sanguíneo. La piel también se vuelve más seca durante la menopausia, lo que se debe a la reducción de la hidratación de la piel y de los lípidos superficiales (producción de sebo). Junto con el envejecimiento cronológico y el fotoenvejecimiento, la deficiencia de estrógenos en la menopausia es uno de los tres factores principales que influye predominantemente en el envejecimiento de la piel.
La terapia de reemplazo hormonal, que consiste en un tratamiento sistémico con estrógeno solo o en combinación con un progestágeno, tiene efectos beneficiosos considerables y bien documentados en la piel de las mujeres posmenopáusicas. Estos beneficios incluyen un mayor contenido de colágeno en la piel, grosor y elasticidad de la piel, hidratación de la piel y lípidos superficiales. Se ha encontrado que el estrógeno tópico tiene efectos beneficiosos similares en la piel. Además, un estudio ha encontrado que la crema tópica de progesterona al 2 % aumenta significativamente la elasticidad y firmeza de la piel y disminuye de manera visible las arrugas en mujeres perimenopáusicas y posmenopáusicas. La hidratación de la piel y los lípidos superficiales, por otro lado, no cambiaron significativamente con la progesterona tópica. Estos hallazgos sugieren que la progesterona, como el estrógeno, también tiene efectos beneficiosos sobre la piel y puede proteger de forma independiente contra el envejecimiento de la piel.
Sexualidad
Líbido
La progesterona y su metabolito neuroesteroide activo, la alopregnanolona, parecen tener una participación importante en la libido de las mujeres.
Homosexualidad
Dra. Diana Fleischman, de la Universidad de Portsmouth, y sus colegas buscaron una relación entre la progesterona y las actitudes sexuales en 92 mujeres. Su investigación, publicada en Archives of Sexual Behavior, encontró que las mujeres que tenían niveles más altos de progesterona obtuvieron puntajes más altos en un cuestionario que medía la motivación homoerótica. También encontraron que los hombres que tenían altos niveles de progesterona tenían más probabilidades de tener puntajes más altos de motivación homoerótica después del cebado afiliativo en comparación con los hombres con bajos niveles de progesterona.
Sistema nervioso
La progesterona, como la pregnenolona y la dehidroepiandrosterona (DHEA), pertenece a un grupo importante de esteroides endógenos llamados neuroesteroides. Se puede metabolizar en todas las partes del sistema nervioso central.
Los neuroesteroides son neuromoduladores y son neuroprotectores, neurogénicos y regulan la neurotransmisión y la mielinización. Los efectos de la progesterona como neuroesteroide están mediados predominantemente a través de sus interacciones con los PR no nucleares, a saber, los mPR y PGRMC1, así como con otros receptores, como los receptores σ1 y nACh.
Daño cerebral
Estudios anteriores han demostrado que la progesterona apoya el desarrollo normal de las neuronas en el cerebro y que la hormona tiene un efecto protector sobre el tejido cerebral dañado. Se ha observado en modelos animales que las hembras tienen una susceptibilidad reducida a la lesión cerebral traumática y se ha planteado la hipótesis de que este efecto protector es causado por el aumento de los niveles circulantes de estrógeno y progesterona en las hembras.
Mecanismo propuesto
El mecanismo de los efectos protectores de la progesterona puede ser la reducción de la inflamación que sigue al traumatismo y la hemorragia cerebrales.
Se cree que el daño ocasionado por una lesión cerebral traumática es causado en parte por la despolarización masiva que conduce a la excitotoxicidad. Una forma en que la progesterona ayuda a aliviar parte de esta excitotoxicidad es bloqueando los canales de calcio dependientes del voltaje que desencadenan la liberación de neurotransmisores. Lo hace manipulando las vías de señalización de los factores de transcripción implicados en esta liberación. Otro método para reducir la excitotoxicidad es regular al alza el GABAA, un receptor de neurotransmisor inhibidor generalizado.
También se ha demostrado que la progesterona previene la apoptosis en las neuronas, una consecuencia común de una lesión cerebral. Lo hace inhibiendo enzimas implicadas en la vía de la apoptosis específicamente en la mitocondria, como la caspasa 3 activada y el citocromo c.
La progesterona no solo ayuda a prevenir daños mayores, sino que también se ha demostrado que ayuda en la neurorregeneración. Uno de los efectos graves de la lesión cerebral traumática incluye edema. Los estudios en animales muestran que el tratamiento con progesterona conduce a una disminución en los niveles de edema al aumentar la concentración de macrófagos y microglia enviados al tejido lesionado. Esto se observó en forma de fugas reducidas de la barrera hematoencefálica en la recuperación secundaria en ratas tratadas con progesterona. Además, se observó que la progesterona tiene propiedades antioxidantes, reduciendo la concentración de radicales libres de oxígeno más rápido que sin ella. También hay evidencia de que la adición de progesterona también puede ayudar a remielinizar los axones dañados debido a un trauma, restaurando parte de la conducción de señales neuronales perdidas. Otra forma en que la progesterona ayuda en la regeneración incluye aumentar la circulación de las células progenitoras endoteliales en el cerebro. Esto ayuda a que crezca nueva vasculatura alrededor del tejido cicatricial, lo que ayuda a reparar el área lesionada.
Adicción
La progesterona mejora la función de los receptores de serotonina en el cerebro, por lo que un exceso o déficit de progesterona tiene el potencial de provocar problemas neuroquímicos significativos. Esto proporciona una explicación de por qué algunas personas recurren a sustancias que mejoran la actividad de la serotonina, como la nicotina, el alcohol y el cannabis, cuando sus niveles de progesterona caen por debajo de los niveles óptimos.
- Las diferencias sexuales en los niveles hormonales pueden inducir a las mujeres a responder de manera diferente que los hombres a la nicotina. Cuando las mujeres experimentan cambios cíclicos o diferentes fases de transición hormonal (menopausia, embarazo, adolescencia), hay cambios en sus niveles de progesterona. Por lo tanto, las mujeres tienen una mayor vulnerabilidad biológica a los efectos de refuerzo de la nicotina en comparación con los hombres y la progesterona pueden utilizarse para contrarrestar esta vulnerabilidad aumentada. Esta información apoya la idea de que la progesterona puede afectar el comportamiento.
- Similar a la nicotina, la cocaína también aumenta la liberación de dopamina en el cerebro. El neurotransmisor está involucrado en el centro de recompensas y es uno de los principales neurotransmisores involucrados con abuso de sustancias y dependencia. En un estudio de los consumidores de cocaína, se informó que la progesterona reducía el antojo y la sensación de ser estimulada por la cocaína. Así, la progesterona se sugirió como un agente que disminuye el ansia de cocaína reduciendo las propiedades dopaminérgicas de la droga.
Sociedad
En un estudio de la Universidad de Amsterdam de 2012 de 120 mujeres, la fase lútea de las mujeres (niveles más altos de progesterona y niveles crecientes de estrógeno) se correlacionó con un nivel más bajo de comportamiento competitivo en escenarios de apuestas y concursos de matemáticas, mientras que su La fase premenstrual (niveles de progesterona en fuerte disminución y niveles de estrógeno en disminución) se correlacionó con un mayor nivel de comportamiento competitivo.
Otros efectos
- La progesterona también tiene un papel en la elasticidad de la piel y la fuerza ósea, en la respiración, en el tejido nervioso y en la sexualidad femenina, y la presencia de receptores de progesterona en ciertos tejidos musculares y grasas puede insinuar un papel en proporciones sexualmente difórficas de aquellos.
- Durante el embarazo, se dice que la progesterona disminuye la irritabilidad uterina.
- Durante el embarazo, la progesterona ayuda a suprimir las respuestas inmunitarias de la madre a los antígenos fetales, lo que impide el rechazo del feto.
- La progesterona eleva los niveles del factor de crecimiento epidérmico-1 (EGF-1), factor que a menudo se utiliza para inducir la proliferación, y se utiliza para sostener culturas, de células madre.
- La progesterona aumenta la temperatura central (función termogénica) durante la ovulación.
- La progesterona reduce el espasmo y relaja el músculo liso. Los Bronchi están ensanchados y el moco regulado. (Las RCP están ampliamente presentes en el tejido submucosal.)
- La progesterona actúa como agente antiinflamatorio y regula la respuesta inmunitaria.
- La progesterona reduce la actividad vesicular.
- La progesterona normaliza la coagulación sanguínea y el tono vascular, los niveles de zinc y cobre, los niveles de oxígeno celular y el uso de tiendas de grasa para energía.
- La progesterona puede afectar la salud de las encías, aumentando el riesgo de gingivitis (inflamación de las encías).
- La progesterona parece prevenir el cáncer de endometrial (involviendo el revestimiento uterino) regulando los efectos del estrógeno.
- La progesterona desempeña un papel importante en la señalización de la liberación de insulina y la función pancreática, y puede afectar la susceptibilidad a la diabetes o diabetes gestacional.
Bioquímica
Biosíntesis
En los mamíferos, la progesterona, como todas las demás hormonas esteroides, se sintetiza a partir de la pregnenolona, que a su vez se deriva del colesterol.
El colesterol sufre una oxidación doble para producir 22R-hidroxicolesterol y luego 20α,22R-dihidroxicolesterol. Este diol vecinal luego se oxida aún más con pérdida de la cadena lateral que comienza en la posición C22 para producir pregnenolona. Esta reacción es catalizada por el citocromo P450scc.
La conversión de pregnenolona en progesterona se lleva a cabo en dos pasos. Primero, el grupo 3β-hidroxilo se oxida a un grupo ceto y segundo, el doble enlace se mueve a C4, desde C5 a través de una reacción de tautomerización ceto/enol. Esta reacción es catalizada por 3β-hidroxiesteroide deshidrogenasa/δ5-4-isomerasa.
La progesterona, a su vez, es el precursor del mineralocorticoide aldosterona y, tras su conversión en 17α-hidroxiprogesterona, del cortisol y la androstenediona. La androstenediona se puede convertir en testosterona, estrona y estradiol, lo que destaca el papel fundamental de la progesterona en la síntesis de testosterona.
La levadura también puede sintetizar pregnenolona y progesterona.
Los ovarios secretan aproximadamente 25 mg de progesterona por día en las mujeres, mientras que las glándulas suprarrenales producen alrededor de 2 mg de progesterona por día.
| Sexo | hormona sexual | Reproducción fase | Sangre Tasa de producción | Gonadal tasa de secreción | metabólico Tasa de autorización | Gama de referencia (nivel sérico) | |
|---|---|---|---|---|---|---|---|
| SI unidades | Non-SI unidades | ||||||
| Hombres | Androstenedione | – | 2.8 mg/día | 1.6 mg/día | 2200 L/día | 2.8–7.3 nmol/L | 80–210 ng/dL |
| Testosterona | – | 6.5 mg/día | 6.2 mg/día | 950 L/día | 6.9–34,7 nmol/L | 200–1000 ng/dL | |
| Estrone | – | 150 μg/día | 110 μg/día | 2050 L/día | 37–250 pmol/L | 10–70 pg/mL | |
| Estradiol | – | 60 μg/día | 50 μg/día | 1600 L/día | " 37–210 pmol/L " | 10–57 pg/mL | |
| Sulfato de Estrone | – | 80 μg/día | Insignificante | 167 L/día | 600–2500 pmol/L | 200–900 pg/mL | |
| Mujeres | Androstenedione | – | 3.2 mg/día | 2.8 mg/día | 2000 L/día | 3.1–12.2 nmol/L | 89–350 ng/dL |
| Testosterona | – | 190 μg/día | 60 μg/día | 500 L/día | 0,7–2,8 nmol/L | 20–81 ng/dL | |
| Estrone | Fase folicular | 110 μg/día | 80 μg/día | 2200 L/día | 110–400 pmol/L | 30–110 pg/mL | |
| Fase luteal | 260 μg/día | 150 μg/día | 2200 L/día | 310–660 pmol/L | 80–180 pg/mL | ||
| Postmenopause | 40 μg/día | Insignificante | 1610 L/día | 22–230 pmol/L | 6–60 pg/mL | ||
| Estradiol | Fase folicular | 90 μg/día | 80 μg/día | 1200 L/día | ■37-360 pmol/L | 10–98 pg/mL | |
| Fase luteal | 250 μg/día | 240 μg/día | 1200 L/día | 699–1250 pmol/L | 190–341 pg/mL | ||
| Postmenopause | 6 μg/día | Insignificante | 910 L/día | ■37–140 pmol/L | 10 a 38 pg/m L | ||
| Sulfato de Estrone | Fase folicular | 100 μg/día | Insignificante | 146 L/día | 700–3600 pmol/L | 250–1300 pg/mL | |
| Fase luteal | 180 μg/día | Insignificante | 146 L/día | 1100–7300 pmol/L | 400–2600 pg/mL | ||
| Progesterona | Fase folicular | 2 mg/día | 1.7 mg/día | 2100 L/día | 0.3–3 nmol/L | 0.1–0.9 ng/mL | |
| Fase luteal | 25 mg/día | 24 mg/día | 2100 L/día | 19–45 nmol/L | 6 a 14 ng/mL | ||
Notas y fuentes Notas: "El concentración de un esteroide en la circulación se determina por la tasa a la que se secreta de las glándulas, la tasa de metabolismo de precursores o prehormonas en el esteroide, y la tasa a la que se extrae por los tejidos y metabolizado. El tasa de secreción de un esteroide se refiere a la secreción total del compuesto de una glándula por unidad tiempo. Las tasas de secreción han sido evaluadas al muestreo del efluente venoso de una glándula con el tiempo y restringiendo la concentración arterial y hormonal venosa periférica. El tasa de limpieza metabólica de un esteroide se define como el volumen de sangre que se ha limpiado completamente de la hormona por unidad tiempo. El Tasa de producción de una hormona esteroides se refiere a la entrada en la sangre del compuesto de todas las fuentes posibles, incluyendo la secreción de las glándulas y la conversión de prohormonas en el esteroide de interés. En estado estable, la cantidad de hormona que entra en la sangre de todas las fuentes será igual a la tasa a la que se está limpiando (tasa de limpieza metabólica) multiplicada por concentración de sangre (tasa de producción = tasa de limpieza metabólica × concentración). Si hay poca contribución del metabolismo prohormona a la piscina circulante de esteroides, entonces la tasa de producción aproximará la tasa de secreción." Fuentes: Ver plantilla. | |||||||
Distribución
La progesterona se une ampliamente a las proteínas plasmáticas, incluidas la albúmina (50 a 54 %) y la transcortina (43 a 48 %). Tiene una afinidad similar por la albúmina en relación con el PR.
Metabolismo
El metabolismo de la progesterona es rápido y extenso y ocurre principalmente en el hígado, aunque las enzimas que metabolizan la progesterona también se expresan ampliamente en el cerebro, la piel y otros tejidos extrahepáticos. La progesterona tiene una vida media de eliminación de solo aproximadamente 5 minutos en circulación. El metabolismo de la progesterona es complejo y puede formar hasta 35 metabolitos no conjugados diferentes cuando se ingiere por vía oral. La progesterona es muy susceptible a la reducción enzimática a través de reductasas e hidroxiesteroide deshidrogenasas debido a su doble enlace (entre las posiciones C4 y C5) y sus dos cetonas (en las posiciones C3 y C20).
La vía metabólica principal de la progesterona es la reducción por la 5α-reductasa y la 5β-reductasa en 5α-dihidroprogesterona dihidrogenada y 5β-dihidroprogesterona, respectivamente. A esto le sigue la reducción adicional de estos metabolitos a través de la 3α-hidroxiesteroide deshidrogenasa y la 3β-hidroxiesteroide deshidrogenasa en alopregnanolona tetrahidrogenada, pregnanolona, isopregnanolona y epipregnanolona. Posteriormente, la 20α-hidroxiesteroide deshidrogenasa y la 20β-hidroxiesteroide deshidrogenasa reducen estos metabolitos para formar los correspondientes pregnanedioles hexahidrogenados (ocho isómeros diferentes en total), que luego se conjugan mediante glucuronidación y/o sulfatación, se liberan del hígado a la circulación y se excretan por riñones a la orina. El principal metabolito de la progesterona en la orina es el isómero 3α,5β,20α del glucurónido de pregnanediol, que se ha encontrado que constituye del 15 al 30% de una inyección de progesterona. Otros metabolitos de la progesterona formados por las enzimas en esta vía incluyen 3α-dihidroprogesterona, 3β-dihidroprogesterona, 20α-dihidroprogesterona y 20β-dihidroprogesterona, así como varios productos combinados de las enzimas además de los ya mencionados. La progesterona también puede hidroxilarse primero (ver más abajo) y luego reducirse. La progesterona endógena se metaboliza aproximadamente en un 50% en 5α-dihidroprogesterona en el cuerpo lúteo, en un 35% en 3β-dihidroprogesterona en el hígado y en un 10% en 20α-dihidroprogesterona.
Porciones relativamente pequeñas de progesterona se hidroxilan a través de la 17α-hidroxilasa (CYP17A1) y la 21-hidroxilasa (CYP21A2) en 17α-hidroxiprogesterona y 11-desoxicorticosterona (21-hidroxiprogesterona), respectivamente, y los pregnanetrioles se forman de manera secundaria a la 17α-hidroxilación. Incluso cantidades más pequeñas de progesterona también pueden hidroxilarse a través de la 11β-hidroxilasa (CYP11B1) y, en menor medida, a través de la aldosterona sintasa (CYP11B2) en 11β-hidroxiprogesterona. Además, la progesterona puede ser hidroxilada en el hígado por otras enzimas del citocromo P450 que no son específicas de los esteroides. La 6β-hidroxilación, que es catalizada principalmente por CYP3A4, es la principal transformación y es responsable de aproximadamente el 70 % del metabolismo de la progesterona mediado por el citocromo P450. Otras rutas incluyen 6α-, 16α- y 16β-hidroxilación. Sin embargo, el tratamiento de mujeres con ketoconazol, un inhibidor potente de CYP3A4, tuvo efectos mínimos sobre los niveles de progesterona, produciendo solo un aumento leve y no significativo, y esto sugiere que las enzimas del citocromo P450 desempeñan solo un papel pequeño en el metabolismo de la progesterona.
Metabolismo de progesterona en humanos |
Niveles
En las mujeres, los niveles de progesterona son relativamente bajos durante la fase preovulatoria del ciclo menstrual, aumentan después de la ovulación y se elevan durante la fase lútea, como se muestra en el diagrama anterior. Los niveles de progesterona tienden a ser inferiores a 2 ng/ml antes de la ovulación y superiores a 5 ng/ml después de la ovulación. Si se produce un embarazo, se libera gonadotropina coriónica humana, manteniendo el cuerpo lúteo y permitiéndole mantener los niveles de progesterona. Entre las semanas 7 y 9, la placenta comienza a producir progesterona en lugar del cuerpo lúteo en un proceso llamado cambio lúteo-placentario.
Después del cambio luteal-placentario, los niveles de progesterona comienzan a aumentar aún más y pueden llegar a 100 a 200 ng/mL a término. Se ha discutido si una disminución en los niveles de progesterona es crítica para el inicio del trabajo de parto y puede ser específico de la especie. Después de la expulsión de la placenta y durante la lactancia, los niveles de progesterona son muy bajos.
Los niveles de progesterona son bajos en niños y mujeres posmenopáusicas. Los hombres adultos tienen niveles similares a los de las mujeres durante la fase folicular del ciclo menstrual.
| Grupo | P4 producción | P4 niveles | ||
|---|---|---|---|---|
| Niños preventivos | ND | 0,06–0,5 ng/m L | ||
| Pubertal girls Etapa I del Tanner (niñez) Etapa de Tanner II (edad 8–12) Etapa III del Tanner (de 10 a 13 años) Etapa IV del Tanner (de 11 a 14 años) Etapa V del Tanner (de 12 a 15 años) Fase folicular (días 1 a 14) Fase luteal (días 15 a 28) | ND ND ND ND ND ND | 0,2 (0,10–0,32) ng/mL 0.30 (0,10–0,51) ng/mL 0,36 (0,10–0,75) ng/mL 1,75 (10–25.0) ng/mL 0,35 (0,13–0,75) ng/mL 2.0–25.0 ng/mL | ||
| Mujeres premenopáusicas Fase folicular (días 1 a 14) Fase luteal (días 15 a 28) Contraceptivo oral (anovulatorio) | 0,75-5,4 mg/día 15–50 mg/día ND | 0,02–1.2 ng/mL 4 a 30 ng/mL 0.1–0.3 ng/m L | ||
| Mujeres posmenopáusicas Mujeres oophorectomizadas Mujeres oophorectomizadas y adrenalectomizadas | ND 1.2 mg/día 0,3 mg/día | 0,03–0,3 ng/m L 0,39 ng/m L ND | ||
| Mujeres embarazadas Primer trimestre (semanas 1–12) Segundo trimestre (semanas 13 a 26) Tercer trimestre (semanas 27 a 40) Postparto (a las 24 horas) | 55 mg/día 92–100 mg/día 190–563 mg/día ND | 9–75 ng/mL 17–146 ng/mL 55–255 ng/mL 19 ng/m L | ||
| Hombres | 0,75-3 mg/día | 0.1–0.3 ng/m L | ||
| Notas: Los niveles medios se dan como un único valor y los rangos se dan después de entre paréntesis. Fuentes: Ver plantilla. | ||||
Rangos
Los resultados de los análisis de sangre siempre deben interpretarse utilizando los rangos de referencia proporcionados por el laboratorio que realizó los resultados. Los rangos de referencia de ejemplo se enumeran a continuación.
| Tipo de persona | Gama de referencia para análisis de sangre | ||
|---|---|---|---|
| Límite inferior | Límite superior | Dependencia | |
| Mujeres - ciclo menstrual | (ver diagrama abajo) | ||
| Mujer - postmenopáusica | ▪0.2 | 1 | ng/mL |
| ▪ | 3 | nmol/L | |
| Mujeres contra anticonceptivos orales | 0.34 | 0.92 | ng/mL |
| 1.1 | 2.9 | nmol/L | |
| Hombres ≥16 años | 0,277 | 0.9 | ng/mL |
| 0,86 | 2.9 | nmol/L | |
| Mujeres o hombres 1 a 9 años | 0.1 | 4.1 o 4.5 | ng/mL |
| 0.3 | 13 | nmol/L | |
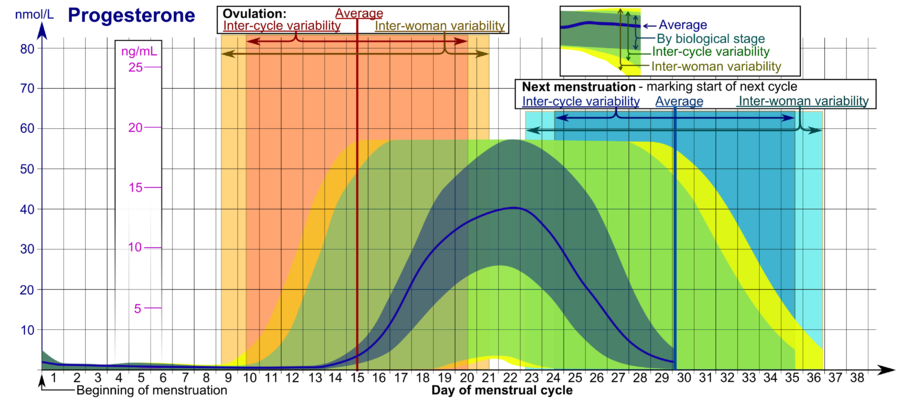
• Los rangos denotados Por etapa biológica puede ser utilizado en ciclos menstruales monitoreados de cerca con respecto a otros marcadores de su progresión biológica, con la escala de tiempo comprimida o estirada a lo mucho más rápido o más lento, respectivamente, el ciclo progresa en comparación con un ciclo promedio.
• Los rangos denotados Variabilidad entre ciclos son más apropiados para utilizar en ciclos no vigilados con sólo el comienzo de la menstruación conocida, pero donde la mujer conoce con precisión su duración promedio del ciclo y el tiempo de ovulación, y que son algo regular, con la escala del tiempo que se comprimió o se estira hasta cuánto la duración promedio del ciclo de una mujer es más corta o más, respectivamente, que el promedio de la población.
• Los rangos denotados Variabilidad entre mujeres son más apropiados para usar cuando se desconocen las longitudes promedio del ciclo y el tiempo de ovulación, pero sólo se da el comienzo de la menstruación.
Fuentes
Animales
La progesterona se produce en grandes cantidades en los ovarios (por el cuerpo lúteo) desde el inicio de la pubertad hasta la menopausia, y también se produce en cantidades más pequeñas en las glándulas suprarrenales después del inicio de la adrenarquia tanto en hombres como en mujeres. En menor medida, la progesterona se produce en el tejido nervioso, especialmente en el cerebro, y también en el tejido adiposo (grasa).
Durante el embarazo humano, los ovarios y la placenta producen progesterona en cantidades cada vez mayores. En un principio, la fuente es el cuerpo lúteo que ha sido "rescatado" por la presencia de gonadotropina coriónica humana (hCG) del producto de la concepción. Sin embargo, después de la octava semana, la producción de progesterona se traslada a la placenta. La placenta utiliza el colesterol materno como sustrato inicial, y la mayor parte de la progesterona producida ingresa a la circulación materna, pero parte es captada por la circulación fetal y utilizada como sustrato para los corticosteroides fetales. A término, la placenta produce alrededor de 250 mg de progesterona por día.
Una fuente animal adicional de progesterona son los productos lácteos. Después del consumo de productos lácteos, el nivel de progesterona biodisponible aumenta.
Plantas
En al menos una planta, Juglans regia, se ha detectado progesterona. Además, los esteroides similares a la progesterona se encuentran en Dioscorea mexicana. Dioscorea mexicana es una planta que forma parte de la familia del ñame originaria de México. Contiene un esteroide llamado diosgenina que se extrae de la planta y se convierte en progesterona. La diosgenina y la progesterona también se encuentran en otras especies de Dioscorea, así como en otras plantas que no están estrechamente relacionadas, como la alholva.
Otra planta que contiene sustancias fácilmente convertibles en progesterona es la Dioscorea pseudojaponica originaria de Taiwán. La investigación ha demostrado que el ñame taiwanés contiene saponinas, esteroides que se pueden convertir en diosgenina y, por lo tanto, en progesterona.
Muchas otras especies de Dioscorea de la familia del ñame contienen sustancias esteroides a partir de las cuales se puede producir progesterona. Entre los más notables están Dioscorea villosa y Dioscorea polygonoides. Un estudio demostró que la Dioscorea villosa contiene un 3,5 % de diosgenina. Se ha encontrado que Dioscorea polygonoides contiene un 2,64 % de diosgenina según lo demostrado por cromatografía de gases-espectrometría de masas. Muchas de las especies Dioscorea que se originan en la familia del ñame crecen en países que tienen climas tropicales y subtropicales.
Uso médico
La progesterona se usa como medicamento. Se usa en combinación con estrógenos principalmente en la terapia hormonal para los síntomas de la menopausia y los niveles bajos de hormonas sexuales en las mujeres. También se usa en mujeres para apoyar el embarazo y la fertilidad y para tratar trastornos ginecológicos. Se ha demostrado que la progesterona previene el aborto espontáneo en mujeres con 1) sangrado vaginal temprano en su embarazo actual y 2) antecedentes de aborto espontáneo. La progesterona se puede tomar por vía oral, a través de la vagina y mediante inyección en el músculo o la grasa, entre otras vías.
Química
La progesterona es un esteroide natural del embarazo y también se conoce como pregn-4-ene-3,20-dione. Tiene un doble enlace (4-eno) entre las posiciones C4 y C5 y dos grupos cetona (3,20-diona), uno en la posición C3 y otro en la posición C20.
Síntesis
La progesterona se produce comercialmente por semisíntesis. Se utilizan dos rutas principales: una de la diosgenina de ñame iniciada por primera vez por Marker en 1940, y otra basada en fitoesteroles de soya ampliados en la década de 1970. También se han informado semisíntesis adicionales (no necesariamente económicas) de progesterona a partir de una variedad de esteroides. Por ejemplo, la cortisona se puede desoxigenar simultáneamente en la posición C-17 y C-21 mediante tratamiento con yodotrimetilsilano en cloroformo para producir 11-ceto-progesterona (cetogestina), que a su vez se puede reducir en la posición 11 para producir progesterona.
Semisíntesis de marcadores
Russell Marker desarrolló en 1940 para la empresa farmacéutica Parke-Davis una semisíntesis económica de progesterona a partir del esteroide vegetal diosgenina aislada del ñame. Esta síntesis se conoce como degradación de Marker.
El intermedio 16-DPA es importante para la síntesis de muchos otros esteroides médicamente importantes. Un enfoque muy similar puede producir 16-DPA a partir de solanina.
Semisíntesis de soja
La progesterona también se puede producir a partir del estigmasterol que se encuentra en el aceite de soja. cf Percy Julián.
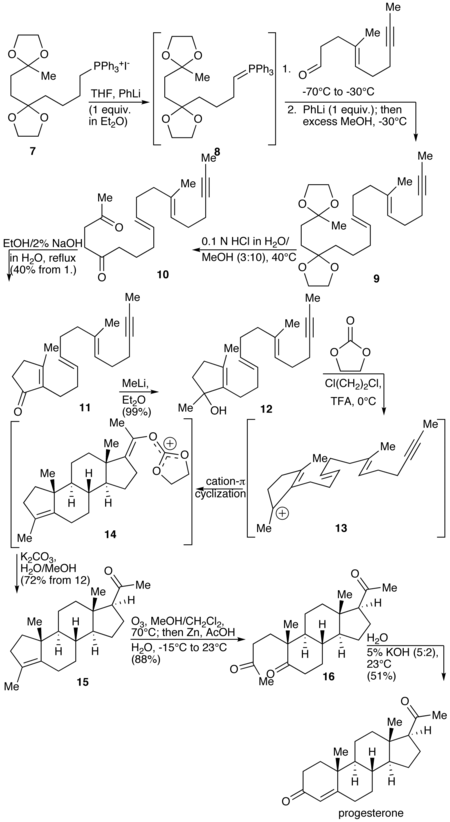
Síntesis total
Una síntesis total de progesterona fue reportada en 1971 por W.S. Johnson. La síntesis comienza con la reacción de la sal de fosfonio 7 con fenil litio para producir el iluro de fosfonio 8. El iluro 8 se hace reaccionar con un aldehído para producir el alqueno 9. Los grupos protectores de cetal de 9 se hidrolizan para producir la dicetona 10, que a su vez se cicla para formar el ciclopentenona 11. La cetona de 11 se hace reaccionar con metil litio para producir el alcohol terciario 12, que a su vez se trata con ácido para producir el catión terciario 13. El paso clave de la síntesis es la ciclación del catión π de 13 en la que los anillos B, C y D del esteroide se forman simultáneamente para producir < b>14. Este paso se asemeja a la reacción de ciclación catiónica utilizada en la biosíntesis de esteroides y, por lo tanto, se denomina biomimético. En el siguiente paso, el ortoéster de enol se hidroliza para producir la cetona 15. Luego, el anillo A del ciclopenteno se abre mediante oxidación con ozono para producir 16. Finalmente, la dicetona 17 sufre una condensación aldólica intramolecular al tratarla con hidróxido de potasio acuoso para producir progesterona.
Historia
George W. Corner y Willard M. Allen descubrieron la acción hormonal de la progesterona en 1929. Entre 1931 y 1932, se había aislado del cuerpo lúteo de animales material cristalino casi puro de alta actividad progestacional y, en 1934, material cristalino puro se había refinado y obtenido progesterona y se había determinado la estructura química de la progesterona. Esto lo logró Adolf Butenandt en el Chemisches Institut de la Universidad Técnica de Danzig, quien extrajo este nuevo compuesto de varios miles de litros de orina.
La síntesis química de progesterona a partir de estigmasterol y pregnanediol se completó ese mismo año. Hasta este momento, varios grupos se referían a la progesterona, conocida genéricamente como hormona del cuerpo lúteo, con diferentes nombres, incluidos corporina, luteína, luteosterona y progestina. En 1935, en el momento de la Segunda Conferencia Internacional sobre la Estandarización de las Hormonas Sexuales en Londres, Inglaterra, se llegó a un compromiso entre los grupos y se creó el nombre progesterona (cetona esteroide progestacional).
Uso veterinario
El uso de pruebas de progesterona en la cría de perros para identificar la ovulación es cada vez más utilizado. Hay varias pruebas disponibles, pero la prueba más confiable es un análisis de sangre con sangre extraída por un veterinario y enviada a un laboratorio para su procesamiento. Los resultados generalmente se pueden obtener entre 24 y 72 horas. La justificación para usar pruebas de progesterona es que el aumento en el número comienza muy cerca del pico preovulatorio de gonadotropinas y continúa durante la ovulación y el estro. Cuando los niveles de progesterona alcanzan ciertos niveles, pueden indicar la etapa de estro en la que se encuentra la hembra. La predicción de la fecha de nacimiento de la camada pendiente puede ser muy precisa si se conoce la fecha de ovulación. Los cachorros dan a luz con un día o dos de 9 semanas de gestación en la mayoría de los casos. Sin embargo, no es posible determinar el embarazo usando pruebas de progesterona una vez que ha tenido lugar un cruce. Esto se debe al hecho de que, en las perras, los niveles de progesterona permanecen elevados durante todo el período estral.
Contenido relacionado
Khat
Cardamomo
Medicina de la obesidad