Hormona luteinizante
Hormona luteinizante (LH, también conocida como hormona luteinizante, lutropina y en ocasiones lutrofina) es una hormona producida por las células gonadotrópicas en la glándula pituitaria anterior. La producción de LH está regulada por la hormona liberadora de gonadotropina (GnRH) del hipotálamo. En las mujeres, un aumento agudo de LH conocido como aumento de LH, desencadena la ovulación y el desarrollo del cuerpo lúteo. En los hombres, donde la LH también se ha denominado hormona estimulante de las células intersticiales (ICSH), estimula la producción de testosterona en las células de Leydig. Actúa sinérgicamente con la hormona foliculoestimulante (FSH).
Estructura
LH es una glicoproteína heterodimérica. Cada unidad monomérica es una molécula de glicoproteína; una subunidad alfa y una beta forman la proteína funcional completa.
Su estructura es similar a la de otras hormonas glicoproteicas, la hormona estimulante del folículo (FSH), la hormona estimulante de la tiroides (TSH) y la gonadotropina coriónica humana (hCG). El dímero de proteína contiene 2 subunidades glicopeptídicas (subunidades alfa y beta etiquetadas) que están asociadas de forma no covalente:
- El subunidades alfa de LH, FSH, TSH y hCG son idénticos, y contienen 92 aminoácidos en humanos pero 96 aminoácidos en casi todas las otras especies vertebradas (hormonas de glucoproteína no existen en invertebrados).
- El beta subunits varían. LH tiene una subunidad beta de 120 aminoácidos (LHB) que confiere su acción biológica específica y es responsable de la especificidad de la interacción con el receptor LH. Esta subunidad beta contiene una secuencia de aminoácidos que exhibe grandes homologías con la de la subunidad beta de hCG y ambos estimulan el mismo receptor. Sin embargo, la subunidad hCG beta contiene 24 aminoácidos adicionales, y las dos hormonas difieren en la composición de sus moieties de azúcar.
La diferente composición de estos oligosacáridos afecta la bioactividad y la velocidad de degradación. La vida media biológica de la LH es de 20 min, más corta que la de la FSH (3 a 4 h) y la hCG (24 h). La vida media biológica de la LH es de 23 horas subcutánea o vida media terminal de 10-12 horas.
Genes
El gen de la subunidad alfa se encuentra en el cromosoma 6q12.21.
El gen de la subunidad beta de la hormona luteinizante está localizado en el grupo de genes LHB/CGB en el cromosoma 19q13.32. En contraste con la actividad del gen alfa, la actividad del gen de la subunidad beta LH está restringida a las células gonadotrópicas de la hipófisis. Está regulado por la hormona liberadora de gonadotropina del hipotálamo. La inhibina, la activina y las hormonas sexuales no afectan la actividad genética para la producción de la subunidad beta de LH.
Función
Tanto en hombres como en mujeres, la LH actúa sobre las células endocrinas de las gónadas para producir andrógenos.
Efectos en mujeres
LH apoya a las células de la teca en los ovarios que proporcionan andrógenos y precursores hormonales para la producción de estradiol. En el momento de la menstruación, la FSH inicia el crecimiento folicular, afectando específicamente a las células de la granulosa. Con el aumento de estrógenos, los receptores de LH también se expresan en el folículo en maduración, lo que hace que produzca más estradiol. Finalmente, cuando el folículo ha madurado por completo, un pico en la producción de 17α-hidroxiprogesterona por parte del folículo inhibe la producción de estrógenos. Previamente, el aumento preovulatorio de LH se atribuía a una disminución en la retroalimentación negativa de GnRH mediada por estrógenos en el hipotálamo, lo que subsecuentemente estimulaba la liberación de LH desde la hipófisis anterior. Sin embargo, estudios más recientes atribuyen el aumento de LH a la retroalimentación positiva del estradiol después de que la producción del folículo dominante supera cierto umbral. Los niveles excepcionalmente altos de estradiol inducen la producción hipotalámica de progesterona, que estimula la secreción elevada de GnRH, lo que desencadena un aumento de LH. El aumento en la producción de LH solo dura de 24 a 48 horas. Este "aumento de LH" desencadena la ovulación, por lo que no solo libera el óvulo del folículo, sino que también inicia la conversión del folículo residual en un cuerpo lúteo que, a su vez, produce progesterona para preparar el endometrio para una posible implantación. La LH es necesaria para mantener la función lútea durante las dos segundas semanas del ciclo menstrual. Si se produce un embarazo, los niveles de LH disminuirán y, en cambio, la función lútea se mantendrá gracias a la acción de la hCG (gonadotropina coriónica humana), una hormona muy similar a la LH pero secretada por la nueva placenta.
Los esteroides gonadales (estrógenos y andrógenos) generalmente tienen efectos de retroalimentación negativos sobre la liberación de GnRH-1 a nivel del hipotálamo y en los gonadotropos, lo que reduce su sensibilidad a la GnRH. La retroalimentación positiva de los estrógenos también ocurre en el eje gonadal de las hembras de los mamíferos y es responsable del pico de LH a mitad del ciclo que estimula la ovulación. Aunque los estrógenos inhiben la liberación de kisspeptina (Kp) de las neuronas kiss1 en el ARC, los estrógenos estimulan la liberación de Kp de las neuronas Kp en el AVPV. Como los estrógenos' los niveles aumentan gradualmente, predomina el efecto positivo, lo que lleva al aumento de LH. Las neuronas secretoras de GABA que inervan las neuronas GnRH-1 también pueden estimular la liberación de GnRH-1. Estas neuronas GABA también poseen ER y pueden ser responsables del aumento de GnRH-1. Parte de la acción inhibitoria de las endorfinas sobre la liberación de GnRH-1 se produce a través de la inhibición de estas neuronas GABA. La ruptura del folículo ovárico en el momento de la ovulación provoca una reducción drástica de la síntesis de estrógenos y un marcado aumento de la secreción de progesterona por parte del cuerpo lúteo en el ovario, restableciendo una retroalimentación predominantemente negativa sobre la secreción hipotalámica de GnRH-1.
Efectos en machos
La LH actúa sobre las células de Leydig de los testículos y está regulada por la hormona liberadora de gonadotropina (GnRH). Las células de Leydig producen testosterona bajo el control de la LH. LH se une a los receptores de LH en la superficie de la membrana de las células de Leydig. La unión a este receptor provoca un aumento del monofosfato de adenosina cíclico (cAMP), un mensajero secundario, que permite que el colesterol se traslade a la mitocondria. Dentro de las mitocondrias, el colesterol se convierte en pregnenolona por CYP11A1. Luego, la pregnenolona se convierte en dehidroepiandrosterona (DHEA). Luego, la DHEA se convierte en androstenediona mediante la 3β-hidroxiesteroide deshidrogenasa (3β-HSD) y finalmente se convierte en testosterona mediante la 17β-hidroxiesteroide deshidrogenasa (HSD17B). El inicio de la pubertad está controlado por dos hormonas principales: la FSH inicia la espermatogénesis y la LH señala la liberación de testosterona, un andrógeno que ejerce actividad tanto endocrina como intratesticular en la espermatogénesis.
La LH se libera de la glándula pituitaria y está controlada por pulsos de hormona liberadora de gonadotropina. Cuando los niveles de testosterona en el torrente sanguíneo son bajos, se estimula la glándula pituitaria para que libere LH. A medida que aumentan los niveles de testosterona, actuará sobre la pituitaria a través de un circuito de retroalimentación negativa e inhibirá la liberación de GnRH y LH en consecuencia. Los andrógenos (incluidas la testosterona y la dihidrotestosterona) inhiben la monoamino oxidasa (MAO) en la glándula pineal, lo que conduce a un aumento de la melatonina y a una reducción de la LH y la FSH por el aumento inducido por la melatonina de la síntesis y secreción de la hormona inhibidora de la gonadotropina (GnIH). La testosterona también se puede aromatizar en estradiol (E2) para inhibir la LH. E2 disminuye la amplitud del pulso y la capacidad de respuesta a la GnRH del hipotálamo a la pituitaria.
Los cambios en los niveles sanguíneos de LH y testosterona y las secreciones del pulso son inducidos por cambios en la excitación sexual en los hombres humanos.
Efectos en el cerebro
Los receptores de la hormona luteinizante están ubicados en áreas del cerebro asociadas con la función cognitiva. El papel de la LH en el sistema nervioso central (SNC) puede ser relevante para comprender y tratar el deterioro cognitivo posmenopáusico.
Investigaciones recientes han observado una relación inversa entre la LH circulante y los niveles de LH en el SNC. Después de la ovariectomía (un procedimiento utilizado para simular la menopausia) en ratones hembra, los niveles de LH circulante aumentan mientras que los niveles de LH en el SNC caen. Los tratamientos que reducen la LH circulante restauran los niveles de LH en el SNC.
Niveles normales
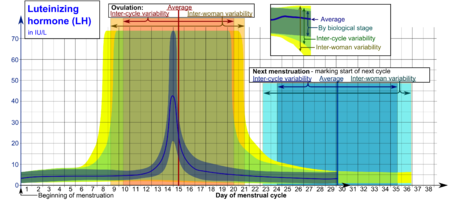
- Los rangos denotados Por etapa biológica puede ser utilizado en ciclos menstruales monitoreados de cerca con respecto a otros marcadores de su progresión biológica, con la escala de tiempo comprimida o estirada a lo mucho más rápido o más lento, respectivamente, el ciclo progresa en comparación con un ciclo promedio.
- Los rangos denotados Variabilidad entre ciclos son más apropiados para utilizar en ciclos no vigilados con sólo el comienzo de la menstruación conocida, pero donde la mujer conoce con precisión su duración promedio del ciclo y el tiempo de ovulación, y que son algo regular, con la escala del tiempo que se comprimió o se estira hasta cuánto la duración promedio del ciclo de una mujer es más corta o más, respectivamente, que el promedio de la población.
- Los rangos denotados Variabilidad entre mujeres son más apropiados para usar cuando se desconocen las longitudes promedio del ciclo y el tiempo de ovulación, pero sólo se da el comienzo de la menstruación.
Los niveles de LH normalmente son bajos durante la niñez y en las mujeres, altos después de la menopausia. Dado que la LH se secreta en pulsos, es necesario seguir su concentración durante un período de tiempo suficiente para obtener información adecuada sobre su nivel en sangre.
Durante los años reproductivos, los niveles típicos oscilan entre 1 y 20 UI/L. Los niveles fisiológicos altos de LH se observan durante el pico de LH (vs) y generalmente duran 48 horas.
En hombres mayores de 18 años, se ha estimado que los rangos de referencia son de 1,8 a 8,6 UI/L.
LH se mide en unidades internacionales (UI). Al cuantificar la cantidad de LH en una muestra en UI, es importante saber con qué estándar internacional se calibró su lote de LH, ya que pueden variar ampliamente de un año a otro. Para la LH urinaria humana, una UI se define más recientemente como 1/189 de una ampolla denominada 96/602 y distribuida por el NIBSC, lo que corresponde a aproximadamente 0,04656 µg de proteína LH por una sola UI, pero las versiones estándar más antiguas todavía se usan ampliamente.
Predicción de la ovulación
La detección de un aumento en la liberación de la hormona luteinizante indica una ovulación inminente. La LH se puede detectar mediante kits de predicción de la ovulación urinaria (OPK, también LH-kit) que se realizan, generalmente a diario, alrededor del momento en que se espera la ovulación. Una conversión de una lectura negativa a positiva sugeriría que la ovulación está a punto de ocurrir dentro de las 24 a 48 horas, dando a las mujeres dos días para tener relaciones sexuales o inseminación artificial con la intención de concebir.
La frecuencia de prueba recomendada difiere entre los fabricantes. Por ejemplo, la prueba Clearblue se realiza a diario y una mayor frecuencia no disminuye el riesgo de pasar por alto un pico de LH. Por otro lado, la empresa china Nantong Egens Biotechnology recomienda utilizar su test dos veces al día. Si se realiza la prueba una vez al día, no se ha encontrado una diferencia significativa entre la prueba de LH por la mañana y por la noche, en relación con las tasas de concepción, y las recomendaciones sobre a qué hora del día realizar la prueba varían entre los fabricantes y los trabajadores de la salud. Las pruebas se pueden leer manualmente con una tira de papel que cambia de color o digitalmente con la ayuda de un sistema electrónico de lectura.
Las pruebas de hormona luteinizante pueden combinarse con pruebas de estradiol en pruebas como el monitor de fertilidad Clearblue.
La sensibilidad de las pruebas de LH se mide en miliunidades internacionales, con pruebas comúnmente disponibles en el rango de 10 a 40 m.i.u. (cuanto menor sea el número, mayor será la sensibilidad).
Como los espermatozoides pueden permanecer viables en la mujer durante varios días, las pruebas de LH no se recomiendan para las prácticas anticonceptivas, ya que el aumento de LH generalmente ocurre después del comienzo de la ventana fértil.
Estados de enfermedad
Exceso
En niños con pubertad precoz de origen pituitario o central, los niveles de LH y FSH pueden estar en el rango reproductivo en lugar de los niveles bajos típicos para su edad.
Durante los años reproductivos, con frecuencia se observa LH relativamente elevada en pacientes con síndrome de ovario poliquístico; sin embargo, sería inusual que tuvieran niveles de LH fuera del rango reproductivo normal.
Los niveles persistentemente altos de LH son indicativos de situaciones en las que la retroalimentación restrictiva normal de las gónadas está ausente, lo que conduce a una producción hipofisaria de LH y FSH. Si bien esto es típico en la menopausia, es anormal en los años reproductivos. Allí puede ser una señal de:
- Menopausa prematura
- Digenesis gonadal, síndrome de Turner, síndrome de Klinefelter
- Castración
- Síndrome de Swyer
- Síndrome de ovario poliquístico
- Ciertas formas de hiperplasia suprarrenal congénita
- Fallo testicular
- Embarazo – BetaHCG puede imitar LH así que las pruebas pueden mostrar LH elevado
Nota: un medicamento para inhibir la secreción de la hormona luteinizante es la butinazocina.
Deficiencia
La disminución de la secreción de LH puede resultar en una falla de la función gonadal (hipogonadismo). Esta condición se manifiesta típicamente en los hombres como una falla en la producción de un número normal de espermatozoides. En las mujeres, se observa comúnmente amenorrea. Las condiciones con secreciones muy bajas de LH incluyen:
- Síndrome de Pasqualini
- Síndrome de Kallmann
- Represión hipotálmica
- Hipopituarismo
- Trastorno de alimentación
- Triada de atleta femenino
- Hiperprolactinemia
- Hipógonadismo
- Terapia de supresión de ganglios
- GnRH antagonista
- Agonista de GnRH (induciendo una estimulación inicial (flare up) seguido de bloqueo permanente del receptor pituitario de GnRH)
Como medicamento
La LH está disponible mezclada con FSH en forma de menotropina y otras formas de gonadotropinas urinarias. Las formas más purificadas de gonadotropinas urinarias pueden reducir la porción de LH en relación con la FSH. La LH recombinante está disponible como lutropina alfa (Luveris). Todos estos medicamentos deben administrarse por vía parenteral. Se usan comúnmente en la terapia de infertilidad para estimular el desarrollo folicular, siendo el más notable en la terapia de FIV.
A menudo, la medicación HCG se utiliza como sustituto de la LH porque activa el mismo receptor. La hCG de uso médico se deriva de la orina de mujeres embarazadas, es menos costosa y tiene una vida media más larga que la LH.
Papel en la fosforilación
La fosforilación es un proceso bioquímico que implica la adición de fosfato a un compuesto orgánico. La esteroidogénesis implica procesos mediante los cuales el colesterol se convierte en hormonas esteroides biológicamente activas. Un estudio reciente muestra que la LH a través de una vía de señalización de PKA regula la fosforilación y localización de DRP1 dentro de las mitocondrias de las células esteroidogénicas del ovario.
Contenido relacionado
Ley de Fick
Presión oncótica
Sinapsis química
Presión osmótica
Neuropil