Entalpía
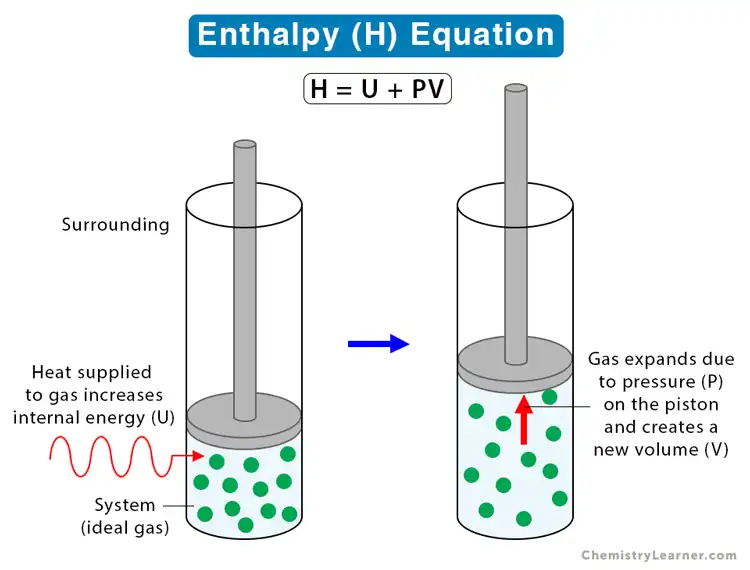
La entalpía, una propiedad de un sistema termodinámico, es la suma de la energía interna del sistema y el producto de su presión y volumen. Es una función de estado utilizada en muchas mediciones en sistemas químicos, biológicos y físicos a una presión constante, que es convenientemente proporcionada por la gran atmósfera ambiental. El término presión-volumen expresa el trabajo requerido para establecer las dimensiones físicas del sistema, es decir, para hacerle espacio desplazando su entorno.El término presión-volumen es muy pequeño para sólidos y líquidos en condiciones comunes y bastante pequeño para gases. Por lo tanto, la entalpía es un sustituto de la energía en los sistemas químicos; enlace, red, solvatación y otras "energías" en química son en realidad diferencias de entalpía. Como función de estado, la entalpía depende únicamente de la configuración final de la energía interna, la presión y el volumen, no del camino seguido para alcanzarla.
En el Sistema Internacional de Unidades (SI), la unidad de medida de la entalpía es el joule. Otras unidades históricas convencionales todavía en uso incluyen la caloría y la unidad térmica británica (BTU).
La entalpía total de un sistema no se puede medir directamente porque la energía interna contiene componentes desconocidos, de difícil acceso o que no son de interés en termodinámica. En la práctica, un cambio en la entalpía es la expresión preferida para mediciones a presión constante porque simplifica la descripción de la transferencia de energía. Cuando también se evita la transferencia de materia dentro o fuera del sistema y no se realiza trabajo eléctrico o de eje, a presión constante el cambio de entalpía es igual a la energía intercambiada con el medio ambiente por calor.
En química, la entalpía estándar de reacción es el cambio de entalpía cuando los reactivos en sus estados estándar (p = 1 bar; generalmente T = 298 K) cambian a productos en sus estados estándar. Esta cantidad es el calor estándar de reacción a presión y temperatura constantes, pero puede medirse por métodos calorimétricos incluso si la temperatura varía durante la medición, siempre que la presión y la temperatura inicial y final correspondan al estado estándar. El valor no depende de la ruta del estado inicial al final porque la entalpía es una función de estado.
Las entalpías de las sustancias químicas generalmente se enumeran para una presión de 1 bar (100 kPa) como estado estándar. Las entalpías y los cambios de entalpía de las reacciones varían en función de la temperatura, pero las tablas generalmente enumeran los calores estándar de formación de sustancias a 25 °C (298 K). Para procesos endotérmicos (absorción de calor), el cambio Δ H es un valor positivo; para procesos exotérmicos (liberación de calor) es negativo.
La entalpía de un gas ideal es independiente de su presión o volumen, y depende únicamente de su temperatura, que se correlaciona con su energía térmica. Los gases reales a temperaturas y presiones comunes a menudo se aproximan mucho a este comportamiento, lo que simplifica el diseño y el análisis termodinámicos prácticos.
Definición
La entalpía H de un sistema termodinámico se define como la suma de su energía interna y el producto de su presión y volumen:H = U + pV,
donde U es la energía interna, p es la presión y V es el volumen del sistema.
La entalpía es una propiedad extensiva; es proporcional al tamaño del sistema (para sistemas homogéneos). Como propiedades intensivas, la entalpía específica h =H/metroestá referenciada a una unidad de masa m del sistema, y la entalpía molar H m esH/norte, donde n es el número de moles. Para sistemas no homogéneos, la entalpía es la suma de las entalpías de los subsistemas componentes:

donde
- H es la entalpía total de todos los subsistemas,
- k se refiere a los diversos subsistemas,
- H k se refiere a la entalpía de cada subsistema.
Un sistema cerrado puede estar en equilibrio termodinámico en un campo gravitatorio estático, de modo que su presión p varíe continuamente con la altitud, mientras que, debido al requisito de equilibrio, su temperatura T es invariable con la altitud. (En consecuencia, la densidad de energía potencial gravitacional del sistema también varía con la altitud). Entonces, la suma de entalpía se convierte en una integral:

donde
- ρ ("rho") es la densidad (masa por unidad de volumen),
- h es la entalpía específica (entalpía por unidad de masa),
- (ρh) representa la densidad de entalpía (entalpía por unidad de volumen),
- dV denota un elemento de volumen infinitesimalmente pequeño dentro del sistema, por ejemplo, el volumen de una capa horizontal infinitesimalmente delgada,por tanto, la integral representa la suma de las entalpías de todos los elementos del volumen.
La entalpía de un sistema homogéneo cerrado es su función de energía H (S, p), con su entropía S [ p ] y su presión p como variables de estado natural que proporcionan una relación diferencial para dH de la forma más simple, derivada de la siguiente manera. Partimos de la primera ley de la termodinámica para sistemas cerrados para un proceso infinitesimal:

donde
- ? Q es una pequeña cantidad de calor que se agrega al sistema,
- ? W es una pequeña cantidad de trabajo realizado por el sistema.
En un sistema homogéneo en el que solo se consideran procesos reversibles o transferencia de calor pura, la segunda ley de la termodinámica da ? Q = T dS, siendo T la temperatura absoluta y dS el cambio infinitesimal en la entropía S del sistema. Además, si solo se realiza trabajo pV, ? W = p dV. Como resultado,

Sumar d (pV) a ambos lados de esta expresión da

o

Asi que

y los coeficientes de las variables naturales diferenciales dS y dp son solo las variables individuales T y V.
Otras expresiones
La expresión anterior de dH en términos de entropía y presión puede resultar desconocida para algunos lectores. También hay expresiones en términos de variables medibles más directamente, como la temperatura y la presión:

Aquí C p es la capacidad calorífica a presión constante y α es el coeficiente de expansión térmica (cúbica):

Con esta expresión se puede, en principio, determinar la entalpía si C p y V se conocen como funciones de p y T. Sin embargo, la expresión es más complicada 
A presión constante, dP = 0, de modo que 
En una forma más general, la primera ley describe la energía interna con términos adicionales relacionados con el potencial químico y el número de partículas de varios tipos. El enunciado diferencial para dH entonces se convierte en

donde μ i es el potencial químico por partícula para una partícula de tipo i, y N i es el número de tales partículas. El último término también se puede escribir como μ i dn i (siendo dn i el número de moles del componente i añadido al sistema y, en este caso, μ i el potencial químico molar) o como μ i dm i (siendo dm i la masa del componente i añadido al sistema y, en este caso, μ i el potencial químico específico).
Funciones características y variables de estado natural
La entalpía, H (S [ p ], p, { N i }), expresa la termodinámica de un sistema en la representación de energía. Como función de estado, sus argumentos incluyen tanto una variable de estado intensiva como varias extensivas. Se dice que las variables de estado S [ p ], p y { N i } son las variables de estado naturalen esta representación. Son adecuados para describir procesos en los que están determinados por factores del entorno. Por ejemplo, cuando una parcela virtual de aire atmosférico se mueve a una altitud diferente, la presión que la rodea cambia y el proceso suele ser tan rápido que hay muy poco tiempo para la transferencia de calor. Esta es la base de la llamada aproximación adiabática que se utiliza en meteorología.
Conjugada con la entalpía, con estos argumentos, la otra función de estado característica de un sistema termodinámico es su entropía, en función, S [ p ](H, p, { N i }), de la misma lista de variables de estado, excepto que la entropía, S [ p ], se reemplaza en la lista por la entalpía, H. Expresa la representación de la entropía. Se dice que las variables de estado H, p y { N i } son las variables de estado naturalen esta representación. Son adecuados para describir procesos en los que se controlan experimentalmente. Por ejemplo, H y p pueden controlarse permitiendo la transferencia de calor y variando solo la presión externa sobre el pistón que establece el volumen del sistema.
Interpretación física
El término U es la energía del sistema, y el término pV puede interpretarse como el trabajo que se requeriría para "hacer espacio" para el sistema si la presión del entorno permaneciera constante. Cuando un sistema, por ejemplo, n moles de un gas de volumen V a presión p y temperatura T, se crea o se lleva a su estado actual desde el cero absoluto, se debe suministrar energía igual a su energía interna U más pV, donde pV es el trabajo realizado al empujar contra la presión ambiental (atmosférica).
En física y mecánica estadística puede ser más interesante estudiar las propiedades internas de un sistema de volumen constante y por lo tanto se utiliza la energía interna. En química, los experimentos a menudo se realizan a presión atmosférica constante y el trabajo de presión-volumen representa un intercambio de energía pequeño y bien definido con la atmósfera, por lo que Δ H es la expresión adecuada para el calor de reacción. Para una máquina térmica, el cambio en su entalpía después de un ciclo completo es igual a cero, ya que el estado final e inicial son iguales.
Relación con el calor
Para discutir la relación entre el aumento de entalpía y el suministro de calor, volvemos a la primera ley para sistemas cerrados, con la convención de signos de la física: dU = δQ − δW, donde el calor δQ es suministrado por conducción, radiación, calentamiento Joule, o la fricción de la agitación por un eje con paletas o por un campo magnético impulsado externamente que actúa sobre un rotor interno (que es trabajo basado en el entorno, pero contribuye al calor basado en el sistema). Lo aplicamos al caso especial con una presión constante en la superficie. En este caso el trabajo viene dado por p dV (donde p es la presión en la superficie, dVes el aumento del volumen del sistema). Los casos de interacción electromagnética de largo alcance requieren variables de estado adicionales en su formulación y no se consideran aquí. En este caso la primera ley dice:

Ahora,

Asi que

Si el sistema está a presión constante, dp = 0 y, en consecuencia, el aumento de entalpía del sistema es igual al calor añadido o cedido:

Esta es la razón por la cual el término ahora obsoleto contenido de calor se utilizó en el siglo XIX.
Aplicaciones
En termodinámica, se puede calcular la entalpía determinando los requisitos para crear un sistema a partir de la "nada"; el trabajo mecánico requerido, pV, difiere según las condiciones que se obtienen durante la creación del sistema termodinámico.
Se debe suministrar energía para remover partículas del entorno para hacer espacio para la creación del sistema, asumiendo que la presión p permanece constante; este es el término pV. La energía suministrada también debe proporcionar el cambio en la energía interna, U, que incluye energías de activación, energías de ionización, energías de mezcla, energías de vaporización, energías de enlace químico, etc. Juntos, estos constituyen el cambio en la entalpía U + pV. Para sistemas a presión constante, sin trabajo externo que no sea el trabajo pV, el cambio de entalpía es el calor recibido por el sistema.
Para un sistema simple con un número constante de partículas a presión constante, la diferencia de entalpía es la cantidad máxima de energía térmica que se puede derivar de un proceso termodinámico isobárico.
Calor de reacción
La entalpía total de un sistema no se puede medir directamente; en su lugar, se mide el cambio de entalpía de un sistema. El cambio de entalpía se define mediante la siguiente ecuación:

donde
- Δ H es el "cambio de entalpía",
- H f es la entalpía final del sistema (en una reacción química, la entalpía de los productos o del sistema en equilibrio),
- Hi es la entalpía inicial del sistema (en una reacción química, la entalpía de los reactivos).
Para una reacción exotérmica a presión constante, el cambio de entalpía del sistema, Δ H, es negativo debido a que los productos de la reacción tienen una entalpía menor que los reactivos, y es igual al calor liberado en la reacción si no se realiza ningún trabajo eléctrico o de eje.. En otras palabras, la disminución general de la entalpía se logra mediante la generación de calor. Por el contrario, para una reacción endotérmica a presión constante, Δ H es positivo e igual al calor absorbido en la reacción.
De la definición de entalpía como H = U + pV, el cambio de entalpía a presión constante es Δ H = Δ U + p Δ V. Sin embargo, para la mayoría de las reacciones químicas, el término de trabajo p Δ V es mucho menor que el cambio de energía interna Δ U, que es aproximadamente igual a Δ H. Como ejemplo, para la combustión de monóxido de carbono 2 CO(g) + O 2 (g) → 2 CO 2 (g), Δ H = −566,0 kJ y Δ U = −563,5 kJ.Dado que las diferencias son tan pequeñas, las entalpías de reacción a menudo se describen como energías de reacción y se analizan en términos de energías de enlace.
Entalpía específica
La entalpía específica de un sistema uniforme se define como h =H/metrodonde m es la masa del sistema. La unidad SI para la entalpía específica es julio por kilogramo. Puede expresarse en otras cantidades específicas por h = u + pv, donde u es la energía interna específica, p es la presión y v es el volumen específico, que es igual a1/ρ, donde ρ es la densidad.
Cambios de entalpía
Un cambio de entalpía describe el cambio de entalpía observado en los constituyentes de un sistema termodinámico cuando experimenta una transformación o reacción química. Es la diferencia entre la entalpía una vez finalizado el proceso, es decir, la entalpía de los productos suponiendo que la reacción se completa, y la entalpía inicial del sistema, es decir, los reactivos. Estos procesos se especifican únicamente por sus estados inicial y final, de modo que el cambio de entalpía para el proceso inverso es el negativo del proceso directo.
Un cambio de entalpía estándar común es la entalpía de formación, que se ha determinado para una gran cantidad de sustancias. Los cambios de entalpía se miden y compilan de forma rutinaria en obras de referencia químicas y físicas, como el Manual de química y física de CRC. La siguiente es una selección de cambios de entalpía comúnmente reconocidos en termodinámica.
Cuando se usa en estos términos reconocidos, el cambio de calificador generalmente se elimina y la propiedad se denomina simplemente entalpía de 'proceso'. Dado que estas propiedades a menudo se usan como valores de referencia, es muy común citarlas para un conjunto estandarizado de parámetros ambientales o condiciones estándar, que incluyen:
- Una presión de una atmósfera (1 atm o 101,325 kPa) o 1 bar
- Una temperatura de 25 °C o 298,15 K
- Una concentración de 1,0 M cuando el elemento o compuesto está presente en solución
- Elementos o compuestos en sus estados físicos normales, es decir, estado estándar
Para tales valores estandarizados, el nombre de la entalpía suele ir precedido del término estándar, por ejemplo , entalpía estándar de formación.
Propiedades químicas:
- Entalpía de reacción, definida como el cambio de entalpía observado en un constituyente de un sistema termodinámico cuando un mol de sustancia reacciona completamente.
- Entalpía de formación, definida como el cambio de entalpía observado en un constituyente de un sistema termodinámico cuando se forma un mol de un compuesto a partir de sus antecedentes elementales.
- Entalpía de combustión, definida como el cambio de entalpía observado en un componente de un sistema termodinámico cuando un mol de una sustancia se quema completamente con oxígeno.
- Entalpía de hidrogenación, definida como el cambio de entalpía observado en un componente de un sistema termodinámico cuando un mol de un compuesto insaturado reacciona completamente con un exceso de hidrógeno para formar un compuesto saturado.
- Entalpía de atomización, definida como el cambio de entalpía requerido para separar completamente un mol de una sustancia en sus átomos constituyentes.
- Entalpía de neutralización, definida como el cambio de entalpía observado en un componente de un sistema termodinámico cuando se forma un mol de agua cuando reaccionan un ácido y una base.
- Entalpía estándar de solución, definida como el cambio de entalpía observado en un componente de un sistema termodinámico cuando un mol de un soluto se disuelve completamente en un exceso de solvente, de modo que la solución se encuentra en una dilución infinita.
- Entalpía estándar de desnaturalización (bioquímica), definida como el cambio de entalpía requerido para desnaturalizar un mol de compuesto.
- Entalpía de hidratación, definida como el cambio de entalpía observado cuando un mol de iones gaseosos se disuelve completamente en agua formando un mol de iones acuosos.
Propiedades físicas:
- Entalpía de fusión, definida como el cambio de entalpía requerido para cambiar completamente el estado de un mol de sustancia de sólido a líquido.
- Entalpía de vaporización, definida como el cambio de entalpía requerido para cambiar completamente el estado de un mol de sustancia de líquido a gas.
- Entalpía de sublimación, definida como el cambio de entalpía requerido para cambiar completamente el estado de un mol de sustancia de sólido a gas.
- Entalpía de red, definida como la energía requerida para separar un mol de un compuesto iónico en iones gaseosos separados a una distancia infinita (es decir, sin fuerza de atracción).
- Entalpía de mezcla, definida como el cambio de entalpía al mezclar dos sustancias químicas (que no reaccionan).
Sistemas abiertos
En los sistemas abiertos termodinámicos, la masa (de sustancias) puede entrar y salir de los límites del sistema. La primera ley de la termodinámica para sistemas abiertos establece: El aumento en la energía interna de un sistema es igual a la cantidad de energía añadida al sistema por el flujo de masa hacia adentro y por el calentamiento, menos la cantidad perdida por el flujo de masa hacia afuera y en la forma del trabajo realizado por el sistema:

donde Uin es la energía interna promedio que ingresa al sistema y Uout es la energía interna promedio que sale del sistema.
La región del espacio encerrada por los límites del sistema abierto generalmente se denomina volumen de control y puede corresponder o no a paredes físicas. Si elegimos la forma del volumen de control de manera que todo el flujo de entrada o salida ocurra perpendicular a su superficie, entonces el flujo de masa hacia el sistema realiza un trabajo como si fuera un pistón de fluido empujando masa hacia el sistema, y el sistema realiza trabajar sobre el flujo de masa hacia afuera como si estuviera impulsando un pistón de fluido. Entonces, se realizan dos tipos de trabajo: el trabajo de flujo descrito anteriormente, que se realiza en el fluido (a menudo también se denomina trabajo pV), y el trabajo en el eje, que se puede realizar en algún dispositivo mecánico, como una turbina o una bomba.
Estos dos tipos de trabajo se expresan en la ecuación

La sustitución en la ecuación anterior por el volumen de control (cv) produce:

La definición de entalpía, H, nos permite usar este potencial termodinámico para tener en cuenta tanto la energía interna como el trabajo pV en fluidos para sistemas abiertos:

Si permitimos que también se mueva la frontera del sistema (por ejemplo, debido al movimiento de los pistones), obtenemos una forma bastante general de la primera ley para sistemas abiertos. En términos de derivadas temporales se lee:

con sumas sobre los diversos lugares k donde se suministra calor, la masa fluye hacia el sistema y los límites se mueven. Los términos Ḣ k representan flujos de entalpía, que se pueden escribir como

con ṁ k el flujo másico y ṅ k el flujo molar en la posición k respectivamente. El términodvk _/dtrepresenta la tasa de cambio del volumen del sistema en la posición k que da como resultado la potencia pV realizada por el sistema. El parámetro P representa todas las demás formas de energía producidas por el sistema, como la energía del eje, pero también puede ser, por ejemplo, energía eléctrica producida por una planta de energía eléctrica.
Tenga en cuenta que la expresión anterior es válida solo si la tasa de flujo de energía cinética se conserva entre la entrada y la salida del sistema. De lo contrario, debe incluirse en el balance de entalpía. Durante la operación en estado estable de un dispositivo (ver turbina, bomba y motor), el promediodU/dtpuede ser igual a cero. Esto produce una expresión útil para la generación de energía promedio para estos dispositivos en ausencia de reacciones químicas:

donde los paréntesis angulares indican promedios de tiempo. La importancia técnica de la entalpía está directamente relacionada con su presencia en la primera ley para sistemas abiertos, tal como se formuló anteriormente.
Diagramas
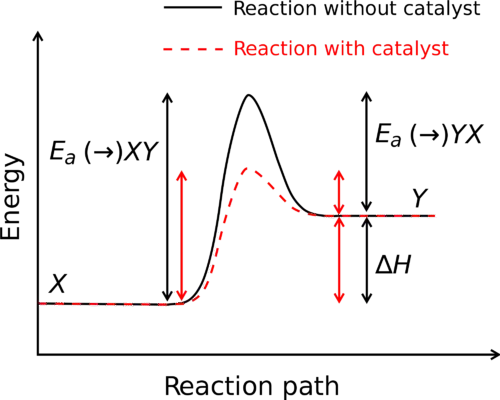
Los valores de entalpía de sustancias importantes se pueden obtener utilizando software comercial. Prácticamente todas las propiedades relevantes de los materiales se pueden obtener en forma tabular o gráfica. Hay muchos tipos de diagramas, como los diagramas h - T, que dan la entalpía específica como función de la temperatura para varias presiones, y los diagramas h - p, que dan h como función de p para varias T. Uno de los diagramas más comunes es el diagrama de entropía específica de temperatura (T – sdiagrama). Proporciona la curva de fusión y los valores de líquido y vapor saturados junto con isobaras e isenthalps. Estos diagramas son herramientas poderosas en manos del ingeniero térmico.
Algunas aplicaciones básicas
Los puntos a a h en la figura juegan un papel en la discusión en esta sección.
| Punto | T (K) | p (barra) | s (kJ/(kg·K)) | h (kJ/kg) |
|---|---|---|---|---|
| un | 300 | 1 | 6.85 | 461 |
| b | 380 | 2 | 6.85 | 530 |
| C | 300 | 200 | 5.16 | 430 |
| d | 270 | 1 | 6.79 | 430 |
| mi | 108 | 13 | 3.55 | 100 |
| F | 77.2 | 1 | 3.75 | 100 |
| gramo | 77.2 | 1 | 2.83 | 28 |
| h | 77.2 | 1 | 5.41 | 230 |
Los puntos eyg son líquidos saturados y el punto h es un gas saturado.
Estrangulamiento
Una de las aplicaciones simples del concepto de entalpía es el llamado proceso de estrangulamiento, también conocido como expansión de Joule-Thomson. Se trata de un flujo adiabático constante de un fluido a través de una resistencia al flujo (válvula, tapón poroso o cualquier otro tipo de resistencia al flujo) como se muestra en la figura. Este proceso es muy importante, ya que está en el corazón de los frigoríficos domésticos, donde es el responsable del descenso de temperatura entre la temperatura ambiente y la del interior del frigorífico. También es la etapa final en muchos tipos de licuefactores.
Para un régimen de flujo de estado estacionario, la entalpía del sistema (rectángulo punteado) tiene que ser constante. Por lo tanto

Dado que el flujo másico es constante, las entalpías específicas en los dos lados de la resistencia al flujo son las mismas:

es decir, la entalpía por unidad de masa no cambia durante la regulación. Las consecuencias de esta relación se pueden demostrar utilizando el diagrama T − s anterior. El punto c está a 200 bar y temperatura ambiente (300 K). Una expansión de Joule-Thomson de 200 bar a 1 bar sigue una curva de entalpía constante de aproximadamente 425 kJ/kg (no se muestra en el diagrama) que se encuentra entre los isenthalps de 400 y 450 kJ/kg y termina en el punto d, que está en un temperatura de aproximadamente 270 K. Por lo tanto, la expansión de 200 bar a 1 bar enfría el nitrógeno de 300 K a 270 K. En la válvula, hay mucha fricción y se produce mucha entropía, pero aún así la temperatura final está por debajo el valor inicial.
El punto e se elige de modo que esté en la línea de líquido saturado con h = 100 kJ/kg. Corresponde aproximadamente con p = 13 bar y T = 108 K. La estrangulación desde este punto hasta una presión de 1 bar termina en la región de dos fases (punto f). Esto significa que una mezcla de gas y líquido sale de la válvula de estrangulamiento. Dado que la entalpía es un parámetro extensivo, la entalpía en f (h f) es igual a la entalpía en g (h g) multiplicada por la fracción líquida en f (x f) más la entalpía en h (hh) multiplicado por la fracción de gas enf (1 − x f). Asi que

Con números: 100 = x f × 28 + (1 − x f) × 230, entonces x f = 0.64. Esto significa que la fracción de masa del líquido en la mezcla de líquido y gas que sale de la válvula de estrangulación es del 64 %.
Compresores
Se aplica una potencia P, por ejemplo, como potencia eléctrica. Si la compresión es adiabática, la temperatura del gas sube. En el caso reversible sería a entropía constante, lo que corresponde a una línea vertical en el diagrama T – s. Por ejemplo, comprimir nitrógeno de 1 bar (punto a) a 2 bar (punto b) daría como resultado un aumento de temperatura de 300 K a 380 K. Para permitir que el gas comprimido salga a la temperatura ambiente T a, el intercambio de calor, p. por agua de enfriamiento, es necesario. En el caso ideal la compresión es isotérmica. El flujo de calor promedio hacia los alrededores es Q̇. Dado que el sistema está en estado estacionario, la primera ley da

La potencia mínima necesaria para la compresión se realiza si la compresión es reversible. En ese caso, la segunda ley de la termodinámica para sistemas abiertos da

La eliminación de Q̇ da por la mínima potencia

Por ejemplo, comprimir 1 kg de nitrógeno de 1 bar a 200 bar cuesta al menos (h c − h a) − T a (s c − s a). Con los datos, obtenidos con el diagrama T – s, encontramos un valor de (430 − 461) − 300 × (5,16 − 6,85) = 476 kJ/kg.
La relación de la potencia se puede simplificar aún más escribiéndola como

Con dh = T ds + v dp, esto da como resultado la relación final

Historia y etimología
El término entalpía se acuñó relativamente tarde en la historia de la termodinámica, a principios del siglo XX. La energía fue introducida en un sentido moderno por Thomas Young en 1802, mientras que la entropía fue acuñada por Rudolf Clausius en 1865. Energía utiliza la raíz de la palabra griega ἔργον (ergon), que significa "trabajo", para expresar la idea de capacidad para realizar un trabajo.. Entropía usa la palabra griega τροπή (tropē) que significa transformación o giro. Entalpía usa la raíz de la palabra griega θάλπος (thalpos) "calor, calor".
El término expresa el concepto obsoleto de contenido de calor, ya que dH se refiere a la cantidad de calor ganado en un proceso solo a presión constante, pero no en el caso general cuando la presión es variable. Josiah Willard Gibbs usó el término "una función de calor para presión constante" para mayor claridad.
La introducción del concepto de "contenido de calor" H está asociada con Benoît Paul Émile Clapeyron y Rudolf Clausius (relación Clausius-Clapeyron, 1850).
El término entalpía apareció impreso por primera vez en 1909. Se atribuye a Heike Kamerlingh Onnes, quien muy probablemente lo introdujo oralmente el año anterior, en la primera reunión del Instituto de Refrigeración en París. Ganó vigencia solo en la década de 1920, en particular con Mollier Steam Tables and Diagrams, publicado en 1927.
Hasta la década de 1920, el símbolo H se usaba, de manera un tanto inconsistente, para "calor" en general. La definición de H como estrictamente limitada a la entalpía o "contenido de calor a presión constante" fue propuesta formalmente por Alfred W. Porter en 1922.
Contenido relacionado
Calor latente
Fuerza nuclear débil
Transformación de la energía