Codón de parada
En biología molecular (específicamente biosíntesis de proteínas), un codón de terminación (o codón de terminación) es un codón (triplete de nucleótidos dentro del ARN mensajero) que señala la terminación del proceso de traducción de la proteína actual. La mayoría de los codones en el ARN mensajero corresponden a la adición de un aminoácido a una cadena polipeptídica en crecimiento, que finalmente puede convertirse en una proteína; los codones de parada señalan la terminación de este proceso mediante la unión de factores de liberación, que hacen que las subunidades ribosómicas se disocien, liberando la cadena de aminoácidos.
Mientras que los codones de inicio necesitan secuencias cercanas o factores de iniciación para comenzar la traducción, un codón de terminación por sí solo es suficiente para iniciar la terminación.
Propiedades
Codones estándar
En el código genético estándar, hay tres codones de terminación diferentes:
| Codon | Código estándar (Tabla de traducción 1) | Nombre | ||
|---|---|---|---|---|
| ADN | ARN | |||
TAG | UAG | STOP = Ter (*) | "Amber" | |
TAA | UAA | STOP = Ter (*) | "ochre" | |
TGA | UGA | STOP = Ter (*) | "opal" (o "umber") | |
Codones de terminación alternativos
Hay variaciones en el código genético estándar y se han encontrado codones de parada alternativos en los genomas mitocondriales de vertebrados, Scenedesmus obliquus y Thraustochytrium.
| Código genético | Traducción cuadro | Codon | Traducción con este código | Traducción estándar | ||||
|---|---|---|---|---|---|---|---|---|
| ADN | ARN | |||||||
| Vertebrate mitocondrial | 2 | AGA | AGA | STOP = Ter (*) | Arg (R) | |||
AGG | AGG | STOP = Ter (*) | Arg (R) | |||||
| Escenasmus obliquus mitocondrial | 22 | TCA | UCA | STOP = Ter (*) | Ser (S) | |||
| Thraustochytrium mitocondrial | 23 | TTA | UUA | STOP = Ter (*) | Leu (L) | |||
| Propiedades bioquímicas aminoáceas | Nonpolar | Polar | Básico | Acidic | Termination: stop codon |
Codones de terminación reasignados
El código genético nuclear es flexible, como lo ilustran los códigos genéticos variantes que reasignan los codones de parada estándar a los aminoácidos.
| Código genético | Traducción cuadro | Codon | condicional traducción | Traducción estándar | ||||
|---|---|---|---|---|---|---|---|---|
| ADN | ARN | |||||||
| Karyorelict nuclear | 27 | TGA | UGA | Ter (*) | o | Trp (W) | Ter (*) | |
| Condylostoma nuclear | 28 | TAA | UAA | Ter (*) | o | Gln (Q) | Ter (*) | |
TAG | UAG | Ter (*) | o | Gln (Q) | Ter (*) | |||
TGA | UGA | Ter (*) | o | Trp (W) | Ter (*) | |||
| Blastocrithidia nuclear | 31 | TAA | UAA | Ter (*) | o | Glu (E) | Ter (*) | |
TAG | UAG | Ter (*) | o | Glu (E) | Ter (*) | |||
Traducción
En 1986, se proporcionó evidencia convincente de que la selenocisteína (Sec) se incorporó cotraduccionalmente. Además, el codón que dirige parcialmente su incorporación en la cadena polipeptídica se identificó como UGA, también conocido como codón de terminación de ópalo. Se han identificado diferentes mecanismos para anular la función de terminación de este codón en procariotas y eucariotas. Una diferencia particular entre estos reinos es que los elementos cis parecen estar restringidos a la vecindad del codón UAG en procariotas mientras que en eucariotas esta restricción no está presente. En cambio, tales lugares parecen desfavorecidos aunque no prohibidos.
En 2003, un artículo histórico describió la identificación de todas las selenoproteínas conocidas en humanos: 25 en total. Se han realizado análisis similares para otros organismos.
El codón UAG puede traducirse en pirrolisina (Pyl) de manera similar.
Distribución genómica
La distribución de los codones de terminación dentro del genoma de un organismo no es aleatoria y puede correlacionarse con el contenido de GC. Por ejemplo, el E. coli El genoma K-12 contiene 2705 TAA (63 %), 1257 TGA (29 %) y 326 TAG (8 %) codones de parada (contenido de GC 50,8 %). También los sustratos para el factor 1 de liberación de codones de parada o el factor 2 de liberación están fuertemente correlacionados con la abundancia de codones de parada. El estudio a gran escala de bacterias con una amplia gama de contenidos de GC muestra que, si bien la frecuencia de aparición de TAA se correlaciona negativamente con el contenido de GC y la frecuencia de aparición de TGA se correlaciona positivamente con el contenido de GC, la frecuencia de aparición del codón de parada TAG, que a menudo es el codón de parada mínimamente utilizado en un genoma, no está influenciado por el contenido de GC.
Reconocimiento
El reconocimiento de codones de terminación en bacterias se ha asociado con el denominado "anticodón tripéptido", un motivo de aminoácidos muy conservado en RF1 (PxT) y RF2 (SPF). Aunque esto está respaldado por estudios estructurales, se demostró que la hipótesis del anticodón tripéptido es una simplificación excesiva.
Nomenclatura
Históricamente, los codones de parada recibieron muchos nombres diferentes, ya que cada uno correspondía a una clase distinta de mutantes que se comportaban de manera similar. Estos mutantes se aislaron primero dentro de los bacteriófagos (T4 y lambda), virus que infectan a la bacteria Escherichia coli. Las mutaciones en los genes virales debilitaron su capacidad infecciosa, a veces creando virus que podían infectar y crecer solo dentro de ciertas variedades de E. coli.
Mutaciones ámbar (UAG)
Fueron el primer conjunto de mutaciones sin sentido que se descubrió, aisladas por Richard H. Epstein y Charles Steinberg y nombradas en honor a su amigo y estudiante graduado de Caltech Harris Bernstein, cuyo apellido significa "ámbar" en alemán (cf. Bernstein).
Los virus con mutaciones ámbar se caracterizan por su capacidad para infectar solo ciertas cepas de bacterias, conocidas como supresores ámbar. Estas bacterias portan su propia mutación que permite una recuperación de la función en los virus mutantes. Por ejemplo, una mutación en el ARNt que reconoce el codón de terminación ámbar permite que la traducción "lea completamente" el codón y producir una proteína de longitud completa, recuperando así la forma normal de la proteína y "suprimiendo" la mutación ámbar. Por lo tanto, los mutantes ámbar son una clase completa de mutantes de virus que pueden crecer en bacterias que contienen mutaciones supresoras de ámbar. También se conocen supresores similares para los codones de terminación ocre y ópalo.
Se han diseñado moléculas de ARNt que contienen aminoácidos no naturales para reconocer el codón de terminación ámbar en el ARN bacteriano. Esta tecnología permite la incorporación de aminoácidos ortogonales (como p-azidofenilalanina) en ubicaciones específicas de la proteína diana.
Mutaciones ocres (UAA)
Fue la segunda mutación del codón de terminación que se descubrió. Con reminiscencias del color amarillo-naranja-marrón habitual asociado con el ámbar, este segundo codón de parada recibió el nombre de "ocre, un pigmento mineral naranja-marrón rojizo.
Los virus mutantes ocre tenían una propiedad similar a los mutantes ámbar en el sentido de que recuperaban la capacidad infecciosa dentro de ciertas cepas supresoras de bacterias. El conjunto de supresores de ocre era distinto de los supresores de ámbar, por lo que se infirió que los mutantes de ocre correspondían a un triplete de nucleótidos diferente. A través de una serie de experimentos de mutación que compararon estos mutantes entre sí y con otros codones de aminoácidos conocidos, Sydney Brenner concluyó que las mutaciones ámbar y ocre correspondían a los tripletes de nucleótidos "UAG" y "UAA".
Mutaciones de ópalo o ámbar (UGA)
El tercer y último codón de terminación en el código genético estándar se descubrió poco después y corresponde al triplete de nucleótidos "UGA".
Para continuar con el tema de los minerales coloreados, el tercer codón sin sentido se conoció como "ópalo", que es un tipo de sílice que muestra una variedad de colores. Las mutaciones sin sentido que crearon este codón de parada prematuro se denominaron más tarde mutaciones de ópalo o mutaciones de ámbar.
Mutaciones y enfermedades
Tonterías
Las mutaciones sin sentido son cambios en la secuencia de ADN que introducen un codón de parada prematuro, lo que hace que cualquier proteína resultante se acorte de forma anormal. Esto a menudo provoca una pérdida de función en la proteína, ya que las partes críticas de la cadena de aminoácidos ya no se ensamblan. Debido a esta terminología, los codones de parada también se conocen como codones sin sentido.
Sin parar
Una mutación continua, también llamada variante de pérdida limitada, es una mutación puntual que ocurre dentro de un codón de parada. Las mutaciones continuas provocan la traducción continua de una cadena de ARNm en lo que debería ser una región no traducida. La mayoría de los polipéptidos resultantes de un gen con una mutación continua pierden su función debido a su longitud extrema y al impacto en el plegamiento normal. Las mutaciones continuas se diferencian de las mutaciones sin sentido en que no crean un codón de parada, sino que lo eliminan. Las mutaciones continuas también difieren de las mutaciones sin sentido, que son mutaciones puntuales en las que se cambia un solo nucleótido para provocar el reemplazo por un aminoácido diferente. Las mutaciones continuas se han relacionado con muchas enfermedades hereditarias, incluidos los trastornos endocrinos, las enfermedades oculares y los trastornos del desarrollo neurológico.
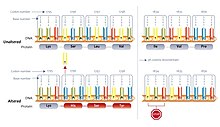
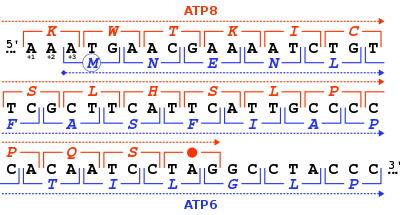
Paradas ocultas
Paradas ocultas son codones sin parada que se leerían como codones de parada si se cambiaran de marco +1 o −1. Estos terminan prematuramente la traducción si el cambio de marco correspondiente (como debido a un deslizamiento de ARN ribosómico) ocurre antes de la parada oculta. Se supone que esto disminuye el desperdicio de recursos en proteínas no funcionales y la producción de citotoxinas potenciales. Investigadores de la Universidad Estatal de Luisiana proponen la hipótesis de la emboscada, en la que se seleccionan paradas ocultas. Los codones que pueden formar paradas ocultas se usan en los genomas con más frecuencia en comparación con los codones sinónimos que, de lo contrario, codificarían el mismo aminoácido. El ARNr inestable en un organismo se correlaciona con una mayor frecuencia de paradas ocultas. Sin embargo, esta hipótesis no pudo ser validada con un conjunto de datos más grande.
Los codones de parada y las paradas ocultas juntas se conocen colectivamente como señales de parada. Investigadores de la Universidad de Memphis encontraron que las proporciones de las señales de parada en los tres marcos de lectura de un genoma (referido como relación de señales de parada de traducción o TSSR) de bacterias genéticamente relacionadas, a pesar de sus grandes diferencias en el contenido de genes, son muy parecidas.. Este valor genómico-TSSR casi idéntico de bacterias genéticamente relacionadas puede sugerir que la expansión del genoma bacteriano está limitada por su sesgo único de señales de parada de esa especie bacteriana.
Lectura traslacional
Lasupresión del codón de parada o lectura traslacional se produce cuando, en la traducción, un codón de parada se interpreta como un codón de sentido, es decir, cuando un aminoácido (estándar) es &# 39;codificado' por el codón de parada. Los ARNt mutados pueden ser la causa de la lectura completa, pero también ciertos motivos de nucleótidos cercanos al codón de terminación. La lectura traslacional es muy común en virus y bacterias, y también se ha encontrado como un principio regulador de genes en humanos, levaduras, bacterias y drosófilas. Este tipo de lectura traduccional endógena constituye una variación del código genético, porque un codón de parada codifica un aminoácido. En el caso de la malato deshidrogenasa humana, el codón de parada se lee con una frecuencia de alrededor del 4%. El aminoácido insertado en el codón de parada depende de la identidad del propio codón de parada: se han encontrado Gln, Tyr y Lys para los codones UAA y UAG, mientras que Cys, Trp y Arg para el codón UGA se han identificado por masa espectrometría La extensión de la lectura en los mamíferos tiene extensiones muy variables y puede diversificar ampliamente el proteoma y afectar la progresión del cáncer.
Usar como marca de agua
En 2010, cuando Craig Venter dio a conocer la primera célula reproductiva completamente funcional controlada por ADN sintético, describió cómo su equipo usaba codones de parada frecuentes para crear marcas de agua en el ARN y el ADN para ayudar a confirmar que los resultados eran realmente sintéticos (y no contaminados o de otra manera).), utilizándolo para codificar los autores' nombres y direcciones de sitios web.
Contenido relacionado
Hélice alfa
Regulación alostérica
Caballito del diablo