Cloruro de aluminio
El
Cloruro de aluminio, también conocido como tricloruro de aluminio, es un compuesto inorgánico con la fórmula AlCl3. Forma un hexahidrato con la fórmula [Al(H2O)6]Cl3, que contiene seis moléculas de agua de hidratación. Tanto la forma anhidra como el hexahidrato son cristales incoloros, pero las muestras suelen estar contaminadas con cloruro de hierro (III), lo que les da un color amarillo.
La forma anhidra es importante comercialmente. Tiene un bajo punto de fusión y ebullición. Se produce y consume principalmente en la producción de aluminio metálico, pero también se utilizan grandes cantidades en otras áreas de la industria química. El compuesto se cita a menudo como ácido de Lewis. Es un ejemplo de un compuesto inorgánico que cambia reversiblemente de polímero a monómero a una temperatura suave.
Estructura
Anhidro

AlCl3 adopta tres estructuras, dependiendo de la temperatura y el estado (sólido, líquido, gas). El AlCl3 sólido tiene una estructura en capas similar a una lámina con iones de cloruro cúbicos muy compactos. En este marco, los centros de Al exhiben una geometría de coordinación octaédrica. El cloruro de itrio (III) adopta la misma estructura, al igual que muchos otros compuestos. Cuando el tricloruro de aluminio está en estado fundido, existe como el dímero Al2Cl6, con aluminio tetracoordinado. Este cambio de estructura está relacionado con la menor densidad de la fase líquida (1,78 g/cm3) frente al tricloruro de aluminio sólido (2,48 g/cm3). Al2Cl6 dímeros También se encuentran en fase vapor. A temperaturas más altas, el Al2Cl6 Los dímeros se disocian en un monómero AlCl3 plano trigonal, que es estructuralmente análogo al BF3. La masa fundida conduce mal la electricidad, a diferencia de los haluros más iónicos como el cloruro de sodio.
El monómero de cloruro de aluminio pertenece al grupo puntual D3h en su forma monomérica y D2h en su forma dimérica.
Hexahidrato
El hexahidrato está formado por [Al(H2O)6]3+ centros catiónicos y aniones cloruro (Cl− ) como contraiones. Los enlaces de hidrógeno unen el catión y los aniones. La forma hidratada del cloruro de aluminio tiene una geometría molecular octaédrica, con el ion aluminio central rodeado por seis moléculas de ligando de agua. Al estar coordinadamente saturado, el hidrato tiene poco valor como catalizador en la alquilación de Friedel-Crafts y reacciones relacionadas.
Usos
Alquilación y acilación de arenos
AlCl3 es un catalizador de ácido de Lewis común para las reacciones de Friedel-Crafts, tanto acilaciones como alquilaciones. Los productos importantes son los detergentes y el etilbenceno. Este tipo de reacciones son el principal uso del cloruro de aluminio, por ejemplo, en la preparación de antraquinona (utilizada en la industria de colorantes) a partir de benceno y fosgeno. En la reacción general de Friedel-Crafts, un cloruro de acilo o haluro de alquilo reacciona con un sistema aromático como se muestra:
La reacción de alquilación se utiliza más ampliamente que la reacción de acilación, aunque su práctica es más exigente técnicamente. Para ambas reacciones, el cloruro de aluminio, así como otros materiales y el equipo, deben estar secos, aunque es necesario un poco de humedad para que la reacción se desarrolle. Están disponibles procedimientos detallados para la alquilación y acilación de arenos.
Un problema general con la reacción de Friedel-Crafts es que a veces se requiere el catalizador de cloruro de aluminio en cantidades estequiométricas completas, porque forma complejos fuertemente con los productos. Esta complicación genera en ocasiones una gran cantidad de residuos corrosivos. Por estas y otras razones similares, el uso de cloruro de aluminio ha sido frecuentemente desplazado por las zeolitas.
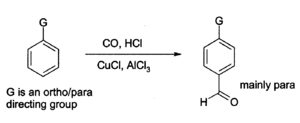
El cloruro de aluminio también se puede utilizar para introducir grupos aldehído en anillos aromáticos, por ejemplo mediante la reacción de Gattermann-Koch que utiliza monóxido de carbono, cloruro de hidrógeno y un cocatalizador de cloruro de cobre(I).
Otras aplicaciones en síntesis orgánica y organometálica
El cloruro de aluminio encuentra una amplia variedad de otras aplicaciones en la química orgánica. Por ejemplo, puede catalizar la reacción eno, como la adición de 3-buten-2-ona (metil vinil cetona) a carvona:
Se utiliza para inducir una variedad de acoplamientos y reordenamientos de hidrocarburos.
El cloruro de aluminio combinado con aluminio en presencia de un areno se puede utilizar para sintetizar complejos metálicos de bis(areno), p.e. bis (benceno) cromo, a partir de ciertos haluros metálicos mediante la síntesis de Fischer-Hafner. La diclorofenilfosfina se prepara mediante la reacción de benceno y tricloruro de fósforo catalizada por cloruro de aluminio.
Reacciones
El cloruro de aluminio anhidro es un poderoso ácido de Lewis, capaz de formar aductos ácido-base de Lewis incluso con bases de Lewis débiles como la benzofenona y el mesitileno. Forma tetracloroaluminato ([AlCl4]− ) en presencia de iones cloruro.
El cloruro de aluminio reacciona con hidruros de calcio y magnesio en tetrahidrofurano formando tetrahidroaluminatos.
Reacciones con el agua
El cloruro de aluminio anhidro es higroscópico y tiene una afinidad muy pronunciada por el agua. Echa humo en el aire húmedo y silba cuando se mezcla con agua líquida cuando los ligandos Cl− se desplazan con moléculas de H2O para formar el hexahidrato [Al(H2O)6]Cl3. La fase anhidra no se puede recuperar calentando el hexahidrato. En cambio, el HCl se pierde dejando hidróxido de aluminio o alúmina (óxido de aluminio):
- [Al(H)2O)6]Cl3 → Al(OH)3 + 3 HCl + 3 H2O
Al igual que los complejos acuosos metálicos, el AlCl3 acuoso es ácido debido a la ionización de los ligandos acuosos.:
- [Al(H)2O)6]3+ [Al(OH)(H)2O)5]2+ + H+
Las soluciones acuosas se comportan de forma similar a otras sales de aluminio que contienen hidratados Al3+ iones, dando un precipitado gelatinoso de hidroxido de aluminio sobre la reacción con diluido hidróxido de sodio:
- AlCl3 + 3 NaOH → Al(OH)3 + 3 NaCl
Síntesis
El cloruro de aluminio se fabrica a gran escala mediante la reacción exotérmica del metal de aluminio con cloro o cloruro de hidrógeno a temperaturas entre 650 y 750 °C (1202 y 1382 °F).
- 2 Al + 3 Cl2 → 2 AlCl3
- 2 Al + 6 HCl → 2 AlCl3 + 3 H2
El cloruro de aluminio se puede formar mediante una única reacción de desplazamiento entre el cloruro de cobre (II) y el aluminio metálico.
- 2 Al + 3 CuCl2 → 2 AlCl3 + 3 Cu
En Estados Unidos en 1993 se produjeron aproximadamente 21.000 toneladas, sin contar las cantidades consumidas en la producción de aluminio.
El tricloruro de aluminio hidratado se prepara disolviendo óxidos de aluminio en ácido clorhídrico. El aluminio metálico también se disuelve fácilmente en ácido clorhídrico, liberando gas hidrógeno y generando un calor considerable. Calentar este sólido no produce tricloruro de aluminio anhidro; el hexahidrato se descompone en hidróxido de aluminio cuando se calienta:
- [Al(H)2O)6]Cl3 → Al(OH)3 + 3 HCl + 3 H2O
El aluminio también forma un cloruro inferior, cloruro de aluminio (I) (AlCl), pero es muy inestable y solo se conoce en la fase de vapor.
Ocurrencia natural
El cloruro de aluminio anhidro no se encuentra como mineral. El hexahidrato, sin embargo, se conoce como el raro mineral cloraluminito. Un mineral de cloruro de aluminio más complejo, básico e hidratado es la cadwaladerita.
Seguridad
El AlCl3 anhidro reacciona vigorosamente con las bases, por lo que se requieren precauciones adecuadas. Puede causar irritación en los ojos, la piel y el sistema respiratorio si se inhala o entra en contacto.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar