Cinamaldehído
Cinnamaldehyde es un compuesto orgánico con la fórmula o C6H5CH=CHCHO. Ocurriendo naturalmente como predominantemente el isómero trans (E), da canela su sabor y olor. Es un fenilpropanoide que es naturalmente sintetizado por la vía shikimate. Este líquido amarillo pálido y viscoso ocurre en la corteza de los árboles de canela y otras especies del género Cinnamomum. El aceite esencial de la corteza de canela es alrededor del 90% de cinnamaldehído. Cinnamaldehyde se descompone a la estireno debido a la oxidación como resultado de malas condiciones de almacenamiento o transporte. Estereno se forma especialmente en alta humedad y altas temperaturas. Esta es la razón por la que la canela contiene pequeñas cantidades de estireno.
Estructura y síntesis
El cinamaldehído fue aislado del aceite esencial de canela en 1834 por Jean-Baptiste Dumas y Eugène-Melchior Péligot y sintetizado en el laboratorio por el químico italiano Luigi Chiozza en 1854.
El producto natural es trans-cinamaldehído. La molécula consta de un anillo de benceno unido a un aldehído insaturado. Como tal, la molécula puede verse como un derivado de la acroleína. Su color se debe a la transición π → π*: una conjugación aumentada en comparación con la acroleína desplaza esta banda hacia lo visible.
Biosíntesis
El cinamaldehído se encuentra ampliamente y compuestos estrechamente relacionados dan lugar a la lignina. Todos estos compuestos se biosintetizan a partir de fenilalanina, que sufre una conversión.
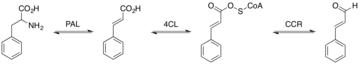
La biosíntesis de cinamaldehído comienza con la desaminación de la L-fenilalanina en ácido cinámico por la acción de la fenilalanina amonialiasa (PAL). PAL cataliza esta reacción mediante una desaminación no oxidativa. Esta desaminación se basa en el grupo protésico MIO de PAL. PAL da lugar al ácido trans-cinámico. En el segundo paso, la 4-cumarato-CoA ligasa (4CL) convierte el ácido cinámico en cinamoil-CoA mediante una ligadura ácido-tiol. 4CL utiliza ATP para catalizar la formación de cinamoil-CoA. 4CL efectúa esta reacción en dos pasos. 4CL forma un anhídrido de hidroxicinamato-AMP, seguido de un ataque nucleófilo al carbonilo del adenilato de acilo. Finalmente, la cinamoil-CoA se reduce mediante NADPH catalizada por CCR (cinamoil-CoA reductasa) para formar cinamaldehído.
Preparación
Existen varios métodos de síntesis de laboratorio, pero el cinamaldehído se obtiene de forma más económica a partir de la destilación al vapor del aceite de corteza de canela. El compuesto se puede preparar a partir de compuestos relacionados como el alcohol cinamílico (la forma alcohólica del cinamaldehído), pero la primera síntesis a partir de compuestos no relacionados fue la condensación aldólica de benzaldehído y acetaldehído; este proceso fue patentado por Henry Richmond el 7 de noviembre de 1950.
Aplicaciones
Como aromatizante
La aplicación más obvia del cinamaldehído es como saborizante en chicles, helados, dulces, líquidos electrónicos y bebidas; Los niveles de uso oscilan entre 9 y 4.900 partes por millón (ppm) (es decir, menos del 0,5%). También se utiliza en algunos perfumes de aromas naturales, dulces o afrutados. Los aromas de almendra, albaricoque, caramelo y otros pueden emplear parcialmente el compuesto por sus agradables olores. El cinamaldehído se puede utilizar como adulterante de alimentos; La cáscara de haya en polvo aromatizada con cinamaldehído se puede comercializar como canela en polvo. Algunos cereales para el desayuno contienen hasta 187 ppm de cinamaldehído.
Como agroquímico
Se ha probado que el cinamaldehído es un insecticida seguro y eficaz contra las larvas de mosquitos. Una concentración de 29 ppm de cinamaldehído mata la mitad de las larvas del mosquito Aedes aegypti en 24 horas. El transcinamaldehído funciona como un potente fumigante y un práctico repelente de mosquitos adultos. También tiene propiedades antibacterianas y antifúngicas.
Usos varios
El cinamaldehído es un inhibidor de la corrosión del acero y otras aleaciones. Se cree que forma una película protectora sobre la superficie del metal.
Derivados
Numerosos derivados del cinamaldehído son comercialmente útiles. El alcohol dihidrocinamílico (3-fenilpropanol) se produce de forma natural, pero se produce mediante doble hidrogenación del cinamaldehído. Tiene fragancias de jacinto y lila. El alcohol cinamílico también se produce de forma natural y tiene olor a lila, pero también se puede producir a partir de cinamaldehído. El dihidrocinamaldehído se produce por hidrogenación selectiva de la subunidad alqueno. La α-amilcinamaldehído y la α-hexilcinamaldehído son fragancias comerciales importantes, pero no se preparan a partir de cinamaldehído. La hidrogenación del cinamaldehído, si se dirige al alqueno, da hidrocinamaldehído.
Toxicología
El cinamaldehído se utiliza en la agricultura debido a su baja toxicidad, pero irrita la piel. El cinamaldehído puede causar estomatitis alérgica de contacto en personas sensibilizadas; sin embargo, se cree que la alergia al compuesto es poco común.
Reparación del ADN
El cinamaldehído es un antimutágeno dietético que inhibe eficazmente las mutaciones tanto inducidas como espontáneas. La evidencia experimental indica que el cinamaldehído induce un tipo de daño en el ADN en la bacteria Escherichia coli y en las células humanas que provoca la reparación recombinacional del ADN que luego reduce las mutaciones espontáneas. En ratones, las aberraciones cromosómicas inducidas por rayos X se redujeron cuando se les administró cinamaldehído por vía oral después de la irradiación con rayos X, tal vez debido a la reparación del ADN estimulada por cinamaldehído.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar
