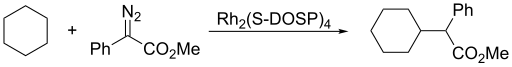Carbeno

En química orgánica, un carbeno es una molécula que contiene un átomo de carbono neutro con una valencia de dos y dos electrones de valencia no compartidos. La fórmula general es R−:C−R' o R=C: donde R representa sustituyentes o átomos de hidrógeno.
El término "carbeno" También puede referirse al compuesto específico :CH2, también llamado metileno, el hidruro original del que se originan todos otros compuestos de carbeno se derivan formalmente. Los carbenos se clasifican en singletes o tripletes, según su estructura electrónica. La mayoría de los carbenos tienen una vida muy corta, aunque se conocen carbenos persistentes. Un carbeno bien estudiado es el diclorocarbeno Cl2C:, que se puede generar in situ. de cloroformo y una base fuerte.
Estructuras y unión

Las dos clases de carbenos son carbenos singletes y tripletes. Los carbenos singlete tienen pares de espines. En el lenguaje de la teoría del enlace de valencia, la molécula adopta una estructura híbrida sp2. Los carbenos tripletes tienen dos electrones desapareados. La mayoría de los carbenos tienen un estado fundamental triplete no lineal, excepto aquellos con sustituyentes de nitrógeno, oxígeno o azufre y haluros unidos al carbono divalente. Los sustituyentes que pueden donar pares de electrones pueden estabilizar el estado singlete deslocalizando el par en un orbital p vacío. Si la energía del estado singlete se reduce lo suficiente, en realidad se convertirá en el estado fundamental.
Los ángulos de enlace son de 125 a 140° para el metileno triplete y de 102° para el metileno singlete (según lo determinado por EPR).
En el caso de los hidrocarburos simples, los carbenos tripletes suelen ser 8 kcal/mol (33 kJ/mol) más estables que los carbenos singlete. La estabilización se atribuye en parte a la regla de máxima multiplicidad de Hund.
Las estrategias para estabilizar los carbenos tripletes son difíciles de alcanzar. Se ha demostrado que el carbeno llamado 9-fluorenilideno es una mezcla que se equilibra rápidamente de estados singlete y triplete con una diferencia de energía de aproximadamente 1,1 kcal/mol (4,6 kJ/mol). Sin embargo, es discutible si los diarilcarbenos como el fluoreno carbeno son verdaderos carbenos porque los electrones pueden deslocalizarse hasta tal punto que en realidad se convierten en birradicales. Los experimentos in silico sugieren que los carbenos tripletes pueden estabilizarse termodinámicamente con heteroátomos electropositivos, como en los sililo y sililoxicarbenos, especialmente los trifluorosililcarbenos.
Reactividad

Los carbenos singlete y triplete exhiben reactividad divergente. Los carbenos singletes generalmente participan en reacciones queletrópicas como electrófilos o nucleófilos. Los carbenos singlete con orbital p vacío deben ser electrófilos. Los carbenos tripletes pueden considerarse dirradicales y participan en adiciones radicales escalonadas. Los carbenos tripletes tienen que pasar por un intermedio con dos electrones desapareados, mientras que los carbenos singletes pueden reaccionar en un solo paso concertado.
Debido a estos dos modos de reactividad, las reacciones del metileno singlete son estereoespecíficas, mientras que las del metileno triplete son estereoselectivas. Esta diferencia se puede utilizar para investigar la naturaleza de un carbeno. Por ejemplo, la reacción del metileno generado a partir de la fotólisis del diazometano con cis-2-buteno o con trans-2-buteno da cada uno un único diastereómero del 1,2- producto dimetilciclopropano: cis de cis y trans de trans, lo que demuestra que el metileno es un singlete. Si el metileno fuera un triplete, no se esperaría que el producto dependiera de la geometría del alqueno inicial, sino más bien de una mezcla casi idéntica en cada caso.
La reactividad de un carbeno particular depende de los grupos sustituyentes. Su reactividad puede verse afectada por los metales. Algunas de las reacciones que pueden realizar los carbenos son inserciones en enlaces C-H, reordenamientos esqueléticos y adiciones a dobles enlaces. Los carbenos se pueden clasificar en nucleofílicos, electrófilos o ambífilos. Por ejemplo, si un sustituyente puede donar un par de electrones, lo más probable es que el carbeno no sea electrófilo. Los alquilcarbenos se insertan mucho más selectivamente que el metileno, que no diferencia entre enlaces C-H primarios, secundarios y terciarios.
Ciclopropanación
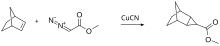
Los carbenos se añaden a los dobles enlaces para formar ciclopropanos. Existe un mecanismo concertado para los carbenos singlete. Los carbenos tripletes no retienen la estereoquímica en la molécula del producto. Las reacciones de adición suelen ser muy rápidas y exotérmicas. El paso lento en la mayoría de los casos es la generación de carbeno. Un reactivo bien conocido empleado para reacciones de alqueno a ciclopropano es el reactivo de Simmons-Smith. Este reactivo es un sistema de cobre, zinc y yodo, donde se cree que el reactivo activo es yoduro de yodometilzinc. El reactivo forma complejos con grupos hidroxi de modo que la adición comúnmente ocurre sin tal grupo.
Inserción C—H

Las inserciones son otro tipo común de reacciones de carbeno. Básicamente, el carbeno se interpone en un enlace existente. El orden de preferencia suele ser:
- X-H bonos donde X no es carbono
- C-H bond
- C-C bono.
Las inserciones pueden ocurrir o no en un solo paso.
Las reacciones de inserción intramolecular presentan nuevas soluciones sintéticas. Generalmente, las estructuras rígidas favorecen que se produzcan tales inserciones. Cuando es posible una inserción intramolecular, no se observan inserciones intermoleculares. En estructuras flexibles, se prefiere la formación de anillos de cinco miembros a la formación de anillos de seis miembros. Tanto las inserciones intermoleculares como las intramoleculares se pueden modificar para la inducción asimétrica eligiendo ligandos quirales en centros metálicos.
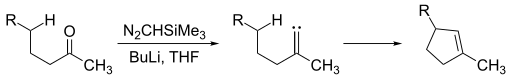
Los alquilideno carbenos son atractivos porque ofrecen la formación de fracciones de ciclopenteno. Para generar un alquiliden carbeno, se puede exponer una cetona a trimetilsilil diazometano.
Dimerización del carbeno

Los carbenos y sus precursores carbenoides pueden sufrir reacciones de dimerización para formar alquenos. Si bien esto suele ser una reacción secundaria no deseada, se puede emplear como herramienta sintética y se ha utilizado una dimerización directa de carbeno metálico en la síntesis de polialquiniletenos.
Los carbenos persistentes existen en equilibrio con sus respectivos dímeros. Esto se conoce como equilibrio de Wanzlick.
Ligandos de carbeno en química organometálica
En especies organometálicas, los complejos metálicos con las fórmulas LnMCRR' a menudo se describen como complejos de carbeno. Sin embargo, estas especies no reaccionan como los carbenos libres y rara vez se generan a partir de precursores de carbeno, excepto los carbenos persistentes. Los complejos de carbeno de metales de transición se pueden clasificar según su reactividad, siendo las dos primeras clases las más claramente definidas:
- Fischer carbenes, en el que el carbeno está unido a un metal que lleva un grupo de electrones que se retira (generalmente un carbonilo). En tales casos el carbono carbenoide es levemente electrofílico.
- Los carbenos Schrock, en los que el carbeno está unido a un metal que lleva un grupo electron-donante. En tales casos el carbono carbenoide es nucleófilo y se asemeja a Reactivo Wittig (que no se consideran derivados del carbeno).
- Los radicales de Carbene, en los que el carbeno está unido a un metal de hoja abierta con el carbono carbeno que posee un carácter radical. Los radicales de Carbene tienen características de ambos carbenes Fischer y Schrock, pero son típicamente intermediarios de reacción de larga duración.

- Los carbenos heterocíclicos (NHC) se derivan de sales de Iidazolium o dihidroimidazolium de deprotonación C. A menudo se implementan como ligandos auxiliares en química organometállica. Tales carbenos son ligandos de espectador que son generalmente donantes de sigma muy fuertes, a menudo haciendo comparaciones con fosfinas. Los mismos ligandos, especialmente cuando están aislados libres del metal, son a veces conocidos como Arduengo o Wanzlick carbenes.
Generación de carbenos
- Un método que es ampliamente aplicable a la síntesis orgánica es la eliminación inducida de los halides de gem-dihalides que emplean reactivos organolito. Queda incierto si bajo estas condiciones se forman carbenos libres o complejo metal-carbeno. Sin embargo, estos metallocarbenes (o carbenoides) dan los productos orgánicos esperados.
- R2CBr2 + BuLi → R2CLi(Br) + BuBr
- R2CLi(Br) → R2C + LiBr
- Para ciclopropanaciones, el zinc se emplea en la reacción Simmons-Smith. En un caso especializado pero instructivo, los compuestos alfa-halomercury pueden ser aislados y separados termolizados. Por ejemplo, el reactivo "Seyferth" libera CCl2 sobre calefacción.
- C6H5HgCCl3 → CCl2 + C6H5HgCl
- Más comúnmente, los carbenos se generan a partir de diazoalkanes, a través de rutas fotolíticas, térmicas o transitorias metálicas. Los catalizadores suelen presentar rodio y cobre. La reacción Bamford-Stevens da carbenos en disolventes apáticos y iones de carbenio en disolventes proticos.
- Eliminación inducida por la base HX de haloformes (CHX3) en condiciones de transmisión de fase.
- También se puede emplear fotolisis de diazirinas y epoxidas. Las diazinas son formas cíclicas de diazoalkanes. La tensión del anillo pequeño hace que la fotoexcitación sea fácil. La fotolisis de epoxidas da compuestos de carbono como productos secundarios. Con epoxidos asimétricos, dos compuestos de carbono diferentes pueden formar potencialmente. La naturaleza de los sustitutos generalmente favorece la formación de uno sobre el otro. Uno de los bonos C-O tendrá un mayor doble carácter de unión y por lo tanto será más fuerte y menos probable que se rompan. Se pueden dibujar estructuras de resonancia para determinar qué parte contribuirá más a la formación de carbonilo. Cuando un sustituto es alquil y otro aryl, el carbono sustituido por aryl es generalmente liberado como un fragmento de carbeno.
- Los carbenos son intermediarios en la reorganización de Wolff
Aplicaciones de los carbenos
Una aplicación a gran escala de los carbenos es la producción industrial de tetrafluoroetileno, el precursor del teflón. El tetrafluoroetileno se genera mediante la intermediación del difluorocarbeno:
- CHClF2 → CF2 + HCl
- 2 CF2 → F2C=CF2
La inserción de carbenos en enlaces C-H se ha explotado ampliamente, p. la funcionalización de materiales poliméricos y el electrocurado de adhesivos. Las aplicaciones se basan en 3-aril-3-trifluorometildiazirinas sintéticas, un precursor de carbeno que puede activarse mediante calor, luz o voltaje.
Historia
Los carbenos fueron postulados por primera vez por Eduard Buchner en 1903 en estudios de ciclopropanación de diazoacetato de etilo con tolueno. En 1912, Hermann Staudinger también convirtió alquenos en ciclopropanos con diazometano y CH2 como intermediario. Doering en 1954 demostró la utilidad sintética del diclorocarbeno.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar