Borohidruro de sodio
borohidruro de sodio, también conocido como tetrahidridoborato de sodio y tetrahidroborato de sodio, es un compuesto inorgánico con la fórmula NaBH4 (a veces escrito como Na[BH4]). Es un sólido cristalino blanco, que generalmente se encuentra como una solución básica acuosa. El borohidruro de sodio es un agente reductor que encuentra aplicación en las industrias de fabricación de papel y tintes. También se utiliza como reactivo en síntesis orgánica.
El compuesto fue descubierto en la década de 1940 por H. I. Schlesinger, quien dirigió un equipo buscando compuestos volátiles de uranio. Los resultados de esta investigación en tiempos de guerra fueron desclasificados y publicados en 1953.
Propiedades
El compuesto es soluble en alcoholes, ciertos éteres y agua, aunque se hidroliza lentamente.
| Solvent | Solubilidad (g/(100 mL)) |
|---|---|
| CH3OH | 13 |
| CH3CH2OH | 3.16 |
| Diglyme | 5.15 |
| (CH3CH2)2O | insoluble |
El borohidruro de sodio es un polvo microcristalino inodoro de color blanco a blanco grisáceo que a menudo forma grumos. Puede purificarse mediante recristalización en diglima tibia (50 °C). El borohidruro de sodio es soluble en disolventes próticos como el agua y los alcoholes inferiores. También reacciona con estos disolventes próticos para producir H2; sin embargo, estas reacciones son bastante lentas. La descomposición completa de una solución de metanol requiere casi 90 min a 20 °C. Se descompone en soluciones acuosas neutras o ácidas, pero es estable a pH 14.
Estructura
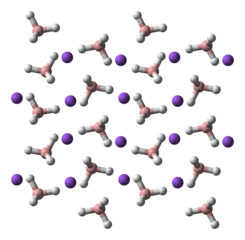
NaBH4 es una sal que consiste en el anión tetraédrico [BH4]-. Se sabe que el sólido existe en tres polimorfos: α, β y γ. La fase estable a temperatura y presión ambiente es α-NaBH4, que es cúbica y adopta una estructura tipo NaCl, en el grupo espacial Fm3m. A una presión de 6,3 GPa, la estructura cambia a tetragonal β-NaBH4 (grupo espacial P421c) y a 8,9 GPa, el ortorrómbico γ-NaBH 4 (grupo espacial Pnma) se convierte en el más estable.
- α-NaBH4
- β-NaBH4
- γ-NaBH4
Síntesis y manipulación
Para la producción comercial de NaBH4, el proceso Brown-Schlesinger y el proceso Bayer son los más métodos populares. En el proceso Brown-Schlesinger, el borohidruro de sodio se prepara industrialmente a partir de hidruro de sodio (producido mediante la reacción de Na y H2) y borato de trimetilo a 250-270 °C:
- B(OCH3)3 + 4 NaH → NaBH4 + 3 NaOCH3
Anualmente se producen millones de kilogramos, superando con creces los niveles de producción de cualquier otro agente reductor de hidruro. En el proceso Bayer, se produce a partir de boratos inorgánicos, incluido el vidrio de borosilicato y el bórax (Na2B4O7):
- Na2B4O7 + 16 Na + 8 H2 + 7 SiO2 → 4 NaBH4 + 7 Na2SiO3
El magnesio es un reductor menos costoso y, en principio, podría usarse en su lugar:
- 8 MgH2 + Na2B4O7 + Na2CO3 → 4 NaBH4 + 8 MgO + CO2
y
- 2 MgH2 + NaBO2 → NaBH4 + 2 MgO
Reactividad
Síntesis orgánica
NaBH4 reduce muchos carbonilos orgánicos, según las condiciones. Por lo general, se utiliza en el laboratorio para convertir cetonas y aldehídos en alcoholes. Estas reducciones se desarrollan en dos etapas, formación del alcóxido seguida de hidrólisis:
- NaBH4 + 4 R2C=O → NaO−CHR2 + B(O−CHR2)3
- NaOCHR2 + B(O−CHR2)3 + 4 H2O → 4 HO−CHR2 + NaOH + B(OH)3
También reduce eficientemente los cloruros de acilo, anhídridos, α-hidroxilactonas, tioésteres e iminas a temperatura ambiente o inferior. Reduce los ésteres de forma lenta e ineficaz con exceso de reactivo y/o temperaturas elevadas, mientras que los ácidos carboxílicos y las amidas no se reducen en absoluto.
Sin embargo, un alcohol, a menudo metanol o etanol, es generalmente el solvente de elección para las reducciones de borohidrido sodio de cetonas y aldehídos. El mecanismo de reducción de la cetona y el aldehído ha sido analizado por estudios cinéticos, y contrariamente a las representaciones populares en libros de texto, el mecanismo no implica un estado de transición de 4 miembros como hidroboración de alkene, o un estado de transición de seis miembros que implica una molécula del solvente de alcohol. Se requiere activación de la unión de hidrógeno, ya que no se produce reducción en un solvente apático como el diglyme. Sin embargo, la orden de tarifas en alcohol es 1.5, mientras que el compuesto de carbono y el borohydride son ambos de primera orden, sugiriendo un mecanismo más complejo que uno que implica un estado de transición de seis miembros que incluye sólo una molécula de alcohol. Se sugirió que la activación simultánea del compuesto de carbono y el borohídrido se produce, a través de la interacción con el alcohol y el ión alkoxide, respectivamente, y que la reacción procede a través de un estado de transición abierto.
Las cetonas α,β-insaturadas tienden a reducirse con NaBH4 en un 1,4 -sentido, aunque a menudo se forman mezclas. La adición de cloruro de cerio mejora la selectividad para la reducción 1,2 de cetonas insaturadas (reducción de Luche). Los ésteres α,β-insaturados también sufren una reducción 1,4 en presencia de NaBH4.
El sistema NaBH4-MeOH, formado por la adición de metanol a borohidruro de sodio en reflujo. THF, reduce los ésteres a los alcoholes correspondientes. Mezclar agua o un alcohol con el borohidruro convierte una parte en éster de hidruro inestable, que es más eficiente en la reducción, pero el reductor finalmente se descompone espontáneamente para producir gas hidrógeno y boratos. La misma reacción también puede ocurrir intramolecularmente: un α-cetoéster se convierte en un diol, ya que el alcohol producido ataca al borohidruro para producir un éster del borohidruro, que luego reduce el éster vecino.
La reactividad de NaBH4 se puede mejorar o aumentar mediante una variedad de compuestos.
Muchos aditivos para modificar la reactividad de borohídrido sodio se han desarrollado como se indica en el siguiente listado incompleto.
| aditivo | aplicaciones sintéticas | página en Smith y marzo | comentario |
|---|---|---|---|
| AlCl3 | reducción de cetonas al metileno | 1837 | |
| BiCl3 | convierte epoxidas a alcoholes allílicos | 1316 | |
| (C6H5Te)2 | reducción de nitroarenes | 1862 | |
| CeCl3 | reducción de cetonas en presencia de aldehídos | 1794 | Luche reduction |
| CoCl2 | reducción de las azides a las minas | 1822 | |
| InCl3 | Hidrogenolisis de bromides alquiles, doble reducción de cetonas insaturadas | 1825, 1793 | |
| LiCl | óxidos de amina a las minas | 1846 | Lithium borohydride |
| NiCl2 | desoxigenación de sulfoxidas, hidrogenolisis de arilos, desulfuración, reducción de nitriles | 1851,1831, 991, 1814 | nickel boride |
| TiCl4 | denitrosatación de nitrosaminas | 1823 | |
| ZnCl2 | reducción de aldehídos | 1793 | |
| ZrCl4 | reducción de los desulfidos, reducción de las cejas a las minas, escote de éteres de arilo | 1853, 1822, 582 |
Oxidación
La oxidación con yodo en tetrahidrofurano produce borano-tetrahidrofurano, que puede reducir los ácidos carboxílicos a alcoholes.
La oxidación parcial del borohidruro con yodo da octahidrotriborato:
- 3 [BH4]− + I2 [B]3H8]− + 2 H2 + 2 I−
Química de coordinación
[BH4]− es un ligando para iones metálicos. Estos complejos de borohidruro a menudo se preparan mediante la acción de NaBH4 (o el LiBH4) en el haluro metálico correspondiente. Un ejemplo es el derivado del titanoceno:
- 2 (C5H5)2TiCl2 + 4 NaBH4 → 2 (C)5H5)2TiBH4 + 4 NaCl + B2H6 + H2
Protonólisis e hidrolisis
NaBH4 reacciona con agua y alcoholes, con la evolución del gas de hidrógeno y la formación del borate correspondiente, la reacción es especialmente rápida a bajo pH. Explorando esta reactividad, el borohídrido de sodio ha sido estudiado como prototipos de la célula de combustible de borohídrido directo.
- NaBH4 + 2 H2O → NaBO2 + 4 H2 (ΔH 0)
Aplicaciones
Fabricación de papel
La aplicación dominante del borohidruro de sodio es la producción de ditionito de sodio a partir de dióxido de azufre: el ditionito de sodio se utiliza como agente blanqueador para la pulpa de madera y en la industria del teñido.
Se ha probado como pretratamiento para la fabricación de pulpa de madera, pero es demasiado costoso para comercializarlo.
Síntesis química
El borohidruro de sodio reduce los aldehídos y las cetonas para dar los alcoholes relacionados. Esta reacción se utiliza en la producción de varios antibióticos, incluidos cloranfenicol, dihidroestreptomicina y tiofenicol. Se preparan varios esteroides y vitamina A utilizando borohidruro de sodio en al menos un paso.
Aplicaciones de nicho o abandonadas
El borohidruro de sodio se ha considerado como una forma de almacenar hidrógeno para vehículos impulsados por hidrógeno, ya que es más seguro (es estable en aire seco) y más eficiente en términos de peso que la mayoría de las otras alternativas. El hidrógeno puede liberarse mediante simple hidrólisis del borohidruro. Sin embargo, tal uso necesitaría un proceso barato, relativamente simple y energéticamente eficiente para reciclar el producto de la hidrólisis, el metaborato de sodio, de nuevo al borohidruro. En 2007 no se disponía de ningún proceso de este tipo.
Aunque no se han alcanzado temperaturas y presiones prácticas para el almacenamiento de hidrógeno, en 2012 se utilizó una nanoestructura núcleo-cubierta de borohidruro de sodio para almacenar, liberar y reabsorber hidrógeno en condiciones moderadas.
Conservadores/restauradores profesionales cualificados han utilizado borohidruro de sodio para minimizar o revertir la decoloración en libros y documentos antiguos.
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar