Aspartato transaminasa
Aspartato transaminasa (AST) o aspartato aminotransferasa, también conocida como AspAT/ASAT/AAT o < b>transaminasa glutámico oxalacética (suero) (GOT, SGOT), es una enzima transaminasa dependiente de piridoxal fosfato (PLP) (EC 2.6.1.1) que fue descrita por primera vez por Arthur Karmen y colegas en 1954. La AST cataliza la transferencia reversible de un grupo α-amino entre aspartato y glutamato y, como tal, es una enzima importante en el metabolismo de los aminoácidos. La AST se encuentra en el hígado, el corazón, el músculo esquelético, los riñones, el cerebro, los glóbulos rojos y la vesícula biliar. El nivel sérico de AST, el nivel sérico de ALT (alanina transaminasa) y su relación (relación AST/ALT) se miden comúnmente clínicamente como biomarcadores de la salud del hígado. Las pruebas son parte de los paneles de sangre.
La vida media de la AST total en la circulación se aproxima a 17 horas y, en promedio, a 87 horas para la AST mitocondrial. La aminotransferasa es eliminada por las células sinusoidales del hígado.
Función
La aspartato transaminasa cataliza la interconversión de aspartato y α-cetoglutarato en oxaloacetato y glutamato.
L-aspartato (Asp) + α-cetoglutarato ↔ oxaloacetato + L-glutamato (Glu)
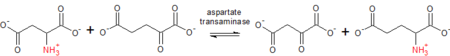
Como transaminasa prototípica, la AST depende de la PLP (vitamina B6) como cofactor para transferir el grupo amino del aspartato o glutamato al cetoácido correspondiente. En el proceso, el cofactor se desplaza entre PLP y la forma de fosfato de piridoxamina (PMP). La transferencia de grupos amino catalizada por esta enzima es crucial tanto en la degradación como en la biosíntesis de aminoácidos. En la degradación de aminoácidos, tras la conversión del α-cetoglutarato en glutamato, el glutamato sufre posteriormente una desaminación oxidativa para formar iones de amonio, que se excretan como urea. En la reacción inversa, el aspartato se puede sintetizar a partir de oxalacetato, que es un intermediario clave en el ciclo del ácido cítrico.
Isoenzimas
Dos isoenzimas están presentes en una amplia variedad de eucariotas. Inhumanos:
- GOT1/cAST, la isoenzima citosólica se deriva principalmente de los glóbulos rojos y el corazón.
- GOT2/mAST, la isoenzima mitocondrial está presente predominantemente en el hígado.
Se cree que estas isoenzimas evolucionaron a partir de una AST ancestral común mediante la duplicación de genes y comparten una homología de secuencia de aproximadamente el 45 %.
También se ha encontrado AST en varios microorganismos, incluido E. coli, H. mediterranei y T. thermophilus. En E. coli, la enzima está codificada por el gen aspC y también se ha demostrado que exhibe la actividad de una transaminasa de aminoácidos aromáticos (EC 2.6.1.57).
Estructura

Se han realizado estudios de cristalografía de rayos X para determinar la estructura de la aspartato transaminasa de diversas fuentes, incluidas las mitocondrias de pollo, el citosol de corazón de cerdo y E. coli. En general, la estructura polipeptídica tridimensional de todas las especies es bastante similar. La AST es dimérica y consta de dos subunidades idénticas, cada una con aproximadamente 400 residuos de aminoácidos y un peso molecular de aproximadamente 45 kD. Cada subunidad está compuesta por un dominio grande y uno pequeño, así como un tercer dominio que consta de los residuos N-terminales 3-14; Estos pocos residuos forman una hebra que une y estabiliza las dos subunidades del dímero. El dominio grande, que incluye los residuos 48-325, une el cofactor PLP mediante un enlace aldimina al grupo ε-amino de Lys258. Otros residuos en este dominio (Asp 222 y Tyr 225) también interactúan con el PLP mediante enlaces de hidrógeno. El dominio pequeño consta de los residuos 15-47 y 326-410 y representa una región flexible que desplaza la enzima de una región "abierta" a una zona "cerrada" conformación tras la unión del sustrato.
Los dos sitios activos independientes están ubicados cerca de la interfaz entre los dos dominios. Dentro de cada sitio activo, un par de residuos de arginina son responsables de la especificidad de la enzima por los sustratos del ácido dicarboxílico: Arg386 interactúa con el grupo carboxilato (α-) proximal del sustrato, mientras que Arg292 forma complejos con el grupo distal (lateral). cadena) carboxilato.
En términos de estructura secundaria, AST contiene elementos α y β. Cada dominio tiene una hoja central de hebras β con hélices α empaquetadas a cada lado.
Mecanismo
La aspartato transaminasa, como ocurre con todas las transaminasas, funciona mediante el reconocimiento de sustrato dual; es decir, es capaz de reconocer y unir selectivamente dos aminoácidos (Asp y Glu) con diferentes cadenas laterales. En cualquier caso, la reacción de las transaminasas consta de dos semirreacciones similares que constituyen lo que se conoce como mecanismo de ping-pong. En la primera media reacción, el aminoácido 1 (p. ej., L-Asp) reacciona con el complejo enzima-PLP para generar el cetoácido 1 (oxalacetato) y la enzima modificada-PMP. En la segunda mitad de la reacción, el cetoácido 2 (α-cetoglutarato) reacciona con la enzima PMP para producir el aminoácido 2 (L-Glu), regenerando la enzima PLP original en el proceso. La formación de un producto racémico (D-Glu) es muy rara.
Los pasos específicos para la semirreacción de Enzima-PLP + aspartato ⇌ Enzima-PMP + oxaloacetato son los siguientes (ver figura); la otra media reacción (no mostrada) se desarrolla de manera inversa, con α-cetoglutarato como sustrato.

- Formación interna de aldimina: En primer lugar, el grupo ε-amino de Lys258 forma un enlace base Schiff con el carbono aldehído para generar una aldimina interna.
- Transaldiminación: La aldimina interna se convierte entonces en una aldimina externa cuando el grupo ε-amino de Lys258 es desplazado por el grupo amino de aspartato. Esta reacción de transaldiminación ocurre a través de un ataque nucleófilo por el grupo amino deprotonado de Asp y procede a través de un intermedio tetraedral. Como este punto, los grupos de carboxilatos de Asp están estabilizados por los grupos de guanidinio de los residuos Arg386 y Arg 292.
- Formación Quinonoides: El hidrógeno adherido al a-carbono de Asp se abstrae (Lys258 se cree que es el aceptor de protones) para formar un intermediario quinononoide.
- Formación de Ketimine: El quinonoide es reprobado, pero ahora en el carbono aldehído, para formar el intermedio de la ketimina.
- Hidrolisis de Ketimina: Finalmente, la ketimina es hidrolizada para formar PMP y oxaloaceta.
Se cree que este mecanismo tiene múltiples pasos que determinan parcialmente la tasa. Sin embargo, se ha demostrado que el paso de unión al sustrato (transaldiminación) impulsa la reacción catalítica.
Importancia clínica
La AST es similar a la alanina transaminasa (ALT) en que ambas enzimas están asociadas con las células del parénquima hepático. La diferencia es que la ALT se encuentra predominantemente en el hígado, con cantidades clínicamente insignificantes en los riñones, el corazón y el músculo esquelético, mientras que la AST se encuentra en el hígado, el corazón (músculo cardíaco), el músculo esquelético, los riñones, el cerebro y el tejido rojo. células de sangre. Como resultado, la ALT es un indicador de inflamación del hígado más específico que la AST, ya que la AST puede estar elevada también en enfermedades que afectan a otros órganos, como el infarto de miocardio, la pancreatitis aguda, la anemia hemolítica aguda, las quemaduras graves, la enfermedad renal aguda, las enfermedades musculoesqueléticas, y trauma.
La AST se definió como un marcador bioquímico para el diagnóstico de infarto agudo de miocardio en 1954. Sin embargo, el uso de AST para dicho diagnóstico ahora es redundante y ha sido reemplazado por las troponinas cardíacas.
Las pruebas de laboratorio siempre deben interpretarse utilizando el rango de referencia del laboratorio que realizó la prueba. A continuación se muestran ejemplos de rangos de referencia:
| Tipo de paciente | Catálogos de referencia |
| Hombre | 8 a 40 UI/L |
| Mujer | 6 a 34 UI/L |
Contenido relacionado
Ley de Fick
Híbrido (biología)
Evolución divergente