Ácido acético (página de datos)
Contenido keyboard_arrow_down
Esta página proporciona datos químicos complementarios sobre ácido acético.
Ficha de datos de seguridad del material
La manipulación de este producto químico puede implicar importantes precauciones de seguridad. Se recomienda encarecidamente que busque la Hoja de datos de seguridad de materiales (MSDS) para este químico de una fuente confiable y siga sus instrucciones.
- PTCL Sitio web de seguridad
- Science Stuff
Estructura y propiedades
| Estructura y propiedades | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Índice de refracción, nD | 1.3716 | ||||||||
| constante dieléctrica, εr | 6.15 ε0 a 20 °C | ||||||||
| Fuerza ósea | ? | ||||||||
| Longitud ósea | ? | ||||||||
| Ángulo de unión | ? | ||||||||
| Susceptibilidad magnética | ? | ||||||||
| Tensión superficial | 26.6 dina/cm a 30 °C | ||||||||
| Viscosidad |
| ||||||||
Propiedades termodinámicas
| Comportamiento de fase | |
|---|---|
| Punto triple | 289.8 K (16.7 °C), ? Pa |
| Punto crítico | 593 K (320 °C), 57.8 bar |
| Punto etico con agua | –26.7 °C |
| Std enthalpy cambio de fusión ΔfusiblesH | +11.7 kJ/mol |
| Cambio de fusión de la entropía Std ΔfusiblesS | 40.5 J/(mol·K) |
| Cambio de vaporización de la enthalpy Std ΔvapH | +23.7 kJ/mol |
| Cambio de vaporización de la entropía Std ΔvapS | ? J/(mol·K) |
| Propiedades sólidas | |
| Cambio de formación enthalpy ΔfH | ? kJ/mol |
| Entropía molar estándar S | ? J/(mol K) |
| Capacidad de calor cp | ? J/(mol K) |
| Propiedades líquidos | |
| Cambio de formación enthalpy ΔfH | 48−3.5 kJ/mol |
| Entropía molar estándar S | 158.0 J/(mol K) |
| Enthalpy de combustión, ΔcH | –876.1 kJ/mol |
| Capacidad de calor cp | 123.1 J/(mol K) |
| Propiedades de gas | |
| Cambio de formación enthalpy ΔfH | –438,1 kJ/mol |
| Entropía molar estándar S | 282.84 J/(mol K) |
| Capacidad de calor cp | 63.4 J/(mol K) |
| constantes de van der Waals | a = 1782.3 L2 kPa/mol2 b = 0,68 litros por topo |
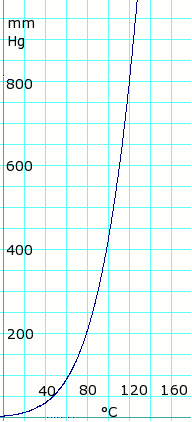
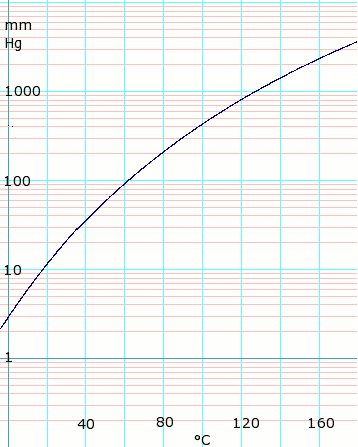
Presión de vapor del líquido
| P en mm Hg | 1 | 10 | 40 | 100 | 400 | 760 | 1520 | 3800 | 7600 | 15200 | 30400 | 45600 | |
| T en °C | –17.2 | 17,5 | 43.0 | 63.0 | 99.0 | 118.1 | 143.5 | 180.3 | 214.0 | 252.0 | 297.0 | — | |
Datos del cuadro obtenidos CRC Manual de Química y Física 44a Ed.
Datos de destilación
| Equilibrio Vapor-liquid para ácido Acético/Water P = 760 mm Hg | ||
| BP Temperatura. °C | % de agua | |
|---|---|---|
| líquido | vapor | |
| 116,5 | 2.2 | 5.8 |
| 114.6 | 5.4 | 12.3 |
| 113.4 | 8.6 | 16.8 |
| 113,5 | 9.9 | 18.3 |
| 113.1 | 10.1 | 18.8 |
| 110.6 | 18.9 | 29.8 |
| 107.8 | 30.3 | 43.3 |
| 106.1 | 41.3 | 54,5 |
| 104,4 | 52.2 | 64.9 |
| 103.1 | 62,4 | 73,5 |
| 102.3 | 69,6 | 79.2 |
| 101.6 | 77.8 | 85.1 |
| 100,8 | 87.6 | 91,4 |
| 100,5 | 92.3 | 94,4 |
| 100.4 | 94,5 | 96.0 |
| 100.1 | 98,5 | 98,9 |
Datos espectrales
| UV-Vis | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| λmax | 207 nm (fase de gas) | ||||||||||||||||||||||||||||||||||||||||
| Coeficiente de extinción, ε | ? | ||||||||||||||||||||||||||||||||||||||||
| IR | |||||||||||||||||||||||||||||||||||||||||
| Principales bandas de absorción |
| ||||||||||||||||||||||||||||||||||||||||
| NMR | |||||||||||||||||||||||||||||||||||||||||
| Proton NMR | δ CDCl3 2.10 (3H), 11.42 (1H) | ||||||||||||||||||||||||||||||||||||||||
| Carbon-13 NMR | δ CDCl3 20.8, 178.1 | ||||||||||||||||||||||||||||||||||||||||
| Otros datos de NMR | |||||||||||||||||||||||||||||||||||||||||
| MS | |||||||||||||||||||||||||||||||||||||||||
| Masas de fragmentos principales | 60 (75%), 45 (90%), 43 (100%), 42 (13%), 15 (17%) | ||||||||||||||||||||||||||||||||||||||||
Contenido relacionado
Ley de Fick
Miscibilidad
Masa molar
Más resultados...