Ligação de hidrogênio
Em química, uma ligação de hidrogênio (ou ligação de H) é uma força de atração principalmente eletrostática entre um átomo de hidrogênio (H) que está ligado covalentemente a um átomo mais eletronegativo "doador" átomo ou grupo (Dn) e outro átomo eletronegativo com um par solitário de elétrons - o aceptor de ligação de hidrogênio (Ac). Tal sistema de interação é geralmente denotado Dn−H···Ac, onde a linha sólida denota uma ligação covalente polar e a linha pontilhada ou tracejada indica a ligação de hidrogênio. Os átomos doadores e receptores mais frequentes são os elementos de segunda linha nitrogênio (N), oxigênio (O) e flúor (F).
As ligações de hidrogênio podem ser intermoleculares (ocorrendo entre moléculas separadas) ou intramoleculares (ocorrendo entre partes da mesma molécula). A energia de uma ligação de hidrogênio depende da geometria, do ambiente e da natureza dos átomos doadores e receptores específicos e pode variar entre 1 e 40 kcal/mol. Isso os torna um pouco mais fortes do que uma interação de van der Waals e mais fracos do que ligações totalmente covalentes ou iônicas. Esse tipo de ligação pode ocorrer em moléculas inorgânicas, como a água, e em moléculas orgânicas, como DNA e proteínas. As pontes de hidrogênio são responsáveis por manter materiais como papel e lã feltrada juntos e por fazer com que folhas de papel separadas grudem umas nas outras após ficarem molhadas e subsequentemente secarem.
A ligação de hidrogênio é responsável por muitas das propriedades físicas e químicas dos compostos de N, O e F que parecem incomuns em comparação com outras estruturas semelhantes. Em particular, a ligação de hidrogênio intermolecular é responsável pelo alto ponto de ebulição da água (100°C) em comparação com os outros hidretos do grupo 16 que possuem ligações de hidrogênio muito mais fracas. A ligação de hidrogênio intramolecular é parcialmente responsável pelas estruturas secundárias e terciárias de proteínas e ácidos nucléicos. Também desempenha um papel importante na estrutura dos polímeros, tanto sintéticos quanto naturais.
Vínculo
Definições e características gerais
Em uma ligação de hidrogênio, o átomo eletronegativo não ligado covalentemente ao hidrogênio é chamado de aceptor de próton, enquanto aquele ligado covalentemente ao hidrogênio é chamado de doador de próton. Embora essa nomenclatura seja recomendada pela IUPAC, no doador de ligação de hidrogênio, o centro H é prótico. O doador é uma base de Lewis. As ligações de hidrogênio são representadas como sistema H···Y, onde os pontos representam a ligação de hidrogênio. Líquidos que exibem ligações de hidrogênio (como a água) são chamados de líquidos associados.
As ligações de hidrogênio surgem de uma combinação de eletrostática (multipolo-multipolo e interações multipolo induzidas por multipolo), covalência (transferência de carga por sobreposição orbital) e dispersão (forças de Londres).
Em ligações de hidrogênio mais fracas, os átomos de hidrogênio tendem a se ligar a elementos como enxofre (S) ou cloro (Cl); mesmo o carbono (C) pode servir como um doador, particularmente quando o carbono ou um de seus vizinhos é eletronegativo (por exemplo, em clorofórmio, aldeídos e acetilenos terminais). Gradualmente, foi reconhecido que existem muitos exemplos de ligações de hidrogênio mais fracas envolvendo doadores diferentes de N, O ou F e/ou aceitador Ac com eletronegatividade próxima à do hidrogênio (em vez de ser muito mais eletronegativa). Embora fraco (≈1 kcal/mol), "não tradicional" interações de ligações de hidrogênio são onipresentes e influenciam estruturas de muitos tipos de materiais.
A definição de ligação de hidrogênio ampliou-se gradualmente ao longo do tempo para incluir essas interações atrativas mais fracas. Em 2011, um Grupo de Trabalho da IUPAC recomendou uma definição moderna baseada em evidências de ligação de hidrogênio, que foi publicada na revista IUPAC Pure and Applied Chemistry. Esta definição especifica:
A ligação de hidrogênio é uma interação atraente entre um átomo de hidrogênio de uma molécula ou um fragmento molecular X-H em que X é mais elétronegativo do que H, e um átomo ou um grupo de átomos na mesma ou outra molécula, em que há evidência de formação de vínculo.
Força de união
As ligações de hidrogênio podem variar em força de fraca (1–2 kJ/mol) a forte (161,5 kJ/mol no íon bifluoreto, HF−2). Entalpias típicas em vapor incluem:
- F-H-H-- Sim. (161,5 kJ/mol ou 38,6 kcal/mol), ilustrado exclusivamente por HF- Sim.2
- - Não. (29 kJ/mol ou 6.9 kcal/mol), ilustrado água-amônia
- O.H. (21 kJ/mol ou 5.0 kcal/mol), água-água ilustrada, álcool-alcool
- Não. (13 kJ/mol ou 3.1 kcal/mol), ilustrado por amônia-amônia
- Não. (8 kJ/mol ou 1,9 kcal/mol), água-amide ilustrada
- Oh!+3·:2 (18 kJ/mol ou 4.3 kcal/mol)
A força das ligações de hidrogênio intermoleculares é mais frequentemente avaliada por medições de equilíbrio entre moléculas contendo unidades doadoras e/ou aceitadoras, mais frequentemente em solução. A força das ligações de hidrogênio intramoleculares pode ser estudada com equilíbrios entre confôrmeros com e sem ligações de hidrogênio. O método mais importante para a identificação de pontes de hidrogênio também em moléculas complicadas é a cristalografia, às vezes também espectroscopia de RMN. Detalhes estruturais, em particular distâncias entre o doador e o receptor que são menores que a soma dos raios de van der Waals, podem ser tomados como indicação da força da ligação de hidrogênio.
Um esquema dá a seguinte classificação um tanto arbitrária: aqueles que são 15 a 40 kcal/mol, 5 a 15 kcal/mol e >0 a 5 kcal/mol são considerados fortes, moderados e fracos, respectivamente.
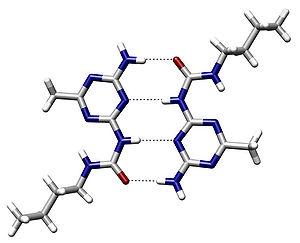
Ponte de hidrogênio assistida por ressonância
A ligação de hidrogênio assistida por ressonância (comumente abreviada como RAHB) é um tipo forte de ligação de hidrogênio. É caracterizada pela deslocalização π que envolve o hidrogênio e não pode ser adequadamente descrita apenas pelo modelo eletrostático. Esta descrição da ligação de hidrogênio foi proposta para descrever distâncias incomumente curtas geralmente observadas entre O=C−OH··· ou ·· ·O=C−C=C−OH.
Detalhes estruturais
A distância X−H é normalmente ≈110 pm, enquanto a distância H···Y é ≈ 160 a 200 horas. O comprimento típico de uma ligação de hidrogênio na água é 197 pm. O ângulo de ligação ideal depende da natureza do doador da ligação de hidrogênio. Os seguintes ângulos de ligação de hidrogênio entre um doador de ácido fluorídrico e vários aceitadores foram determinados experimentalmente:
| Aceitação | Geometria VSEPR | Ângulo (°) |
|---|---|---|
| HCN. | linear linear linear | 180 |
| H. H. H.2CO.H. | Planar de trigo | 120 |
| H. H. H.2O | pirâmide | 46. |
| H. H. H.2S. | pirâmide | 89 |
| Então...2· | trigonometria | 142 |
Espectroscopia
Fortes ligações de hidrogênio são reveladas por deslocamentos de downfield no espectro 1H NMR. Por exemplo, o protão ácido no tautomer enol de acetylacetone aparece em δ δ H. H. H.{displaystyle delta _{text{H}}}15,5, que é cerca de 10 ppm downfield de um álcool convencional.
No espectro IR, a ligação de hidrogênio muda a frequência de alongamento X−H para energia mais baixa (ou seja, a frequência de vibração diminui). Essa mudança reflete um enfraquecimento da ligação X−H. Certas ligações de hidrogênio - ligações de hidrogênio impróprias - mostram um deslocamento para o azul da frequência de alongamento X−H e uma diminuição no comprimento da ligação. H-bonds também podem ser medidos por mudanças de modo vibracional IR do aceitador. O modo amida I dos carbonilos da cadeia principal nas α-hélices muda para frequências mais baixas quando eles formam ligações H com grupos hidroxila da cadeia lateral. A dinâmica das estruturas de ligação de hidrogênio na água pode ser sondada por esta vibração de alongamento OH. Na rede de ligações de hidrogênio em cristais plásticos iônicos orgânicos próticos (POIPCs), que são um tipo de material de mudança de fase exibindo transições de fase sólido-sólido antes da fusão, a espectroscopia de infravermelho de temperatura variável pode revelar a dependência da temperatura das ligações de hidrogênio e a dinâmica de tanto os ânions quanto os cátions. O súbito enfraquecimento das ligações de hidrogênio durante a transição de fase sólido-sólido parece estar associado ao início da desordem de orientação ou rotação dos íons.
Considerações teóricas
A ligação de hidrogênio é de interesse teórico persistente. De acordo com uma descrição moderna O:H−O integra tanto o par solitário O:H intermolecular ":" não-ligante e a ligação covalente polar H-O intramolecular associada ao acoplamento repulsivo O-O.
Cálculos químicos quânticos das constantes de potencial inter-resíduo relevantes (constantes de complacência) revelaram grandes diferenças entre ligações de H individuais do mesmo tipo. Por exemplo, a ligação de hidrogênio N−H···N interresíduo central entre guanina e citosina é muito mais forte em comparação com a ligação N− ligação H···N entre o par adenina-timina.
Teoricamente, a resistência das ligações de hidrogênio pode ser avaliada usando o índice NCI, índice de interações não covalentes, que permite visualizar essas interações não covalentes, como o próprio nome indica, usando a densidade eletrônica do sistema.
A partir de interpretações das anisotropias no perfil Compton do gelo comum que a ligação de hidrogênio é parcialmente covalente. No entanto, essa interpretação foi contestada.
Em geral, a ligação de hidrogênio pode ser vista como um campo escalar eletrostático dependente da métrica entre duas ou mais ligações intermoleculares. Isso é ligeiramente diferente dos estados ligados intramoleculares de, por exemplo, ligações covalentes ou iônicas; no entanto, a ligação de hidrogênio geralmente ainda é um fenômeno de estado ligado, uma vez que a energia de interação tem uma soma líquida negativa. A teoria inicial da ligação de hidrogênio proposta por Linus Pauling sugeria que as ligações de hidrogênio tinham uma natureza covalente parcial. Essa interpretação permaneceu controversa até que as técnicas de RMN demonstraram a transferência de informações entre núcleos ligados por ligações de hidrogênio, uma façanha que só seria possível se a ligação de hidrogênio contivesse algum caráter covalente.
História
O conceito de ligação de hidrogênio já foi desafiador. Linus Pauling credita a T. S. Moore e T. F. Winmill a primeira menção da ligação de hidrogênio, em 1912. Moore e Winmill usaram a ligação de hidrogênio para explicar o fato de que o hidróxido de trimetilamônio é uma base mais fraca que o hidróxido de tetrametilamônio. A descrição da ligação de hidrogênio em seu ambiente mais conhecido, a água, veio alguns anos depois, em 1920, de Latimer e Rodebush. Nesse artigo, Latimer e Rodebush citam o trabalho de um colega cientista de seu laboratório, Maurice Loyal Huggins, dizendo: “Sr. Huggins deste laboratório, em algum trabalho ainda não publicado, usou a ideia de um núcleo de hidrogênio mantido entre dois átomos como uma teoria em relação a certos compostos orgânicos."
Pontes de hidrogênio em pequenas moléculas
Água
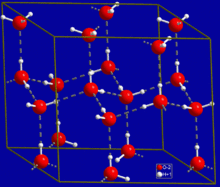
Um exemplo onipresente de ligação de hidrogênio é encontrado entre as moléculas de água. Em uma molécula de água discreta, existem dois átomos de hidrogênio e um átomo de oxigênio. O caso mais simples é um par de moléculas de água com uma ligação de hidrogênio entre elas, que é chamado de dímero de água e é freqüentemente usado como um sistema modelo. Quando mais moléculas estão presentes, como é o caso da água líquida, mais ligações são possíveis porque o oxigênio de uma molécula de água tem dois pares de elétrons isolados, cada um dos quais pode formar uma ligação de hidrogênio com um hidrogênio em outra molécula de água. Isso pode se repetir de forma que cada molécula de água esteja ligada ao H com até quatro outras moléculas, conforme mostrado na figura (duas por meio de seus dois pares solitários e duas por meio de seus dois átomos de hidrogênio). A ligação de hidrogênio afeta fortemente a estrutura cristalina do gelo, ajudando a criar uma rede hexagonal aberta. A densidade do gelo é menor que a densidade da água na mesma temperatura; assim, a fase sólida da água flutua no líquido, ao contrário da maioria das outras substâncias.
O alto ponto de ebulição da água líquida é devido ao alto número de ligações de hidrogênio que cada molécula pode formar, em relação à sua baixa massa molecular. Devido à dificuldade de quebrar essas ligações, a água tem um ponto de ebulição, ponto de fusão e viscosidade muito altos em comparação com líquidos semelhantes não unidos por ligações de hidrogênio. A água é única porque seu átomo de oxigênio tem dois pares solitários e dois átomos de hidrogênio, o que significa que o número total de ligações de uma molécula de água é de até quatro.
O número de pontes de hidrogênio formadas por uma molécula de água líquida varia com o tempo e a temperatura. A partir das simulações de água líquida TIP4P a 25 °C, estimou-se que cada molécula de água participa de uma média de 3,59 ligações de hidrogênio. A 100 °C, esse número diminui para 3,24 devido ao aumento do movimento molecular e diminuição da densidade, enquanto a 0 °C, o número médio de ligações de hidrogênio aumenta para 3,69. Outro estudo encontrou um número muito menor de ligações de hidrogênio: 2,357 a 25°C. No entanto, definir e contar as ligações de hidrogênio não é simples.
Como a água pode formar ligações de hidrogênio com doadores e aceitadores de prótons de soluto, ela pode inibir competitivamente a formação de ligações de hidrogênio intermoleculares ou intramoleculares de soluto. Consequentemente, as ligações de hidrogênio entre ou dentro das moléculas de soluto dissolvidas na água são quase sempre desfavoráveis em relação às ligações de hidrogênio entre a água e os doadores e aceitadores de ligações de hidrogênio nesses solutos. As pontes de hidrogênio entre as moléculas de água têm um tempo de vida médio de 10−11 segundos, ou 10 picossegundos.
Pontes de hidrogênio bifurcadas e sobrecoordenadas na água
Um único átomo de hidrogênio pode participar de duas ligações de hidrogênio, em vez de uma. Este tipo de ligação é chamada de "bifurcada" (dividido em dois ou "duas bifurcações"). Pode existir, por exemplo, em moléculas orgânicas naturais ou sintéticas complexas. Tem sido sugerido que um átomo de hidrogênio bifurcado é um passo essencial na reorientação da água.
As ligações de hidrogênio do tipo aceitador (terminando nos pares solitários de um oxigênio) são mais propensas a formar bifurcação (é chamado de oxigênio supercoordenado, OCO) do que as ligações de hidrogênio do tipo doador, começando nos mesmos hidrogênios do oxigênio.
Outros líquidos
Por exemplo, o fluoreto de hidrogênio - que tem três pares solitários no átomo de F, mas apenas um átomo de H - pode formar apenas duas ligações; (amônia tem o problema oposto: três átomos de hidrogênio, mas apenas um par solitário).
- H. H. H.- Sim. - Sim. F)) )) )) H. H. H.- Sim. - Sim. F)) )) )) H. H. H.- Sim. - Sim. FNão. (H-F**H-F**H-F)}
Outras manifestações de ligação de hidrogênio do solvente
- O aumento do ponto de fusão, ponto de ebulição, solubilidade e viscosidade de muitos compostos podem ser explicados pelo conceito de ligação de hidrogênio.
- Azeotropia negativa de misturas de HF e água.
- O fato de que o gelo é menos denso do que a água líquida é devido a uma estrutura de cristal estabilizada por ligações de hidrogênio.
- Pontos de ebulição dramaticamente maiores NH3, H. H. H.2O, e HF em comparação com os análogos mais pesados PH3, H. H. H.2S, e HCl, onde a ligação a hidrogénio está ausente.
- Viscosidade do ácido fosfórico anidro e do glicerol.
- Formação de Dimer em ácidos carboxílicos e formação de hexamer em fluoreto de hidrogênio, que ocorrem mesmo na fase de gás, resultando em desvios brutos da lei de gás ideal.
- Formação de Pentamer de água e álcool em solventes apolares.
Pontes de hidrogênio em polímeros
A ligação de hidrogênio desempenha um papel importante na determinação das estruturas tridimensionais e das propriedades adotadas por muitas proteínas sintéticas e naturais. Comparado com C−C, C-O e C-N ligações que compreendem a maioria dos polímeros, as ligações de hidrogênio são muito mais fracas, talvez 5%. Assim, as ligações de hidrogênio podem ser quebradas por meios químicos ou mecânicos, mantendo a estrutura básica do esqueleto do polímero. Essa hierarquia de forças de ligação (ligações covalentes sendo mais fortes que as ligações de hidrogênio sendo mais fortes que as forças de van der Waals) é relevante nas propriedades de muitos materiais.
DNA
Nessas macromoléculas, a ligação entre partes da mesma macromolécula faz com que ela se dobre em uma forma específica, o que ajuda a determinar o papel fisiológico ou bioquímico da molécula. Por exemplo, a estrutura de dupla hélice do DNA se deve em grande parte às pontes de hidrogênio entre seus pares de bases (bem como às interações de empilhamento pi), que ligam uma fita complementar à outra e permitem a replicação.
Proteínas
Na estrutura secundária das proteínas, as pontes de hidrogênio se formam entre os oxigênios do esqueleto e os hidrogênios da amida. Quando o espaçamento dos resíduos de aminoácidos que participam de uma ligação de hidrogênio ocorre regularmente entre as posições i e i + 4, um alfa-hélice é formada. Quando o espaçamento é menor, entre as posições i e i + 3, forma-se uma hélice 310. Quando duas fitas são unidas por ligações de hidrogênio envolvendo resíduos alternados em cada fita participante, uma folha beta é formada. As pontes de hidrogênio também desempenham um papel na formação da estrutura terciária da proteína por meio da interação dos grupos R. (Veja também dobramento de proteínas).
Sistemas de ligações H bifurcadas são comuns em proteínas transmembranares alfa-helicoidais entre a amida principal C=O do resíduo i como o H- aceitador de ligação e dois doadores de ligação H do resíduo i + 4: a amida principal N−H e uma hidroxila ou tiol de cadeia lateral H+. A preferência energética do sistema hidroxila ou tiol de ligação H bifurcada é -3,4 kcal/mol ou -2,6 kcal/mol, respectivamente. Este tipo de ligação de H bifurcada fornece um parceiro de ligação de H intra-helicoidal para cadeias laterais polares, como serina, treonina e cisteína dentro dos ambientes de membrana hidrofóbica.
O papel das pontes de hidrogênio no dobramento de proteínas também tem sido associado à estabilização de proteínas induzida por osmólitos. Osmólitos protetores, como trealose e sorbitol, deslocam o equilíbrio de enovelamento da proteína para o estado enovelado, de maneira dependente da concentração. Embora a explicação predominante para a ação do osmólito se baseie em efeitos de volume excluídos que são de natureza entrópica, experimentos de dicroísmo circular (CD) mostraram que o osmólito age por meio de um efeito entálpico. O mecanismo molecular para o seu papel na estabilização de proteínas ainda não está bem estabelecido, embora vários mecanismos tenham sido propostos. Simulações computacionais de dinâmica molecular sugerem que os osmólitos estabilizam as proteínas modificando as pontes de hidrogênio na camada de hidratação da proteína.
Vários estudos têm mostrado que as pontes de hidrogênio desempenham um papel importante para a estabilidade entre subunidades em proteínas multiméricas. Por exemplo, um estudo da sorbitol desidrogenase mostrou uma importante rede de pontes de hidrogênio que estabiliza a estrutura quaternária tetramérica dentro da família de proteínas sorbitol desidrogenase de mamíferos.
Uma ligação de hidrogênio da espinha dorsal da proteína incompletamente protegida do ataque da água é um dehidron. Dehydrons promovem a remoção de água através de proteínas ou ligação de ligantes. A desidratação exógena aumenta a interação eletrostática entre os grupos amida e carbonila desprotegindo suas cargas parciais. Além disso, a desidratação estabiliza a ligação de hidrogênio desestabilizando o estado não ligado que consiste em cargas isoladas desidratadas.
A lã, sendo uma fibra de proteína, é mantida unida por pontes de hidrogênio, fazendo com que a lã retraia quando esticada. No entanto, a lavagem a altas temperaturas pode quebrar permanentemente as pontes de hidrogénio e uma peça de roupa pode perder permanentemente a sua forma.
Celulose
As ligações de hidrogênio são importantes na estrutura da celulose e fibras derivadas, como algodão e linho.
Polímeros sintéticos
As propriedades de muitos polímeros sintéticos são afetadas por pontes de hidrogênio dentro e/ou entre as cadeias. No nylon, existem pontes de hidrogênio entre os grupos carbonila e amina na unidade de repetição de amida. Eles ligam efetivamente cadeias adjacentes, que reforçam o material. As ligações de hidrogênio também afetam a fibra de aramida, onde as ligações de hidrogênio estabilizam as cadeias lineares lateralmente. Os eixos da corrente são alinhados ao longo do eixo da fibra, tornando as fibras extremamente rígidas e fortes. As redes de ligações de hidrogênio tornam os polímeros naturais e sintéticos sensíveis aos níveis de umidade na atmosfera porque as moléculas de água podem se difundir na superfície e interromper a rede. Alguns polímeros são mais sensíveis do que outros. Assim, os nylons são mais sensíveis que as aramidas, e o nylon 6 mais sensível que o nylon-11.
Ligação de hidrogênio simétrica
Uma ligação de hidrogênio simétrica é um tipo especial de ligação de hidrogênio em que o próton é espaçado exatamente a meio caminho entre dois átomos idênticos. A força da ligação com cada um desses átomos é igual. É um exemplo de uma ligação de quatro elétrons de três centros. Este tipo de vínculo é muito mais forte do que um vínculo "normal" ligação de hidrogênio. A ordem de ligação efetiva é 0,5, então sua força é comparável a uma ligação covalente. É visto no gelo a alta pressão e também na fase sólida de muitos ácidos anidros, como o ácido fluorídrico e o ácido fórmico a alta pressão. Também é visto no íon bifluoreto [F···H···F]−. Devido à severa restrição estérica, a forma protonada da esponja de prótons (1,8-bis(dimetilamino)naftaleno) e seus derivados também possuem pontes de hidrogênio simétricas ([N···H··· N]+), embora no caso de Proton Sponge protonado, o conjunto esteja dobrado.
Ligação de di-hidrogênio
A ligação de hidrogênio pode ser comparada com a ligação de di-hidrogênio estreitamente relacionada, que também é uma interação de ligação intermolecular envolvendo átomos de hidrogênio. Essas estruturas são conhecidas há algum tempo e bem caracterizadas por cristalografia; no entanto, uma compreensão de sua relação com a ligação de hidrogênio convencional, ligação iônica e ligação covalente permanece incerta. Geralmente, a ligação de hidrogênio é caracterizada por um aceptor de prótons que é um par solitário de elétrons em átomos não metálicos (principalmente nos grupos de nitrogênio e calcogênio). Em alguns casos, esses aceitadores de prótons podem ser ligações pi ou complexos metálicos. Na ligação di-hidrogênio, no entanto, um hidreto de metal serve como aceptor de prótons, formando assim uma interação hidrogênio-hidrogênio. A difração de nêutrons mostrou que a geometria molecular desses complexos é semelhante às ligações de hidrogênio, pois o comprimento da ligação é muito adaptável ao sistema doador de hidrogênio/complexo metálico.
Aplicação a drogas
A ligação de hidrogênio é relevante para o design de medicamentos. De acordo com a regra dos cinco de Lipinski, a maioria das drogas ativas por via oral não tem mais do que cinco doadores de ligações de hidrogênio e menos de dez aceptores de ligações de hidrogênio. Essas interações existem entre os centros de nitrogênio-hidrogênio e oxigênio-hidrogênio. Muitas drogas, no entanto, não obedecem a essas "regras".
Contenido relacionado
El Nino
Álcool amílico
Vírus DNA