Ouro
Ouro é um elemento químico com o símbolo Au (do latim aurum & #39;ouro') e número atômico 79. Isso o torna um dos elementos de maior número atômico que ocorrem naturalmente. É um metal brilhante, ligeiramente amarelo-alaranjado, denso, macio, maleável e dúctil em sua forma pura. Quimicamente, o ouro é um metal de transição e um elemento do grupo 11. É um dos elementos químicos menos reativos e é sólido em condições padrão.
O ouro geralmente ocorre em estado livre (estado nativo), como pepitas ou grãos, em rochas, veios e depósitos aluviais. Ocorre em uma série de soluções sólidas com o elemento nativo prata (como no eletro), naturalmente ligado a outros metais como cobre e paládio, e inclusões minerais como a pirita. Menos comumente, ocorre em minerais como compostos de ouro, geralmente com telúrio (teluretos de ouro).
O ouro é resistente à maioria dos ácidos, embora se dissolva em água régia (uma mistura de ácido nítrico e ácido clorídrico), formando um ânion tetracloroaurato solúvel. O ouro é insolúvel apenas em ácido nítrico, que dissolve prata e metais básicos, propriedade há muito usada para refinar ouro e confirmar a presença de ouro em substâncias metálicas, dando origem ao termo "teste de ácido". O ouro se dissolve em soluções alcalinas de cianeto, que são usadas em mineração e galvanoplastia. O ouro também se dissolve em mercúrio, formando ligas de amálgama, e como o ouro age simplesmente como um soluto, esta não é uma reação química.
Um elemento relativamente raro, o ouro é um metal precioso que tem sido usado para cunhagem, joias e outras artes ao longo da história registrada. No passado, um padrão-ouro era frequentemente implementado como política monetária. As moedas de ouro deixaram de ser cunhadas como moeda circulante na década de 1930, e o padrão-ouro mundial foi abandonado por um sistema de moeda fiduciária após as medidas de choque de Nixon em 1971.
Em 2020, o maior produtor mundial de ouro foi a China, seguida pela Rússia e Austrália. Um total de cerca de 201.296 toneladas de ouro existe acima do solo, em 2020. Isso é igual a um cubo com cada lado medindo aproximadamente 21,7 metros (71 pés). O consumo mundial do ouro novo produzido é de cerca de 50% em joias, 40% em investimentos e 10% na indústria. A alta maleabilidade, ductilidade, resistência à corrosão e à maioria das outras reações químicas e a condutividade elétrica do ouro levaram ao seu uso contínuo em conectores elétricos resistentes à corrosão em todos os tipos de dispositivos computadorizados (seu principal uso industrial). O ouro também é usado em proteção infravermelha, produção de vidro colorido, folheação de ouro e restauração dentária. Certos sais de ouro ainda são usados como anti-inflamatórios na medicina.
Características
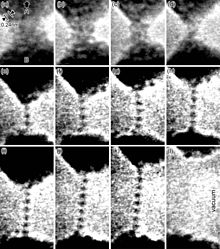
O ouro é o mais maleável de todos os metais. Ele pode ser estirado em um fio de largura de átomo único e, em seguida, esticado consideravelmente antes de quebrar. Esses nanofios se distorcem por meio da formação, reorientação e migração de discordâncias e gêmeos de cristal sem endurecimento perceptível. Um único grama de ouro pode ser batido em uma folha de 1 metro quadrado (11 sq ft) e uma onça avoirdupois em 300 pés quadrados (28 m2). A folha de ouro pode ser batida fina o suficiente para se tornar semitransparente. A luz transmitida aparece azul-esverdeada, porque o ouro reflete fortemente o amarelo e o vermelho. Essas folhas semitransparentes também refletem fortemente a luz infravermelha, tornando-as úteis como escudos infravermelhos (calor radiante) em visores de trajes resistentes ao calor e em visores solares para trajes espaciais. O ouro é um bom condutor de calor e eletricidade.
O ouro tem uma densidade de 19,3 g/cm3, quase idêntica à do tungstênio em 19,25 g/cm3; como tal, o tungstênio tem sido usado na falsificação de barras de ouro, como o revestimento de uma barra de tungstênio com ouro. Em comparação, a densidade do chumbo é 11,34 g/cm3, e a do elemento mais denso, ósmio, é 22,588±0,015 g/cm3.
Cor
Enquanto a maioria dos metais é cinza ou branco prateado, o ouro é ligeiramente amarelo avermelhado. Essa cor é determinada pela frequência das oscilações do plasma entre os elétrons de valência do metal, na faixa ultravioleta para a maioria dos metais, mas na faixa visível para o ouro devido a efeitos relativísticos que afetam os orbitais em torno dos átomos de ouro. Efeitos semelhantes conferem uma tonalidade dourada ao césio metálico.
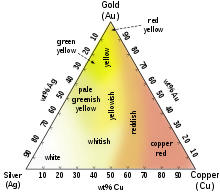
As ligas de ouro coloridas comuns incluem o distinto ouro rosa de dezoito quilates criado pela adição de cobre. Ligas contendo paládio ou níquel também são importantes em joias comerciais, pois produzem ligas de ouro branco. A liga de ouro-cobre de quatorze quilates é quase idêntica em cor a certas ligas de bronze, e ambas podem ser usadas para produzir distintivos policiais e outros. Ligas de ouro de quatorze e dezoito quilates com prata sozinha aparecem amarelo-esverdeadas e são chamadas de ouro verde. O ouro azul pode ser feito ligando-se ao ferro, e o ouro púrpura pode ser feito ligando-se ao alumínio. Menos comumente, a adição de manganês, índio e outros elementos pode produzir cores de ouro mais incomuns para várias aplicações.
O ouro coloidal, usado por microscopistas eletrônicos, é vermelho se as partículas forem pequenas; partículas maiores de ouro coloidal são azuis.
Isótopos
O ouro tem apenas um isótopo estável, 197
Au, que também é seu único isótopo de ocorrência natural, então o ouro é um elemento mononuclídico e monoisotópico. Trinta e seis radioisótopos foram sintetizados, variando em massa atômica de 169 a 205. O mais estável deles é 195
Au com um meia-vida de 186,1 dias. O menos estável é 171
Au, que decai por emissão de prótons com uma meia-vida de 30 µs. A maioria dos radioisótopos de ouro com massas atômicas abaixo de 197 decai por alguma combinação de emissão de prótons, decaimento α e decaimento β+. As exceções são 195
Au, que decai por captura eletrônica, e 196
Au, que decai mais frequentemente por captura eletrônica (93%) com um menor caminho de decaimento β- (7%). Todos os radioisótopos de ouro com massas atômicas acima de 197 decaem por decaimento β−.
Pelo menos 32 isômeros nucleares também foram caracterizados, variando em massa atômica de 170 a 200. Dentro desse intervalo, apenas 178
Au, 180
Au, 181
Au , 182
Au e 188
Au não possuem isômeros. O isômero mais estável do ouro é 198m2
Au com meia-vida de 2,27 dias. O isômero menos estável do ouro é 177m2
Au com meia-vida de apenas 7 ns. 184m1
Au tem três caminhos de decaimento: decaimento β+, transição isomérica e decaimento alfa. Nenhum outro isômero ou isótopo de ouro tem três caminhos de decaimento.
Síntese
A possível produção de ouro a partir de um elemento mais comum, como o chumbo, tem sido um assunto de investigação humana, e a disciplina antiga e medieval da alquimia freqüentemente se concentrava nisso; no entanto, a transmutação dos elementos químicos não se tornou possível até a compreensão da física nuclear no século XX. A primeira síntese de ouro foi conduzida pelo físico japonês Hantaro Nagaoka, que sintetizou ouro a partir de mercúrio em 1924 por bombardeio de nêutrons. Uma equipe americana, trabalhando sem conhecimento do estudo anterior de Nagaoka, realizou o mesmo experimento em 1941, obtendo o mesmo resultado e mostrando que os isótopos de ouro produzidos por ele eram todos radioativos. Em 1980, Glenn Seaborg transmutou vários milhares de átomos de bismuto em ouro no Laboratório Lawrence Berkeley. O ouro pode ser fabricado em um reator nuclear, mas isso é altamente impraticável e custaria muito mais do que o valor do ouro produzido.
Química
Embora o ouro seja o mais nobre dos metais nobres, ele ainda forma muitos compostos diversos. O estado de oxidação do ouro em seus compostos varia de -1 a +5, mas Au(I) e Au(III) dominam sua química. Au(I), conhecido como íon áureo, é o estado de oxidação mais comum com ligantes moles como tioéteres, tiolatos e organofosfinas. Compostos de Au(I) são tipicamente lineares. Um bom exemplo é Au(CN)−2, que é a forma solúvel de ouro encontrada na mineração. Os haletos de ouro binários, como AuCl, formam cadeias poliméricas em zigue-zague, novamente apresentando coordenação linear em Au. A maioria dos medicamentos à base de ouro são derivados de Au(I).
Au(III) (referido como áurico) é um estado de oxidação comum e é ilustrado pelo cloreto de ouro(III), Au2Cl6. Os centros de átomos de ouro em complexos de Au(III), como outros compostos d8, são tipicamente quadrados planares, com ligações químicas que possuem caráter covalente e iônico. O cloreto de ouro(I,III) também é conhecido, um exemplo de um complexo de valência mista.
O ouro não reage com o oxigênio em nenhuma temperatura e, até 100 °C, é resistente ao ataque do ozônio.
Alguns halogênios livres reagem com o ouro. O ouro é fortemente atacado pelo flúor em calor vermelho fosco para formar fluoreto de ouro(III) AuF3. O ouro em pó reage com o cloro a 180 °C para formar cloreto de ouro(III) AuCl3. Ouro reage com bromo a 140 °C para formar brometo de ouro(III) AuBr3, mas reage apenas muito lentamente com iodo para formar iodeto de ouro (I) AuI.
O ouro não reage diretamente com o enxofre, mas o sulfeto de ouro(III) pode ser feito passando sulfeto de hidrogênio por uma solução diluída de cloreto de ouro(III) ou ácido cloráurico.
Ao contrário do enxofre, o fósforo reage diretamente com o ouro em temperaturas elevadas para produzir fosfeto de ouro (Au2P3).
O ouro se dissolve facilmente em mercúrio à temperatura ambiente para formar um amálgama e forma ligas com muitos outros metais em temperaturas mais altas. Estas ligas podem ser produzidas para modificar a dureza e outras propriedades metalúrgicas, para controlar o ponto de fusão ou para criar cores exóticas.
O ouro não é afetado pela maioria dos ácidos. Não reage com ácido fluorídrico, clorídrico, bromídrico, iodídrico, sulfúrico ou nítrico. Ele reage com ácido selênico e é dissolvido em água régia, uma mistura 1:3 de ácido nítrico e ácido clorídrico. O ácido nítrico oxida o metal em íons +3, mas apenas em quantidades mínimas, normalmente indetectáveis no ácido puro por causa do equilíbrio químico da reação. No entanto, os íons são removidos do equilíbrio pelo ácido clorídrico, formando AuCl−4, ou ácido cloroáurico, permitindo assim uma maior oxidação.
O ouro também não é afetado pela maioria das bases. Não reage com hidróxido de potássio ou sódio aquoso, sólido ou fundido. No entanto, reage com cianeto de sódio ou potássio em condições alcalinas quando o oxigênio está presente para formar complexos solúveis.
Os estados de oxidação comuns do ouro incluem +1 (ouro(I) ou compostos áureos) e +3 (ouro(III) ou compostos áuricos). Os íons de ouro em solução são prontamente reduzidos e precipitados como metal pela adição de qualquer outro metal como agente redutor. O metal adicionado é oxidado e dissolvido, permitindo que o ouro seja deslocado da solução e recuperado como um precipitado sólido.
Estados de oxidação raros
Os estados de oxidação menos comuns do ouro incluem -1, +2 e +5.
O estado de oxidação −1 ocorre em auridos, compostos que contêm o ânion Au−. O auride de césio (CsAu), por exemplo, cristaliza no motivo cloreto de césio; auretos de rubídio, potássio e tetrametilamônio também são conhecidos. O ouro tem a maior afinidade eletrônica de qualquer metal, em 222,8 kJ/mol, tornando o Au− um estável espécies análogas aos haletos.
O ouro também tem um estado de oxidação -1 em complexos covalentes com os metais de transição do grupo 4, como no tetraauride de titânio e nos compostos análogos de zircônio e háfnio. Espera-se que esses produtos químicos formem dímeros em ponte de ouro de maneira semelhante ao hidreto de titânio (IV).
Compostos de ouro(II) são geralmente diamagnéticos com ligações Au-Au, como [Au(CH2)2P(C6H5 )2]2Cl2. A evaporação de uma solução de Au(OH)3 em concentrado H2SO4 produz cristais vermelhos de sulfato de ouro (II), Au2(SO4)2. Originalmente considerado um composto de valência mista, foi demonstrado que contém Au4+ 2 cátions, análogo ao íon mercúrio(I) mais conhecido, Hg2+2. Um complexo de ouro(II), o cátion tetraxenonoouro(II), que contém xenônio como ligante, ocorre em [AuXe4](Sb2F11)2.
Pentafluoreto de ouro, junto com seu ânion derivado, AuF−6 , e seu complexo de diflúor, heptafluoreto de ouro, é o único exemplo de ouro(V), o estado de oxidação mais alto verificado.
Alguns compostos de ouro exibem ligação aurofílica, que descreve a tendência dos íons de ouro de interagir em distâncias muito longas para ser uma ligação Au-Au convencional, mas mais curta que a ligação van der Waals. Estima-se que a interação seja comparável em força à de uma ligação de hidrogênio.
Os compostos de aglomerados bem definidos são numerosos. Em alguns casos, o ouro tem um estado de oxidação fracionário. Um exemplo representativo é a espécie octaédrica {Au(P(C6H5)3)}2+ 6.
Origem
Produção de ouro no universo
Acredita-se que o ouro tenha sido produzido na nucleossíntese de supernovas e da colisão de estrelas de nêutrons, e que esteja presente na poeira a partir da qual o Sistema Solar se formou.
Tradicionalmente, acredita-se que o ouro no universo tenha se formado pelo processo r (captura rápida de nêutrons) na nucleossíntese de supernova, mas mais recentemente foi sugerido que o ouro e outros elementos mais pesados que o ferro também podem ser produzidos em quantidade por o processo r na colisão de estrelas de nêutrons. Em ambos os casos, os espectrômetros de satélite inicialmente detectaram apenas indiretamente o ouro resultante. No entanto, em agosto de 2017, as assinaturas espectroscópicas de elementos pesados, incluindo ouro, foram observadas por observatórios eletromagnéticos no evento de fusão de estrelas de nêutrons GW170817, depois que detectores de ondas gravitacionais confirmaram o evento como uma fusão de estrelas de nêutrons. Os modelos astrofísicos atuais sugerem que este único evento de fusão de estrelas de nêutrons gerou entre 3 e 13 massas terrestres de ouro. Essa quantidade, juntamente com as estimativas da taxa de ocorrência desses eventos de fusão de estrelas de nêutrons, sugere que tais fusões podem produzir ouro suficiente para explicar a maior parte da abundância desse elemento no universo.
Teorias da origem dos asteroides
Como a Terra foi fundida quando foi formada, quase todo o ouro presente na Terra primitiva provavelmente afundou no núcleo planetário. Portanto, a maior parte do ouro que está na crosta e no manto da Terra, em um modelo que se acredita ter sido entregue à Terra mais tarde, por impactos de asteróides durante o bombardeio pesado tardio, cerca de 4 bilhões de anos atrás.
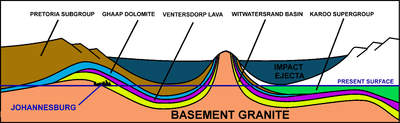
O ouro que pode ser alcançado por humanos foi, em um caso, associado a um impacto de asteroide específico. O asteróide que formou a estrutura de impacto de Vredefort há 2,020 bilhões de anos é frequentemente creditado por semear a bacia de Witwatersrand, na África do Sul, com os depósitos de ouro mais ricos da Terra. No entanto, esse cenário agora é questionado. As rochas de ouro de Witwatersrand foram depositadas entre 700 e 950 milhões de anos antes do impacto de Vredefort. Além disso, essas rochas contendo ouro foram cobertas por uma espessa camada de lavas de Ventersdorp e o supergrupo de rochas do Transvaal antes do impacto do meteoro e, portanto, o ouro não chegou realmente ao asteroide/meteorito. O que o impacto de Vredefort conseguiu, no entanto, foi distorcer a bacia de Witwatersrand de tal forma que as rochas contendo ouro foram trazidas para a atual superfície de erosão em Joanesburgo, em Witwatersrand, logo dentro da borda dos 300 km originais (190 mi) cratera de diâmetro causada pelo impacto do meteoro. A descoberta do depósito em 1886 lançou a Witwatersrand Gold Rush. Cerca de 22% de todo o ouro que existe hoje na Terra foi extraído dessas rochas de Witwatersrand.
Teorias do retorno do manto
Apesar do impacto acima, acredita-se que muito do restante do ouro na Terra tenha sido incorporado ao planeta desde o seu início, quando os planetesimais formaram o manto do planeta, no início da criação da Terra. Em 2017, um grupo internacional de cientistas estabeleceu que o ouro "veio à superfície da Terra das regiões mais profundas do nosso planeta", o manto, evidenciado por suas descobertas no Maciço do Deseado, na Patagônia argentina.
Ocorrência
Na Terra, o ouro é encontrado em minérios em rochas formadas a partir do período pré-cambriano. Na maioria das vezes ocorre como um metal nativo, normalmente em uma solução sólida de metal com prata (isto é, como uma liga de ouro/prata). Essas ligas geralmente têm um teor de prata de 8 a 10%. Electrum é ouro elementar com mais de 20% de prata e é comumente conhecido como ouro branco. A cor de Electrum varia de dourado-prateado a prateado, dependendo do teor de prata. Quanto mais prata, menor a gravidade específica.
O ouro nativo ocorre como partículas muito pequenas a microscópicas embutidas na rocha, geralmente junto com quartzo ou minerais de sulfeto, como o "ouro dos tolos", que é uma pirita. Estes são chamados de depósitos de filão. O metal em estado nativo também é encontrado na forma de flocos livres, grãos ou pepitas maiores que foram erodidas de rochas e acabam em depósitos aluviais chamados depósitos de placer. Esse ouro livre é sempre mais rico na superfície exposta dos veios auríferos, devido à oxidação dos minerais que o acompanham, seguida pelo intemperismo; e pela lavagem da poeira em córregos e rios, onde ela se acumula e pode ser soldada pela ação da água para formar pepitas.
O ouro às vezes ocorre combinado com telúrio como os minerais calaverita, krenerita, nagyagita, petzita e silvanita (ver minerais de telureto) e como o raro bismuto maldonita (Au2Bi) e antimonida aurostibita (AuSb2). O ouro também ocorre em ligas raras com cobre, chumbo e mercúrio: os minerais auricuprida (Cu3Au), novodneprite (AuPb3) e weishanite ((Au,Ag)3Hg2).
Pesquisas recentes sugerem que os micróbios às vezes podem desempenhar um papel importante na formação de depósitos de ouro, transportando e precipitando ouro para formar grãos e pepitas que se acumulam em depósitos aluviais.
Outro estudo recente afirmou que a água em falhas vaporiza durante um terremoto, depositando ouro. Quando ocorre um terremoto, ele se move ao longo de uma falha. A água geralmente lubrifica as falhas, preenchendo fraturas e saliências. Cerca de 10 quilômetros (6,2 milhas) abaixo da superfície, sob temperaturas e pressões muito altas, a água carrega altas concentrações de dióxido de carbono, sílica e ouro. Durante um terremoto, o desvio de falha repentinamente se abre mais. A água dentro do vazio vaporiza instantaneamente, transformando-se em vapor e forçando a sílica, que forma o quartzo mineral e o ouro dos fluidos para as superfícies próximas.
Água do mar
Os oceanos do mundo contêm ouro. As concentrações medidas de ouro no Atlântico e Nordeste do Pacífico são 50–150 femtomol/L ou 10–30 partes por quatrilhão (cerca de 10–30 g/km3). Em geral, as concentrações de ouro para as amostras do Atlântico Sul e do Pacífico Central são as mesmas (~ 50 femtomol/L), mas menos certas. As águas profundas do Mediterrâneo contêm concentrações ligeiramente mais altas de ouro (100–150 femtomol/L) atribuídas à poeira trazida pelo vento e/ou rios. A 10 partes por quatrilhão, os oceanos da Terra conteriam 15.000 toneladas de ouro. Esses números são três ordens de grandeza menores do que os relatados na literatura antes de 1988, indicando problemas de contaminação com os dados anteriores.
Várias pessoas afirmaram ser capazes de recuperar economicamente o ouro da água do mar, mas se enganaram ou agiram de forma intencional. Prescott Jernegan executou uma fraude de ouro da água do mar nos Estados Unidos na década de 1890, assim como um fraudador inglês no início de 1900. Fritz Haber pesquisou a extração de ouro da água do mar em um esforço para ajudar a pagar as reparações da Alemanha após a Primeira Guerra Mundial. Com base nos valores publicados de 2 a 64 ppb de ouro na água do mar, uma extração comercialmente bem-sucedida parecia possível. Após a análise de 4.000 amostras de água rendendo uma média de 0,004 ppb, ficou claro que a extração não seria possível e ele encerrou o projeto.
História

Esta figura de raft Muisca está em exposição no Museu do Ouro, Bogotá, Colômbia.
O mais antigo metal registrado empregado por humanos parece ser o ouro, que pode ser encontrado livre ou "nativo". Pequenas quantidades de ouro natural foram encontradas em cavernas espanholas usadas durante o final do período paleolítico, c. 40.000 aC.
Os artefatos de ouro mais antigos do mundo são da Bulgária e datam do 5º milênio aC (4.600 aC a 4.200 aC), como os encontrados na necrópole de Varna perto do lago Varna e na costa do Mar Negro, que se acredita serem o mais antigo "bem datado" descoberta de artefatos de ouro na história. Vários achados búlgaros pré-históricos são considerados não menos antigos - os tesouros de ouro de Hotnitsa, Durankulak, artefatos do assentamento Kurgan de Yunatsite perto de Pazardzhik, o tesouro de ouro Sakar, bem como contas e joias de ouro encontradas no assentamento Kurgan de Provadia - Solnitsata (“poço de sal”). No entanto, o ouro de Varna costuma ser chamado de o mais antigo, pois esse tesouro é o maior e mais diversificado.
Os artefatos de ouro provavelmente fizeram sua primeira aparição no Egito Antigo no início do período pré-dinástico, no final do quinto milênio aC e no início do quarto, e a fundição foi desenvolvida durante o curso do quarto milênio; artefatos de ouro aparecem na arqueologia da Baixa Mesopotâmia durante o início do quarto milênio. A partir de 1990, os artefatos de ouro encontrados no cemitério da caverna Wadi Qana do 4º milênio aC na Cisjordânia foram os primeiros do Levante. Artefatos de ouro, como os chapéus de ouro e o disco de Nebra, apareceram na Europa Central a partir da Idade do Bronze do segundo milênio aC.
O mais antigo mapa conhecido de uma mina de ouro foi desenhado na 19ª Dinastia do Antigo Egito (1320–1200 aC), enquanto a primeira referência escrita ao ouro foi registrada na 12ª dinastia por volta de 1900 aC. Os hieróglifos egípcios de 2600 aC descrevem o ouro, que o rei Tushratta do Mitanni afirmou ser "mais abundante do que a sujeira". No Egito. O Egito e especialmente a Núbia tiveram os recursos para torná-los grandes áreas produtoras de ouro durante grande parte da história. Um dos primeiros mapas conhecidos, conhecido como Mapa do Papiro de Turim, mostra a planta de uma mina de ouro na Núbia junto com indicações da geologia local. Os métodos de trabalho primitivos são descritos por Strabo e Diodorus Siculus, e incluíam atear fogo. Grandes minas também estavam presentes no Mar Vermelho, onde hoje é a Arábia Saudita.
O ouro é mencionado nas cartas de Amarna numeradas 19 e 26 por volta do século 14 aC.
O ouro é mencionado com frequência no Antigo Testamento, começando com Gênesis 2:11 (em Havilah), a história do bezerro de ouro e muitas partes do templo, incluindo a menorá e o altar de ouro. No Novo Testamento, está incluído nos presentes dos Magos nos primeiros capítulos de Matthew. O Livro do Apocalipse 21:21 descreve a cidade de Nova Jerusalém como tendo ruas - feita de ouro puro, claro como cristal ". Diz-se que a exploração de ouro no canto sudeste do Mar Negro é dada a partir da época de Midas, e esse ouro foi importante no estabelecimento do que provavelmente é a primeira cunhagem do mundo em Lydia por volta de 610 aC. A lenda do lã de ouro que data do século VIII aC pode se referir ao uso de lamas para prender a poeira de ouro dos depósitos de placer no mundo antigo. Desde o século VI ou V aC, o Chu (estado) circulou o Ying Yuan, um tipo de moeda de ouro quadrada.
Na metalurgia romana, novos métodos para extrair ouro em larga escala foram desenvolvidos pela introdução de métodos de mineração hidráulica, especialmente na hispânia a partir de 25 aC e em Dacia a partir de 106 dC em diante. Uma de suas maiores minas estava em Las Medulas em León, onde sete longos aquedutos lhes permitiram sacudir a maior parte de um grande depósito aluvial. As minas em Roşia Montană, na Transilvânia, também eram muito grandes e até muito recentemente, ainda extraídas pelos métodos de OpenCast. Eles também exploraram depósitos menores na Grã-Bretanha, como depósitos de placer e rock duro em Dolacothi. Os vários métodos que eles usaram são bem descritos por Plínio, o Velho em sua Enciclopédia, Naturalis Historia escrita no final do primeiro século dC.
Durante a Mansa Musa (governante do Império Mali de 1312 a 1337) Hajj para Meca em 1324, ele passou pelo Cairo em julho de 1324 e teria sido acompanhada por um trem de camelo que incluía milhares de pessoas e quase Cem camelos, onde ele doou tanto ouro que deprimiu o preço no Egito por mais de uma década, causando alta inflação. Um historiador árabe contemporâneo comentou:
O ouro estava a um preço alto no Egito até que chegaram naquele ano. O mithqal não foi abaixo de 25 dirhams e foi geralmente acima, mas a partir desse momento o seu valor caiu e diminuiu no preço e permaneceu barato até agora. O mithqal não excede 22 dirhams ou menos. Este tem sido o estado dos assuntos por cerca de doze anos até hoje por causa da grande quantidade de ouro que eles trouxeram para o Egito e passou lá [...].
—Chihab Al-Umari, Reino do Mali
A exploração européia das Américas foi alimentada em grande parte por relatos dos ornamentos de ouro exibidos em grande profusão pelos povos nativos americanos, especialmente na Mesoamérica, Peru, Equador e Colômbia. Os astecas consideravam o ouro como o produto dos deuses, chamando -o literalmente "excrementos de Deus"; ( teocuitlatl em Nahuatl), e depois que Moctezuma II foi morto, a maior parte desse ouro foi enviada para a Espanha. No entanto, para os povos indígenas da América do Norte, o ouro foi considerado inútil e eles viram um valor muito maior em outros minerais diretamente relacionados à sua utilidade, como obsidiana, pederneira e ardósia. El Dorado é aplicado a uma história lendária na qual pedras preciosas foram encontradas em abundância fabulosa, juntamente com moedas de ouro. O conceito de El Dorado passou por várias transformações e, eventualmente, os relatos do mito anterior também foram combinados com os de uma cidade perdida lendária. El Dorado, foi o termo usado pelo Império Espanhol para descrever um chefe tribal mítico (ZIPA) do povo nativo de Muisca na Colômbia, que, como ritual de iniciação, se cobriu com poeira dourada e submersa no lago Guatavita. As lendas em torno de El Dorado mudaram com o tempo, pois passou de ser homem, uma cidade, para um reino e depois finalmente para um império.
A partir do início do período moderno, a exploração e colonização européia da África Ocidental foram impulsionadas em grande parte por relatos de depósitos de ouro na região, que acabou sendo referido pelos europeus como a costa de ouro " Do final do século XV ao início do século XIX, o comércio europeu na região estava focado principalmente em ouro, juntamente com marfim e escravos. O comércio de ouro na África Ocidental foi dominado pelo Império Ashanti, que inicialmente negociou com os portugueses antes de se ramificar e negociar com comerciantes britânicos, franceses, espanhóis e dinamarqueses. Os desejos britânicos de garantir o controle dos depósitos de ouro na África Ocidental tiveram um papel nas guerras anglo-ashanti do final do século XIX, que viu o Império Ashanti anexado pela Grã-Bretanha.
Gold desempenhou um papel na cultura ocidental, como causa de desejo e corrupção, como contado nas fábulas de crianças como Rumpelstiltskin - onde Rumpelstiltskin transforma o feno em ouro para a filha do camponês em troca para Seu filho quando ela se torna uma princesa - e o roubo da galinha que coloca ovos dourados em Jack e o feijão.O prêmio principal nos Jogos Olímpicos e muitas outras competições esportivas é a medalha de ouro.
75% dos atualmente responsáveis pelo ouro foram extraídos desde 1910, dois terços desde 1950.
Um dos principais objetivos dos alquimistas era produzir ouro de outras substâncias, como o chumbo - presumivelmente pela interação com uma substância mítica chamada pedra do filósofo. Tentar produzir ouro levou os alquimistas a descobrir sistematicamente o que pode ser feito com substâncias, e isso lançou a fundação para a química de hoje, que pode produzir ouro (embora semeconomicamente) usando transmutação nuclear. Seu símbolo para o ouro era o círculo com um ponto em seu centro (☉), que também era o símbolo astrológico e o antigo caráter chinês do Sol.
A cúpula da rocha é coberta com um vidro dourado ultrafino. O Sikh Golden Temple, o Harmandir Sahib, é um edifício coberto de ouro. Da mesma forma, o templo budista de Wat Phra Kaew Emerald (WAT) na Tailândia tem estátuas e telhados ornamentais de folhas douradas. Algumas coroas européias do rei e da rainha eram feitas de ouro, e o ouro foi usado para a coroa nupcial desde a antiguidade. Um texto talmúdico antigo por volta de 100 anúncios descreve Rachel, esposa do rabino Akiva, recebendo A " Jerusalém do ouro " (diadema). Uma coroa do enterro grego feita de ouro foi encontrada em um túmulo por volta de 370 aC.
Etimologia
"Ouro" é cognato com palavras semelhantes em muitas línguas germânicas, derivando via proto-germânico *gulþą do proto-indo-europeu *ǵʰelh₃- ("brilhar, brilhar; ser amarelo ou verde").
O símbolo Au vem do latim: aurum, a palavra latina para "ouro". O ancestral proto-indo-europeu de aurum era *h₂é-h₂us-o-, que significa "brilho". Esta palavra é derivada da mesma raiz (proto-indo-europeu *h₂u̯es- "ao amanhecer") como *h₂éu̯sōs, o ancestral da palavra latina Aurora, " amanhecer". Presumivelmente, essa relação etimológica está por trás da afirmação frequente em publicações científicas de que aurum significava "amanhecer brilhante".
Cultura
Na cultura popular, o ouro é um alto padrão de excelência, frequentemente usado em prêmios. Grandes conquistas são freqüentemente recompensadas com ouro, na forma de medalhas de ouro, troféus de ouro e outras condecorações. Os vencedores de eventos atléticos e outras competições classificadas geralmente recebem uma medalha de ouro. Muitos prêmios, como o Prêmio Nobel, também são feitos de ouro. Outras estátuas e prêmios de prêmios são representados em ouro ou banhados a ouro (como o Oscar, o Globo de Ouro, o Emmy Awards, a Palma de Ouro e o British Academy Film Awards).
Aristóteles em sua ética usou o simbolismo do ouro ao se referir ao que hoje é conhecido como meio-termo dourado. Da mesma forma, o ouro está associado a princípios perfeitos ou divinos, como no caso da proporção áurea e da regra de ouro. O ouro está ainda associado à sabedoria do envelhecimento e da fruição. O quinquagésimo aniversário de casamento é de ouro. Os últimos anos mais valorizados ou bem-sucedidos de uma pessoa às vezes são considerados "anos dourados". O auge de uma civilização é chamado de idade de ouro.
Religião
Em algumas formas de cristianismo e judaísmo, o ouro tem sido associado tanto ao sagrado quanto ao mal. No Livro do Êxodo, o Bezerro de Ouro é um símbolo de idolatria, enquanto no Livro do Gênesis, Abraão foi dito ser rico em ouro e prata, e Moisés foi instruído a cobrir o Propiciatório da Arca da Aliança com puro ouro. Na iconografia bizantina, os halos de Cristo, da Virgem Maria e dos santos costumam ser dourados.
No Islã, o ouro (junto com a seda) é freqüentemente citado como sendo proibido para os homens usarem. Abu Bakr al-Jazaeri, citando um hadith, disse que "[o] uso de seda e ouro é proibido aos homens de minha nação, e eles são lícitos para suas mulheres". Isso, no entanto, não foi aplicado de forma consistente ao longo da história, por ex. no Império Otomano. Além disso, pequenos detalhes dourados nas roupas, como bordados, podem ser permitidos.
Na mitologia e na religião grega antiga, Theia era vista como a deusa do ouro, da prata e de outras pedras preciosas.
Segundo Cristóvão Colombo, aqueles que possuíam algo de ouro possuíam algo de grande valor na Terra e uma substância para até levar as almas ao paraíso.
As alianças de casamento são normalmente feitas de ouro. É duradouro e não é afetado pela passagem do tempo e pode ajudar no simbolismo do anel dos votos eternos perante Deus e na perfeição que o casamento significa. Nas cerimônias de casamento cristãs ortodoxas, o casal é adornado com uma coroa de ouro (embora alguns optem por coroas de flores) durante a cerimônia, um amálgama de ritos simbólicos.
Em 24 de agosto de 2020, arqueólogos israelenses descobriram um tesouro de moedas de ouro islâmicas antigas perto da cidade central de Yavne. A análise da coleção extremamente rara de 425 moedas de ouro indicou que elas eram do final do século IX. Datando de cerca de 1.100 anos atrás, as moedas de ouro eram do califado abássida.
Produção
De acordo com o Serviço Geológico dos Estados Unidos em 2016, cerca de 5.726.000.000 onças troy (178.100 t) de ouro foram contabilizadas, das quais 85% permanecem em uso ativo.
Mineração e prospecção
Desde a década de 1880, a África do Sul tem sido a fonte de uma grande proporção do suprimento mundial de ouro, e cerca de 22% do ouro atualmente contabilizado é da África do Sul. A produção em 1970 representava 79% da oferta mundial, cerca de 1.480 toneladas. Em 2007, a China (com 276 toneladas) ultrapassou a África do Sul como o maior produtor mundial de ouro, a primeira vez desde 1905 que a África do Sul não era o maior.
Em 2020, a China foi o principal país minerador de ouro do mundo, seguida por Rússia, Austrália, Estados Unidos, Canadá e Gana.
Na América do Sul, o polêmico projeto Pascua Lama visa à exploração de ricas jazidas nas altas montanhas do Deserto do Atacama, na fronteira entre Chile e Argentina.
Estima-se que até um quarto da produção global anual de ouro se origina da mineração artesanal ou de pequena escala.
A cidade de Joanesburgo, localizada na África do Sul, foi fundada como resultado da Corrida do Ouro de Witwatersrand, que resultou na descoberta de alguns dos maiores depósitos naturais de ouro da história registrada. Os campos de ouro estão confinados às bordas norte e noroeste da bacia de Witwatersrand, que é uma camada de rochas arqueanas de 5 a 7 km (3,1 a 4,3 milhas) de espessura localizada, na maioria dos lugares, nas profundezas do Estado Livre, Gauteng e províncias vizinhas. Essas rochas de Witwatersrand estão expostas na superfície de Witwatersrand, dentro e ao redor de Joanesburgo, mas também em trechos isolados a sudeste e sudoeste de Joanesburgo, bem como em um arco ao redor do Vredefort Dome, que fica próximo ao centro da bacia de Witwatersrand. A partir dessas exposições superficiais, a bacia mergulha extensivamente, exigindo que parte da mineração ocorra em profundidades de quase 4.000 m (13.000 pés), tornando-as, especialmente as minas de Savuka e TauTona a sudoeste de Joanesburgo, as minas mais profundas da Terra. O ouro é encontrado apenas em seis áreas onde os rios arqueanos do norte e noroeste formaram extensos deltas de rios trançados de seixos antes de drenar para o "mar de Witwatersrand" onde o resto dos sedimentos de Witwatersrand foram depositados.
A Segunda Guerra dos Bôeres de 1899–1901 entre o Império Britânico e os Bôeres Africâneres foi, pelo menos em parte, sobre os direitos dos mineiros e a posse da riqueza do ouro na África do Sul.
Durante o século XIX, as corridas de ouro ocorreram sempre que grandes depósitos de ouro eram descobertos. A primeira descoberta documentada de ouro nos Estados Unidos foi na mina de ouro de Reed, perto de Georgeville, Carolina do Norte, em 1803. A primeira grande greve de ouro nos Estados Unidos ocorreu em uma pequena cidade do norte da Geórgia chamada Dahlonega. Outras corridas de ouro ocorreram na Califórnia, Colorado, The Black Hills, Otago, na Nova Zelândia, vários locais em toda a Austrália, Witwatersrand na África do Sul e o Klondike no Canadá.
A mina de Grasberg, localizada em Papua, na Indonésia, é a maior mina de ouro do mundo.Extração e refino
A extração de ouro é mais econômica em depósitos grandes e facilmente extraídos. Notas de minério de apenas 0,5 partes por milhão (ppm) podem ser econômicas. Os graus de minério típicos em minas de poço aberto são de 1 a 5 ppm; As notas de minério nas minas subterrâneas ou de hard rock geralmente são de pelo menos 3 ppm. Como os graus de minério de 30 ppm geralmente são necessários antes que o ouro seja visível a olho nu, na maioria das minas de ouro, o ouro é invisível.Os custos médios de mineração e extração de ouro foram de cerca de US $ 317 por onça de Troy em 2007, mas isso pode variar amplamente, dependendo do tipo de mineração e da qualidade do minério; A produção global de minas era de 2.471,1 toneladas.
Após a produção inicial, o ouro é frequentemente refinado industrialmente pelo processo Wohlwill, baseado em eletrólise ou pelo processo Miller, que é a cloração no fundido. O processo Wohlwill resulta em maior pureza, mas é mais complexo e é aplicado apenas em instalações em pequena escala. Outros métodos de teste e purificação de quantidades menores de ouro incluem separação e inquérito, além de métodos de conteúdo, ou refino com base na dissolução do ouro em Aqua regia.
A partir de 2020, a quantidade de dióxido de carbono co 2 produzido na mineração de um quilograma de ouro são 16 toneladas, enquanto a reciclagem de um quilograma de ouro produz 53 kg de co 2 equivalente. Aproximadamente 30 % da oferta global de ouro é reciclada e não é extraída a partir de 2020.
As empresas estão começando a adotar a reciclagem de ouro, incluindo empresas de joalheria, como empresas de coleta de gerações e computadores, incluindo a Dell.
consumo
| Pais | 2009 | 2010 | 2011 | 2012 | 2013 |
|---|---|---|---|---|---|
| 442.37 | 745.70 | 986.3 | 864 | 974 | |
| 376.96 | 42,00 | 92. | 81. | 112. | |
| 150.28 | 128.61 | 195. | 161 | 190 | |
| 75.16 | 74.07 | 143 | 118 | 175.2 | |
| 77.75 | 72.95 | 69.1 | 5,5 | 72.2 | |
| 60.12. | 67.50 | 76.7 | 8. | 73.3 | |
| 67.60 | 63.37 | 60.9 | 58.1 | 77.1 | |
| 56.68 | 53.43 | 36 | 47.8 | 57.3 | |
| Quatro. | 32.75 | 55 | 5. | 68 | |
| 31.75 | 27.35 | 22.6 | 11 de Setembro | 23.4 | |
| Outros países do Golfo Pérsico | 24.10 | 21.97 | 22 | 199. | 24.6 |
| 21.85 | 18.50 | -30.1. | 7.6 | 21.3 | |
| 18.83 | 15.87 | 15.5 | 1/2.2 | 17.5 | |
| 15.08 | 14.36 | 100.8 | 77 | 92.2 | |
| 7.33 | 6.28 | 107.4 | 80.9 | 140.1 | |
| Total | 1466.86 | 1770.71 | 27 de Dezembro. | 247 | 312. |
| Países | 256. | 254.0 | 390.4 | 39,5 | 450.7 |
| Total geral | 1718.46 | 2024.71 | 3176.52 | 287. | 357. |
O consumo do ouro produzido no mundo é de cerca de 50% em joias, 40% em investimentos e 10% na indústria.
De acordo com o World Gold Council, a China foi o maior consumidor individual de ouro do mundo em 2013, ultrapassando a Índia.
Poluição
A produção de ouro está associada à contribuição para a poluição perigosa.
O minério de ouro de baixo teor pode conter menos de um metal de ouro ppm; esse minério é moído e misturado com cianeto de sódio para dissolver o ouro. O cianeto é um produto químico altamente venenoso, que pode matar criaturas vivas quando exposto em quantidades mínimas. Muitos derramamentos de cianeto de minas de ouro ocorreram em países desenvolvidos e em desenvolvimento, matando a vida aquática em longos trechos de rios afetados. Ambientalistas consideram esses eventos grandes desastres ambientais. Até trinta toneladas de minério usado podem ser despejadas como resíduos para a produção de uma onça troy de ouro. Os depósitos de minério de ouro são a fonte de muitos elementos pesados, como cádmio, chumbo, zinco, cobre, arsênico, selênio e mercúrio. Quando os minerais contendo sulfeto nesses depósitos de minério são expostos ao ar e à água, o sulfeto se transforma em ácido sulfúrico que, por sua vez, dissolve esses metais pesados, facilitando sua passagem para as águas superficiais e subterrâneas. Este processo é chamado de drenagem ácida de mina. Esses depósitos de minério de ouro são resíduos altamente perigosos de longo prazo, perdendo apenas para depósitos de lixo nuclear.
Era comum usar mercúrio para recuperar ouro do minério, mas hoje o uso de mercúrio é amplamente limitado a mineradores individuais de pequena escala. Quantidades mínimas de compostos de mercúrio podem atingir corpos d'água, causando contaminação por metais pesados. O mercúrio pode então entrar na cadeia alimentar humana na forma de metilmercúrio. O envenenamento por mercúrio em humanos causa danos incuráveis à função cerebral e retardo grave.
A extração de ouro também é uma indústria altamente intensiva em energia, extraindo minério de minas profundas e moendo a grande quantidade de minério para posterior extração química requer quase 25 kWh de eletricidade por grama de ouro produzido.
Uso monetário
O ouro tem sido amplamente utilizado em todo o mundo como dinheiro, para troca indireta eficiente (versus troca) e para armazenar riqueza em hordas. Para fins de troca, as balas produzem moedas padronizadas de ouro, barras e outras unidades de peso e pureza fixa.
As primeiras moedas conhecidas contendo ouro foram atingidas em Lydia, Ásia Menor, por volta de 600 aC. A moeda talento de ouro em uso durante os períodos da história grega antes e durante o tempo da vida de Homer pesava entre 8,42 e 8,75 gramas. De uma preferência anterior no uso de prata, as economias européias restabeleceram a cunhagem de ouro como cunhagem durante os séculos XIII e XIV.
Bills (que amadurecem em moedas de ouro) e certificados de ouro (conversíveis em moeda de ouro no banco emissor) adicionados ao estoque circulante de dinheiro padrão -ouro na maioria das economias industriais do século XIX. Em preparação para a Primeira Guerra Mundial, as nações em guerra se mudaram para padrões fracionários de ouro, inflando suas moedas para financiar o esforço de guerra. Pós-guerra, os países vitoriosos, principalmente a Grã-Bretanha, restauraram gradualmente a conversão de ouro, mas os fluxos internacionais de ouro por meio de notas de câmbio permaneceram embargados; Remessas internacionais foram feitas exclusivamente para negociações bilaterais ou para pagar reparações de guerra.
Após a Segunda Guerra Mundial, o ouro foi substituído por um sistema de moedas nominalmente conversíveis relacionadas por taxas de câmbio fixas após o sistema Bretton Woods. Os padrões de ouro e a convertibilidade direta das moedas em ouro foram abandonados pelos governos mundiais, liderados em 1971 pelos Estados Unidos ' Recusa em resgatar seus dólares em ouro. A moeda fiduciária agora preenche a maioria dos papéis monetários. A Suíça foi o último país a amarrar sua moeda ao ouro; Isso foi encerrado por um referendo em 1999.
Os bancos centrais continuam mantendo uma parte de suas reservas líquidas como ouro de alguma forma, e trocas de metais como a London Bullion Market Association ainda transações claras denominadas em ouro, incluindo futuros contratos de entrega. Hoje, a saída de mineração de ouro está diminuindo. Com o forte crescimento das economias no século XX e o aumento das câmbio, as reservas de ouro do mundo e seu mercado comercial se tornaram uma pequena fração de todos os mercados e as taxas de câmbio fixas de moedas ao ouro foram substituídas por preços flutuantes Para contrato futuro de ouro e ouro. Embora o estoque de ouro cresça apenas 1% ou 2% ao ano, muito pouco metal é consumido irremediavelmente. O inventário acima do solo satisfaria muitas décadas de usos industriais e até artesanais a preços atuais.A proporção de ouro (finura das ligas é medida por Karat (K). O ouro puro (denominado comercialmente Fine Gold) é designado como 24 karat, abreviado 24K. As moedas em ouro inglesas destinadas à circulação de 1526 até a década de 1930 eram tipicamente uma liga de 22k padrão chamada Crown Gold, para dureza (moedas de ouro americanas para circulação após 1837 contêm uma liga de 0,900 ouro fino, ou 21,6 kt).
Embora os preços de alguns metais do grupo de platina possam ser muito mais altos, o ouro tem sido considerado o mais desejável dos metais preciosos e seu valor foi usado como padrão para muitas moedas. O ouro tem sido usado como um símbolo de pureza, valor, realeza e particularmente papéis que combinam essas propriedades. O ouro como um sinal de riqueza e prestígio foi ridicularizado por Thomas mais em seu tratado utopia . Naquela ilha imaginária, o ouro é tão abundante que é usado para fazer correntes para escravos, utensílios de mesa e assentos de lavatório. Quando os embaixadores de outros países chegam, vestidos com jóias de ouro e distintivos ostensivos, os utópicos os confundem com servos servos, prestando homenagem ao mais modestamente vestido de sua festa.
O código de moeda ISO 4217 de ouro é XAU. Muitos detentores de ouro o armazenam em forma de moedas ou barras de ouro como uma cobertura contra a inflação ou outras interrupções econômicas, embora sua eficácia tenha sido questionada; Historicamente, não se provou confiável como um instrumento de hedge. Moedas de ouro modernas para fins de investimento ou colecionador não requerem boas propriedades de desgaste mecânico; Eles são tipicamente ouro fino em 24k, embora a águia dourada americana e o soberano de ouro britânico continuem a ser cunhado em 22k (0,92) metal na tradição histórica, e o Krugerrand sul -africano, lançado pela primeira vez em 1967, também é 22k (0,92).
A edição especial moeda de folhas de bordo de ouro canadense contém o ouro de mais alta pureza de qualquer moeda de ouro, a 99,999% ou 0,99999, enquanto a edição popular Canadian Gold Maple Leaf Moeda tem uma pureza de 99,99%. Em 2006, a Casa da Moeda dos Estados Unidos começou a produzir a moeda americana de ouro de Buffalo Gold com uma pureza de 99,99%. Os cangurus australianos de ouro foram cunhados pela primeira vez em 1986, como a pepita de ouro australiana, mas mudou o design reverso em 1989. Outras moedas modernas incluem a moeda austríaca de bérola da Filarmônica de Viena e a panda de ouro chinesa.
preço
Em setembro de 2017, o ouro é avaliado em cerca de US $ 42 por grama (US $ 1.300 por onça de troy).
Como outros metais preciosos, o ouro é medido pelo peso de Troy e por gramas. A proporção de ouro na liga é medida por karat (k), com 24 karat (24k) sendo de ouro puro (100%) e menor número de karat proporcionalmente menor (18k = 75%). A pureza de uma barra de ouro ou moeda também pode ser expressa como uma figura decimal que varia de 0 a 1, conhecida como Finidade Millesimal, como 0,995 sendo quase pura.
O preço do ouro é determinado através da negociação nos mercados de ouro e derivativos, mas um procedimento conhecido como fixação de ouro em Londres, originário de setembro de 1919, fornece um preço diário de referência para o setor. A fixação da tarde foi introduzida em 1968 para fornecer um preço quando os mercados dos EUA estiverem abertos.
História
Historicamente, a moeda de ouro era amplamente utilizada como moeda; Quando o dinheiro foi introduzido, normalmente era um recibo resgatável para moedas ou barras de ouro. Em um sistema monetário conhecido como padrão -ouro, um certo peso de ouro recebeu o nome de uma unidade de moeda. Por um longo período, o governo dos Estados Unidos estabeleceu o valor do dólar americano, de modo que uma onça de Troy era igual a US $ 20,67 (US $ 0,665 por grama), mas em 1934 o dólar foi desvalorizado para US $ 35,00 por onça de Troy (US $ 0,889/g). Em 1961, estava se tornando difícil manter esse preço, e um pool de bancos americanos e europeus concordou em manipular o mercado para impedir a desvalorização da moeda contra o aumento da demanda de ouro.
Em 17 de março de 1968, as circunstâncias econômicas causaram o colapso da piscina de ouro, e um esquema de preços de duas camadas foi estabelecido em que o ouro ainda era usado para liquidar contas internacionais no antigo US $ 35,00 por onça troy (US $ 1,13/g), mas o O preço do ouro no mercado privado foi autorizado a flutuar; Esse sistema de preços de duas camadas foi abandonado em 1975, quando o preço do ouro foi deixado para encontrar seu nível de livre mercado. Os bancos centrais ainda possuem reservas históricas de ouro como uma loja de valor, embora o nível esteja geralmente em declínio. O maior depositário de ouro do mundo é o do Federal Reserve Bank dos EUA em Nova York, que detém cerca de 3% do ouro conhecido por existir e contabilizou hoje, assim como o depositário de ouro da mesma forma de Bullion nos EUA em Fort Knox. Em 2005, o World Gold Council estimou que a oferta total total de ouro é de 3.859 toneladas e a demanda em 3.754 toneladas, dando um superávit de 105 toneladas.Após 15 de agosto de 1971 Nixon Shock, o preço começou a aumentar bastante e, entre 1968 e 2000, o preço do ouro variou amplamente, de uma alta de US $ 850 por onça de Troy (US $ 27,33/g) em 21 de janeiro de 1980, a uma baixa de US $ 252,90 por onça Troy (US $ 8,13/g) em 21 de junho de 1999 (Fixação de ouro de Londres). Os preços aumentaram rapidamente em relação a 2001, mas a alta de 1980 não foi excedida até 3 de janeiro de 2008, quando foi estabelecido um novo máximo de US $ 865,35 por onça de Troy. Outro preço recorde foi estabelecido em 17 de março de 2008, a US $ 1023,50 por onça de Troy (US $ 32,91/g).
No final de 2009, os mercados de ouro experimentaram impulso renovado para cima devido ao aumento da demanda e a um dólar enfraquecedor dos EUA. Em 2 de dezembro de 2009, o ouro atingiu um novo fechamento alto em US $ 1.217,23. O Gold reuniu ainda mais altos em maio de 2010, depois que a crise da dívida da União Europeia provocou uma compra adicional de ouro como um ativo seguro. Em 1 de março de 2011, o Gold atingiu uma nova alta de todos os tempos de US $ 1432,57, com base em preocupações com os investidores em relação à agitação em andamento no norte da África e no Oriente Médio.
De abril de 2001 a agosto de 2011, spot preços de ouro mais do que o quintuplicado em valor em relação ao dólar americano, atingindo uma nova alta de US $ 1.913,50 em 23 de agosto de 2011, provocando especulações de que o longo mercado de baixa secular havia terminado e um touro O mercado havia retornado. No entanto, o preço começou um declínio lento em relação a US $ 1200 por onça de Troy no final de 2014 e 2015.
Em agosto de 2020, o preço do ouro chegou a US $ 2060 por onça após um crescimento total de 59% de agosto de 2018 a outubro de 2020, um período durante o qual superou o retorno total da NASDAQ de 54%.
Os futuros de ouro são negociados na Bolsa Comex. Esses contatos custam US $ por onça de troy (1 onça de troy = 31.1034768 gramas). Abaixo estão as especificações do contrato CQG que descrevem os contratos futuros:
| Ouro (GCA) | |
|---|---|
| Troca: | COMÉRCIO |
| Sector: | Metal |
| Tamanho da gravata: | 0.1 |
| Valor: | 10 USD |
| BPV: | 100. |
| Denominação: | USD / USD |
| Lugar decimal: | 1 |
Usos medicinais
Aplicações medicinais de ouro e seus complexos têm uma longa história que remonta a milhares de anos. Vários complexos de ouro foram aplicados para tratar a artrite reumatóide, sendo o mais frequentemente usado aurotiomalato, aurotioglucose e auranofina. Os compostos de ouro (i) e ouro (III) foram investigados como possíveis medicamentos anticâncer. Para complexos de ouro (iii), a redução ao ouro (0/i) em condições fisiológicas deve ser considerada. Os complexos estáveis podem ser gerados usando diferentes tipos de sistemas de ligantes bi, tri- e tetradentados, e sua eficácia foi demonstrada in vitro e in vivo.
Outras aplicações
Jóias
Devido à suavidade do ouro puro (24k), geralmente é ligado a metais básicos para uso em joias, alterando sua dureza e ductilidade, ponto de fusão, cor e outras propriedades. Ligas com classificação de quilates mais baixa, normalmente 22k, 18k, 14k ou 10k, contêm porcentagens mais altas de cobre ou outros metais básicos ou prata ou paládio na liga. O níquel é tóxico e sua liberação do ouro branco de níquel é controlada pela legislação na Europa. As ligas de paládio-ouro são mais caras do que as que usam níquel. As ligas de ouro branco de alto quilate são mais resistentes à corrosão do que a prata pura ou a prata de lei. O artesanato japonês de Mokume-gane explora os contrastes de cores entre ligas de ouro coloridas laminadas para produzir efeitos decorativos de veios de madeira.
Em 2014, a indústria de joias de ouro estava crescendo, apesar da queda nos preços do ouro. A demanda no primeiro trimestre de 2014 elevou o faturamento para US$ 23,7 bilhões, de acordo com um relatório do World Gold Council.
A solda de ouro é usada para unir os componentes de joias de ouro por meio de solda ou brasagem de alta temperatura. Se o trabalho for de qualidade marcante, a liga de solda de ouro deve corresponder à finura (pureza) do trabalho, e as fórmulas da liga são fabricadas para combinar com a cor do ouro amarelo e branco. A solda de ouro geralmente é feita em pelo menos três faixas de ponto de fusão, chamadas de Fácil, Médio e Duro. Usando a solda dura de alto ponto de fusão primeiro, seguida por soldas com pontos de fusão progressivamente mais baixos, os ourives podem montar itens complexos com várias juntas soldadas separadas. O ouro também pode ser transformado em linha e usado em bordados.
Eletrônicos
Apenas 10% do consumo mundial de ouro novo produzido vai para a indústria, mas de longe o uso industrial mais importante para o ouro novo é na fabricação de conectores elétricos livres de corrosão em computadores e outros dispositivos elétricos. Por exemplo, de acordo com o World Gold Council, um telefone celular típico pode conter 50 mg de ouro, no valor de cerca de 2 dólares e 82 centavos. Mas como quase um bilhão de telefones celulares são produzidos a cada ano, um valor de ouro de US$ 2,82 em cada telefone adiciona US$ 2,82 bilhões em ouro apenas a partir deste aplicativo. (Preços atualizados até novembro de 2022)
Embora o ouro seja atacado por cloro livre, sua boa condutividade e resistência geral à oxidação e corrosão em outros ambientes (incluindo resistência a ácidos não clorados) levaram ao seu uso industrial generalizado na era eletrônica como revestimento de camada fina nos conectores elétricos, garantindo assim uma boa conexão. Por exemplo, o ouro é usado nos conectores dos cabos eletrônicos mais caros, como cabos de áudio, vídeo e USB. O benefício de usar ouro sobre outros metais conectores, como estanho, nessas aplicações, tem sido debatido; os conectores de ouro são frequentemente criticados por especialistas em audiovisual como desnecessários para a maioria dos consumidores e vistos simplesmente como uma jogada de marketing. No entanto, o uso de ouro em outras aplicações em contatos deslizantes eletrônicos em atmosferas altamente úmidas ou corrosivas e em contatos com um custo de falha muito alto (certos computadores, equipamentos de comunicação, espaçonaves, motores de aviões a jato) permanece muito comum.
Além dos contatos elétricos deslizantes, o ouro também é usado em contatos elétricos devido à sua resistência à corrosão, condutividade elétrica, ductilidade e ausência de toxicidade. Os contatos do interruptor são geralmente submetidos a tensões de corrosão mais intensas do que os contatos deslizantes. Fios finos de ouro são usados para conectar dispositivos semicondutores a seus invólucros por meio de um processo conhecido como wire bonding.
A concentração de elétrons livres no metal ouro é 5,91×1022 cm−3. O ouro é altamente condutor de eletricidade e tem sido usado para fiação elétrica em algumas aplicações de alta energia (somente a prata e o cobre são mais condutores por volume, mas o ouro tem a vantagem de resistência à corrosão). Por exemplo, fios elétricos de ouro foram usados durante alguns dos experimentos atômicos do Projeto Manhattan, mas grandes fios de prata de alta corrente foram usados nos ímãs separadores de isótopos de calutron no projeto.
Estima-se que 16% do ouro atualmente contabilizado no mundo e 22% da prata do mundo estejam contidos em tecnologia eletrônica no Japão.
Medicina
Compostos metálicos e de ouro são usados há muito tempo para fins medicinais. O ouro, geralmente como metal, é talvez o remédio administrado mais antigamente (aparentemente por praticantes xamânicos) e conhecido por Dioscórides. Nos tempos medievais, o ouro era frequentemente visto como benéfico para a saúde, na crença de que algo tão raro e belo só podia ser saudável. Mesmo alguns esoteristas modernos e formas de medicina alternativa atribuem ao ouro metálico um poder de cura.
No século 19, o ouro tinha a reputação de ser um ansiolítico, uma terapia para distúrbios nervosos. Depressão, epilepsia, enxaqueca e problemas glandulares, como amenorreia e impotência, foram tratados e, principalmente, o alcoolismo (Keeley, 1897).
O aparente paradoxo da própria toxicologia da substância sugere a possibilidade de sérias lacunas na compreensão da ação do ouro na fisiologia. Apenas sais e radioisótopos de ouro têm valor farmacológico, uma vez que o ouro elementar (metálico) é inerte a todos os produtos químicos que encontra dentro do corpo (por exemplo, o ouro ingerido não pode ser atacado pelo ácido estomacal). Alguns sais de ouro têm propriedades anti-inflamatórias e atualmente dois ainda são usados como fármacos no tratamento de artrite e outras condições semelhantes nos EUA (aurotiomalato de sódio e auranofina). Esses medicamentos foram explorados como um meio de ajudar a reduzir a dor e o inchaço da artrite reumatóide e também (historicamente) contra a tuberculose e alguns parasitas.
As ligas de ouro são usadas em odontologia restauradora, especialmente em restaurações dentárias, como coroas e pontes permanentes. As ligas de ouro' a leve maleabilidade facilita a criação de uma superfície de acoplamento molar superior com outros dentes e produz resultados geralmente mais satisfatórios do que aqueles produzidos pela confecção de coroas de porcelana. O uso de coroas de ouro em dentes mais proeminentes, como incisivos, é favorecido em algumas culturas e desencorajado em outras.
Preparações de ouro coloidal (suspensões de nanopartículas de ouro) em água são de cor vermelha intensa e podem ser feitas com tamanhos de partícula rigidamente controlados de até algumas dezenas de nanômetros por redução de cloreto de ouro com íons citrato ou ascorbato. O ouro coloidal é usado em aplicações de pesquisa em medicina, biologia e ciência dos materiais. A técnica de rotulagem imunogold explora a capacidade das partículas de ouro para adsorver moléculas de proteína em suas superfícies. Partículas de ouro coloidal revestidas com anticorpos específicos podem ser usadas como sondas para a presença e posição de antígenos nas superfícies das células. Em cortes ultrafinos de tecidos visualizados por microscopia eletrônica, os marcadores de imuno-ouro aparecem como pontos redondos extremamente densos na posição do antígeno.
O ouro, ou ligas de ouro e paládio, são aplicados como revestimento condutor em espécimes biológicos e outros materiais não condutores, como plásticos e vidro, para serem vistos em um microscópio eletrônico de varredura. O revestimento, que geralmente é aplicado por pulverização catódica com plasma de argônio, tem um papel triplo nessa aplicação. A condutividade elétrica muito alta do ouro drena carga elétrica para a terra, e sua densidade muito alta fornece poder de parada para elétrons no feixe de elétrons, ajudando a limitar a profundidade em que o feixe de elétrons penetra no espécime. Isso melhora a definição da posição e topografia da superfície do espécime e aumenta a resolução espacial da imagem. O ouro também produz uma alta saída de elétrons secundários quando irradiado por um feixe de elétrons, e esses elétrons de baixa energia são a fonte de sinal mais comumente usada no microscópio eletrônico de varredura.
O isótopo ouro-198 (meia-vida de 2,7 dias) é usado na medicina nuclear, em alguns tratamentos contra o câncer e no tratamento de outras doenças.
Cozinha
- O ouro pode ser usado em alimentos e tem o E número 175. Em 2016, a Autoridade Europeia para a Segurança Alimentar publicou um parecer sobre a reavaliação do ouro como aditivo alimentar. As preocupações incluíram a possível presença de minúsculas quantidades de nanopartículas de ouro no aditivo alimentar, e que as nanopartículas de ouro foram mostradas como genotóxicos em células mamíferas in vitro.
- Folha de ouro, floco ou pó é usado em e em alguns alimentos gourmet, notavelmente doces e bebidas como ingrediente decorativo. O floco de ouro foi usado pela nobreza na Europa medieval como uma decoração em alimentos e bebidas,
- Danziger Goldwasser (em alemão: Gold water of Danzig) ou Goldwasser (em inglês: Água do ouro) é um licor herbal alemão tradicional produzido no que é hoje Gdańsk, Polônia, e Schwabach, Alemanha, e contém flocos de folha de ouro. Há também alguns coquetéis caros (c. $1000) que contêm flocos de folha de ouro. No entanto, uma vez que o ouro metálico é inerte para toda a química corporal, não tem gosto, não fornece nutrição, e deixa o corpo inalterado.
- Vark é uma folha metálica composta por um metal puro que às vezes é ouro, e é usado para decorar doces na cozinha sul-asiática.
Diversos
- O ouro produz uma cor vermelha profunda e intensa quando usado como agente de coloração em vidro de cranberry.
- Na fotografia, os toners de ouro são usados para mudar a cor de brometo de prata preto-e-branco impressões para tons marrom ou azul, ou para aumentar sua estabilidade. Usado em estampas de sépia, os toners de ouro produzem tons vermelhos. Kodak publicou fórmulas para vários tipos de toners de ouro, que usam ouro como o cloreto.
- O ouro é um bom refletor de radiação eletromagnética, como luz infravermelha e visível, bem como ondas de rádio. É usado para os revestimentos protetores em muitos satélites artificiais, em faceplates protetoras de infravermelhos em ternos de proteção térmica e capacetes de astronautas, e em aviões de guerra eletrônica, como o EA-6B Prowler.
- O ouro é usado como a camada reflexiva em alguns CDs high-end.
- Os automóveis podem usar ouro para blindagem de calor. McLaren usa folha de ouro no compartimento do motor de seu modelo F1.
- O ouro pode ser fabricado tão fino que parece semi-transparente. É usado em algumas janelas de cockpit de aeronaves para de-icing ou anti-icing por passar a eletricidade através dele. O calor produzido pela resistência do ouro é suficiente para evitar que o gelo se forma.
- O ouro é atacado e dissolve-se em soluções alcalinas de potássio ou cianeto de sódio, para formar o cianeto de ouro de sal — uma técnica que tem sido usada na extração de ouro metálico de minérios no processo de cianeto. Cianeto de ouro é o eletrólito usado na galvanoplastia comercial de ouro em metais comuns e eletroformagem.
- As soluções de cloreto de ouro (ácido clorídrico) são usadas para fazer ouro coloidal pela redução com íons de citrato ou ascorbato. Cloreto de ouro e óxido de ouro são usados para fazer cranberry ou vidro de cor vermelha, que, como suspensões de ouro coloidal, contém nanopartículas de ouro esférico de tamanho uniforme.
- O ouro, quando dispersado em nanopartículas, pode atuar como um catalisador heterogêneo de reações químicas.
Toxicidade
O ouro metálico puro (elemental) não é tóxico e não irritante quando ingerido e às vezes é usado como decoração de alimentos na forma de folha de ouro. O ouro metálico também é um componente das bebidas alcoólicas Goldschläger, Gold Strike e Goldwasser. O ouro metálico é aprovado como aditivo alimentar na UE (E175 no Codex Alimentarius). Embora o íon de ouro seja tóxico, a aceitação do ouro metálico como aditivo alimentar se deve à sua relativa inércia química e resistência à corrosão ou à transformação em sais solúveis (compostos de ouro) por qualquer processo químico conhecido que possa ser encontrado no ser humano. corpo.
Compostos solúveis (sais de ouro), como o cloreto de ouro, são tóxicos para o fígado e os rins. Os sais comuns de cianeto de ouro, como o cianeto de ouro e potássio, usados na galvanoplastia de ouro, são tóxicos em virtude de seu teor de cianeto e ouro. Existem casos raros de envenenamento letal por ouro por cianeto de ouro e potássio. A toxicidade do ouro pode ser melhorada com a terapia de quelação com um agente como o dimercaprol.
O metal dourado foi eleito o Alérgeno do Ano em 2001 pela American Contact Dermatitis Society; as alergias de contato com ouro afetam principalmente as mulheres. Apesar disso, o ouro é um alérgeno de contato relativamente não potente, em comparação com metais como o níquel.
Uma amostra do fungo Aspergillus niger foi encontrada crescendo em uma solução de mineração de ouro; e descobriu-se que continha complexos de cianometal, como ouro, prata, cobre, ferro e zinco. O fungo também desempenha um papel na solubilização de sulfetos de metais pesados.
Contenido relacionado
Ligando
Lantanídeo
Glicolise