Fórmula química
Em química, uma fórmula química é uma forma de apresentar informações sobre as proporções químicas dos átomos que constituem um determinado composto químico ou molécula, usando símbolos de elementos químicos, números e, às vezes, também outros símbolos, como parênteses, hífens, colchetes, vírgulas e sinais mais (+) e menos (-). Estes são limitados a uma única linha tipográfica de símbolos, que podem incluir subscritos e sobrescritos. Uma fórmula química não é um nome químico e não contém palavras. Embora uma fórmula química possa implicar em certas estruturas químicas simples, não é o mesmo que uma fórmula estrutural química completa. As fórmulas químicas podem especificar totalmente a estrutura apenas das moléculas e substâncias químicas mais simples e geralmente são mais limitadas em poder do que nomes químicos e fórmulas estruturais.
Os tipos mais simples de fórmulas químicas são chamados de fórmulas empíricas, que usam letras e números indicando as proporções numéricas de átomos de cada tipo. Fórmulas moleculares indicam os números simples de cada tipo de átomo em uma molécula, sem nenhuma informação sobre a estrutura. Por exemplo, a fórmula empírica da glicose é CH2O (duas vezes mais átomos de hidrogênio que carbono e oxigênio), enquanto sua fórmula molecular é C6H12< /sub>O6 (12 átomos de hidrogênio, seis átomos de carbono e oxigênio).
Às vezes, uma fórmula química é complicada por ser escrita como uma fórmula condensada (ou fórmula molecular condensada, ocasionalmente chamada de "fórmula semi-estrutural"), que transmite informações adicionais sobre as maneiras particulares pelas quais os átomos estão quimicamente ligados, seja em ligações covalentes, ligações iônicas ou várias combinações desses tipos. Isso é possível se a ligação relevante for fácil de mostrar em uma dimensão. Um exemplo é a fórmula molecular/química condensada do etanol, que é CH3−CH2−OH ou CH3CH2OH. No entanto, mesmo uma fórmula química condensada é necessariamente limitada em sua capacidade de mostrar relações complexas de ligação entre átomos, especialmente átomos que possuem ligações com quatro ou mais substituintes diferentes.
Uma vez que uma fórmula química deve ser expressa como uma única linha de símbolos de elementos químicos, muitas vezes ela não pode ser tão informativa quanto uma verdadeira fórmula estrutural, que é uma representação gráfica da relação espacial entre átomos em compostos químicos (veja, por exemplo, o figura para as fórmulas estruturais e químicas do butano, à direita). Por razões de complexidade estrutural, uma única fórmula química condensada (ou fórmula semi-estrutural) pode corresponder a diferentes moléculas, conhecidas como isômeros. Por exemplo, a glicose compartilha sua fórmula molecular C6H12< /sub>O6 com vários outros açúcares, incluindo frutose, galactose e manose. Existem nomes químicos equivalentes lineares que podem e especificam exclusivamente qualquer fórmula estrutural complexa (consulte a nomenclatura química), mas esses nomes devem usar muitos termos (palavras), em vez de símbolos simples de elementos, números e símbolos tipográficos que definem uma fórmula química.
Fórmulas químicas podem ser usadas em equações químicas para descrever reações químicas e outras transformações químicas, como a dissolução de compostos iônicos em uma solução. Embora, como observado, as fórmulas químicas não tenham todo o poder das fórmulas estruturais para mostrar as relações químicas entre os átomos, elas são suficientes para acompanhar o número de átomos e o número de cargas elétricas nas reações químicas, equilibrando assim as equações químicas de modo que essas equações pode ser usado em problemas químicos envolvendo conservação de átomos e conservação de carga elétrica.
Visão geral
Uma fórmula química identifica cada elemento constituinte pelo seu símbolo químico e indica o número proporcional de átomos de cada elemento. Nas fórmulas empíricas, essas proporções começam com um elemento-chave e, em seguida, atribuem números de átomos dos outros elementos no composto, por razões para o elemento-chave. Para compostos moleculares, esses números de razão podem ser expressos como números inteiros. Por exemplo, a fórmula empírica do etanol pode ser escrita C2H6O porque todas as moléculas de etanol contêm dois átomos de carbono, seis átomos de hidrogênio e um átomo de oxigênio. Alguns tipos de compostos iônicos, no entanto, não podem ser escritos com fórmulas empíricas inteiramente inteiras. Um exemplo é o carboneto de boro, cuja fórmula de CBn é uma variável Razão de números não inteiros com n variando de mais de 4 a mais de 6,5.
Quando o composto químico da fórmula consiste em moléculas simples, as fórmulas químicas geralmente empregam maneiras de sugerir a estrutura da molécula. Esses tipos de fórmulas são conhecidos como fórmulas moleculares e fórmulas condensadas. Uma fórmula molecular enumera o número de átomos para refletir aqueles na molécula, de modo que a fórmula molecular da glicose seja C6 H12O6 em vez da fórmula empírica da glicose, que é < span class="chemf nowrap">CH2O. No entanto, exceto para substâncias muito simples, as fórmulas químicas moleculares carecem de informações estruturais necessárias e são ambíguas.
Para moléculas simples, uma fórmula condensada (ou semi-estrutural) é um tipo de fórmula química que pode implicar totalmente em uma fórmula estrutural correta. Por exemplo, o etanol pode ser representado pela fórmula química condensada CH3CH2OH e éter dimetílico pela fórmula condensada CH3OCH3. Essas duas moléculas têm as mesmas fórmulas empíricas e moleculares (C2H6O), mas podem ser diferenciados pelas fórmulas condensadas mostradas, que são suficientes para representar a estrutura completa desses compostos orgânicos simples.
Fórmulas químicas condensadas também podem ser usadas para representar compostos iônicos que não existem como moléculas discretas, mas ainda assim contêm aglomerados ligados covalentemente dentro deles. Esses íons poliatômicos são grupos de átomos que estão ligados covalentemente e têm uma carga iônica geral, como o sulfato [SO4]2− ion. Cada íon poliatômico em um composto é escrito individualmente para ilustrar os agrupamentos separados. Por exemplo, o composto hexóxido de dicloro tem uma fórmula empírica ClO3 e uma fórmula molecular Cl2O6, mas em líquido ou formas sólidas, este composto é mostrado mais corretamente por uma fórmula iônica condensada [ClO2]+[ClO4]-, que ilustra que este composto consiste em [ClO2] + íons e [ClO4]− íons. Nesses casos, a fórmula condensada só precisa ser complexa o suficiente para mostrar pelo menos uma de cada espécie iônica.
As fórmulas químicas descritas aqui são distintas dos nomes sistemáticos químicos muito mais complexos que são usados em vários sistemas de nomenclatura química. Por exemplo, um nome sistemático para glicose é (2R,3S,4R,5R) -2,3,4,5,6-pentahidroxihexanal. Este nome, interpretado pelas regras por trás dele, especifica totalmente a fórmula estrutural da glicose, mas o nome não é uma fórmula química como geralmente entendida e usa termos e palavras não usados em fórmulas químicas. Esses nomes, ao contrário das fórmulas básicas, podem representar fórmulas estruturais completas sem gráficos.
Tipos
Fórmula empírica
Em química, a fórmula empírica de um produto químico é uma expressão simples do número relativo de cada tipo de átomo ou proporção dos elementos no composto. Fórmulas empíricas são o padrão para compostos iônicos, como CaCl2, e para macromoléculas, como < span class="chemf nowrap">SiO2. Uma fórmula empírica não faz referência a isomeria, estrutura ou número absoluto de átomos. O termo empírico refere-se ao processo de análise elementar, uma técnica de química analítica usada para determinar a composição percentual relativa de uma substância química pura por elemento.
Por exemplo, o hexano tem uma fórmula molecular de C6H14, e (para um de seus isômeros, n-hexano) uma fórmula estrutural CH3 CH2CH2CH2CH2CH3, implicando que tem uma estrutura de cadeia de 6 átomos de carbono e 14 átomos de hidrogênio. No entanto, a fórmula empírica do hexano é C3H7< /sub>. Da mesma forma, a fórmula empírica para o peróxido de hidrogênio, H2O2< /sub>, é simplesmente HO, expressando a proporção de 1:1 dos elementos componentes. O formaldeído e o ácido acético têm a mesma fórmula empírica, CH2O. Esta é a fórmula química real do formaldeído, mas o ácido acético tem o dobro do número de átomos.
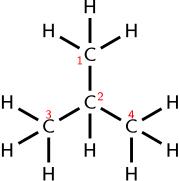
Fórmula molecular
Fórmula molecular: C4H. H. H.10.
Fórmula condensada: CH3CH2CH2CH3
As fórmulas moleculares indicam os números simples de cada tipo de átomo em uma molécula de uma substância molecular. Elas são as mesmas que as fórmulas empíricas para moléculas que possuem apenas um átomo de um tipo específico, mas, caso contrário, podem ter números maiores. Um exemplo da diferença é a fórmula empírica da glicose, que é CH2O ( proporção 1:2:1), enquanto sua fórmula molecular é C6H12O6 (número de átomos 6:12:6). Para água, ambas as fórmulas são H2O. Uma fórmula molecular fornece mais informações sobre uma molécula do que sua fórmula empírica, mas é mais difícil de estabelecer.
Uma fórmula molecular mostra o número de elementos em uma molécula e determina se é um composto binário, composto ternário, composto quaternário ou tem ainda mais elementos.
Fórmula estrutural
Além de indicar o número de átomos de cada molécula elementa, uma fórmula estrutural indica como os átomos estão organizados e mostra (ou sugere) as ligações químicas entre os átomos. Existem vários tipos de fórmulas estruturais focadas em diferentes aspectos da estrutura molecular.
Os dois diagramas mostram duas moléculas que são isômeros estruturais uma da outra, pois ambas possuem a mesma fórmula molecular C4H10, mas eles têm fórmulas estruturais diferentes conforme mostrado.
Fórmula condensada
A conectividade de uma molécula geralmente tem uma forte influência em suas propriedades físicas e químicas e em seu comportamento. Duas moléculas compostas pelos mesmos números dos mesmos tipos de átomos (ou seja, um par de isômeros) podem ter propriedades químicas e/ou físicas completamente diferentes se os átomos estiverem conectados de forma diferente ou em posições diferentes. Nesses casos, uma fórmula estrutural é útil, pois ilustra quais átomos estão ligados a quais outros. A partir da conectividade, muitas vezes é possível deduzir a forma aproximada da molécula.
Uma fórmula condensada (ou semi-estrutural) pode representar os tipos e o arranjo espacial das ligações em uma substância química simples, embora não especifique necessariamente isômeros ou estruturas complexas. Por exemplo, o etano consiste em dois átomos de carbono ligados entre si, com cada átomo de carbono tendo três átomos de hidrogênio ligados a ele. Sua fórmula química pode ser representada como CH3CH3. No etileno existe uma ligação dupla entre os átomos de carbono (e assim cada carbono possui apenas dois hidrogênios), portanto a fórmula química pode ser escrita: CH2CH2, e o fato de que existe uma dupla ligação entre os carbonos é implícito porque o carbono tem uma valência de quatro. No entanto, um método mais explícito é escrever H2C=CH2 ou menos comumente H2C::CH2. As duas linhas (ou dois pares de pontos) indicam que uma ligação dupla conecta os átomos de cada lado deles.
Uma ligação tripla pode ser expressa com três linhas (HC≡CH) ou três pares de pontos (HC:::CH ), e se houver ambigüidade, uma única linha ou um par de pontos pode ser usado para indicar uma única ligação.
Moléculas com vários grupos funcionais iguais podem ser expressas colocando o grupo repetido entre colchetes. Por exemplo, isobutano pode ser escrito (CH3)3< /sub>CH. Esta fórmula estrutural condensada implica uma conectividade diferente de outras moléculas que podem ser formadas usando os mesmos átomos nas mesmas proporções (isômeros). A fórmula (CH3)3CH< /span> implica um átomo de carbono central conectado a um átomo de hidrogênio e três grupos metil (CH3). O mesmo número de átomos de cada elemento (10 hidrogênios e 4 carbonos, ou C4H10) pode ser usado para fazer uma molécula de cadeia linear, n-butano: CH3CH2CH2 CH3.
Lei da composição
Em qualquer composto químico, os elementos sempre se combinam na mesma proporção entre si. Esta é a lei da composição constante.
A lei da composição constante diz que, em qualquer composto químico em particular, todas as amostras desse composto serão feitas dos mesmos elementos na mesma proporção ou razão. Por exemplo, qualquer molécula de água é sempre composta de dois átomos de hidrogênio e um átomo de oxigênio na proporção de 2:1. Se olharmos para as massas relativas de oxigênio e hidrogênio em uma molécula de água, veremos que 94% da massa de uma molécula de água é representada pelo oxigênio e os 6% restantes são a massa de hidrogênio. Esta proporção de massa será a mesma para qualquer molécula de água.
Nomes químicos em resposta às limitações das fórmulas químicas
O alceno chamado but-2-eno possui dois isômeros, cuja fórmula química CH3< /sub>CH=CHCH3 não identifica. A posição relativa dos dois grupos metil deve ser indicada por notação adicional indicando se os grupos metil estão no mesmo lado da ligação dupla (cis ou Z) ou no lados opostos entre si (trans ou E).
Como observado acima, para representar as fórmulas estruturais completas de muitos compostos orgânicos e inorgânicos complexos, pode ser necessária uma nomenclatura química que vai muito além dos recursos disponíveis usados acima em fórmulas condensadas simples. Veja a nomenclatura IUPAC de química orgânica e a nomenclatura IUPAC de química inorgânica 2005 para exemplos. Além disso, sistemas de nomenclatura linear, como o Identificador químico internacional (InChI), permitem que um computador construa uma fórmula estrutural, e o sistema simplificado de entrada de linha molecular (SMILES) permite uma entrada ASCII mais legível por humanos. No entanto, todos esses sistemas de nomenclatura vão além dos padrões das fórmulas químicas e, tecnicamente, são sistemas de nomenclatura química, não sistemas de fórmulas.
Polímeros em fórmulas condensadas
Para polímeros em fórmulas químicas condensadas, os parênteses são colocados ao redor da unidade de repetição. Por exemplo, uma molécula de hidrocarboneto descrita como CH3(CH2)50CH3, é uma molécula com cinquenta unidades repetidas. Se o número de unidades repetidas for desconhecido ou variável, a letra n pode ser usada para indicar esta fórmula: CH3(CH2)n CH3.
Íons em fórmulas condensadas
Para íons, a carga de um determinado átomo pode ser indicada com um sobrescrito à direita. Por exemplo, Na+ ou Cu2 +. A carga total em uma molécula carregada ou um íon poliatômico também pode ser mostrada desta forma, como para o hidrônio, H3O+, ou sulfato, SO< span>2−4. Observe que + e - são usados no lugar de +1 e -1, respectivamente.
Para íons mais complexos, colchetes [ ] são frequentemente usados para incluir a fórmula iônica, como em [B12 H12]2−, que é encontrado em compostos como dodecaborato de césio, Cs2[B12H12]. Parênteses () podem ser aninhados dentro de colchetes para indicar uma unidade repetida, como em cloreto de hexamminecobalto(III), [Co(NH3)6]3+Cl-3. Aqui, (NH3)6 indica que o íon contém seis grupos ammina (NH3) ligados ao cobalto e [ ] abrange toda a fórmula do íon com carga +3.
Isto é estritamente opcional; uma fórmula química é válida com ou sem informação de ionização, e o cloreto de hexamminecobalto(III) pode ser escrito como [Co(NH3)6]3+Cl− 3 ou [Co(NH3)6]Cl3. Os colchetes, como parênteses, se comportam em química como na matemática, agrupando termos - eles não são empregados especificamente apenas para estados de ionização. Neste último caso aqui, os parênteses indicam 6 grupos todos da mesma forma, ligados a outro grupo de tamanho 1 (o átomo de cobalto), e então todo o feixe, como um grupo, está ligado a 3 átomos de cloro. No primeiro caso, fica mais claro que a ligação que liga os cloros é iônica, e não covalente.
Isótopos
Embora os isótopos sejam mais relevantes para a química nuclear ou química de isótopos estáveis do que para a química convencional, diferentes isótopos podem ser indicados com um sobrescrito prefixado em uma fórmula química. Por exemplo, o íon fosfato contendo fósforo radioativo-32 é [32PO4]3−. Além disso, um estudo envolvendo proporções isotópicas estáveis pode incluir a molécula 18O 16O.
Um subscrito à esquerda às vezes é usado de forma redundante para indicar o número atômico. Por exemplo, 8O2 para dioxigênio e 16
< sub style="font-size:inherit;line-height:inherit;vertical-align:baseline">8O
2 para as espécies isotópicas mais abundantes de dioxigênio. Isso é conveniente ao escrever equações para reações nucleares, a fim de mostrar o equilíbrio de carga com mais clareza.
Átomos aprisionados
O símbolo @ (arroba) indica um átomo ou molécula presa dentro de uma gaiola, mas não ligada quimicamente a ela. Por exemplo, um buckminsterfulereno (C60) com um átomo (M) seria simplesmente representado como < span class="chemf nowrap">MC60 independentemente de M estar dentro do fulereno sem ligação química ou fora, ligado a um dos carbonos átomos. Usando o símbolo @, isso seria denotado M@C60 se M estivesse dentro da rede de carbono. Um exemplo não fulereno é [As@Ni12As20 ]3−, um íon no qual um átomo de arsênico (As) está preso em uma gaiola formada pelos outros 32 átomos.
Esta notação foi proposta em 1991 com a descoberta de gaiolas de fulereno (fulerenos endoédricos), que podem prender átomos como La para formar, por exemplo, La@C60 ou La@C82. A escolha do símbolo foi explicada pelos autores como sendo concisa, prontamente impressa e transmitida eletronicamente (o sinal de arroba está incluído no ASCII, no qual se baseiam os esquemas de codificação de caracteres mais modernos), e os aspectos visuais que sugerem a estrutura de um endoédrico fulereno.
Fórmulas químicas não estequiométricas
As fórmulas químicas geralmente usam números inteiros para cada elemento. No entanto, existe uma classe de compostos, chamados de compostos não estequiométricos, que não podem ser representados por inteiros pequenos. Essa fórmula pode ser escrita usando frações decimais, como em Fe0,95O, ou pode incluir um parte variável representada por uma letra, como em Fe1−xO, onde x é normalmente muito menor que 1.
Formas gerais para compostos orgânicos
Uma fórmula química usada para uma série de compostos que diferem uns dos outros por uma unidade constante é chamada de fórmula geral. Gera uma série homóloga de fórmulas químicas. Por exemplo, álcoois podem ser representados pela fórmula CnH2n + 1OH (n ≥ 1), dando os homólogos metanol, etanol, propanol para 1 ≤ n ≤ 3.
Sistema de colinas
O sistema de Hill (ou notação de Hill) é um sistema de escrita de fórmulas químicas empíricas, fórmulas químicas moleculares e componentes de uma fórmula condensada de modo que o número de átomos de carbono em uma molécula seja indicado primeiro, o número de átomos de hidrogênio em seguida, e então o número de todos os outros elementos químicos subseqüentemente, em ordem alfabética dos símbolos químicos. Quando a fórmula não contém carbono, todos os elementos, incluindo o hidrogênio, são listados em ordem alfabética.
Ao classificar fórmulas de acordo com o número de átomos de cada elemento presente na fórmula de acordo com essas regras, com diferenças em elementos ou números anteriores sendo tratados como mais significativos do que diferenças em qualquer elemento ou número posterior - como classificar strings de texto em ordem lexicográfica - é possível agrupar fórmulas químicas no que é conhecido como ordem do sistema Hill.
O sistema Hill foi publicado pela primeira vez por Edwin A. Hill, do Escritório de Marcas e Patentes dos Estados Unidos, em 1900. É o sistema mais comumente usado em bancos de dados químicos e índices impressos para classificar listas de compostos.
Uma lista de fórmulas na ordem do sistema Hill é organizada alfabeticamente, como acima, com elementos de uma letra vindo antes de símbolos de duas letras quando os símbolos começam com a mesma letra (assim, "B" vem antes de & #34;Be", que vem antes de "Br").
As fórmulas de exemplo a seguir são escritas usando o sistema Hill e listadas na ordem Hill:
- BrI
- BrClH2Si
- CC4
- CH3Eu...
- C2H. H. H.5B.
- H. H. H.2O4S
Contenido relacionado
Célula eletroquímica
Cristal
Processo endotérmico
Isomeria cis-trans
Hélio