Febre tifóide
Febre tifóide, também conhecida como tifóide, é uma doença causada pela bactéria Salmonella do sorotipo Typhi. Os sintomas variam de leves a graves e geralmente começam de seis a 30 dias após a exposição. Freqüentemente, há um início gradual de febre alta ao longo de vários dias. Isso geralmente é acompanhado por fraqueza, dor abdominal, prisão de ventre, dores de cabeça e vômitos leves. Algumas pessoas desenvolvem erupção cutânea com manchas rosadas. Em casos graves, as pessoas podem sentir confusão. Sem tratamento, os sintomas podem durar semanas ou meses. A diarreia pode ser grave, mas é incomum. Outras pessoas podem transmiti-lo sem serem afetadas, mas ainda assim são contagiosas. A febre tifóide é um tipo de febre entérica, junto com a febre paratifóide. Acredita-se que S. enterica Typhi infecte e se replique apenas em humanos.
A febre tifóide é causada pela bactéria Salmonella enterica subsp. enterica sorovar Typhi crescendo nos intestinos, placas de Peyer, gânglios linfáticos mesentéricos, baço, fígado, vesícula biliar, medula óssea e sangue. A febre tifóide é transmitida pela ingestão ou ingestão de alimentos ou água contaminados com fezes de uma pessoa infectada. Os factores de risco incluem acesso limitado a água potável e saneamento deficiente. Aqueles que ainda não foram expostos a ele e ingerem água potável ou alimentos contaminados correm maior risco de desenvolver sintomas. Apenas humanos podem ser infectados; não há reservatórios animais conhecidos.
O diagnóstico é feito através da cultura e identificação de S. enterica Typhi em amostras de pacientes ou detectar uma resposta imune ao patógeno em amostras de sangue. Recentemente, novos avanços na recolha e análise de dados em grande escala permitiram aos investigadores desenvolver melhores diagnósticos, tais como a detecção de alterações na abundância de pequenas moléculas no sangue que podem indicar especificamente febre tifóide. As ferramentas de diagnóstico em regiões onde a febre tifóide é mais prevalente são bastante limitadas na sua precisão e especificidade, e o tempo necessário para um diagnóstico adequado, a crescente propagação da resistência aos antibióticos e o custo dos testes são também dificuldades para os sistemas de saúde com poucos recursos.
Uma vacina contra a febre tifóide pode prevenir cerca de 40% a 90% dos casos durante os primeiros dois anos. A vacina pode ter algum efeito por até sete anos. Para pessoas de alto risco ou pessoas que viajam para áreas onde é comum, a vacinação é recomendada. Outros esforços para evitá-la incluem o fornecimento de água potável, bom saneamento e lavagem das mãos. Até que uma infecção seja confirmada como eliminada, a pessoa infectada não deve preparar comida para outras pessoas. A febre tifóide é tratada com antibióticos como azitromicina, fluoroquinolonas ou cefalosporinas de terceira geração. A resistência a estes antibióticos tem vindo a desenvolver-se, o que tornou o tratamento mais difícil.
Em 2015, foram notificados 12,5 milhões de novos casos de febre tifóide. A doença é mais comum na Índia. As crianças são mais comumente afetadas. A febre tifóide diminuiu no mundo desenvolvido na década de 1940 como resultado da melhoria do saneamento e do uso de antibióticos. Todos os anos, cerca de 400 casos são relatados nos EUA e cerca de 6.000 pessoas têm febre tifóide. Em 2015, resultou em cerca de 149.000 mortes em todo o mundo – abaixo das 181.000 em 1990. Sem tratamento, o risco de morte pode chegar a 20%. Com tratamento, fica entre 1% e 4%.
Did you mean:Typhus is a different disease. Owing to their similar symptoms, they were not recognized as distinct diseases until the 1800s. "Typhoid " means "resembling typhus ".
Sinais e sintomas
Classicamente, a progressão da febre tifóide não tratada tem três estágios distintos, cada um com duração de cerca de uma semana. Ao longo dessas etapas, o paciente fica exausto e emaciado.
- Na primeira semana, a temperatura corporal aumenta lentamente, e as flutuações de febre são vistas com a bradicardia relativa (sinal de gordura), mal-estar, dor de cabeça e tosse. Um nariz sangrento (epistaxis) é visto em um quarto dos casos, e a dor abdominal também é possível. Uma diminuição no número de células brancas circulantes (leukopenia) ocorre com eosinopenia e linfocitose relativa; as culturas sanguíneas são positivas para S. Enterica subsp. enterica serovar Typhi. O teste de Widal é geralmente negativo.
- Na segunda semana, a pessoa é muitas vezes muito cansada para se levantar, com febre alta em planalto em torno de 40 °C (104 °F) e bradicardia (dissociação esfigmotérmica ou sinal de Faget), classicamente com uma onda de pulso dicrotic. Delirium pode ocorrer, onde o paciente é muitas vezes calmo, mas às vezes fica agitado. Este delírio deu a tifoide o apelido de "febre nervosa". Os pontos de rosa aparecem no peito inferior e no abdômen em cerca de um terço dos pacientes. Rônquios (respirando sons) são ouvidos na base dos pulmões. O abdômen é distendido e doloroso no quadrante inferior direito, onde um som rutilante pode ser ouvido. A diarreia pode ocorrer nesta fase, mas a constipação também é comum. O baço e o fígado são aumentados (hepatoesplenomegalia) e terno, e as transaminases do fígado são elevadas. O teste de Widal é fortemente positivo, com anticorpos antiO e antiH. As culturas de sangue às vezes ainda são positivas.
- Na terceira semana de febre tifóide, uma série de complicações podem ocorrer:
- A febre ainda é muito alta e oscila muito pouco mais de 24 horas. A desidratação se inscreve junto com a desnutrição, e o paciente é delirante. Um terço das pessoas afetadas desenvolvem uma erupção macular no tronco.
- hemorragia intestinal devido ao sangramento nas manchas de Peyer congestionadas ocorre; isso pode ser muito sério, mas geralmente não é fatal.
- A perfuração intestinal no ileum distal é uma complicação muito séria e muitas vezes fatal. Pode ocorrer sem sintomas alarmantes até que a septicemia ou a peritonite difusa se insira.
- Doenças respiratórias como pneumonia e bronquite aguda
- Encephalitis
- Sintomas neuropsiquiátricos (descritos como "delirium mutuante" ou "vígil"), com a escolha de leitos ou objetos imaginários.
- Abcessos metastáticos, colecistite, endocardite e osteíte.
- Baixa contagem de plaquetas (trombocitopenia) às vezes é visto.
Causas

Bactérias
A bactéria Gram-negativa que causa a febre tifóide é a Salmonella enterica subsp. enterica sorovar Typhi. Com base no esquema de subtipagem MLST, os dois principais tipos de sequência do S. Typhi são ST1 e ST2, que são difundidos globalmente. A análise filogeográfica global mostrou a dominância de um haplótipo 58 (H58), que provavelmente se originou na Índia durante o final da década de 1980 e agora está se espalhando pelo mundo com resistência a múltiplas drogas. Um esquema de genotipagem mais detalhado foi relatado em 2016 e agora está sendo amplamente utilizado. Este esquema reclassificou a nomenclatura do H58 para o genótipo 4.3.1.
Transmissão
Ao contrário de outras cepas de Salmonella, nenhum animal portador de febre tifóide é conhecido. Os humanos são os únicos portadores conhecidos da bactéria. S. entérica subsp. enterica sorovar Typhi é transmitida pela via fecal-oral de pessoas infectadas e de portadores assintomáticos da bactéria. Um portador humano assintomático é alguém que ainda excreta a bactéria tifóide nas fezes um ano após o estágio agudo da infecção.

Diagnóstico
O diagnóstico é feito por qualquer cultura de sangue, medula óssea ou fezes e com o teste de Widal (demonstração de anticorpos contra antígenos de Salmonella O-somático e H-flagelar). Em epidemias e países menos ricos, depois de excluir a malária, disenteria ou pneumonia, geralmente é realizado um período de ensaio terapêutico com cloranfenicol enquanto se aguarda os resultados do teste Widal e das culturas de sangue e fezes.
Teste Widal
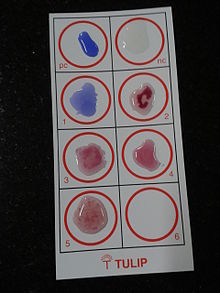
O teste Widal é usado para identificar anticorpos específicos no soro de pessoas com febre tifóide usando interações antígeno-anticorpo.
Neste teste, o soro é misturado com uma suspensão bacteriana morta de salmonela com antígenos específicos. Se o soro do paciente contém anticorpos contra esses antígenos, eles se ligam a eles, formando aglomerados. Se não ocorrer aglomeração, o teste é negativo. O teste Widal é demorado e sujeito a falsos positivos significativos. Também pode ser falsamente negativo em pessoas recentemente infectadas. Mas, ao contrário do teste Typhidot, o teste Widal quantifica a amostra com títulos.
Testes de diagnóstico rápido
Testes de diagnóstico rápido, como Tubex, Typhidot e Test-It, mostraram precisão diagnóstica moderada.
Tifidote
Typhidot é baseado na presença de anticorpos IgM e IgG específicos para um antígeno OMP específico de 50Kd. Este teste é realizado em uma membrana de nitrato de celulose onde um S. typhi proteína da membrana externa é anexada como linhas de teste fixas. Ele identifica separadamente os anticorpos IgM e IgG. IgM mostra infecção recente; IgG significa infecção remota.
A almofada de amostra deste kit contém ouro coloidal IgG anti-humano ou ouro anti-IgM humano. Se a amostra contiver anticorpos IgG e IgM contra esses antígenos, eles reagirão e ficarão vermelhos. O teste de tifido torna-se positivo 2–3 dias após a infecção.
Duas faixas coloridas indicam um teste positivo. Uma única faixa de controle indica um teste negativo. Uma única primeira linha fixa ou nenhuma banda indica um teste inválido. A maior limitação do Typhidot é que não é quantitativo, apenas positivo ou negativo.
Teste Tubex
O teste Tubex contém dois tipos de partículas: partículas magnéticas marrons revestidas com antígeno e partículas indicadoras azuis revestidas com anticorpo O9. Durante o teste, se houver anticorpos presentes no soro, eles se fixarão nas partículas magnéticas marrons e se depositarão na base, enquanto as partículas indicadoras azuis permanecerão na solução, produzindo uma cor azul, o que significa que o teste é positivo.
Se o soro não contiver anticorpo, as partículas azuis se ligam às partículas marrons e se depositam no fundo, produzindo uma solução incolor, o que significa que o teste é negativo.
Prevenção

O saneamento e a higiene são importantes para prevenir a febre tifóide. Pode se espalhar apenas em ambientes onde as fezes humanas podem entrar em contato com alimentos ou água potável. A preparação cuidadosa dos alimentos e a lavagem das mãos são cruciais para prevenir a febre tifóide. A industrialização contribuiu muito para a eliminação da febre tifóide, pois eliminou os riscos para a saúde pública associados à presença de esterco de cavalo nas vias públicas, o que deu origem a um grande número de moscas, que são vetores de muitos patógenos, incluindo Salmonella spp. De acordo com estatísticas dos Centros de Controle e Prevenção de Doenças dos EUA, a cloração da água potável levou a reduções dramáticas na transmissão da febre tifóide.
Vacinação
Duas vacinas contra febre tifóide são licenciadas para uso na prevenção da febre tifóide: a vacina oral viva Ty21a (vendida como Vivotif pela Crucell Switzerland AG) e a vacina polissacarídica injetável contra febre tifóide (vendida como Typhim Vi pela Sanofi Pasteur e Typherix pela GlaxoSmithKline). Ambos são eficazes e recomendados para viajantes em áreas onde a febre tifóide é endêmica. Os reforços são recomendados a cada cinco anos para a vacina oral e a cada dois anos para a forma injetável. Uma vacina mais antiga, de células inteiras mortas, ainda é utilizada em países onde as preparações mais recentes não estão disponíveis, mas esta vacina já não é recomendada porque tem mais efeitos secundários (principalmente dor e inflamação no local da injecção).

Para ajudar a diminuir as taxas de febre tifóide nos países em desenvolvimento, a Organização Mundial da Saúde (OMS) endossou o uso de um programa de vacinação a partir de 1999. A vacinação provou ser eficaz no controle de surtos em áreas de alta incidência e também é muito cara. eficaz: os preços são normalmente inferiores a 1 dólar por dose. Como o preço é baixo, as comunidades atingidas pela pobreza estão mais dispostas a tirar partido das vacinas. Embora os programas de vacinação contra a febre tifóide tenham se mostrado eficazes, eles por si só não conseguem eliminar a febre tifóide. Combinar vacinas com esforços de saúde pública é a única forma comprovada de controlar esta doença.
Desde a década de 1990, a OMS recomenda duas vacinas contra a febre tifóide. A vacina ViPS é administrada por injeção e a Ty21a por cápsulas. Recomenda-se que apenas pessoas com mais de dois anos sejam vacinadas com a vacina ViPS, e ela requer revacinação após 2–3 anos, com eficácia de 55%–72%. A vacina Ty21a é recomendada para pessoas com cinco anos ou mais, com duração de 5 a 7 anos, com eficácia de 51% a 67%. As duas vacinas provaram ser seguras e eficazes no controlo de doenças epidémicas em múltiplas regiões.
Também está disponível uma versão da vacina combinada com uma vacina contra hepatite A.
Os resultados de um ensaio de fase 3 da vacina conjugada contra a febre tifóide (TCV), em dezembro de 2019, relataram 81% menos casos entre crianças.
Tratamento
Terapia de reidratação oral
A redescoberta da terapia de reidratação oral na década de 1960 proporcionou uma maneira simples de prevenir muitas das mortes por doenças diarreicas em geral.
Antibióticos
Quando a resistência é incomum, o tratamento de escolha é uma fluoroquinolona, como a ciprofloxacina. Caso contrário, uma cefalosporina de terceira geração, como ceftriaxona ou cefotaxima, é a primeira escolha. Cefixima é uma alternativa oral adequada.
Tratada adequadamente, a febre tifóide não é fatal na maioria dos casos. Antibióticos como ampicilina, cloranfenicol, trimetoprima-sulfametoxazol, amoxicilina e ciprofloxacina têm sido comumente usados para tratá-la. O tratamento com antibióticos reduz a taxa de letalidade para cerca de 1%.
Sem tratamento, alguns pacientes desenvolvem febre sustentada, bradicardia, hepatoesplenomegalia, sintomas abdominais e, ocasionalmente, pneumonia. Em pacientes de pele branca, manchas rosadas, que desaparecem com a pressão, aparecem na pele do tronco em até 20% dos casos. Na terceira semana, os casos não tratados podem desenvolver complicações gastrointestinais e cerebrais, que podem ser fatais em 10% a 20% dos casos. As maiores taxas de letalidade são relatadas em crianças menores de 4 anos. Cerca de 2% a 5% das pessoas que contraem febre tifóide tornam-se portadores crônicos, pois as bactérias persistem no trato biliar após a resolução dos sintomas.
Cirurgia
A cirurgia geralmente é indicada se ocorrer perfuração intestinal. Um estudo encontrou uma taxa de mortalidade em 30 dias de 9% (8/88) e infecções de sítio cirúrgico de 67% (59/88), com o fardo da doença suportado predominantemente por países com poucos recursos.
Para o tratamento cirúrgico, a maioria dos cirurgiões prefere o fechamento simples da perfuração com drenagem do peritônio. A ressecção do intestino delgado é indicada para pacientes com múltiplas perfurações. Se o tratamento antibiótico não conseguir erradicar o transporte hepatobiliar, a vesícula biliar deve ser ressecada. A colecistectomia às vezes é bem sucedida, especialmente em pacientes com cálculos biliares, mas nem sempre é bem sucedida na erradicação do estado de portador devido à persistência da infecção hepática.
Resistência
Como a resistência à ampicilina, cloranfenicol, sulfametoxazol-trimetoprim e estreptomicina é agora comum, esses agentes não são mais usados como tratamento de primeira linha da febre tifóide. A febre tifóide resistente a esses agentes é conhecida como febre tifóide multirresistente.
A resistência à ciprofloxacina é um problema crescente, especialmente no subcontinente indiano e no Sudeste Asiático. Muitos centros estão mudando da ciprofloxacina para a ceftriaxona como primeira linha para o tratamento de suspeitas de febre tifóide originárias da América do Sul, Índia, Paquistão, Bangladesh, Tailândia ou Vietnã. Além disso, foi sugerido que a azitromicina é melhor no tratamento da febre tifóide resistente do que os medicamentos fluoroquinolonas e a ceftriaxona. A azitromicina pode ser administrada por via oral e é mais barata que a ceftriaxona, que é administrada por injeção.
Existe um problema separado com os testes laboratoriais para redução da suscetibilidade à ciprofloxacina; as recomendações atuais são que os isolados devem ser testados simultaneamente contra a ciprofloxacina (CIP) e contra o ácido nalidíxico (NAL), que os isolados sensíveis ao CIP e ao NAL devem ser relatados como "sensíveis à ciprofloxacina", e que os isolados sensíveis ao A CIP, mas não a NAL, deve ser relatada como “sensibilidade reduzida à ciprofloxacina”. Mas uma análise de 271 isolados descobriu que cerca de 18% dos isolados com suscetibilidade reduzida às fluoroquinolonas, a classe à qual o CIP pertence (MIC 0,125–1,0 mg/L), não seriam detectados por este método.
Epidemiologia
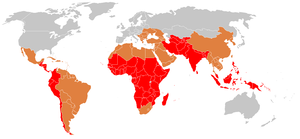
Em 2000, a febre tifóide causou cerca de 21,7 milhões de doenças e 217 mil mortes. Ocorre com mais frequência em crianças e adultos jovens entre 5 e 19 anos. Em 2013, resultou em cerca de 161.000 mortes – abaixo das 181.000 em 1990. Os bebés, crianças e adolescentes no centro-sul e no Sudeste Asiático têm as taxas mais elevadas de febre tifóide. Os surtos também são frequentemente relatados na África Subsaariana e no Sudeste Asiático. Em 2000, mais de 90% da morbilidade e mortalidade devido à febre tifóide ocorreram na Ásia. Nos EUA, ocorrem cerca de 400 casos a cada ano, 75% dos quais são adquiridos durante viagens internacionais.
Antes da era dos antibióticos, a taxa de letalidade da febre tifóide era de 10% a 20%. Hoje, com tratamento imediato, é inferior a 1%, mas 3% a 5% das pessoas infectadas desenvolvem uma infecção crónica na vesícula biliar. Desde S. entérica subsp. enterica sorovar Typhi é restrita a humanos, esses portadores crônicos tornam-se o reservatório crucial, que pode persistir por décadas para maior disseminação da doença, complicando ainda mais sua identificação e tratamento. Ultimamente, o estudo de S. entérica subsp. enterica sorovar Typhi associada a um grande surto e a um portador no nível do genoma fornece uma nova visão sobre a patogênese do patógeno.
Nos países industrializados, as melhorias no saneamento da água e no manejo dos alimentos reduziram o número de casos de febre tifóide. As nações em desenvolvimento têm as taxas mais altas. Estas áreas não têm acesso a água potável, sistemas de saneamento adequados e instalações de saúde adequadas. Nestas áreas, esse acesso às necessidades básicas de saúde pública não é esperado num futuro próximo.
Em 2004–2005, um surto na República Democrática do Congo resultou em mais de 42.000 casos e 214 mortes. Desde novembro de 2016, o Paquistão teve um surto de febre tifóide extensivamente resistente aos medicamentos (XDR).
Na Europa, um relatório baseado em dados de 2017 obtidos do Sistema Europeu de Vigilância (TESSy) sobre a distribuição de casos confirmados de febre tifóide e paratifóide concluiu que 22 países da UE/EEE notificaram um total de 1.098 casos, 90,9% dos quais foram relacionados a viagens, adquiridos principalmente durante viagens ao Sul da Ásia.
Surtos
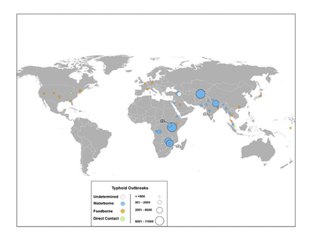
- Praga de Atenas (suspeito).
- Surto "Burning Fever" entre os indígenas americanos. Entre 1607 e 1624, 85% da população no rio James morreu de uma epidemia de tifoide. A Organização Mundial da Saúde estima que o número de mortos foi superior a 6.000 durante este período.
- Maidstone, Kent surto em 1897-1898: 1.847 pacientes foram registrados para ter febre tifoide. Este surto é notável porque foi a primeira vez que uma vacina tifoide foi implantada durante um surto civil. A vacina de Almoth Edward Wright foi oferecida a 200 prestadores de cuidados de saúde, e dos 84 indivíduos que receberam a vacina, nenhum desenvolveu tifoide enquanto 4 que não haviam sido vacinados ficaram doentes.
- Exército americano na guerra hispano-americana: registros do governo estimam que mais de 21.000 tropas tinham tifoide, resultando em 2.200 mortes.
- Em 1902 convidados em banquetes prefeitos em Southampton e Winchester, a Inglaterra ficou doente e quatro morreu, incluindo o reitor de Winchester, depois de consumir ostras. A infecção foi devido a ostras provenientes de Emsworth, onde as camas de ostras tinham sido contaminadas com esgoto cru.
- Jamaica Plain bairro, Boston em 1908 - ligado à entrega de leite. Veja a seção de história, "portadores" para mais detalhes.
- Surto em Nova York que empregou Mary Mallon - 51 casos e 3 mortes de 1907 a 1915.
- Aberdeen, Escócia, no verão de 1964 - remonta a carne enlatada contaminada originada da Argentina vendida nos mercados. Mais de 500 pacientes foram quarentena no hospital por um mínimo de quatro semanas, e o surto foi contido sem nenhuma morte.
- Dushanbe, Tajiquistão, em 1996-1997: 10.677 casos relatados, 108 mortes.
- Kinshasa, Democrata República do Congo, em 2004: 43.000 casos e mais de 200 mortes. Um estudo prospectivo de espécimes coletados na mesma região entre 2007 e 2011 revelou cerca de um terço das amostras obtidas de amostras de pacientes foram resistentes a múltiplos antibióticos.
- Kampala, Uganda em 2015: 10.230 casos relatados.
Histórico
Descrições iniciais
A peste de Atenas, durante a Guerra do Peloponeso, foi provavelmente um surto de febre tifóide. Durante a guerra, os atenienses recuaram para uma cidade murada para escapar do ataque dos espartanos. Este afluxo maciço de seres humanos para um espaço concentrado sobrecarregou as infra-estruturas de abastecimento de água e de resíduos, provavelmente conduzindo a condições insalubres, uma vez que a água doce se tornou mais difícil de obter e os resíduos se tornaram mais difíceis de recolher e remover para além dos muros da cidade. Em 2006, o exame dos restos mortais de um cemitério coletivo em Atenas, na época da peste (~430 a.C.), revelou que fragmentos de DNA semelhantes ao DNA moderno de S. Typhi foram detectados, enquanto Yersinia pestis (peste), Rickettsia prowazekii (tifo), Mycobacterium tuberculosis, vírus da varíola bovina e Bartonella henselae não foram detectados em nenhum dos restos mortais testados.
É possível que o imperador romano Augusto César tenha tido um abscesso no fígado ou febre tifóide e tenha sobrevivido usando banhos de gelo e compressas frias como forma de tratamento para a febre. Há uma estátua do médico grego Antonius Musa, que tratou sua febre.
Definição e evidência de transmissão
Os médicos franceses Pierre-Fidele Bretonneau e Pierre-Charles-Alexandre Louis são responsáveis por descrever a febre tifóide como uma doença específica, única do tifo. Ambos os médicos realizaram autópsias em indivíduos que morreram em Paris devido à febre – e indicaram que muitos tinham lesões nas placas de Peyer que se correlacionavam com sintomas distintos antes da morte. Os médicos britânicos eram céticos quanto à diferenciação entre febre tifóide e tifo porque ambos eram endêmicos na Grã-Bretanha naquela época. No entanto, na França, apenas a febre tifóide estava presente circulando na população. Pierre-Charlles-Alexandre Louis também realizou estudos de caso e análises estatísticas para demonstrar que a febre tifóide era contagiosa - e que as pessoas que já tinham a doença pareciam estar protegidas. Posteriormente, vários médicos americanos confirmaram essas descobertas, e então Sir William Jenner convenceu todos os céticos remanescentes de que a febre tifóide é uma doença específica reconhecível por lesões nas placas de Peyer, examinando sessenta e seis autópsias de pacientes com febre e concluindo que os sintomas de dores de cabeça, diarreia, erupções cutâneas e dor abdominal estavam presentes apenas em pacientes que apresentavam lesões intestinais após a morte; essas observações solidificaram a associação da doença com o trato intestinal e deram a primeira pista sobre a via de transmissão.
Em 1847, William Budd soube de uma epidemia de febre tifóide em Clifton e identificou que todos os 13 dos 34 residentes que contraíram a doença retiravam água potável do mesmo poço. Notavelmente, esta observação foi feita dois anos antes de John Snow publicar pela primeira vez uma versão inicial da sua teoria de que a água contaminada era o canal central para a transmissão da cólera. Mais tarde, Budd tornou-se oficial de saúde de Bristol e garantiu o abastecimento de água potável, além de documentar mais evidências de febre tifóide como uma doença transmitida pela água ao longo de sua carreira.
Causa
O cientista polonês Tadeusz Browicz descreveu um bacilo curto nos órgãos e fezes de vítimas de febre tifóide em 1874. Browicz conseguiu isolar e cultivar os bacilos, mas não chegou ao ponto de insinuar ou provar que eles causavam a doença.
Em abril de 1880, três meses antes da publicação de Eberth, Edwin Klebs descreveu bacilos curtos e filamentosos nas placas de Peyer em vítimas de febre tifóide. O papel da bactéria na doença foi especulado, mas não confirmado.
Em 1880, Karl Joseph Eberth descreveu um bacilo que ele suspeitava ser a causa da febre tifóide. Eberth recebe o crédito por descobrir a bactéria definitivamente, isolando com sucesso a mesma bactéria de 18 das 40 vítimas de febre tifóide e não conseguindo descobrir a bactéria presente em qualquer dispositivo de 'controle'. vítimas de outras doenças. Em 1884, o patologista Georg Theodor August Gaffky (1850–1918) confirmou as descobertas de Eberth. Gaffky isolou a mesma bactéria que Eberth do baço de uma vítima de febre tifóide e foi capaz de cultivar a bactéria em meio sólido. O organismo recebeu nomes como bacilo de Eberth, Eberthella Typhi e bacilo de Gaffky-Eberth. Hoje, o bacilo que causa a febre tifóide tem o nome científico de Salmonella enterica sorovar Typhi.
Cloração da água
A maioria dos países desenvolvidos teve taxas decrescentes de febre tifóide ao longo da primeira metade do século XX devido às vacinações e aos avanços no saneamento e higiene públicos. Em 1893 foram feitas tentativas de clorar o abastecimento de água em Hamburgo, Alemanha e em 1897 Maidstone, Inglaterra, foi a primeira cidade a ter todo o seu abastecimento de água clorado. Em 1905, após um surto de febre tifóide, a cidade de Lincoln, na Inglaterra, instituiu a cloração permanente da água. A primeira desinfecção permanente de água potável nos EUA foi feita em 1908 no abastecimento de água de Jersey City, Nova Jersey. O crédito pela decisão de construir o sistema de cloração foi dado a John L. Leal. A instalação de cloração foi projetada por George W. Fuller.
Surtos em grupos militares itinerantes levaram à criação da bolsa Lyster em 1915; uma bolsa com torneira que pode ser pendurada em uma árvore ou poste, cheia de água, e vem com uma pastilha de cloração para jogar na água. A bolsa Lyster foi essencial para a sobrevivência dos soldados americanos na Guerra do Vietnã.
Transmissão direta e operadoras
Houve vários casos de entregadores de leite espalhando febre tifóide pelas comunidades que atendiam. Embora a febre tifóide não seja transmitida através do leite em si, houve vários exemplos de distribuidores de leite em muitos locais que diluíram o seu leite com água contaminada ou limparam as garrafas de vidro onde o leite foi colocado com água contaminada. Boston teve dois casos desse tipo na virada do século XX. Em 1899, houve 24 casos de febre tifóide atribuídos a um único leiteiro, cuja esposa havia morrido de febre tifóide uma semana antes do surto. Em 1908, J. J. Fallon, que também era leiteiro, morreu de febre tifóide. Após sua morte e a confirmação do diagnóstico de febre tifóide, a cidade conduziu uma investigação dos sintomas e casos de febre tifóide ao longo de seu percurso e encontrou evidências de um surto significativo. Um mês após o surto ter sido relatado pela primeira vez, o Boston Globe publicou uma breve declaração declarando o fim do surto, afirmando que “na Planície da Jamaica há um ligeiro aumento, sendo o total de 272 casos”. Em toda a cidade há um total de 348 casos." Houve pelo menos uma morte relatada durante este surto: a Sra. Sophia S. Engstrom, de 46 anos. A febre tifóide continuou a devastar o bairro de Jamaica Plain, em particular ao longo de 1908, e várias outras pessoas foram mortas devido à febre tifóide, embora esses casos fossem não está explicitamente ligada ao surto. Naquela época, o bairro de Jamaica Plain era o lar de muitos imigrantes pobres e da classe trabalhadora, principalmente da Irlanda.
A portadora mais notória da febre tifóide, mas de forma alguma a mais destrutiva, foi Mary Mallon, conhecida como Maria Tifóide. Embora outros casos de propagação de febre tifóide de pessoa para pessoa fossem conhecidos na época, o conceito de portador assintomático, capaz de transmitir a doença, havia apenas sido levantado como hipótese e ainda não identificado ou comprovado. Mary Mallon tornou-se o primeiro exemplo conhecido de portador assintomático de uma doença infecciosa, tornando a febre tifóide a primeira doença conhecida a ser transmissível através de hospedeiros assintomáticos. Os casos e mortes causadas por Mallon ocorreram principalmente em famílias de classe alta da cidade de Nova York. Na época em que Mallon era cozinheiro pessoal de famílias de classe alta, a cidade de Nova York relatava de 3.000 a 4.500 casos de febre tifóide anualmente. No verão de 1906, duas filhas de uma família rica e empregadas domésticas que trabalhavam em sua casa adoeceram com febre tifóide. Depois de investigar as fontes de água domésticas e descartar a possibilidade de contaminação da água, a família contratou o engenheiro civil George Soper para conduzir uma investigação sobre a possível origem da febre tifóide na casa. Soper se descreveu como um “lutador de epidemias”. A sua investigação descartou muitas fontes de alimentos e levou-o a questionar se o cozinheiro que a família contratou pouco antes do surto doméstico, Mallon, era a fonte. Como ela já havia saído e começado a trabalhar em outro lugar, ele começou a procurá-la para obter uma amostra de fezes. Quando ele finalmente conseguiu conhecer Mallon pessoalmente, ele a descreveu dizendo: “Mary tinha uma boa figura e poderia ter sido chamada de atlética se não fosse um pouco pesada”. Nos relatos da perseguição de Mallon por Soper, seu único remorso parece ser o fato de não ter recebido crédito suficiente por sua busca incansável e publicação de informações de identificação pessoal dela, afirmando que a mídia “me rouba” de qualquer crédito que pertença à descoberta do primeiro portador de febre tifóide encontrado na América. No final das contas, 51 casos e 3 mortes foram suspeitos de serem causados por Mallon.
Em 1924, a cidade de Portland, Oregon, sofreu um surto de febre tifóide, que consistiu em 26 casos e 5 mortes, todas mortes devido a hemorragia intestinal. Concluiu-se que todos os casos se deviam a um único trabalhador de uma fazenda de leite, que liberava grandes quantidades do patógeno da febre tifóide na urina. Identificação incorreta da doença, devido a resultados imprecisos do teste Widal, atraso na identificação do portador e tratamento adequado. No final das contas, foram necessárias quatro amostras de secreções diferentes de todos os trabalhadores do setor leiteiro para identificar com sucesso o portador. Após a descoberta, o trabalhador do laticínio foi colocado em quarentena forçada por sete semanas, e amostras regulares foram coletadas, na maioria das vezes as amostras de fezes não revelavam febre tifóide e muitas vezes a urina produzia o patógeno. O portador foi relatado como tendo 72 anos e apresentando excelente saúde e sem sintomas. O tratamento farmacêutico diminuiu a quantidade de bactérias secretadas, porém, a infecção nunca foi totalmente eliminada da urina, e o portador foi liberado “sob ordens de nunca mais se envolver na manipulação de alimentos para consumo humano”. No momento da divulgação, os autores observaram que “por mais de cinquenta anos ele ganhou a vida principalmente ordenhando vacas e sabe pouco sobre outras formas de trabalho, deve-se esperar que a vigilância mais próxima seja necessária para garantir que ele não se envolva novamente nesta ocupação.
De modo geral, no início do século 20, a profissão médica começou a identificar portadores da doença e evidências de transmissão independente da contaminação da água. Em uma publicação da American Medical Association de 1933, os médicos & #39; o tratamento de portadores assintomáticos é melhor resumido pela frase de abertura “Os portadores do bacilo tifóide são uma ameaça”. Na mesma publicação, é apresentada a primeira estimativa oficial de portadores de febre tifóide: 2 a 5% de todos os pacientes com febre tifóide, e distingue entre portadores temporários e portadores crônicos. Os autores estimam ainda que existem quatro a cinco mulheres portadoras crónicas para cada homem portador, embora não tenham oferecido dados que expliquem esta afirmação de uma diferença de género na taxa de portadores de febre tifóide. Quanto ao tratamento, os autores sugerem: "Quando reconhecidos, os portadores devem ser orientados quanto ao descarte de excretas, bem como à importância da limpeza pessoal. Eles devem ser proibidos de manusear alimentos ou bebidas destinados a terceiros, e seus movimentos e paradeiro devem ser comunicados aos agentes de saúde pública.

Atualmente, existem portadores de febre tifóide em todo o mundo, mas a maior incidência de infecção assintomática provavelmente ocorrerá nos países do Sul/Sudeste Asiático e da África Subsaariana. O departamento de saúde pública do condado de Los Angeles rastreia os portadores de febre tifóide e relata anualmente o número de portadores identificados no condado; entre 2006 e 2016, foram identificados 0-4 novos casos de portadores de febre tifóide por ano. Os casos de febre tifóide devem ser notificados no prazo de um dia útil a partir da identificação. A partir de 2018, os portadores de febre tifóide crônica deverão assinar um "Contrato de Transportadora" e são obrigados a testar a eliminação da febre tifóide duas vezes por ano, de preferência a cada 6 meses. As transportadoras podem ser dispensadas de seus acordos mediante o cumprimento da "liberação" requisitos, com base na conclusão de um plano de tratamento personalizado elaborado com profissionais médicos. Requisitos de liberação de transportadores fecais ou da vesícula biliar: 6 amostras negativas consecutivas de fezes e urina submetidas em intervalos de 1 mês ou mais, começando pelo menos 7 dias após o término da terapia. Requisitos de liberação de portadores urinários ou renais: 6 amostras de urina negativas consecutivas submetidas em intervalos de 1 mês ou mais, começando pelo menos 7 dias após o término da terapia.
Devido à natureza dos casos assintomáticos, muitas questões permanecem sobre como os indivíduos são capazes de tolerar a infecção por longos períodos de tempo, como identificar tais casos e opções eficientes de tratamento. Os investigadores estão actualmente a trabalhar para compreender a infecção assintomática por espécies de Salmonella, estudando infecções em animais de laboratório, o que acabará por levar a melhores opções de prevenção e tratamento para portadores de febre tifóide. Em 2002, John Gunn descreveu a capacidade da Salmonella sp. para formar biofilmes em cálculos biliares em camundongos, fornecendo um modelo para estudar o transporte na vesícula biliar. Denise Monack e Stanley Falkow descreveram um modelo de camundongo de infecção intestinal e sistêmica assintomática em 2004, e Monack demonstrou que uma subpopulação de superespalhadores é responsável pela maior parte da transmissão para novos hospedeiros, seguindo a regra 80/20 da doença transmissão, e que a microbiota intestinal provavelmente desempenha um papel na transmissão. O modelo de rato de Monack permite o transporte a longo prazo de salmonela nos gânglios linfáticos mesentéricos, baço e fígado.
Desenvolvimento de vacinas

O bacteriologista britânico Almroth Edward Wright desenvolveu pela primeira vez uma vacina eficaz contra a febre tifóide na Escola de Medicina do Exército em Netley, Hampshire. Foi introduzido em 1896 e usado com sucesso pelos britânicos durante a Segunda Guerra dos Bôeres na África do Sul. Naquela época, a febre tifóide costumava matar mais soldados na guerra do que os perdidos devido ao combate inimigo. Wright desenvolveu ainda mais sua vacina em um departamento de pesquisa recém-inaugurado na St Mary's Hospital Medical School, em Londres, a partir de 1902, onde estabeleceu um método para medir substâncias protetoras (opsonina) no sangue humano. A versão de Wright da vacina contra a febre tifóide foi produzida cultivando a bactéria à temperatura corporal em caldo e depois aquecendo a bactéria a 60 °C para 'inativar pelo calor'. o patógeno, matando-o, mantendo intactos os antígenos de superfície. A bactéria morta pelo calor foi então injetada em um paciente. Para mostrar evidências da eficácia da vacina, Wright coletou amostras de soro de pacientes várias semanas após a vacinação e testou a capacidade do soro de aglutinar bactérias tifóides vivas. Um resultado "positivo" O resultado foi representado pela aglomeração de bactérias, indicando que o corpo estava produzindo anti-soro (agora chamado de anticorpos) contra o patógeno.
Citando o exemplo da Segunda Guerra dos Bôeres, durante a qual muitos soldados morreram de doenças facilmente evitáveis, Wright convenceu o Exército Britânico de que deveriam ser produzidas 10 milhões de doses de vacina para as tropas enviadas para a Frente Ocidental, economizando assim até metade um milhão de vidas durante a Primeira Guerra Mundial. O Exército Britânico foi o único combatente no início da guerra a ter as suas tropas totalmente imunizadas contra a bactéria. Pela primeira vez, as baixas devido ao combate excederam as causadas por doenças.
Em 1909, Frederick F. Russell, um médico do Exército dos EUA, adotou a vacina contra febre tifóide de Wright para uso no Exército e, dois anos depois, seu programa de vacinação tornou-se o primeiro em que um exército inteiro foi imunizado. Eliminou a febre tifóide como uma causa significativa de morbidade e mortalidade nas forças armadas dos EUA. A vacinação contra febre tifóide para militares americanos tornou-se obrigatória em 1911. Antes da vacina, a taxa de febre tifóide nas forças armadas era de 14.000 ou mais por 100.000 soldados. Na Primeira Guerra Mundial, a taxa de febre tifóide em soldados americanos era de 37 por 100.000.
Durante a Segunda Guerra Mundial, o exército dos Estados Unidos autorizou o uso de uma vacina trivalente – contendo patógenos tifóides inativados pelo calor, Paratyphi A e Paratyphi B.
Em 1934, a descoberta do antígeno capsular Vi por Arthur Felix e S. R. Margaret Pitt permitiu o desenvolvimento da vacina mais segura do antígeno Vi – que é amplamente utilizada atualmente. Arthur Felix e Margaret Pitt também isolaram a cepa Ty2, que se tornou a cepa parental da Ty21a, a cepa usada hoje como vacina viva atenuada para a febre tifóide.
Antibióticos e resistência
O cloranfenicol foi isolado de Streptomyces por David Gotlieb durante a década de 1940. Em 1948, médicos do exército americano testaram sua eficácia no tratamento de pacientes com febre tifóide em Kuala Lumpur, na Malásia. Os indivíduos que receberam um tratamento completo eliminaram a infecção, enquanto os pacientes que receberam uma dose mais baixa tiveram uma recaída. Os portadores assintomáticos continuaram a eliminar bacilos apesar do tratamento com cloranfenicol - apenas os pacientes doentes melhoraram com o cloranfenicol. A resistência ao cloranfenicol tornou-se frequente no Sudeste Asiático na década de 1950 e hoje o cloranfenicol é usado apenas como último recurso devido à alta prevalência de resistência.
Terminologia
A doença tem sido referida por vários nomes, frequentemente associados a sintomas, como febre gástrica, febre entérica, tifo abdominal, febre remitente infantil, febre lenta, febre nervosa, febre pitogênica, febre do dreno e febre baixa.
Sociedade e cultura
Pessoas notáveis
- O imperador Augusto de Roma (suspeito baseado no registro histórico, mas não confirmado), sobreviveu.
- Alberto, príncipe consorte, marido da rainha Vitória do Reino Unido, morreu em 24 dias após o primeiro registro de "sentir horrivelmente doente". Morreu 14 de dezembro de 1861 depois de sofrer perda de apetite, insônia, febre, calafrios, transpiração profusa, vômitos, manchas de erupção, delírios, incapacidade de reconhecer membros da família, agravando a erupção no abdômen, uma mudança na cor da língua, então finalmente um estado de fadiga extrema. O médico assistente William Jenner, especialista em febre tifóide na época, diagnosticou-o.
- Eduardo VII do Reino Unido, filho da rainha Vitória, enquanto ainda Príncipe de Gales, teve um caso quase fatal de febre tifoide.
- O czar Nicolau II da Rússia, sobreviveu, a doença foi por volta de 1900-1901.
- William Henry Harrison, o 9o presidente dos Estados Unidos da América, morreu 32 dias em seu mandato, em 1841. Este é o termo mais curto servido por um presidente dos Estados Unidos.
- Wilbur Wright, co-inventor do avião com seu irmão Orville morreu de tifoide 32 anos antes de Orville.
- Stephen A. Douglas, opositor político de Abraham Lincoln em 1858 e 1860, morreu de tifoide em 3 de junho de 1861.
- Ignacio Zaragoza, general mexicano e político, morreu aos 33 anos de febre tifóide em 8 de setembro de 1862.
- William Wallace Lincoln, filho do presidente Abraham e Mary Todd Lincoln, morreu de tifoide em 1862.
- A princesa Leopoldina do Brasil, filha do imperador Pedro II, morreu de tifoide em 1871.
- Martha Bulloch Roosevelt, mãe do presidente Theodore Roosevelt e avó paterna de Eleanor Roosevelt, morreu de febre tifoide em 1884.
- Mary Mallon, "Typhoid Mary" - ver seção de história, "portadores" para mais detalhes
- Leland Stanford Jr., filho do magnata americano e político A. Leland Stanford e eponym da Leland Stanford Junior University, morreu de febre tifoide em 1884 aos 15 anos de idade.
- Três dos cinco filhos de Louis Pasteur morreram de febre tifoide.
- Gerard Manley Hopkins, poeta inglês, morreu de febre tifoide em 1889.
- Lizzie van Zyl, reclusa sul-africana do campo de concentração de Bloemfontein durante a Segunda Guerra Boer, morreu de febre tifoide em 1901.
- Dr HJH 'Tup' Scott, capitão da equipe de críquete australiana de 1886 que visitou a Inglaterra, morreu de tifoide em 1910.
- Arnold Bennett, romancista inglês, morreu em 1932 de tifoide, dois meses depois de beber um copo de água em um hotel de Paris para provar que era seguro.
- Hakaru Hashimoto, Cientista médico japonês, morreu de febre tifoide em 1934.
- John Buford, oficial da cavalaria da União durante a Guerra Civil, morreu de febre tifóide em 16 de dezembro de 1863.
Contenido relacionado
Analgésico
Índice de massa corporal
Método do muco cervical
Heroína
Malária