Eletro-negatividade
Eletronegatividade, simbolizada como χ, é a tendência de um átomo de um determinado elemento químico atrair elétrons compartilhados (ou densidade eletrônica) ao formar uma ligação química. A eletronegatividade de um átomo é afetada tanto por seu número atômico quanto pela distância em que seus elétrons de valência residem do núcleo carregado. Quanto maior a eletronegatividade associada, mais um átomo ou um grupo substituinte atrai elétrons. A eletronegatividade serve como uma maneira simples de estimar quantitativamente a energia de ligação e o sinal e a magnitude da polaridade química de uma ligação, que caracteriza uma ligação ao longo da escala contínua de ligação covalente a ligação iônica. O termo vagamente definido eletropositividade é o oposto de eletronegatividade: caracteriza a tendência de um elemento de doar elétrons de valência.
No nível mais básico, a eletronegatividade é determinada por fatores como a carga nuclear (quanto mais prótons um átomo tiver, mais "atração" ele terá sobre os elétrons) e o número e a localização de outros elétrons nas camadas atômicas (quanto mais elétrons um átomo tiver, mais longe do núcleo os elétrons de valência estarão e, como resultado, menos carga positiva eles experimentarão - tanto por causa de sua maior distância do núcleo quanto porque os outros elétrons nos orbitais do núcleo de energia mais baixa atuará para proteger os elétrons de valência do núcleo carregado positivamente).
O termo "eletronegatividade" foi introduzido por Jöns Jacob Berzelius em 1811, embora o conceito fosse conhecido antes disso e estudado por muitos químicos, incluindo Avogadro. Apesar de sua longa história, uma escala precisa de eletronegatividade não foi desenvolvida até 1932, quando Linus Pauling propôs uma escala de eletronegatividade que depende de energias de ligação, como um desenvolvimento da teoria de ligação de valência. Foi demonstrado que se correlaciona com várias outras propriedades químicas. A eletronegatividade não pode ser medida diretamente e deve ser calculada a partir de outras propriedades atômicas ou moleculares. Vários métodos de cálculo foram propostos e, embora possa haver pequenas diferenças nos valores numéricos da eletronegatividade, todos os métodos mostram as mesmas tendências periódicas entre os elementos.
O método de cálculo mais utilizado é o originalmente proposto por Linus Pauling. Isso dá uma quantidade adimensional, comumente chamada de escala de Pauling (χr), em uma escala relativa que vai de 0,79 a 3,98 (hidrogênio = 2,20). Quando outros métodos de cálculo são usados, é convencional (embora não obrigatório) citar os resultados em uma escala que cobre o mesmo intervalo de valores numéricos: isso é conhecido como eletronegatividade em unidades de Pauling.
Como geralmente é calculado, a eletronegatividade não é uma propriedade de um átomo sozinho, mas sim uma propriedade de um átomo em uma molécula. Mesmo assim, a eletronegatividade de um átomo está fortemente correlacionada com a primeira energia de ionização, e negativamente correlacionada com a afinidade eletrônica. É de se esperar que a eletronegatividade de um elemento varie com seu ambiente químico, mas geralmente é considerada uma propriedade transferível, ou seja, valores semelhantes serão válidos em diversas situações.
Césio é o elemento menos eletronegativo (0,79); flúor é o máximo (3,98).
Métodos de cálculo
Paulizando a eletronegatividade
Pauling propôs pela primeira vez o conceito de eletronegatividade em 1932 para explicar por que a ligação covalente entre dois átomos diferentes (A–B) é mais forte que a média das ligações A–A e B–B. De acordo com a teoria da ligação de valência, da qual Pauling foi um proponente notável, essa "estabilização adicional" da ligação heteronuclear é devido à contribuição de formas canônicas iônicas para a ligação.
A diferença de eletronegatividade entre os átomos A e B é dada por:
Como apenas as diferenças de eletronegatividade são definidas, é necessário escolher um ponto de referência arbitrário para construir uma escala. O hidrogênio foi escolhido como referência, pois forma ligações covalentes com uma grande variedade de elementos: sua eletronegatividade foi fixada primeiro em 2,1, depois revisada para 2,20. Também é necessário decidir qual dos dois elementos é o mais eletronegativo (equivalente a escolher um dos dois sinais possíveis para a raiz quadrada). Isso geralmente é feito usando "intuição química": no exemplo acima, brometo de hidrogênio se dissolve em água para formar íons H+ e Br−, então pode-se assumir que o bromo é mais eletronegativo que o hidrogênio. No entanto, em princípio, uma vez que as mesmas eletronegatividades devem ser obtidas para quaisquer dois compostos de ligação, os dados são de fato sobredeterminados e os sinais são únicos uma vez que um ponto de referência tenha sido fixado (geralmente, para H ou F).
Para calcular a eletronegatividade de Pauling para um elemento, é necessário ter dados sobre as energias de dissociação de pelo menos dois tipos de ligações covalentes formadas por esse elemento. A. L. Allred atualizou os valores originais de Pauling em 1961 para levar em conta a maior disponibilidade de dados termodinâmicos, e são esses valores "revistos de Pauling" valores de eletronegatividade mais usados.
O ponto essencial da eletronegatividade de Pauling é que existe uma fórmula semi-empírica subjacente, bastante precisa, para energias de dissociação, a saber:
Estas são equações aproximadas, mas são válidas com boa precisão. Pauling obteve a primeira equação observando que uma ligação pode ser aproximadamente representada como uma superposição mecânica quântica de uma ligação covalente e dois estados de ligação iônica. A energia covalente de uma ligação é aproximada, por cálculos mecânicos quânticos, da média geométrica das duas energias de ligações covalentes das mesmas moléculas, e há energia adicional que vem de fatores iônicos, ou seja, caráter polar da ligação.
A média geométrica é aproximadamente igual à média aritmética - que é aplicada na primeira fórmula acima - quando as energias são de valor semelhante, por exemplo, exceto para os elementos altamente eletropositivos, onde há uma diferença maior de duas dissociações energias; a média geométrica é mais precisa e quase sempre dá excesso de energia positiva, devido à ligação iônica. A raiz quadrada desse excesso de energia, observa Pauling, é aproximadamente aditiva e, portanto, pode-se introduzir a eletronegatividade. Assim, são essas fórmulas semi-empíricas para energia de ligação que fundamentam o conceito de eletronegatividade de Pauling.
As fórmulas são aproximadas, mas esta aproximação grosseira é de facto relativamente boa e dá a intuição certa, com a noção da polaridade da ligação e alguma fundamentação teórica em mecânica quântica. As eletronegatividades são então determinadas para melhor ajustar os dados.
Em compostos mais complexos, há um erro adicional, pois a eletronegatividade depende do ambiente molecular de um átomo. Além disso, a estimativa de energia só pode ser usada para ligações simples, não para ligações múltiplas. A entalpia de formação de uma molécula contendo apenas ligações simples pode ser posteriormente estimada com base em uma tabela de eletronegatividade, e depende dos constituintes e da soma dos quadrados das diferenças de eletronegatividades de todos os pares de átomos ligados. Tal fórmula para estimar energia normalmente tem um erro relativo da ordem de 10%, mas pode ser usada para obter uma ideia qualitativa aproximada e compreensão de uma molécula.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10. | 11 | 12 | 13 | 14 | 15 | 16. | 17. | 18. | ||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grupo → | |||||||||||||||||||
| ↓ Período | |||||||||||||||||||
| 1 | H. H. H. 2.20 | Ele. | |||||||||||||||||
| 2 | Li 0,98 | Ser 1.57 | B 2.04 | C 2.55 | N 3.04 | O 3.44 | F 3.98 | Não. | |||||||||||
| 3 | Nao 0,93 | Mg 1.3. | Al. 1.6.6 | Si 1.90 | P 2.19 | S 2.58 | Cl 3.16 | Ar | |||||||||||
| 4 | KK 0,802 | Ca. 1.00 | Sc 1.3. | Ti 1.54 | V 1.6.3 | C. 1.6 | Mn. 1.55 | Fe 1,83 | Co 1.88 | Ni 1.9.1 | Cu 1.90 | Zn 1.65 | Ga 1.8.1 | Ge 2.01 | Como 2.18 | Se 2.55 | B. 2.96 | Kr 3.00 | |
| 5 | Rb 0,802 | Sr. 0,95 | Y 1.22 | Zr 1.3. | Nb 1.6 | Mo 2.16 | TC 1. | Ru 2.2 | Rh 2.28 | Pd 2.20 | Agrupamento 1.93 | Cd 1.6.9 | Em 1.78 | Sn 1.96 | Sb 2.05 | Te 2. | Eu... 2.66 | Xe 2.60 | |
| 6 | C 0,789 | Bando 0,809 | Lu 1.27 | Hf 1.3. | Ta. 1.5. | W 2.36 | Repito 1. | Os 2.2 | Ir. 2.20 | Pt 2.28 | Au! 2.54 | Hg 2.00 | ? 1.6.2 | PB 1,8 | B. 2.02 | Po 2.0 | Em 2.2 | RN 2.2 | |
| 7 | Pe. > 0,79 | Ra 0.9. | Lr. 1.3. | Rf | Db | Sg | B. | H. | Mt | D | RG | Cn | Não. | Fl | Mc | LV | T | Og | |
| La 1.1.1. | Ce 1.12 | Pr 1.13 | Nd 1.14 | Pm – | Sm 1.17 | Eu sei. – | Gd 1.2. | TB 1.1.1. | Dy! 1.22 | Ho. 1.23 | Er. 1.24 | T m 1.25 | Yb – | ||||||
| Acções 1.1.1. | O quê? 1.3. | Pai. 1.5. | U 1.38 | Np 1.3. | Puxa. 1.28 | Am 1.13 | Cm 1.28 | Bk. 1.3. | Cf 1.3. | E 1.3. | F m 1.3. | Md. 1.3. | Não. 1.3. | ||||||
Ver também: Eletronegatividades dos elementos (página de dados)
Não há fontes confiáveis para Pm, Eu e Yb além da gama de 1.1–1.2; veja Pauling, Linus (1960). A natureza do vínculo químico. 3a ed., Cornell University Press, p. 93.
- ^ A elétronegatividade do francium foi escolhida por Pauling como 0,7, próximo ao do césio (também avaliado 0,7 naquele ponto). O valor base do hidrogênio foi posteriormente aumentado em 0,10 e a elétronegatividade do cásio foi mais tarde refinada para 0,79; no entanto, não foram feitas refinamentos para o francium como nenhum experimento foi realizado. No entanto, o franco é esperado e, em pequena medida, observado ser mais elétronegativo do que o césio. Consulte o francium para obter detalhes.
- ^ Ver Brown, Geoffrey (2012). A Terra Inacessível: Uma visão integrada da sua estrutura e composição. Springer Science & Business Media. p. 88. ISBN 9789401115162.
Eletronegatividade de Mulliken
Robert S. Mulliken propôs que a média aritmética da primeira energia de ionização (Ei) e a afinidade eletrônica (Eea) deveriam ser uma medida da tendência de um átomo para atrair elétrons:
Como esta definição não depende de uma escala relativa arbitrária, também foi denominada eletronegatividade absoluta, com as unidades de quilojoules por mol ou elétron-volts. No entanto, é mais comum usar uma transformação linear para transformar esses valores absolutos em valores que se assemelham aos valores de Pauling mais familiares. Para energias de ionização e afinidades eletrônicas em elétron-volts,
A eletronegatividade Mulliken só pode ser calculada para um elemento cuja afinidade eletrônica é conhecida. Os valores medidos estão disponíveis para 72 elementos, enquanto os valores aproximados foram estimados ou calculados para os demais elementos.
Às vezes, diz-se que a eletronegatividade Mulliken de um átomo é o negativo do potencial químico. Ao inserir as definições energéticas do potencial de ionização e afinidade eletrônica na eletronegatividade de Mulliken, é possível mostrar que o potencial químico de Mulliken é uma aproximação por diferença finita da energia eletrônica em relação ao número de elétrons., ou seja,
Eletronegatividade de Allred–Rochow
A. Louis Allred e Eugene G. Rochow consideraram que a eletronegatividade deveria estar relacionada à carga experimentada por um elétron na "superfície" de um átomo: Quanto maior a carga por unidade de área da superfície atômica, maior a tendência desse átomo de atrair elétrons. A carga nuclear efetiva, Zeff, experimentada pelos elétrons de valência pode ser estimada usando as regras de Slater, enquanto a área da superfície de um átomo em uma molécula pode ser calculada ser proporcional ao quadrado do raio covalente, rcov. Quando rcov é expresso em picômetros,
Equalização de eletronegatividade de Sanderson
R.T. Sanderson também observou a relação entre a eletronegatividade de Mulliken e o tamanho atômico e propôs um método de cálculo baseado no recíproco do volume atômico. Com o conhecimento dos comprimentos de ligação, o modelo de Sanderson permite estimar as energias de ligação em uma ampla gama de compostos. O modelo de Sanderson também foi usado para calcular geometria molecular, energia de elétrons s, constantes de acoplamento spin-spin de NMR e outros parâmetros para compostos orgânicos. Este trabalho fundamenta o conceito de equalização de eletronegatividade, que sugere que os elétrons se distribuem ao redor de uma molécula para minimizar ou equalizar a eletronegatividade de Mulliken. Este comportamento é análogo à equalização do potencial químico na termodinâmica macroscópica.
Eletronegatividade de Allen
Talvez a definição mais simples de eletronegatividade seja a de Leland C. Allen, que propôs que ela está relacionada à energia média dos elétrons de valência em um átomo livre,
onde εs,p são as energias de um elétron dos elétrons s e p no átomo livre e ns,p são o número de elétrons s e p na camada de valência. É comum aplicar um fator de escala, 1,75 × 10−3 para energias expressas em quilojoules por mol ou 0,169 para energias medidas em elétron-volts, para fornecer valores numericamente semelhantes às eletronegatividades de Pauling.
As energias de um elétron podem ser determinadas diretamente a partir de dados espectroscópicos e, portanto, as eletronegatividades calculadas por esse método às vezes são chamadas de eletronegatividades espectroscópicas. Os dados necessários estão disponíveis para quase todos os elementos, e este método permite a estimativa de eletronegatividades para elementos que não podem ser tratados por outros métodos, por ex. francium, que tem uma eletronegatividade de Allen de 0,67. No entanto, não está claro o que deve ser considerado como elétrons de valência para os elementos dos blocos d e f, o que leva a uma ambigüidade de suas eletronegatividades calculadas pelo método de Allen.
Nesta escala, o néon tem a maior eletronegatividade de todos os elementos, seguido pelo flúor, hélio e oxigênio.
| Grupo → | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10. | 11 | 12 | 13 | 14 | 15 | 16. | 17. | 18. |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ↓ Período | ||||||||||||||||||
| 1 | H. H. H. 2.300 | Ele. 4.160 | ||||||||||||||||
| 2 | Li 0,912 | Ser 1.576 | B 2.051 | C 2.544 | N 3.066 | O 3.610 | F 4.193 | Não. 4.787 | ||||||||||
| 3 | Nao 0,86 | Mg 1.293 | Al. 1.613 | Si 1.916 | P 2.253 | S 2.589 | Cl 2.869 | Ar 3.242 | ||||||||||
| 4 | KK 0,7534 | Ca. 1.034 | Sc 1.19 | Ti 1.38 | V 1.53 | C. 1.65 | Mn. 1.75 | Fe 1.80 | Co 1.84 | Ni 1.88 | Cu 1,805 | Zn 1.588 | Ga 1.756 | Ge 1.994 | Como 2.211 | Se 2.424. | B. 2.685 | Kr 2.966 |
| 5 | Rb 0,7506 | Sr. 0,963 | Y 1.12 | Zr 1.3. | Nb 1.4. | Mo 1.4. | TC 1.51 | Ru 1.54 | Rh 1.56 | Pd 1.58 | Agrupamento 1,8 | Cd 1.521 | Em 1.6.56 | Sn 1.824 | Sb 1.984 | Te 2.158. | Eu... 2.359 | Xe 2.582 |
| 6 | C 0.659 | Bando 0,81 | Lu 1.09 | Hf 1.16 | Ta. 1.3. | W 1.4. | Repito 1.60 | Os 1.65 | Ir. 1.68 | Pt 1.72 | Au! 1.92 | Hg 1.765 | ? 1.789 | PB 1.854 | B. 2.01 | Po 2.19 | Em 2.39 | RN 2.60 |
| 7 | Pe. 0,67 | Ra 0,809 | ||||||||||||||||
| Ver também: Eletronegatividades dos elementos (página de dados) | ||||||||||||||||||
Correlação da eletronegatividade com outras propriedades
A grande variedade de métodos de cálculo de eletronegatividades, que fornecem resultados que se correlacionam bem uns com os outros, é uma indicação do número de propriedades químicas que podem ser afetadas pela eletronegatividade. A aplicação mais óbvia das eletronegatividades está na discussão da polaridade da ligação, para a qual o conceito foi introduzido por Pauling. Em geral, quanto maior a diferença de eletronegatividade entre dois átomos, mais polar será a ligação que será formada entre eles, com o átomo com maior eletronegatividade estando na extremidade negativa do dipolo. Pauling propôs uma equação para relacionar o "caráter iônico" de uma ligação à diferença de eletronegatividade dos dois átomos, embora isso tenha caído um pouco em desuso.
Várias correlações foram mostradas entre as frequências de alongamento infravermelho de certas ligações e as eletronegatividades dos átomos envolvidos: no entanto, isso não é surpreendente, pois essas frequências de alongamento dependem em parte da força de ligação, que entra no cálculo das eletronegatividades de Pauling. Mais convincentes são as correlações entre eletronegatividade e deslocamentos químicos na espectroscopia de NMR ou deslocamentos de isômeros na espectroscopia de Mössbauer (veja a figura). Ambas as medições dependem da densidade do elétron s no núcleo e, portanto, são uma boa indicação de que as diferentes medidas de eletronegatividade realmente descrevem "a capacidade de um átomo em uma molécula de atrair elétrons para si".
Tendências na eletronegatividade
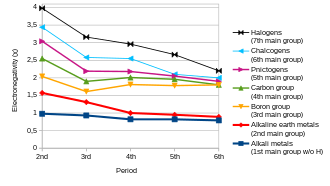
Tendências periódicas
Em geral, a eletronegatividade aumenta ao passar da esquerda para a direita ao longo de um período e diminui ao descer um grupo. Portanto, o flúor é o mais eletronegativo dos elementos (sem contar os gases nobres), enquanto o césio é o menos eletronegativo, pelo menos daqueles elementos para os quais dados substanciais estão disponíveis. Isso levaria a crer que o fluoreto de césio é o composto cuja ligação apresenta o caráter mais iônico.
Existem algumas exceções a esta regra geral. O gálio e o germânio têm eletronegatividades mais altas que o alumínio e o silício, respectivamente, devido à contração do bloco d. Elementos do quarto período imediatamente após a primeira linha dos metais de transição têm raios atômicos excepcionalmente pequenos porque os elétrons 3d não são eficazes em proteger a carga nuclear aumentada, e o tamanho atômico menor se correlaciona com maior eletronegatividade (ver Allred-Rochow eletronegatividade e Sanderson eletronegatividade acima). A eletronegatividade anormalmente alta do chumbo, em particular quando comparada ao tálio e ao bismuto, é um artefato da eletronegatividade que varia com o estado de oxidação: sua eletronegatividade se adapta melhor às tendências se for cotado para o estado +2 com um valor de Pauling de 1,87 em vez do +4 estado.
Variação da eletronegatividade com número de oxidação
Na química inorgânica, é comum considerar um único valor de eletronegatividade como válido para a maioria das propriedades "normais" situações. Embora esta abordagem tenha a vantagem da simplicidade, é claro que a eletronegatividade de um elemento não é uma propriedade atômica invariável e, em particular, aumenta com o estado de oxidação do elemento.
Allred usou o método de Pauling para calcular eletronegatividades separadas para diferentes estados de oxidação de um punhado de elementos (incluindo estanho e chumbo) para os quais havia dados suficientes disponíveis. No entanto, para a maioria dos elementos, não há compostos covalentes diferentes suficientes para os quais as energias de dissociação de ligação sejam conhecidas para tornar essa abordagem viável. Isso é particularmente verdadeiro para os elementos de transição, onde os valores citados de eletronegatividade são geralmente, necessariamente, médias de vários estados de oxidação diferentes e onde as tendências de eletronegatividade são mais difíceis de ver como resultado.
| Ácido | Fórmula | Chlorine oxidação Estado | pKKum |
|---|---|---|---|
| Ácido hipocloro | HClO | + 1 | + 7,5 |
| Ácido cloroso | HClO2 | +3 | +2.0 |
| Ácido clorídrico | HClO3 | +5 | -1.0 |
| Ácido perclórico | HClO4 | +7 | - Sim. |
Os efeitos químicos desse aumento da eletronegatividade podem ser vistos tanto nas estruturas de óxidos e haletos quanto na acidez de óxidos e oxoácidos. Portanto CrO3 e Mn2O7 são óxidos ácidos com baixos pontos de fusão, enquanto Cr2O3 é anfotérico e Mn2O3 é um óxido completamente básico.
O efeito também pode ser visto claramente nas constantes de dissociação pKa dos oxoácidos do cloro. O efeito é muito maior do que poderia ser explicado pela carga negativa sendo compartilhada entre um número maior de átomos de oxigênio, o que levaria a uma diferença de pKa de log10(1⁄4) = –0,6 entre ácido hipocloroso e ácido perclórico. À medida que o estado de oxidação do átomo de cloro central aumenta, mais densidade de elétrons é extraída dos átomos de oxigênio para o cloro, diminuindo a carga negativa parcial de átomos de oxigênio individuais. Ao mesmo tempo, a carga parcial positiva no hidrogênio aumenta com um estado de oxidação mais alto. Isso explica a acidez aumentada observada com um estado de oxidação crescente nos oxoácidos de cloro.
Esquema de eletronegatividade e hibridização
A eletronegatividade de um átomo muda dependendo da hibridização do orbital empregado na ligação. Os elétrons nos orbitais s são mantidos mais firmemente do que os elétrons nos orbitais p. Portanto, uma ligação a um átomo que emprega um orbital híbrido spx para ligação será mais fortemente polarizada para aquele átomo quando o orbital híbrido tiver mais caráter s. Ou seja, quando as eletronegatividades são comparadas para diferentes esquemas de hibridização de um determinado elemento, a ordem χ(sp3) < χ(sp2) < χ(sp) se mantém (a tendência também deve se aplicar a índices de hibridização não inteira). Embora isso seja verdadeiro em princípio para qualquer elemento do grupo principal, os valores para a eletronegatividade específica da hibridação são citados com mais frequência para o carbono. Na química orgânica, essas eletronegatividades são frequentemente invocadas para prever ou racionalizar as polaridades das ligações em compostos orgânicos contendo ligações duplas e triplas ao carbono.
| Hibridização | χ (Pauling) |
|---|---|
| C(sp)3) | 2.3. |
| C(sp)2) | 2. |
| C(sp) | 3.1 |
| 'generic' C | 2.5. |
Eletronegatividade de grupo
Na química orgânica, a eletronegatividade está mais associada a diferentes grupos funcionais do que a átomos individuais. Os termos eletronegatividade de grupo e eletronegatividade do substituinte são usados como sinônimos. No entanto, é comum distinguir entre o efeito indutivo e o efeito de ressonância, que podem ser descritos como σ- e π-eletronegatividades, respectivamente. Existem várias relações lineares de energia livre que foram usadas para quantificar esses efeitos, das quais a equação de Hammett é a mais conhecida. Os parâmetros de Kabachnik são eletronegatividades de grupo para uso na química de organofosforados.
Eletropositividade
Eletropositividade é uma medida da capacidade de um elemento de doar elétrons e, portanto, formar íons positivos; assim, é o antípoda da eletronegatividade.
Esse é principalmente um atributo dos metais, o que significa que, em geral, quanto maior o caráter metálico de um elemento, maior a eletropositividade. Portanto, os metais alcalinos são os mais eletropositivos de todos. Isso porque eles possuem um único elétron em sua camada externa e, por estar relativamente distante do núcleo do átomo, é facilmente perdido; em outras palavras, esses metais têm baixas energias de ionização.
Enquanto a eletronegatividade aumenta ao longo dos períodos na tabela periódica e diminui nos grupos descendentes, a eletropositividade diminui ao longo dos períodos (da esquerda para a direita) e aumenta nos grupos descendentes. Isso significa que os elementos no canto superior direito da tabela periódica de elementos (oxigênio, enxofre, cloro, etc.) terão a maior eletronegatividade, e aqueles no canto inferior esquerdo (rubídio, césio e frâncio) a maior eletropositividade.