Doença de Lafora
A doença de LaFora é um distúrbio genético raro, de início adulto e autossômico, que resulta na epilepsia da mioclonia e geralmente resulta na morte vários anos após o início dos sintomas. A doença é caracterizada pelo acúmulo de corpos de inclusão, conhecidos como corpos Lafora, dentro do citoplasma das células no coração, fígado, músculo e pele. A doença de LaFora também é uma doença neurodegenerativa que causa prejuízo no desenvolvimento de neurônios corticais cerebrais (cerebrais) e é um transtorno do metabolismo do glicogênio.
A doença de LaFora (LD) foi descrita pelo neuropatologista espanhol Gonzalo Rodríguez LaFora (1886-1971) em 1911, enquanto dirigia a seção de neuropatologia no Hospital do Governo para Mental Insane (NIH atual, EUA)Lafora é uma doença rara, o que significa que é muito rara em crianças, adolescentes e adultos em todo o mundo. No entanto, a doença de Lafora tem maior incidência entre crianças e adolescentes com ascendência de regiões onde as relações consanguíneas são comuns, nomeadamente o Mediterrâneo (Norte de África, Sul da Europa), Médio Oriente, Índia e Paquistão. Os cães também podem ter a condição. Em cães, a doença de Lafora pode ocorrer espontaneamente em qualquer raça, mas o Dachshund Miniature Wire Haired, o Bassett Hound e o Beagle são predispostos à LD.
A maioria dos pacientes humanos com esta doença não vive além dos vinte e cinco anos, e geralmente leva à morte dentro de dez anos após aparecer os sintomas. Os sintomas de início tardio desta doença podem começar em qualquer idade, dependendo dos genes afetados. Atualmente, não há cura para esta doença, mas existem maneiras de lidar com sintomas por meio de tratamentos e medicamentos.Sinais e sintomas
Os sintomas da doença de Lafora começam a se desenvolver durante os primeiros anos da adolescência e progridem com o passar do tempo. Antes disso, geralmente não há indicação da presença da doença, embora em alguns casos a doença se apresente como um distúrbio de aprendizagem por volta dos 5 anos de idade. Em casos extremamente raros, os sintomas podem não aparecer até a 3ª década de vida, embora esses casos tenham uma progressão mais lenta do que a LD típica. A característica mais comum da doença de Lafora são as convulsões relatadas principalmente como convulsões occipitais e mioclônicas, com alguns casos de convulsões tônico-clônicas generalizadas, convulsões de ausência atípica e convulsões atônicas e parciais complexas. Outros sintomas comuns com as convulsões são ataques de queda, ataxia, cegueira temporária, alucinações visuais e uma demência dramática e de rápido desenvolvimento.
Outros sinais e sintomas comuns associados à doença de Lafora são alterações comportamentais devido à frequência das convulsões. Com o tempo, os afetados com a doença de Lafora apresentam alterações cerebrais que causam confusão, dificuldades de fala, depressão, declínio da função intelectual, julgamento prejudicado e memória prejudicada. Se áreas do cerebelo forem afetadas por convulsões, é comum ver problemas de fala, coordenação e equilíbrio em pacientes com Lafora.
Para cães que são afetados pela doença de Lafora, os sintomas comuns são rápidos, tremendo ou empurrando da cabeça de cabeça para trás, vocalizações agudas que podem indicar que o cachorro está em pânico, apreensões e - como a doença Progride - demência, cegueira e perda de equilíbrio.
Dez anos após o desenvolvimento dos sintomas, a expectativa de vida diminui. As pessoas que avançam para a idade adulta tendem a perder a capacidade de realizar tarefas cotidianas sozinhas, o que pode exigir cuidados integrais. Se os sintomas progredirem muito rapidamente ou em tenra idade, os pacientes recebem cuidados abrangentes, que - além da medicação - significam apoio durante as atividades diárias, tanto física quanto mentalmente.
genética
A doença de Lafora é um distúrbio autossômico recessivo, causado por mutações de perda de função no gene laforin glicogênio fosfatase (EPM2A) ou no gene malin E3 ubiquitina ligase (NHLRC1). Essas mutações em qualquer um desses dois genes levam à formação de poliglucosana ou formação de corpo lafora no citoplasma do coração, fígado, músculo e pele.
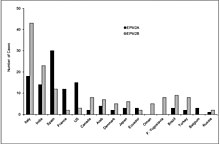
'Gráfico 1' mostra os dados de 250 famílias afetadas pela doença de Lafora e a distribuição dos casos em todo o mundo. O gráfico mostra que há um número muito grande de casos na Itália por causa de uma maior ocorrência da mutação do gene EPM2A em comparação com qualquer outro país do mundo.
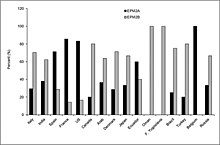
'Gráfico 2' mostra a distribuição percentual dos casos de uma mutação do gene EPM2A ou uma mutação do gene EPM2B (NHLRC1). 42% dos casos são causados por EPM2A e 58% são causados por EPM2B (NHLRC1). A mutação mais comum no gene EPM2A é a mutação R241X. Esta mutação genética é a causa de 17% dos casos de doença de Lafora causados por EPM2A.
EPM2A codifica a proteína laforina, uma fosfatase de dupla especificidade que atua nos carboidratos removendo os fosfatos.
NHLRC1 codifica a proteína malin, uma E3 ubiquitina ligase, que regula a quantidade de laforin.
Laforin é essencial para fazer a estrutura normal de uma molécula de glicogênio. Quando a mutação ocorre no gene EPM2A, a proteína laforina é regulada negativamente e menos quantidade desta proteína está presente ou nenhuma é produzida. Se também houver uma mutação no gene NHLRC1 que produz a proteína malina, então a laforina não pode ser regulada e, portanto, menos dela é produzida.
Menos Laforin significa mais fosforilação do glicogênio, causando alterações conformacionais, tornando-o insolúvel, levando a um acúmulo de glicogênio deformado, que tem efeitos neurotóxicos.
Na mutação da laforina, o glicogênio seria hiperfosforilado; isso foi confirmado em camundongos knock-out para laforina.
A literatura de pesquisa também sugere que a atividade excessiva da glicogênio sintase, a enzima chave na síntese de glicogênio, pode levar à formação de poliglucosanos e pode ser inativada por fosforilação em vários resíduos de aminoácidos por muitas moléculas, incluindo GSK-3beta, Proteína fosfatase 1 e malina.
Como as moléculas enzimáticas defeituosas participam da produção dessas moléculas (GSK-3beta, PP1 e malina), a atividade excessiva da glicogênio sintase ocorre em combinação com mutações na laforina que fosforila o excesso de glicogênio produzido, tornando-o insolúvel. O principal jogador que falta é a ubiquitina. Não é capaz de degradar a quantidade em excesso dos corpos lafora insolúveis. Como surgem mutações na malina, uma ubiquitina ligase e3, esta interfere diretamente na degradação da laforina, fazendo com que a laforina não seja degradada. Neste caso, a laforina é então hiperfosforilada.
Corpos Lafora
A doença de Lafora se distingue pela presença de inclusões chamadas corpos de Lafora no citoplasma das células. Os corpos de Lafora são agregados de poliglucosanos ou moléculas de glicogênio com formato anormal. O glicogênio em pacientes com doença de Lafora tem comprimentos de cadeia anormais, o que faz com que sejam insolúveis, se acumulem e tenham um efeito neurotóxico.
Para que o glicogênio seja solúvel, deve haver cadeias curtas e uma alta frequência de pontos de ramificação, mas isso não é encontrado no glicogênio em pacientes com Lafora. Os pacientes com LD têm cadeias mais longas que têm arranjos agrupados de pontos de ramificação que formam áreas cristalinas de dupla hélice, tornando mais difícil para eles limpar a barreira hematoencefálica. O glicogênio em pacientes com DL também possui níveis mais elevados de fosfato e está presente em maiores quantidades.
Diagnóstico
A doença de Lafora é diagnosticada através da realização de uma série de testes por um neurologista, epileptologista (pessoa especializada em epilepsia) ou geneticista. Para confirmar o diagnóstico, são necessários um EEG, ressonância magnética e testes genéticos. Uma biópsia também pode ser necessária para detectar e confirmar a presença de corpos de Lafora na pele.
Epidemiologia
Todos os relatórios publicados sobre a doença de Lafora mostraram que a prevalência geral da doença é de cerca de 4 casos por milhão de indivíduos em todo o mundo. A doença de Lafora é muito mais prevalente em países com maior número de casos de endogamia. Normalmente, esses locais são geograficamente ou culturalmente mais isolados do mundo em geral.
Tratamento
Não há cura para a doença de Lafora, sendo o tratamento limitado ao controle das convulsões por meio de medicamentos antiepilépticos e anticonvulsivantes. O tratamento geralmente é baseado nos sintomas específicos do indivíduo e na gravidade desses sintomas. Alguns exemplos de medicamentos incluem valproato, levetiracetam, topiramato, benzodiazepínicos ou perampanel. Embora os sintomas e as convulsões possam ser controlados por um longo período com o uso de drogas antiepilépticas, os sintomas irão progredir e os pacientes perderão a capacidade de realizar atividades diárias levando a uma taxa de sobrevivência de aproximadamente 10 anos após o início dos sintomas. A qualidade de vida piora com o passar dos anos, com alguns pacientes precisando de uma sonda de alimentação para obter a nutrição e a medicação de que precisam para continuar vivendo, mas não necessariamente funcionando. Recentemente, a metformina foi aprovada para o tratamento.
Pesquisa
A doença recebeu o nome de Gonzalo Rodríguez Lafora (1886–1971), um neuropatologista espanhol que primeiro reconheceu pequenos corpos de inclusão em pacientes de Lafora no início e meados do século XX.
Pesquisas recentes investigaram se a inibição da síntese de glicogênio por meio da restrição da ingestão de glicose poderia potencialmente interromper a formação dos corpos de Lafora em neurônios em modelos de camundongos com deficiência de laforina, ao mesmo tempo em que reduzia as chances de convulsões.
Pesquisadores nos EUA, Canadá e Europa formaram a Lafora Epilepsy Cure Initiative com financiamento do National Institutes of Health. O grupo pretende interromper o processo de como as mutações em laforin e malin interferem no metabolismo normal de carboidratos em modelos de camundongos.
Contenido relacionado
Ligamento
Odontologia
Abscesso cerebral