Datação por radiocarbono

A datação por radiocarbono (também chamada de datação por carbono ou datação por carbono 14) é um método para determinar a idade de um objeto contendo material orgânico usando as propriedades do radiocarbono, um isótopo radioativo de carbono.
O método foi desenvolvido no final da década de 1940 na Universidade de Chicago por Willard Libby. Baseia-se no fato de que o radiocarbono (14
C) é constantemente criado na atmosfera da Terra pela interação de raios cósmicos com nitrogênio atmosférico. O resultado 14
C combina-se com o oxigênio atmosférico para formar dióxido de carbono radioativo, que é incorporado às plantas pela fotossíntese; os animais então adquirem 14
C comendo as plantas. Quando o animal ou planta morre, ele para de trocar carbono com seu ambiente e, posteriormente, a quantidade de 14
C que contém começa a diminuir como o 14
C sofre decaimento radioativo. Medindo a proporção de 14
C em uma amostra de uma planta ou animal morto, como um pedaço de madeira ou um fragmento de osso, fornece informações que podem ser usadas para calcular quando o animal ou planta morreu. Quanto mais antiga for uma amostra, menos 14
C deve ser detectado, e porque a meia-vida de 14
C (o período de tempo após o qual metade de uma determinada amostra terá decaído) é de cerca de 5.730 anos, as datas mais antigas que podem ser medidas com segurança por este processo data de aproximadamente 50.000 anos atrás (neste intervalo cerca de 99,8% do 14
C terá decaído), embora especial os métodos de preparação ocasionalmente tornam possível uma análise precisa de amostras mais antigas. Em 1960, Libby recebeu o Prêmio Nobel de Química por seu trabalho.
Pesquisas estão em andamento desde a década de 1960 para determinar qual a proporção de 14
C na atmosfera foi superior a 50.000 anos. Os dados resultantes, na forma de uma curva de calibração, são agora usados para converter uma determinada medição de radiocarbono numa amostra numa estimativa da idade civil da amostra. Outras correções devem ser feitas para levar em conta a proporção de 14
C em diferentes tipos de organismos (fracionamento) e os vários níveis de 14
C em toda a biosfera (efeitos de reservatório). Complicações adicionais provêm da queima de combustíveis fósseis, como carvão e petróleo, e dos testes nucleares acima do solo realizados nas décadas de 1950 e 1960.
Porque o tempo necessário para converter materiais biológicos em combustíveis fósseis é substancialmente maior do que o tempo necessário para sua 14
C para decair abaixo dos níveis detectáveis, os combustíveis fósseis quase não contêm 14
C. Como resultado, a partir do final do século XIX, houve uma queda notável na proporção de 14
C na atmosfera como o o dióxido de carbono gerado pela queima de combustíveis fósseis começou a se acumular. Por outro lado, os testes nucleares aumentaram a quantidade de 14
C na atmosfera, que atingiu um máximo em cerca de 1965 de quase o dobro da quantidade presente na atmosfera antes dos testes nucleares.
A medição do radiocarbono foi originalmente feita com dispositivos de contagem beta, que contavam a quantidade de radiação beta emitida pelo 14
C átomos em uma amostra. Mais recentemente, a espectrometria de massa com acelerador tornou-se o método de escolha; conta todos os 14
C átomos de C na amostra e não apenas os poucos que decaem durante as medições; portanto, pode ser usado com amostras muito menores (tão pequenas quanto sementes de plantas individuais) e fornece resultados muito mais rapidamente. O desenvolvimento da datação por radiocarbono teve um impacto profundo na arqueologia. Além de permitir uma datação mais precisa em sítios arqueológicos do que os métodos anteriores, permite a comparação de datas de eventos em grandes distâncias. As histórias da arqueologia referem-se frequentemente ao seu impacto como a “revolução do radiocarbono”. A datação por radiocarbono permitiu datar transições importantes na pré-história, como o fim da última era glacial e o início do Neolítico e da Idade do Bronze em diferentes regiões.
Plano de fundo
Histórico
Em 1939, Martin Kamen e Samuel Ruben, do Laboratório de Radiação de Berkeley, iniciaram experimentos para determinar se algum dos elementos comuns na matéria orgânica tinha isótopos com meias-vidas longas o suficiente para serem valiosos na pesquisa biomédica. Eles sintetizaram 14
C usando o acelerador cíclotron do laboratório e logo descobriu que a meia-vida do átomo era muito mais tempo do que se pensava anteriormente. Isto foi seguido por uma previsão de Serge A. Korff, então empregado no Instituto Franklin na Filadélfia, de que a interação de nêutrons térmicos com 14
N na atmosfera superior criaria 14
C. Anteriormente, pensava-se que 14
C teria maior probabilidade de ser criado por deuterons interagindo com 13
C. Em algum momento durante a Segunda Guerra Mundial, Willard Libby, que então estava em Berkeley, soube da pesquisa de Korff e concebeu a ideia de que poderia ser possível usar radiocarbono para datação.
Em 1945, Libby mudou-se para a Universidade de Chicago, onde começou seu trabalho em datação por radiocarbono. Ele publicou um artigo em 1946 no qual propôs que o carbono na matéria viva poderia incluir 14
C bem como carbono não radioativo. Libby e vários colaboradores começaram a fazer experiências com metano coletado em estações de esgoto em Baltimore e, após enriquecer isotopicamente suas amostras, conseguiram demonstrar que continham 14
C. Por outro lado, o metano criado a partir do petróleo não apresentou atividade de radiocarbono devido à sua idade. Os resultados foram resumidos num artigo publicado na Science em 1947, no qual os autores comentaram que os seus resultados implicavam que seria possível datar materiais contendo carbono de origem orgânica.
Libby e James Arnold testaram a teoria da datação por radiocarbono analisando amostras com idades conhecidas. Por exemplo, duas amostras retiradas dos túmulos de dois reis egípcios, Zoser e Sneferu, datadas independentemente de 2.625 aC, mais ou menos 75 anos, foram datadas por medição de radiocarbono em uma média de 2.800 aC, mais ou menos 250 anos. Estes resultados foram publicados na revista Science em dezembro de 1949. 11 anos após o seu anúncio, mais de 20 laboratórios de datação por radiocarbono foram criados em todo o mundo. Em 1960, Libby recebeu o Prêmio Nobel de Química por este trabalho.
Detalhes físicos e químicos
Na natureza, o carbono existe como três isótopos: dois estáveis e não radioativos (carbono-12 ( 12
C) e carbono -13 (13
C) e um carbono-14 radioativo (14
C), também conhecido como "radiocarbono"). A meia-vida de 14
C (o tempo que leva para metade de uma determinada quantidade de 14
C para decair) é de cerca de 5.730 anos, portanto, pode-se esperar que sua concentração na atmosfera diminua ao longo de milhares de anos, mas 14
C é constantemente produzido na baixa estratosfera e na alta troposfera, principalmente pelos raios cósmicos galácticos e, em menor grau, pelos raios cósmicos solares. Esses raios cósmicos geram nêutrons à medida que viajam pela atmosfera, que podem atingir o nitrogênio-14 (14
N) átomos e transformá-los em 14
C. A seguinte reação nuclear é o principal caminho pelo qual 14
C é criado:
n + 14
7N
→ 14
6C
+ p
onde n representa um nêutron ep representa um próton.
Depois de produzido, o 14
C combina rapidamente com o oxigênio (O) na atmosfera para formar primeiro monóxido de carbono (CO) e, finalmente, dióxido de carbono (CO
2</sub ).
14C + O2 → 14CO + O
14CO + OH → 14 CO2 + H
O dióxido de carbono produzido desta forma difunde-se na atmosfera, é dissolvido no oceano e é absorvido pelas plantas através da fotossíntese. Os animais comem as plantas e, finalmente, o radiocarbono é distribuído por toda a biosfera. A proporção de 14
C para 12
C tem aproximadamente 1,25 partes de 14
C a 1012 partes de 12
C. Além disso, cerca de 1% dos átomos de carbono são do isótopo estável 13
C.
A equação para o decaimento radioativo de 14
C é:
14
6C
→ 14
7N
+
e−
+
ν
e
Ao emitir uma partícula beta (um elétron, e−) e um antineutrino de elétron (
<sub style="font-size:inherit;line-height:inherit;vertical-align:baseline" ν
e), um dos nêutrons no 14
C núcleo muda para um próton e o estilo 14
O núcleo C reverte para o isótopo estável (não radioativo) 14
N.
Princípios
Durante a sua vida, uma planta ou animal está em equilíbrio com o seu ambiente, trocando carbono com a atmosfera ou através da sua dieta. Terá, portanto, a mesma proporção de 14
C como a atmosfera, ou no caso de animais ou plantas marinhas, com o oceano. Depois de morrer, ele deixa de adquirir 14
C, mas o 14
C dentro de seu material biológico nesse momento continuará a decair e, portanto, a proporção de 14
C para 12
C em seus restos diminuirá gradualmente. Porque 14
C decai a uma taxa conhecida, a proporção de radiocarbono pode ser usada para determinar quanto tempo se passou desde uma determinada amostra parou de trocar carbono – quanto mais antiga a amostra, menos 14
C será deixado.
A equação que rege o decaimento de um isótopo radioativo é:
N= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =N0e- Sim. - Sim. λ λ )Não. N=N_{0},e^{-lambda t},}
onde N0 é o número de átomos do isótopo na amostra original (no tempo t = 0, quando o organismo de onde a amostra foi coletada morreu), e N é o número de átomos restantes após o tempo t. λ é uma constante que depende do isótopo específico; para um determinado isótopo, é igual ao inverso da vida média – ou seja, o tempo médio ou esperado que um determinado átomo sobreviverá antes de sofrer decaimento radioativo. A vida média, denotada por τ, de 14
C é 8.267 anos, então a equação acima pode ser reescrito como:
)= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =I (N0/N))) 8267 anos{displaystyle t=ln(N_{0}/N)cdot {text{8267 years}}}
Presume-se que a amostra originalmente tinha o mesmo 14
C/12
<sub style="font-size:inherit;line-height:inherit;vertical-align:baseline" Razão C como a razão na atmosfera, e como o tamanho da amostra é conhecido, o número total de átomos na amostra pode ser calculado, resultando em N0, o número de 14
C átomos na amostra original. Medição de N, o número de 14
C átomos atualmente na amostra, permite o cálculo de t, a idade da amostra, usando a equação acima.
A meia-vida de um isótopo radioativo (geralmente denotada por t1/2) é um conceito mais familiar do que a vida média, portanto, embora as equações acima sejam expressas em termos da média -life, é mais comum citar o valor de 14
Cé meia-vida do que sua vida média. O valor atualmente aceito para a meia-vida de 14
C é 5.700 ± 30 anos. Isso significa que depois de 5.700 anos, apenas metade do 14
C permanecerá; um quarto permanecerá após 11.400 anos; um oitavo após 17.100 anos; e assim por diante.
Os cálculos acima fazem diversas suposições, como o nível de 14
C na atmosfera permaneceu constante ao longo do tempo. Na verdade, o nível de 14
C na atmosfera variou significativamente e, como resultado, os valores fornecidos pela equação acima foram ser corrigido usando dados de outras fontes. Isso é feito por curvas de calibração (discutidas abaixo), que convertem uma medida de 14
C em uma amostra em uma idade estimada do calendário. Os cálculos envolvem diversas etapas e incluem um valor intermediário denominado "idade do radiocarbono", que é a idade em "anos de radiocarbono" da amostra: uma idade citada em anos de radiocarbono significa que nenhuma curva de calibração foi usada − os cálculos para anos de radiocarbono assumem que a 14
C/12
C não mudou ao longo do tempo.
O cálculo da idade do radiocarbono também requer o valor da meia-vida de 14
C. No artigo de Libby de 1949, ele usou um valor de 5.720 ± 47 anos, baseado na pesquisa de Engelkemeir et al. Este valor estava notavelmente próximo do valor moderno, mas pouco depois o valor aceite foi revisto para 5568 ± 30 anos, e este valor esteve em uso durante mais de uma década. Foi revisado novamente no início da década de 1960 para 5.730 ± 40 anos, o que significava que muitas datas calculadas em artigos publicados antes disso estavam incorretas (o erro na meia-vida é de cerca de 3%). Para consistência com esses primeiros artigos, foi acordado na Conferência de Radiocarbono de 1962 em Cambridge (Reino Unido) usar a "meia-vida de Libby" de 5568 anos. As idades do radiocarbono ainda são calculadas usando esta meia-vida e são conhecidas como "Idade do Radiocarbono Convencional". Como a curva de calibração (IntCal) também informa 14
C concentração usando esta idade convencional, qualquer idade convencional calibrada em relação à curva IntCal produzirá uma idade calibrada correta. Quando uma data é citada, o leitor deve estar ciente de que se for uma data não calibrada (um termo usado para datas dadas em anos de radiocarbono) pode diferir substancialmente da melhor estimativa da data real do calendário, tanto porque usa o valor errado para a meia-vida de 14
C, e porque nenhuma correção (calibração) foi aplicada para a variação histórica de 14
C na atmosfera ao longo do tempo.
Reservatório de troca de carbono

C em cada reservatório
O carbono está distribuído pela atmosfera, pela biosfera e pelos oceanos; estes são referidos coletivamente como reservatório de troca de carbono, e cada componente também é referido individualmente como reservatório de troca de carbono. Os diferentes elementos do reservatório de troca de carbono variam na quantidade de carbono que armazenam e no tempo que leva para o 14
C gerado pelos raios cósmicos para se misturar totalmente com eles. Isso afeta a proporção de 14
C para 12
C nos diferentes reservatórios e, portanto, as idades de radiocarbono das amostras originadas em cada reservatório. A atmosfera, que é onde 14
C é gerado, contém cerca de 1,9% do carbono total nos reservatórios, e o 14
C contém mixagens em menos de sete anos. A proporção de 14
C para 12
C na atmosfera é considerada a linha de base para os outros reservatórios: se outro reservatório tiver uma proporção menor de 14
C para 12
C, indica que o carbono é mais antigo e, portanto, alguns dos 14
C decaiu ou o reservatório está recebendo carbono que não está na linha de base atmosférica. A superfície do oceano é um exemplo: contém 2,4% do carbono no reservatório de troca, mas há apenas cerca de 95% dessa quantidade 14
C como seria de esperar se a proporção fosse a mesma da atmosfera. O tempo que leva para o carbono da atmosfera se misturar com a superfície do oceano é de apenas alguns anos, mas as águas superficiaistambém recebem água do oceano profundo, que contém mais de 90% do carbono no reservatório. A água nas profundezas do oceano leva cerca de 1.000 anos para circular de volta pelas águas superficiais e, portanto, as águas superficiais contêm uma combinação de água mais antiga, com 14
C, e água recentemente na superfície, com 14
C em equilíbrio com a atmosfera.
As criaturas que vivem na superfície do oceano têm a mesma 14
Razões C conforme a água em que vivem e como resultado de o 14
C/12
C, a idade do radiocarbono da vida marinha é normalmente de cerca de 400 anos. Os organismos terrestres estão em equilíbrio mais próximo com a atmosfera e têm a mesma 14
C/12
C relação como a atmosfera. Esses organismos contêm cerca de 1,3% do carbono do reservatório; os organismos marinhos têm uma massa inferior a 1% dos terrestres e não são mostrados no diagrama. A matéria orgânica morta acumulada, tanto de plantas como de animais, excede a massa da biosfera por um factor de quase 3, e como esta matéria já não troca carbono com o seu ambiente, tem um 14
C/12 Razão
C inferior à da biosfera.
Considerações sobre namoro
A variação no 14
C/12
C em diferentes partes do reservatório de troca de carbono significa que um cálculo direto da idade de uma amostra com base na quantidade de 14
C que ele contém geralmente dará um resultado incorreto. Existem várias outras possíveis fontes de erro que precisam ser consideradas. Os erros são de quatro tipos gerais:
- variações na 14
C/12
C razão na atmosfera, tanto geograficamente como ao longo do tempo; - fracionamento isotópico;
- variações na 14
C/12
C proporção em diferentes partes do reservatório; - contaminação.
Variação atmosférica
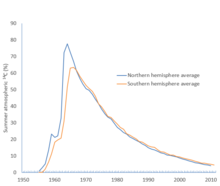
C para os hemisférios norte e sul, mostrando excesso percentual acima dos níveis pré-bomb. O Tratado de Prova Parcial entrou em vigor em 10 de outubro de 1963.
Nos primeiros anos de uso da técnica, entendia-se que ela dependia da 14
Classe C/12
C tendo permanecido a mesma ao longo dos últimos milhares de anos. Para verificar a precisão do método, foram testados vários artefatos datáveis por outras técnicas; os resultados dos testes estavam razoavelmente de acordo com as verdadeiras idades dos objetos. Com o tempo, porém, começaram a aparecer discrepâncias entre a cronologia conhecida das dinastias egípcias mais antigas e as datas de radiocarbono dos artefactos egípcios. Nem a cronologia egípcia pré-existente nem o novo método de datação por radiocarbono poderiam ser considerados precisos, mas uma terceira possibilidade era que o 14
C/12
A proporção C mudou ao longo do tempo. A questão foi resolvida pelo estudo dos anéis das árvores: a comparação de séries sobrepostas de anéis das árvores permitiu a construção de uma sequência contínua de dados dos anéis das árvores que abrangeu 8.000 anos. (Desde então, a série de dados dos anéis das árvores foi estendida para 13.900 anos.) Na década de 1960, Hans Suess conseguiu usar a sequência dos anéis das árvores para mostrar que as datas derivadas do radiocarbono eram consistentes com as datas atribuídas pelos egiptólogos. Isso foi possível porque embora as plantas anuais, como o milho, tenham uma 14
C/12
C que reflete a proporção atmosférica no momento em que estavam crescendo, as árvores apenas adicionam material ao seu anel mais externo em um determinado ano, enquanto os anéis internos das árvores não recebem seu 14
C reabastecido e, em vez disso, começa a perder 14
C através da decadência. Portanto, cada anel preserva um registro da atmosfera 14
C/12
</sub Proporção C do ano em que cresceu. A datação por carbono da madeira dos próprios anéis das árvores fornece a verificação necessária sobre a atmosfera14
C/12
C proporção: com uma amostra de data conhecida e uma medida do valor de N (o número de átomos de 14
C restante na amostra), a equação de datação por carbono permite o cálculo de N0 – o número de átomos de 14
C na amostra no momento em que o anel da árvore foi formado – e, portanto, o 14
C/12
C na atmosfera naquele momento. Munido dos resultados da datação por carbono dos anéis das árvores, tornou-se possível construir curvas de calibração destinadas a corrigir os erros causados pela variação ao longo do tempo no 14
C/12
C. Essas curvas são descritas com mais detalhes abaixo.
O carvão e o petróleo começaram a ser queimados em grandes quantidades durante o século XIX. Ambos são suficientemente antigos para conter pouco ou nenhum 14
C e, como resultado, o CO
2 lançado diluiu substancialmente o 14
C/ 12
Proporção C. Datar um objeto do início do século 20 fornece, portanto, uma data aparente mais antiga que a data verdadeira. Pela mesma razão, 14
C concentrações nas vizinhanças de grandes cidades são inferiores à média atmosférica. Este efeito dos combustíveis fósseis (também conhecido como efeito Suess, em homenagem a Hans Suess, que o relatou pela primeira vez em 1955) representaria apenas uma redução de 0,2% em 14
C se o carbono adicional dos combustíveis fósseis fosse distribuído por todo o reservatório de troca de carbono, mas devido ao longo atraso na mistura com o oceano profundo, o efeito real é uma redução de 3%.
Um efeito muito maior vem dos testes nucleares acima do solo, que liberaram um grande número de nêutrons na atmosfera, resultando na criação de 14
C. De cerca de 1950 até 1963, quando os testes nucleares atmosféricos foram proibidos, estima-se que várias toneladas de 14
C foram criados. Se tudo isso extra 14
C tivesse sido imediatamente espalhado por todo o reservatório de troca de carbono, isso teria levado a um aumento no 14
C/12
C proporção de apenas alguns por cento, mas o efeito imediato foi quase dobrar a quantidade de 14
C na atmosfera, com o nível de pico ocorrendo em 1964 para o hemisfério norte e em 1966 para o hemisfério sul. Desde então, o nível caiu, à medida que este pulso de bomba ou 'bomba de carbono' foi lançado. (como às vezes é chamado) se infiltra no resto do reservatório.
Fracionamento isotópico
A fotossíntese é o principal processo pelo qual o carbono se move da atmosfera para os seres vivos. Em vias fotossintéticas 12
C é absorvido um pouco mais facilmente do que 13
C, que por sua vez é mais facilmente absorvido do que 14
C. A absorção diferencial dos três isótopos de carbono leva a 13
C/12
C e 14
C/12
Proporções de C em plantas que diferem das proporções na atmosfera. Este efeito é conhecido como fracionamento isotópico.
Para determinar o grau de fracionamento que ocorre em uma determinada planta, as quantidades de ambos 12
C e 13
C isótopos são medidos e os 13
C /12
C é então comparada a uma proporção padrão conhecida como PDB. O 13
C/12
C proporção é usada em vez de 14
C/12
C porque o primeiro é muito mais fácil de medir, e o último pode ser facilmente derivado: o esgotamento de 13
C relativo a 12
C é proporcional à diferença nas massas atômicas dos dois isótopos, então o esgotamento para 14
C é o dobro do esgotamento de 13
C. O fracionamento de 13
C, conhecido como δ13C, é calculado da seguinte forma:
δ δ C13= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =((C13C12)amostra(C13C12)padrão- Sim. - Sim. 1)× × 1000{displaystyle delta {ce {^{13}C}}=left({frac {left({frac) {{ce {^{13}C}}}{{ce {^{12}C}}right)_{text{sample}}}{left({frac {{ce {^{13}C}}}{{ce {^{12}C}}right)_{text{standard}}}}-1right)times 1000} (em inglês)
onde o sinal ‰ indica partes por mil. Porque o padrão PDB contém uma proporção incomumente alta de 13
C, mais medido δ13C são negativos.

| Material | Típico δ13C gama |
|---|---|
| PDB | 0 |
| Plankton marinho | -22‰ para -17 ( |
| Plantas de C3 | -30‰ para -22 ( |
| Plantas de C4 | -15‰ para -9 ( |
| Atmosférica CO 2 | -8 (em inglês) |
| Marinha CO 2 | -32‰ para -13 ( |
Para organismos marinhos, os detalhes das reações de fotossíntese são menos compreendidos, e os valores de δ13C para organismos fotossintéticos marinhos dependem da temperatura. Em temperaturas mais altas, CO
2 tem baixa solubilidade em água, o que significa que há menos CO
2 disponível para as reações fotossintéticas. Nessas condições, o fracionamento é reduzido e, em temperaturas acima de 14 °C (57 °F), o δ13C os valores são correspondentemente mais altos, enquanto em temperaturas mais baixas, CO
2 torna-se mais solúvel e, portanto, mais disponível para os organismos marinhos.
O valor de δ13C para animais depende de sua dieta. Um animal que come alimentos com valores altos de δ13C terá valores mais altos de δ 13C do que aquele que come alimentos com δ13C. Os próprios processos bioquímicos do animal também podem impactar os resultados: por exemplo, tanto os minerais ósseos quanto o colágeno ósseo normalmente têm uma concentração mais alta de 13
C do que é encontrado na dieta do animal, embora por diferentes razões bioquímicas. O enriquecimento do osso 13
C também implica que o material excretado está esgotado em 13
C relativo à dieta.
Desde 13
C representa cerca de 1% do carbono em uma amostra, o 13
C/12
A proporção C pode ser medida com precisão pela massa espectrometria. Valores típicos de δ13C foram encontrados experimentalmente para muitas plantas, bem como para diferentes partes de animais, como como colágeno ósseo, mas ao datar uma determinada amostra é melhor determinar diretamente o valor δ13C dessa amostra do que confiar nos valores publicados.
A troca de carbono entre o CO
2 e o carbonato na superfície do oceano também está sujeito a fracionamento, com 14
C na atmosfera é mais provável do que 12
C para se dissolver no oceano. O resultado é um aumento geral na 14
C/12
Razão C no oceano de 1,5%, em relação ao 14
C/12
C proporção na atmosfera. Este aumento em 14
C a concentração cancela quase exatamente a diminuição causada pela ressurgência de água (contendo água antiga e, portanto, 14
C-esgotado, carbono) do oceano profundo, de modo que medições diretas de 14
C são semelhantes às medições para o resto da biosfera. A correção do fracionamento isotópico, como é feito para todas as datas de radiocarbono para permitir a comparação entre os resultados de diferentes partes da biosfera, dá uma idade aparente de cerca de 400 anos para as águas superficiais dos oceanos.
Efeitos de reservatório
A hipótese original do reservatório de troca de Libby presumia que 14
C/ 12
A razão C no reservatório de troca é constante em todo o mundo, mas desde então foi descoberto que existem várias causas de variação na razão através do reservatório.
Efeito marinho
O CO
2 na atmosfera é transferido para o oceano dissolvendo-se na água superficial como íons carbonato e bicarbonato; ao mesmo tempo, os íons carbonato na água retornam ao ar como CO
2. Este processo de troca traz 14
C da atmosfera para as águas superficiais do oceano, mas o 14
C assim introduzido leva muito tempo para se infiltrar por todo o volume do oceano. As partes mais profundas do oceano misturam-se muito lentamente com as águas superficiais e a mistura é desigual. O principal mecanismo que traz águas profundas à superfície é a ressurgência, que é mais comum em regiões mais próximas do equador. A ressurgência também é influenciada por fatores como a topografia do fundo do oceano local e da costa, o clima e os padrões de vento. No geral, a mistura de águas profundas e superficiais leva muito mais tempo do que a mistura de CO
2 com as águas superficiais, e como como resultado, a água de algumas áreas oceânicas profundas tem uma idade aparente de radiocarbono de vários milhares de anos. Upwelling mistura esse "velho" água com as águas superficiais, dando às águas superficiais uma idade aparente de cerca de várias centenas de anos (após correção do fracionamento). Este efeito não é uniforme – o efeito médio é de cerca de 400 anos, mas existem desvios locais de várias centenas de anos para áreas geograficamente próximas umas das outras. Esses desvios podem ser contabilizados na calibração, e os usuários de software como o CALIB podem fornecer como entrada a correção apropriada para a localização de suas amostras. O efeito também se aplica a organismos marinhos, como conchas, e mamíferos marinhos, como baleias e focas, que têm idades de radiocarbono que parecem ter centenas de anos.
Efeito hemisfério
Os hemisférios norte e sul têm sistemas de circulação atmosférica que são suficientemente independentes um do outro para que haja um notável intervalo de tempo na mistura entre os dois. O atmosférico 14
C/12
C é mais baixa no hemisfério sul, com uma idade adicional aparente de cerca de 40 anos para resultados de radiocarbono do sul em comparação com o norte. Isto ocorre porque a maior área de superfície do oceano no hemisfério sul significa que há mais trocas de carbono entre o oceano e a atmosfera do que no norte. Como a superfície do oceano está esgotada em 14
C por causa do efeito marinho, 14
C é removido da atmosfera sul mais rapidamente do que no norte. O efeito é reforçado pela forte ressurgência em torno da Antártica.
Outros efeitos
Se o carbono na água doce for parcialmente adquirido de carbono envelhecido, como rochas, o resultado será uma redução na 14
C/12
C proporção na água. Por exemplo, rios que passam sobre calcário, que é composto principalmente de carbonato de cálcio, adquirirão íons carbonato. Da mesma forma, as águas subterrâneas podem conter carbono derivado das rochas por onde passaram. Essas rochas geralmente são tão antigas que não contêm mais nenhum 14
C, então esse carbono diminui o 14
C/12
C proporção da água que entra, o que pode levar a idades aparentes de milhares de anos tanto para a água afetada quanto para as plantas e organismos de água doce que nela vivem. Isto é conhecido como efeito da água dura porque está frequentemente associado a íons de cálcio, que são característicos da água dura; outras fontes de carbono, como o húmus, podem produzir resultados semelhantes e também podem reduzir a idade aparente se forem de origem mais recente que a amostra. O efeito varia muito e não há compensação geral que possa ser aplicada; Geralmente são necessárias pesquisas adicionais para determinar o tamanho do deslocamento, por exemplo, comparando a idade do radiocarbono das conchas de água doce depositadas com o material orgânico associado.
Erupções vulcânicas ejetam grandes quantidades de carbono no ar. O carbono é de origem geológica e não possui 14
C, então o estilo 14
C/12
C na vizinhança do vulcão está diminuída em relação a nas redondezas. Vulcões adormecidos também podem emitir carbono envelhecido. As plantas que fotossintetizam esse carbono também têm menor 14
C/12
Razões C: por exemplo, descobriu-se que as plantas na vizinhança da caldeira das Furnas, nos Açores, tinham idades aparentes que variavam entre 250 anos e 3320 anos.
Contaminação
Qualquer adição de carbono a uma amostra de idade diferente fará com que a data medida seja imprecisa. A contaminação com carbono moderno faz com que uma amostra pareça mais jovem do que realmente é: o efeito é maior para amostras mais antigas. Se uma amostra com 17.000 anos for contaminada de modo que 1% da amostra seja carbono moderno, ela parecerá 600 anos mais jovem; para uma amostra de 34 mil anos, a mesma quantidade de contaminação causaria um erro de 4 mil anos. Contaminação com carbono antigo, sem restos 14
C, causa um erro na outra direção independente da idade – uma amostra contaminada com 1 % de carbono antigo parecerá ser cerca de 80 anos mais velho do que realmente é, independentemente da data da amostra.
Amostras
As amostras para datação precisam ser convertidas em um formato adequado para medir o 14
C conteúdo; isso pode significar conversão para a forma gasosa, líquida ou sólida, dependendo da técnica de medição a ser utilizada. Antes que isso possa ser feito, a amostra deve ser tratada para remover qualquer contaminação e quaisquer constituintes indesejados. Isto inclui a remoção de contaminantes visíveis, tais como radículas que podem ter penetrado na amostra desde o seu enterramento. Lavagens com álcalis e ácidos podem ser usadas para remover a contaminação por ácidos húmicos e carbonatos, mas deve-se tomar cuidado para evitar a remoção da parte da amostra que contém o carbono a ser testado.
Considerações materiais
- É comum reduzir uma amostra de madeira para apenas o componente celulose antes de testar, mas uma vez que isso pode reduzir o volume da amostra para 20% do seu tamanho original, o teste de toda a madeira é frequentemente realizado também. O carvão é frequentemente testado, mas é provável que seja necessário tratamento para remover contaminantes.
- Osso não queimado pode ser testado; é habitual namorar usando colágeno, a fração de proteína que permanece após a lavagem do material estrutural do osso. A hidroxiprolina, um dos aminoácidos constituintes no osso, foi considerada uma vez um indicador confiável, uma vez que não era conhecido por ocorrer, exceto no osso, mas desde então foi detectado em águas subterrâneas.
- Para o osso queimado, a testabilidade depende das condições em que o osso foi queimado. Se o osso foi aquecido em condições de redução, ele (e matéria orgânica associada) pode ter sido carbonizado. Neste caso, a amostra é muitas vezes utilizável.
- As cascas de ambos os organismos marinhos e terrestres consistem quase inteiramente de carbonato de cálcio, seja como aragonita ou como calcita, ou alguma mistura dos dois. O carbonato de cálcio é muito suscetível à dissolução e recristalização; o material recrystallized conterá o carbono do ambiente da amostra, que pode ser de origem geológica. Se o teste do shell recristalizado é inevitável, às vezes é possível identificar o material original do shell de uma sequência de testes. Também é possível testar conquiolina, uma proteína orgânica encontrada na casca, mas constitui apenas 1–2% do material da casca.
- Os três principais componentes de turfa são ácido húmico, húmus e ácido fúlvico. Destes, os humins dão a data mais confiável como eles são insolúvel em alcalino e menos propensos a conter contaminantes do ambiente da amostra. Uma dificuldade particular com turfa seca é a remoção de rootlets, que provavelmente são difíceis de distinguir do material da amostra.
- O solo contém material orgânico, mas por causa da probabilidade de contaminação por ácido húmico de origem mais recente, é muito difícil obter datas de radiocarbono satisfatórias. É preferível peneirar o solo para fragmentos de origem orgânica, e datar os fragmentos com métodos que são tolerantes de pequenos tamanhos de amostra.
- Outros materiais que foram datados com sucesso incluem marfim, papel, têxteis, sementes individuais e grãos, palha de dentro tijolos de lama, e restos de comida carbonizada encontrados em cerâmica.
Preparação e tamanho
Especialmente para amostras mais antigas, pode ser útil enriquecer a quantidade de 14
C na amostra antes do teste. Isto pode ser feito com uma coluna de difusão térmica. O processo leva cerca de um mês e requer uma amostra cerca de dez vezes maior do que seria necessário de outra forma, mas permite uma medição mais precisa da 14
C /12
C em material antigo e estende a idade máxima que pode ser relatada de forma confiável.
Uma vez removida a contaminação, as amostras devem ser convertidas em um formato adequado à tecnologia de medição a ser utilizada. Onde o gás é necessário, CO
2 é amplamente utilizado. Para amostras a serem utilizadas em contadores de cintilação líquida, o carbono deve estar na forma líquida; a amostra é normalmente convertida em benzeno. Para espectrometria de massa de acelerador, alvos de grafite sólido são os mais comuns, embora CO
2 também pode ser usado.
A quantidade de material necessária para o teste depende do tipo de amostra e da tecnologia utilizada. Existem dois tipos de tecnologia de teste: detectores que registram radioatividade, conhecidos como contadores beta, e espectrômetros de massa aceleradores. Para contadores beta, normalmente é necessária uma amostra pesando pelo menos 10 gramas (0,35 onças). A espectrometria de massa do acelerador é muito mais sensível e podem ser usadas amostras contendo apenas 0,5 miligramas de carbono.
Medição e resultados

C é agora mais comumente feito com um espectrômetro de massa acelerador
Durante décadas depois que Libby realizou os primeiros experimentos de datação por radiocarbono, a única maneira de medir o 14
C em uma amostra era detectar o decaimento radioativo de átomos de carbono individuais. Nesta abordagem, o que é medido é a atividade, em número de eventos de decaimento por unidade de massa por período de tempo, da amostra. Este método também é conhecido como 'contagem beta', porque são as partículas beta emitidas pelo 14
C átomos que são detectados. No final da década de 1970, uma abordagem alternativa tornou-se disponível: contar diretamente o número de 14
C e 12
átomos de C em uma determinada amostra, por meio de espectrometria de massa com acelerador, geralmente chamada de AMS. AMS conta o 14
C/12
C proporção diretamente, em vez da atividade da amostra, mas medições de atividade e 14
C/12
C pode ser convertida exatamente uma na outra. Durante algum tempo, os métodos de contagem beta foram mais precisos que o AMS, mas o AMS é agora mais preciso e tornou-se o método de escolha para medições de radiocarbono. Além da precisão aprimorada, o AMS tem outras duas vantagens significativas sobre a contagem beta: ele pode realizar testes precisos em amostras muito pequenas para a contagem beta e é muito mais rápido - uma precisão de 1% pode ser alcançada em minutos com o AMS, que é muito mais rápido do que seria possível com a tecnologia mais antiga.
Contagem beta
O primeiro detector de Libby foi um contador Geiger projetado por ele mesmo. Ele converteu o carbono em sua amostra em negro de fumo (fuligem) e cobriu a superfície interna de um cilindro com ele. Este cilindro foi inserido no contador de forma que o fio de contagem ficasse dentro do cilindro da amostra, para que não houvesse material entre a amostra e o fio. Qualquer material interposto teria interferido na detecção de radioatividade, uma vez que as partículas beta emitidas por 14
C são tão fracos que metade é parado por uma espessura de alumínio de 0,01 mm (0,00039 pol.).
O método de Libby logo foi substituído por contadores proporcionais de gás, que eram menos afetados pelo carbono da bomba (o adicional 14
C criado por testes de armas nucleares). Esses contadores registram explosões de ionização causadas pelas partículas beta emitidas pelo 14
Átomos C; as explosões são proporcionais à energia da partícula, de modo que outras fontes de ionização, como a radiação de fundo, podem ser identificadas e ignoradas. Os contadores são cercados por blindagem de chumbo ou aço, para eliminar a radiação de fundo e reduzir a incidência de raios cósmicos. Além disso, são utilizados detectores anticoincidência; esses eventos registrados fora do contador e qualquer evento registrado simultaneamente dentro e fora do contador são considerados eventos estranhos e ignorados.
A outra tecnologia comum usada para medir 14
C atividade é a contagem de cintilação líquida, que foi inventada em 1950, mas que tinha esperar até o início da década de 1960, quando foram desenvolvidos métodos eficientes de síntese de benzeno, para se tornar competitivo com a contagem de gases; depois de 1970, os contadores de líquidos tornaram-se a escolha tecnológica mais comum para laboratórios de datação recém-construídos. Os contadores funcionam detectando flashes de luz causados pelas partículas beta emitidas por 14
C à medida que interagem com um agente fluorescente adicionado ao benzeno. Assim como os contadores de gás, os contadores de cintilação líquida requerem blindagem e contadores de anticoincidência.
Tanto para o contador proporcional de gás quanto para o contador de cintilação líquida, o que é medido é o número de partículas beta detectadas em um determinado período de tempo. Como a massa da amostra é conhecida, ela pode ser convertida em uma medida padrão de atividade em unidades de contagens por minuto por grama de carbono (cpm/g C) ou becquerels por kg (Bq/kg C, em unidades SI). Cada dispositivo de medição também é usado para medir a atividade de uma amostra em branco - uma amostra preparada a partir de carbono com idade suficiente para não ter atividade. Isso fornece um valor para a radiação de fundo, que deve ser subtraído da atividade medida da amostra que está sendo datada para obter a atividade atribuível exclusivamente ao 14
</sub C. Além disso, é medida uma amostra com uma atividade padrão, para fornecer uma linha de base para comparação.
Espectrometria de massa do acelerador
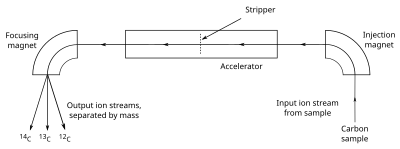
AMS conta os átomos de 14
C e 12
C em uma determinada amostra, determinando o 14
C/12
C diretamente. A amostra, muitas vezes na forma de grafite, é feita para emitir íons C− (átomos de carbono com uma única carga negativa), que são injetados em um acelerador. Os íons são acelerados e passam por um stripper, que remove vários elétrons para que os íons emerjam com carga positiva. Os íons, que podem ter de 1 a 4 cargas positivas (C+ a C4+), dependendo do projeto do acelerador, são então passados através de um ímã que curva sua caminho; os íons mais pesados são menos curvados que os mais leves, de modo que os diferentes isótopos emergem como fluxos separados de íons. Um detector de partículas então registra o número de íons detectados no 14
Fluxo C, mas desde o volume de 12
C (e 13
C, necessário para calibração) é muito grande para detecção de íons individuais, as contagens são determinadas medindo a corrente elétrica criada em um copo de Faraday. A grande carga positiva induzida pelo removedor força moléculas como 13
CH, que tem um peso próximo o suficiente de 14
C para interferir nas medições, para dissociar, para que não sejam detectadas. A maioria das máquinas AMS também mede o δ13C da amostra, para uso no cálculo da amostra' era do radiocarbono. O uso de AMS, em oposição a formas mais simples de espectrometria de massa, é necessário devido à necessidade de distinguir os isótopos de carbono de outros átomos ou moléculas com massa muito próxima, como 14
<sub style="font-size:inherit;line-height:inherit;vertical-align:baseline" N e 13
CH. Tal como acontece com a contagem beta, são utilizadas amostras em branco e amostras padrão. Dois tipos diferentes de branco podem ser medidos: uma amostra de carbono morto que não sofreu nenhum processamento químico, para detectar qualquer fundo de máquina, e uma amostra conhecida como branco de processo feito de carbono morto que é processado no material alvo exatamente da mesma maneira. como a amostra que está sendo datada. Qualquer 14
C sinal do espaço em branco de fundo da máquina provavelmente será causado por feixes de íons que não seguiram o caminho esperado dentro o detector ou por hidretos de carbono, como 12
CH
2 ou 13
CH. Um 14
C sinal do branco do processo mede a quantidade de contaminação introduzida durante a preparação da amostra. Essas medidas são utilizadas no cálculo subsequente da idade da amostra.
Cálculos
Os cálculos a serem realizados nas medições realizadas dependem da tecnologia utilizada, uma vez que os contadores beta medem a radioatividade da amostra enquanto o AMS determina a proporção dos três diferentes isótopos de carbono na amostra.
Para determinar a idade de uma amostra cuja atividade foi medida por contagem beta, a razão entre sua atividade e a atividade do padrão deve ser encontrada. Para determinar isso, uma amostra em branco (de carbono antigo ou morto) é medida e uma amostra de atividade conhecida é medida. As amostras adicionais permitem que erros como radiação de fundo e erros sistemáticos na configuração do laboratório sejam detectados e corrigidos. O material de amostra padrão mais comum é o ácido oxálico, como o padrão HOxII, do qual 1.000 lb (450 kg) foi preparado pelo Instituto Nacional de Padrões e Tecnologia (NIST) em 1977 a partir de colheitas de beterraba francesa.
Os resultados dos testes AMS estão na forma de proporções de 12
C, 13
C e 14
C, que são usados para calcular Fm, a "fração moderna". Isso é definido como a proporção entre 14
C/12
Razão C na amostra e 14
C/ 12
razão C no carbono moderno, que por sua vez é definida como a 14
C/12
C razão que teria sido medida em 1950 se não houvesse efeito dos combustíveis fósseis.
Tanto a contagem beta quanto os resultados do AMS devem ser corrigidos para fracionamento. Isso é necessário porque materiais diferentes da mesma idade, que devido ao fracionamento têm 14
C/12
C, parecerão ter idades diferentes porque o 14
C/12
A proporção C é considerada o indicador de idade. Para evitar isso, todas as medições de radiocarbono são convertidas para a medição que teria sido observada se a amostra fosse feita de madeira, que possui um δ13
Valor C de −25‰.
Uma vez corrigido o 14
C/12
C é conhecida, uma "era do radiocarbono" é calculado usando:
Idade= = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = = =- Sim. - Sim. I (F m))) 8033anos{displaystyle {text{Age}}=-ln({text{Fm}})cdot 8033{text{ years}}}
O cálculo usa 8.033 anos, a vida média derivada da meia-vida de Libby de 5.568 anos, e não 8.267 anos, a vida média derivada do valor moderno mais preciso de 5.730 anos. O valor de Libby para a meia-vida é usado para manter a consistência com os primeiros resultados dos testes de radiocarbono; as curvas de calibração incluem uma correção para isso, garantindo assim a precisão das idades finais do calendário relatadas.
Erros e confiabilidade
A confiabilidade dos resultados pode ser melhorada aumentando o tempo de teste. Por exemplo, se a contagem dos decaimentos beta durante 250 minutos for suficiente para dar um erro de ± 80 anos, com 68% de confiança, então duplicar o tempo de contagem para 500 minutos permitirá uma amostra com apenas metade 14
C a ser medido com o mesmo prazo de erro de 80 anos.
A datação por radiocarbono geralmente é limitada à datação de amostras com menos de 50.000 anos de idade, já que amostras mais antigas têm 14
C ser mensurável. Datas mais antigas foram obtidas usando técnicas especiais de preparação de amostras, amostras grandes e tempos de medição muito longos. Estas técnicas podem permitir a medição de datas até 60.000 e, em alguns casos, até 75.000 anos antes do presente.
As datas de radiocarbono são geralmente apresentadas com um intervalo de um desvio padrão (geralmente representado pela letra grega sigma como 1σ) em cada lado da média. No entanto, um intervalo de datas de 1σ representa apenas um nível de confiança de 68%, portanto a verdadeira idade do objeto que está sendo medido pode estar fora do intervalo de datas citado. Isto foi demonstrado em 1970 por uma experiência realizada pelo laboratório de radiocarbono do Museu Britânico, na qual foram feitas medições semanais na mesma amostra durante seis meses. Os resultados variaram amplamente (embora consistentemente com uma distribuição normal de erros nas medições) e incluíram vários intervalos de datas (de confiança 1σ) que não se sobrepunham. As medições incluíram uma com intervalo de cerca de 4.250 a cerca de 4.390 anos atrás, e outra com intervalo de cerca de 4.520 a cerca de 4.690 anos.
Erros no procedimento também podem levar a erros nos resultados. Se 1% do benzeno numa amostra de referência moderna evaporar acidentalmente, a contagem de cintilação dará uma idade de radiocarbono que é demasiado jovem por volta dos 80 anos.
Calibração

Os cálculos fornecidos acima produzem datas em anos de radiocarbono: ou seja, datas que representam a idade que a amostra teria se 14
C /12
A proporção C tem sido constante historicamente. Embora Libby tivesse apontado já em 1955 a possibilidade de que esta suposição estivesse incorreta, foi só quando as discrepâncias começaram a acumular-se entre as idades medidas e as datas históricas conhecidas dos artefactos que se tornou claro que seria necessário aplicar uma correção às idades do radiocarbono para obter datas do calendário.
Para produzir uma curva que possa ser usada para relacionar anos civis com anos de radiocarbono, é necessária uma sequência de amostras datadas com segurança que possam ser testadas para determinar a sua idade de radiocarbono. O estudo dos anéis das árvores levou à primeira sequência: pedaços individuais de madeira apresentam sequências características de anéis que variam em espessura devido a fatores ambientais, como a quantidade de chuva em um determinado ano. Esses fatores afetam todas as árvores de uma área, portanto, examinar sequências de anéis de árvores de madeira antiga permite a identificação de sequências sobrepostas. Desta forma, uma sequência ininterrupta de anéis de árvores pode ser estendida até muito longe no passado. A primeira sequência publicada, baseada em anéis de pinheiro bristlecone, foi criada por Wesley Ferguson. Hans Suess usou esses dados para publicar a primeira curva de calibração para datação por radiocarbono em 1967. A curva mostrou dois tipos de variação da linha reta: uma flutuação de longo prazo com um período de cerca de 9.000 anos, e uma variação de curto prazo, frequentemente referida como "manobras", com um período de décadas. Suess disse que traçou a linha que mostra as oscilações do "schwung cósmico", com o que ele quis dizer que as variações foram causadas por forças extraterrestres. Durante algum tempo não ficou claro se as manobras eram reais ou não, mas agora estão bem estabelecidas. Estas flutuações de curto prazo na curva de calibração são agora conhecidas como efeitos de Vries, em homenagem a Hessel de Vries.
Uma curva de calibração é usada tomando a data de radiocarbono relatada por um laboratório e lendo essa data no eixo vertical do gráfico. O ponto onde esta linha horizontal cruza a curva dará a idade do calendário da amostra no eixo horizontal. Isto é o inverso da forma como a curva é construída: um ponto no gráfico é derivado de uma amostra de idade conhecida, como um anel de árvore; quando é testado, a idade do radiocarbono resultante fornece um ponto de dados para o gráfico.

Nos trinta anos seguintes, muitas curvas de calibração foram publicadas usando uma variedade de métodos e abordagens estatísticas. Estas foram substituídas pela série de curvas IntCal, começando com IntCal98, publicada em 1998 e atualizada em 2004, 2009, 2013 e 2020. As melhorias nessas curvas são baseadas em novos dados coletados de anéis de árvores, varves, corais, plantas macrofósseis, espeleotemas e foraminíferos. Os dados do IntCal20 incluem curvas separadas para os hemisférios norte e sul, pois diferem sistematicamente devido ao efeito hemisférico. A curva sul (SHCAL20) baseia-se em dados independentes, sempre que possível, e deriva da curva norte, adicionando o deslocamento médio para o hemisfério sul, onde não havia dados diretos disponíveis. Há também uma curva de calibração marítima separada, MARINE20. Para um conjunto de amostras formando uma sequência com uma separação conhecida no tempo, essas amostras formam um subconjunto da curva de calibração. A sequência pode ser comparada com a curva de calibração e a melhor correspondência com a sequência estabelecida. Esta "combinação de manobras" A técnica pode levar a uma datação mais precisa do que é possível com datas individuais por radiocarbono. A correspondência de manobra pode ser usada em locais onde há um platô na curva de calibração e, portanto, pode fornecer uma data muito mais precisa do que os métodos de interceptação ou probabilidade são capazes de produzir. A técnica não se restringe aos anéis das árvores; por exemplo, uma sequência de tefra estratificada na Nova Zelândia, que se acredita ser anterior à colonização humana das ilhas, foi datada de 1314 dC ± 12 anos por correspondência de manobra. As oscilações também significam que a leitura de uma data a partir de uma curva de calibração pode fornecer mais de uma resposta: isso ocorre quando a curva oscila para cima e para baixo o suficiente para que a idade do radiocarbono intercepte a curva em mais de um lugar, o que pode levar a um resultado de radiocarbono sendo relatado como duas faixas etárias distintas, correspondendo às duas partes da curva que a idade do radiocarbono interceptou.
Técnicas estatísticas Bayesianas podem ser aplicadas quando há diversas datas de radiocarbono a serem calibradas. Por exemplo, se uma série de datas de radiocarbono for obtida de diferentes níveis em uma sequência estratigráfica, a análise Bayesiana pode ser usada para avaliar datas que são discrepantes e pode calcular distribuições de probabilidade melhoradas, com base na informação prévia de que a sequência deve ser ordenada no tempo.. Quando a análise bayesiana foi introduzida, seu uso era limitado pela necessidade de utilização de computadores mainframe para realizar os cálculos, mas a técnica já foi implementada em programas disponíveis para computadores pessoais, como o OxCal.
Datas dos relatórios
Vários formatos para citar resultados de radiocarbono foram usados desde a datação das primeiras amostras. A partir de 2019, o formato padrão exigido pela revista Radiocarbon é o seguinte.
As datas não calibradas devem ser relatadas como "laboratório: C14({}14C}}} ano ± gama BP", onde:
- laboratório identifica o laboratório que testou a amostra e o ID da amostra
- C14({}14C}}} ano é a determinação do laboratório da idade da amostra, em anos de radiocarbono
- gama é a estimativa laboratorial do erro na idade, a 1σ confiança.
- "BP" significa "antes do presente", referindo-se a uma data de referência de 1950, de modo que "500 BP" significa o ano de AD 1450.
Por exemplo, a data não calibrada "UtC-2020: 3510 ± 60 BP" indica que a amostra foi testada pelo Utrecht van der Graaff Laboratorium ("UtC"), onde tem um número de amostra de "2020", e que a idade não calibrada é 3510 anos antes do presente, ± 60 anos. Às vezes, são usados formulários relacionados: por exemplo, "2,3 ka BP" significa 2.300 anos de radiocarbono antes do presente (ou seja, 350 aC), e "14
C ano BP" pode ser usado para distinguir a data não calibrada de uma data derivada de outro método de datação, como a termoluminescência.
Calibrado 14
C datas são frequentemente relatadas como "cal BP", "cal BC& #34;, ou "cal AD", novamente com 'BP' referindo-se ao ano de 1950 como a data zero. Radiocarbon oferece duas opções para relatar datas calibradas. Um formato comum é "cal intervalo de datas confiança", onde:
- data limite é a gama de datas correspondentes ao nível de confiança dado
- confiança indica o nível de confiança para a faixa de data dada.
Por exemplo, "cal 1220–1281 DC (1σ)" significa uma data calibrada para a qual a data verdadeira está entre 1220 DC e 1281 DC, com um nível de confiança de '1 sigma', ou aproximadamente 68%. As datas calibradas também podem ser expressas como "BP" em vez de usar "BC" e "AD". A curva utilizada para calibrar os resultados deve ser a última curva IntCal disponível. As datas de calibração também devem identificar quaisquer programas, como o OxCal, usados para realizar a calibração. Além disso, um artigo na Radiocarbon em 2014 sobre convenções de relatórios de datas de radiocarbono recomenda que informações sejam fornecidas sobre o tratamento da amostra, incluindo o material da amostra, métodos de pré-tratamento e medições de controle de qualidade; que a citação do software utilizado para calibração deve especificar o número da versão e quaisquer opções ou modelos utilizados; e que a data calibrada deve ser fornecida com as probabilidades associadas para cada faixa.
Uso em arqueologia
Interpretação
Um conceito-chave na interpretação de datas de radiocarbono é a associação arqueológica: qual é a verdadeira relação entre dois ou mais objetos num sítio arqueológico? Acontece frequentemente que uma amostra para datação por radiocarbono pode ser retirada diretamente do objeto de interesse, mas também há muitos casos em que isso não é possível. Os bens funerários de metal, por exemplo, não podem ser datados por radiocarbono, mas podem ser encontrados numa sepultura com um caixão, carvão ou outro material que se possa presumir ter sido depositado ao mesmo tempo. Nestes casos, a data do caixão ou do carvão é indicativa da data de deposição dos bens funerários, devido à relação funcional direta entre os dois. Há também casos em que não há relação funcional, mas a associação é razoavelmente forte: por exemplo, uma camada de carvão numa lixeira fornece uma data que tem uma relação com a lixeira.
A contaminação é particularmente preocupante na datação de materiais muito antigos obtidos em escavações arqueológicas e é necessário muito cuidado na seleção e preparação dos espécimes. Em 2014, Thomas Higham e colaboradores sugeriram que muitas das datas publicadas para os artefactos de Neandertal são demasiado recentes devido à contaminação por “carbono jovem”.
À medida que uma árvore cresce, apenas o anel mais externo da árvore troca carbono com o seu ambiente, portanto a idade medida para uma amostra de madeira depende de onde a amostra é retirada. Isto significa que as datas de radiocarbono nas amostras de madeira podem ser anteriores à data em que a árvore foi derrubada. Além disso, se um pedaço de madeira for utilizado para múltiplos fins, pode haver um atraso significativo entre o corte da árvore e a utilização final no contexto em que se encontra. Isso costuma ser chamado de problema da madeira velha. Um exemplo é a trilha da Idade do Bronze em Withy Bed Copse, na Inglaterra; a pista foi construída com madeira que claramente foi trabalhada para outros fins antes de ser reutilizada na pista. Outro exemplo é a madeira flutuante, que pode ser usada como material de construção. Nem sempre é possível reconhecer a reutilização. Outros materiais podem apresentar o mesmo problema: por exemplo, sabe-se que o betume foi utilizado por algumas comunidades neolíticas para impermeabilizar cestos; a idade de radiocarbono do betume será maior do que a mensurável pelo laboratório, independentemente da idade real do contexto, portanto, testar o material da cesta fornecerá uma idade enganosa se não for tomado cuidado. Uma questão separada, relacionada à reutilização, é a do uso prolongado ou da deposição retardada. Por exemplo, um objecto de madeira que permaneça em uso durante um longo período terá uma idade aparente superior à idade real do contexto em que está depositado.
Use fora da arqueologia
A arqueologia não é o único campo que faz uso da datação por radiocarbono. As datas de radiocarbono também podem ser usadas em geologia, sedimentologia e estudos de lagos, por exemplo. A capacidade de datar amostras minúsculas usando AMS significa que os paleobotânicos e paleoclimatologistas podem usar a datação por radiocarbono diretamente no pólen purificado a partir de sequências de sedimentos ou em pequenas quantidades de material vegetal ou carvão. As datas de material orgânico recuperado de estratos de interesse podem ser usadas para correlacionar estratos em diferentes locais que parecem ser semelhantes em termos geológicos. A datação do material de um local fornece informações de data sobre o outro local, e as datas também são usadas para colocar estratos na linha do tempo geológica geral.
O radiocarbono também é utilizado para datar o carbono libertado pelos ecossistemas, particularmente para monitorizar a libertação de carbono antigo que foi previamente armazenado nos solos como resultado de perturbações humanas ou alterações climáticas. Avanços recentes nas técnicas de coleta de campo também permitem a datação por radiocarbono do metano e do dióxido de carbono, que são importantes gases de efeito estufa.
Aplicativos notáveis
Limite Pleistoceno/Holoceno na Floresta Fóssil de Two Creeks
O Pleistoceno é uma época geológica que começou há cerca de 2,6 milhões de anos. O Holoceno, a época geológica atual, começa há cerca de 11.700 anos, quando termina o Pleistoceno. Estabelecer a data desta fronteira – que é definida pelo forte aquecimento climático – com a maior precisão possível tem sido um objectivo dos geólogos durante grande parte do século XX. Em Two Creeks, em Wisconsin, uma floresta fóssil foi descoberta (Two Creeks Buried Forest State Natural Area), e pesquisas subsequentes determinaram que a destruição da floresta foi causada pelo avanço do gelo de Valders, o último movimento de gelo para o sul antes do final de o Pleistoceno naquela área. Antes do advento da datação por radiocarbono, as árvores fossilizadas foram datadas correlacionando sequências de camadas de sedimentos depositadas anualmente em Two Creeks com sequências na Escandinávia. Isto levou a estimativas de que as árvores tinham entre 24.000 e 19.000 anos de idade e, portanto, esta foi considerada a data do último avanço da glaciação de Wisconsin antes do seu recuo final marcar o fim do Pleistoceno na América do Norte. Em 1952, Libby publicou datas de radiocarbono para várias amostras do local de Two Creeks e de dois locais semelhantes próximos; a média das datas foi de 11.404 AP com um erro padrão de 350 anos. Este resultado não foi calibrado, pois a necessidade de calibração das idades do radiocarbono ainda não foi compreendida. Outros resultados durante a próxima década apoiaram uma data média de 11.350 AP, com os resultados considerados os mais precisos em média 11.600 AP. Houve resistência inicial a estes resultados por parte de Ernst Antevs, o paleobotânico que trabalhou na série varve escandinava, mas as suas objecções foram eventualmente desconsideradas por outros geólogos. Na década de 1990, amostras foram testadas com AMS, produzindo datas (não calibradas) variando de 11.640 AP a 11.800 AP, ambas com erro padrão de 160 anos. Posteriormente, uma amostra da floresta fóssil foi utilizada em um teste interlaboratorial, com resultados fornecidos por mais de 70 laboratórios. Esses testes produziram uma idade média de 11.788 ± 8 BP (confiança 2σ) que, quando calibrada, fornece um intervalo de datas de 13.730 a 13.550 cal BP. As datas de radiocarbono de Two Creeks são agora consideradas um resultado chave no desenvolvimento da compreensão moderna da glaciação norte-americana no final do Pleistoceno.
Manuscritos do Mar Morto

Em 1947, foram descobertos pergaminhos em cavernas perto do Mar Morto que continham escritos em hebraico e aramaico, muitos dos quais se acredita terem sido produzidos pelos essênios, uma pequena seita judaica. Esses pergaminhos são de grande importância no estudo dos textos bíblicos porque muitos deles contêm a versão mais antiga conhecida dos livros da Bíblia hebraica. Uma amostra do envoltório de linho de um desses pergaminhos, o Grande Rolo de Isaías, foi incluída em uma análise de 1955 por Libby, com uma idade estimada de 1.917 ± 200 anos. Com base numa análise do estilo de escrita, foram feitas estimativas paleográficas da idade de 21 anos dos pergaminhos, e amostras da maioria destes, juntamente com outros pergaminhos que não tinham sido datados paleograficamente, foram testadas por dois laboratórios da AMS na década de 1990. Os resultados variaram em idade desde o início do século 4 aC até meados do século 4 dC. Em todos os casos, exceto em dois, os pergaminhos foram determinados como estando dentro de 100 anos da idade paleograficamente determinada. O pergaminho de Isaías foi incluído no teste e descobriu-se que tinha dois intervalos de datas possíveis com um nível de confiança de 2σ, devido ao formato da curva de calibração naquele ponto: há 15% de chance de que ele date de 355 a 295 a.C., e uma chance de 84% de datar de 210 a 45 AC. Posteriormente, essas datas foram criticadas com base no fato de que, antes de os pergaminhos serem testados, eles haviam sido tratados com óleo de rícino moderno para facilitar a leitura da escrita; argumentou-se que a falta de remoção suficiente do óleo de mamona teria feito com que as tâmaras fossem muito jovens. Vários artigos foram publicados apoiando e se opondo às críticas.
Impacto
Logo após a publicação do artigo de Libby de 1949 na Science, universidades de todo o mundo começaram a estabelecer laboratórios de datação por radiocarbono e, no final da década de 1950, havia mais de 20 laboratórios
ativos. span class="chemf nowrap">14
C laboratórios de pesquisa. Rapidamente se tornou evidente que os princípios da datação por radiocarbono eram válidos, apesar de certas discrepâncias, cujas causas permaneciam então desconhecidas.
O desenvolvimento da datação por radiocarbono teve um impacto profundo na arqueologia – frequentemente descrito como a "revolução do radiocarbono". Nas palavras do antropólogo R. E. Taylor, "14
Dados C criaram um mundo a pré-história é possível ao contribuir com uma escala de tempo que transcende as fronteiras locais, regionais e continentais". Ele fornece uma datação mais precisa dentro dos sítios do que os métodos anteriores, que geralmente derivam da estratigrafia ou de tipologias (por exemplo, de ferramentas de pedra ou cerâmica); também permite comparação e sincronização de eventos em grandes distâncias. O advento da datação por radiocarbono pode até ter levado a melhores métodos de campo em arqueologia, uma vez que um melhor registro de dados leva a uma associação mais firme de objetos com as amostras a serem testadas. Esses métodos de campo aprimorados às vezes eram motivados por tentativas de provar que um 14
C estava incorreta. Taylor também sugere que a disponibilidade de informações sobre datas definidas libertou os arqueólogos da necessidade de concentrar grande parte de sua energia na determinação das datas de suas descobertas e levou a uma expansão das questões que os arqueólogos estavam dispostos a pesquisar. Por exemplo, a partir da década de 1970, questões sobre a evolução do comportamento humano foram vistas com muito mais frequência na arqueologia.
A estrutura de datação fornecida pelo radiocarbono levou a uma mudança na visão predominante de como as inovações se espalharam pela Europa pré-histórica. Os investigadores já pensavam que muitas ideias se espalhavam por difusão através do continente, ou por invasões de povos trazendo consigo novas ideias culturais. À medida que as datações por radiocarbono começaram a provar que estas ideias estavam erradas em muitos casos, tornou-se evidente que estas inovações devem por vezes ter surgido localmente. Isso foi descrito como uma “segunda revolução por radiocarbono” e, com relação à pré-história britânica, o arqueólogo Richard Atkinson caracterizou o impacto da datação por radiocarbono como “radical [...] terapia" para a "doença progressiva do invasorismo". De forma mais ampla, o sucesso da datação por radiocarbono estimulou o interesse em abordagens analíticas e estatísticas de dados arqueológicos. Taylor também descreveu o impacto do AMS e a capacidade de obter medições precisas a partir de amostras muito pequenas, como o início de uma terceira revolução do radiocarbono.
Ocasionalmente, técnicas de datação por radiocarbono datam um objeto de interesse popular, por exemplo, o Sudário de Turim, um pedaço de pano de linho que alguns acreditam conter uma imagem de Jesus Cristo após sua crucificação. Três laboratórios separados dataram amostras de linho do Sudário em 1988; os resultados apontaram para origens do século XIV, levantando dúvidas sobre a autenticidade do sudário como uma suposta relíquia do século I.
Os pesquisadores estudaram outros isótopos criados por raios cósmicos para determinar se eles também poderiam ser usados para auxiliar na datação de objetos de interesse arqueológico; tais isótopos incluem 3He, 10Be, 21Ne, 26Al e 36Cl. Com o desenvolvimento do AMS na década de 1980, tornou-se possível medir estes isótopos com precisão suficiente para que constituíssem a base de técnicas úteis de datação, que foram aplicadas principalmente à datação de rochas. Isótopos radioativos de ocorrência natural também podem formar a base de métodos de datação, como na datação por potássio-argônio, datação argônio-argônio e datação em série de urânio. Outras técnicas de datação de interesse para os arqueólogos incluem termoluminescência, luminescência opticamente estimulada, ressonância de spin de elétrons e datação por traços de fissão, bem como técnicas que dependem de faixas ou camadas anuais, como dendrocronologia, tefrocronologia e cronologia varva.
Contenido relacionado
Frequência fundamental
Fusão a frio
Célula eletroquímica
Partícula elementar
Pressão osmótica




