Colesterol
Colesterol é qualquer um de uma classe de certas moléculas orgânicas chamadas lipídios. É um esterol (ou esteróide modificado), um tipo de lipídio. O colesterol é biossintetizado por todas as células animais e é um componente estrutural essencial das membranas celulares animais. Quando isolado quimicamente, é um sólido cristalino amarelado.
O colesterol também serve como um precursor para a biossíntese de hormônios esteróides, ácidos biliares e vitamina D. O colesterol é o principal esterol sintetizado por todos os animais. Nos vertebrados, as células hepáticas normalmente produzem as maiores quantidades. Está ausente entre os procariontes (bactérias e archaea), embora existam algumas exceções, como Mycoplasma, que requerem colesterol para crescer.
François Poulletier de la Salle identificou pela primeira vez o colesterol na forma sólida em cálculos biliares em 1769. No entanto, foi somente em 1815 que o químico Michel Eugène Chevreul chamou o composto de "colesterina".
Etimologia
A palavra colesterol vem do grego antigo chole- 'bile' e estereos 'sólido', seguido pelo sufixo químico -ol para um álcool.
Fisiologia
O colesterol é essencial para toda a vida animal, com cada célula capaz de sintetizá-lo por meio de um complexo processo de 37 etapas. Isso começa com a via do mevalonato ou HMG-CoA redutase, o alvo das estatinas, que abrange as primeiras 18 etapas. Isso é seguido por 19 etapas adicionais para converter o lanosterol resultante em colesterol.
Um homem humano pesando 68 kg (150 lb) normalmente sintetiza cerca de 1 grama (1.000 mg) de colesterol por dia, e seu corpo contém cerca de 35 g, principalmente contido nas membranas celulares. A ingestão dietética diária típica de colesterol para um homem nos Estados Unidos é de 307 mg.
A maior parte do colesterol ingerido é esterificado, o que faz com que seja mal absorvido pelo intestino. O corpo também compensa a absorção do colesterol ingerido reduzindo sua própria síntese de colesterol. Por essas razões, o colesterol nos alimentos, sete a dez horas após a ingestão, tem pouco ou nenhum efeito sobre as concentrações de colesterol no sangue. Porém, durante as primeiras sete horas após a ingestão do colesterol, à medida que as gorduras absorvidas vão sendo distribuídas pelo corpo na água extracelular pelas diversas lipoproteínas (que transportam todas as gorduras da água para fora das células), as concentrações aumentam.
As plantas produzem colesterol em quantidades muito pequenas. Em maiores quantidades, eles produzem fitoesteróis, substâncias quimicamente semelhantes que podem competir com o colesterol pela reabsorção no trato intestinal, reduzindo potencialmente a reabsorção do colesterol. Quando as células do revestimento intestinal absorvem os fitoesteróis, no lugar do colesterol, elas geralmente excretam as moléculas de fitoesteróis de volta ao trato gastrointestinal, um importante mecanismo de proteção. A ingestão de fitoesteróis de ocorrência natural, que abrange esteróis e estanóis vegetais, varia entre ≈200–300 mg/dia, dependendo dos hábitos alimentares. Dietas experimentais vegetarianas especialmente projetadas foram produzidas produzindo mais de 700 mg/dia.
Função
Membranas
O colesterol compõe cerca de 30% de todas as membranas celulares animais. É necessário para construir e manter as membranas e modular a fluidez da membrana na faixa de temperaturas fisiológicas. O grupo hidroxila de cada molécula de colesterol interage com as moléculas de água ao redor da membrana, assim como as cabeças polares dos fosfolipídios e esfingolipídios da membrana, enquanto o esteróide volumoso e a cadeia de hidrocarbonetos estão embutidos na membrana, ao lado da cadeia apolar de ácidos graxos do colesterol. outros lipídios. Por meio da interação com as cadeias de ácidos graxos fosfolipídicos, o colesterol aumenta o empacotamento da membrana, o que altera a fluidez da membrana e mantém a integridade da membrana, de modo que as células animais não precisam construir paredes celulares (como as plantas e a maioria das bactérias). A membrana permanece estável e durável sem ser rígida, permitindo que as células animais mudem de forma e os animais se movam.
A estrutura do anel tetracíclico do colesterol contribui para a fluidez da membrana celular, pois a molécula está em uma conformação trans, tornando toda a cadeia lateral do colesterol rígida e plana. Nesse papel estrutural, o colesterol também reduz a permeabilidade da membrana plasmática a solutos neutros, íons de hidrogênio e íons de sódio.
Apresentação do substrato
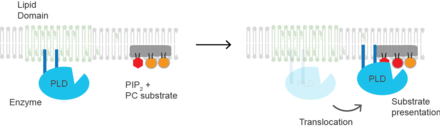
O colesterol regula o processo biológico de apresentação de substratos e as enzimas que utilizam a apresentação de substratos como mecanismo de sua ativação. (PLD2) é um exemplo bem definido de uma enzima ativada pela apresentação do substrato. A enzima é palmitoilada, fazendo com que a enzima trafegue para domínios lipídicos dependentes de colesterol, às vezes chamados de "jangadas lipídicas". O substrato da fosfolipase D é a fosfatidilcolina (PC) que é insaturada e de baixa abundância nas jangadas lipídicas. O PC localiza-se na região desordenada da célula junto com o lipídio poliinsaturado fosfatidilinositol 4,5-bifosfato (PIP2). PLD2 tem um domínio de ligação PIP2. Quando a concentração de PIP2 na membrana aumenta, o PLD2 deixa os domínios dependentes de colesterol e se liga ao PIP2, onde obtém acesso ao seu substrato PC e inicia a catálise com base na apresentação do substrato.
Sinalização
O colesterol também está envolvido em processos de sinalização celular, auxiliando na formação de jangadas lipídicas na membrana plasmática, que aproximam proteínas receptoras com altas concentrações de moléculas de segundo mensageiro. Em múltiplas camadas, o colesterol e os fosfolipídios, ambos isolantes elétricos, podem facilitar a velocidade de transmissão de impulsos elétricos ao longo do tecido nervoso. Para muitas fibras neuronais, uma bainha de mielina, rica em colesterol por ser derivada de camadas compactadas de células de Schwann ou membranas de oligodendrócitos, fornece isolamento para uma condução de impulsos mais eficiente. Acredita-se que a desmielinização (perda de mielina) seja parte da base da esclerose múltipla.
O colesterol se liga e afeta o controle de vários canais iônicos, como o receptor nicotínico de acetilcolina, o receptor GABAA e o retificador interno do canal de potássio. O colesterol também ativa o receptor alfa relacionado ao estrogênio (ERRα) e pode ser o ligante endógeno para o receptor. A natureza constitutivamente ativa do receptor pode ser explicada pelo fato de que o colesterol é onipresente no corpo. A inibição da sinalização ERRα pela redução da produção de colesterol foi identificada como um mediador chave dos efeitos das estatinas e dos bisfosfonatos nos ossos, músculos e macrófagos. Com base nesses achados, foi sugerido que o ERRα deveria ser desorfanizado e classificado como um receptor de colesterol.
Precursor químico
Dentro das células, o colesterol também é uma molécula precursora de várias vias bioquímicas. Por exemplo, é a molécula precursora para a síntese da vitamina D no metabolismo do cálcio e de todos os hormônios esteróides, incluindo os hormônios da glândula adrenal cortisol e aldosterona, bem como os hormônios sexuais progesterona, estrogênio e testosterona e seus derivados.
Epiderme
O estrato córneo é a camada mais externa da epiderme. É composto de corneócitos terminalmente diferenciados e enucleados que residem dentro de uma matriz lipídica, como "tijolos e argamassa." Juntamente com as ceramidas e os ácidos graxos livres, o colesterol forma a argamassa lipídica, uma barreira impermeável à água que evita a perda de água por evaporação. Como regra geral, a matriz lipídica epidérmica é composta por uma mistura equimolar de ceramidas (~50% em peso), colesterol (~25% em peso) e ácidos graxos livres (~15% em peso), com menor quantidades de outros lípidos também estão presentes. O sulfato de colesterol atinge sua maior concentração na camada granular da epiderme. O esteroide sulfato sulfatase então diminui sua concentração no estrato córneo, a camada mais externa da epiderme. A abundância relativa de sulfato de colesterol na epiderme varia em diferentes locais do corpo, com o calcanhar do pé apresentando a menor concentração.
Metabolismo
O colesterol é reciclado no corpo. O fígado excreta colesterol em fluidos biliares, que são então armazenados na vesícula biliar, que os excreta em uma forma não esterificada (via bile) no trato digestivo. Normalmente, cerca de 50% do colesterol excretado é reabsorvido pelo intestino delgado de volta à corrente sanguínea.
Biossíntese e regulação
Biossíntese
Todas as células animais (existem exceções nos invertebrados) fabricam colesterol, tanto para estrutura de membrana quanto para outros usos, com taxas de produção relativas variando de acordo com o tipo de célula e a função do órgão. Cerca de 80% da produção diária total de colesterol ocorre no fígado e nos intestinos; outros locais de taxas de síntese mais altas incluem o cérebro, as glândulas adrenais e os órgãos reprodutivos.
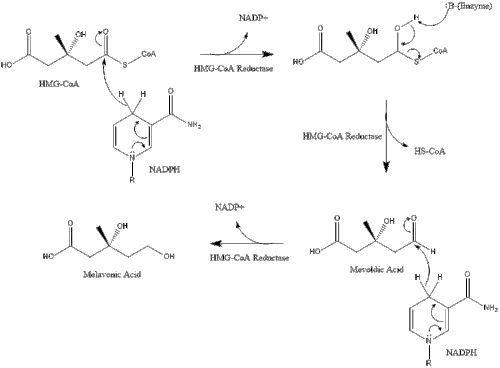
A síntese dentro do corpo começa com a via do mevalonato, onde duas moléculas de acetil CoA se condensam para formar acetoacetil-CoA. Isto é seguido por uma segunda condensação entre acetil CoA e acetoacetil-CoA para formar 3-hidroxi-3-metilglutaril CoA (HMG-CoA).
Esta molécula é então reduzida a mevalonato pela enzima HMG-CoA redutase. A produção de mevalonato é a etapa limitante e irreversível da síntese do colesterol e é o local de ação das estatinas (uma classe de medicamentos para redução do colesterol).
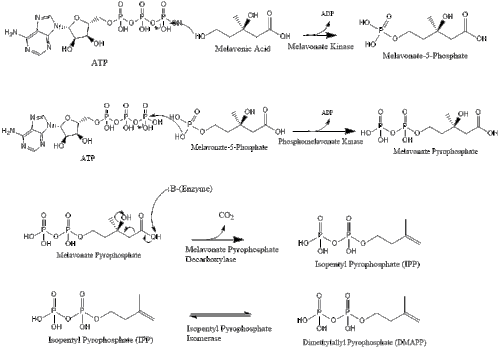
O mevalonato é finalmente convertido em isopentenil pirofosfato (IPP) através de duas etapas de fosforilação e uma etapa de descarboxilação que requer ATP.
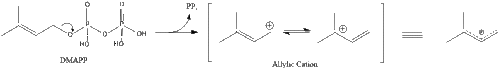
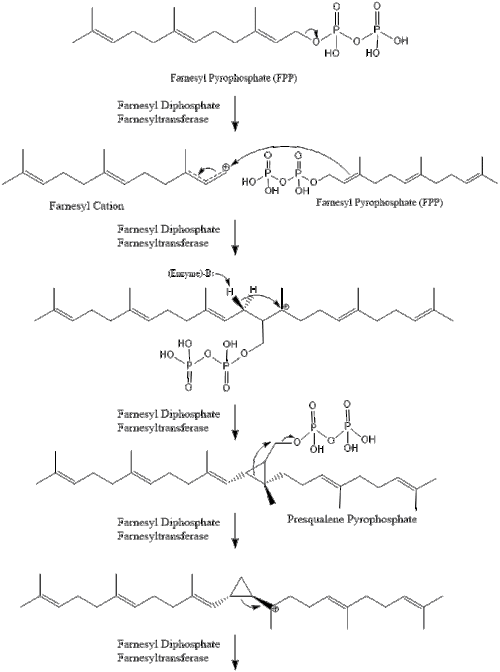
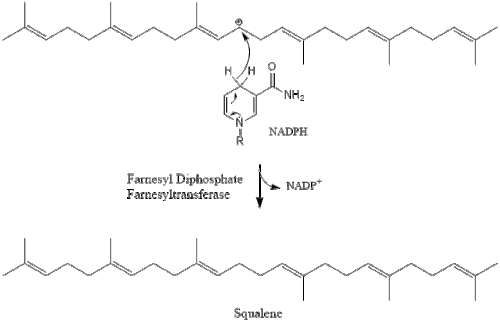
Três moléculas de isopentenil pirofosfato condensam-se para formar farnesil pirofosfato através da ação da geranil transferase.
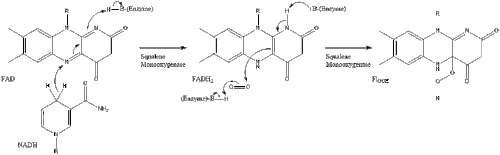
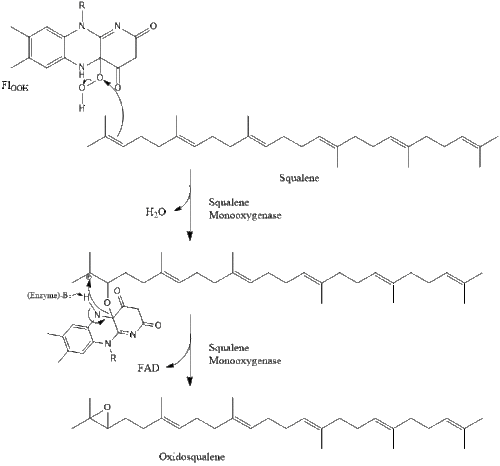
Duas moléculas de farnesil pirofosfato então se condensam para formar o esqualeno pela ação da esqualeno sintase no retículo endoplasmático.
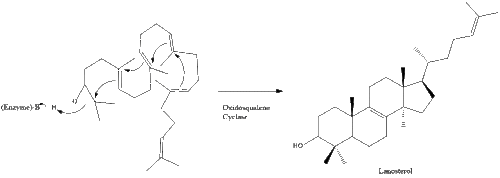
A oxidosqualeno ciclase então cicliza o esqualeno para formar o lanosterol.
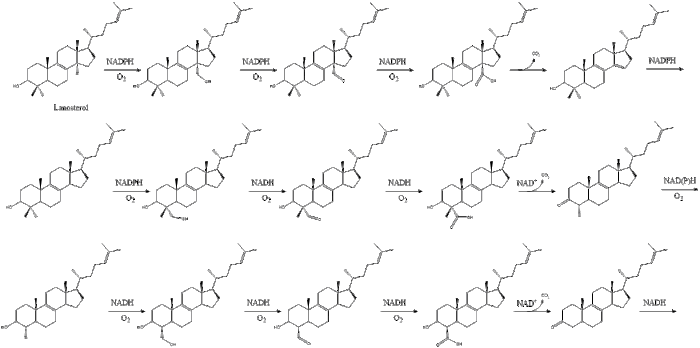
Finalmente, o lanosterol é convertido em colesterol por meio de uma das duas vias, a via de Bloch ou a via de Kandutsch-Russell. As 19 etapas finais do colesterol contêm NADPH e oxigênio para ajudar a oxidar grupos metil para remoção de carbonos, mutases para mover grupos alcenos e NADH para ajudar a reduzir cetonas.
Konrad Bloch e Feodor Lynen dividiram o Prêmio Nobel de Fisiologia ou Medicina em 1964 por suas descobertas sobre alguns dos mecanismos e métodos de regulação do colesterol e do metabolismo dos ácidos graxos.
Regulação da síntese de colesterol
A biossíntese do colesterol é diretamente regulada pelos níveis de colesterol presentes, embora os mecanismos homeostáticos envolvidos sejam apenas parcialmente compreendidos. Uma maior ingestão de alimentos leva a uma diminuição líquida na produção endógena, enquanto uma menor ingestão de alimentos tem o efeito oposto. O principal mecanismo regulatório é a detecção do colesterol intracelular no retículo endoplasmático pela proteína SREBP (proteína 1 e 2 de ligação do elemento regulatório do esterol). Na presença de colesterol, o SREBP liga-se a duas outras proteínas: SCAP (proteína ativadora de clivagem do SREBP) e INSIG-1. Quando os níveis de colesterol caem, o INSIG-1 se dissocia do complexo SREBP-SCAP, o que permite que o complexo migre para o aparelho de Golgi. Aqui SREBP é clivado por S1P e S2P (site-1 protease e site-2 protease), duas enzimas que são ativadas por SCAP quando os níveis de colesterol estão baixos.
O SREBP clivado então migra para o núcleo e atua como um fator de transcrição para se ligar ao elemento regulador de esteróis (SRE), que estimula a transcrição de muitos genes. Entre eles estão o receptor de lipoproteína de baixa densidade (LDL) e a HMG-CoA redutase. O receptor de LDL elimina o LDL circulante da corrente sanguínea, enquanto a HMG-CoA redutase leva a um aumento na produção endógena de colesterol. Grande parte dessa via de sinalização foi esclarecida pelo Dr. Michael S. Brown e pelo Dr. Joseph L. Goldstein na década de 1970. Em 1985, eles receberam o Prêmio Nobel de Fisiologia ou Medicina por seu trabalho. Seu trabalho subsequente mostra como a via SREBP regula a expressão de muitos genes que controlam a formação e o metabolismo de lipídios e a alocação de combustível corporal.
A síntese de colesterol também pode ser desativada quando os níveis de colesterol estão altos. A HMG-CoA redutase contém um domínio citosólico (responsável por sua função catalítica) e um domínio de membrana. O domínio da membrana detecta sinais para sua degradação. Concentrações crescentes de colesterol (e outros esteróis) causam uma alteração no estado de oligomerização desse domínio, o que o torna mais suscetível à destruição pelo proteassoma. A atividade dessa enzima também pode ser reduzida pela fosforilação por uma proteína quinase ativada por AMP. Como essa quinase é ativada pelo AMP, que é produzido quando o ATP é hidrolisado, segue-se que a síntese de colesterol é interrompida quando os níveis de ATP estão baixos.
Transporte de plasma e regulação da absorção
Como uma molécula isolada, o colesterol é apenas minimamente solúvel em água ou hidrofílico. Por causa disso, ele se dissolve no sangue em concentrações extremamente pequenas. Para ser transportado de forma eficaz, o colesterol é embalado em lipoproteínas, partículas discóides complexas com proteínas anfifílicas externas e lipídios, cujas superfícies voltadas para fora são solúveis em água e as superfícies voltadas para dentro são solúveis em lipídios. Isso permite que ele viaje pelo sangue por meio de emulsificação. O colesterol não ligado, sendo anfipático, é transportado na superfície monocamada da partícula de lipoproteína junto com fosfolipídios e proteínas. Os ésteres de colesterol ligados a ácidos graxos, por outro lado, são transportados dentro do núcleo gorduroso hidrofóbico da lipoproteína, juntamente com os triglicerídeos.
Existem vários tipos de lipoproteínas no sangue. Em ordem crescente de densidade, eles são quilomícrons, lipoproteína de densidade muito baixa (VLDL), lipoproteína de densidade intermediária (IDL), lipoproteína de baixa densidade (LDL) e lipoproteína de alta densidade (HDL). Proporções de proteína/lipídeo mais baixas resultam em lipoproteínas menos densas. O colesterol dentro de diferentes lipoproteínas é idêntico, embora alguns sejam transportados como seu nativo "livre" álcool (o grupo colesterol-OH voltado para a água que envolve as partículas), enquanto outros como ésteres de ácidos graxos, também conhecidos como ésteres de colesterol, dentro das partículas.
As partículas de lipoproteínas são organizadas por apolipoproteínas complexas, tipicamente 80 a 100 proteínas diferentes por partícula, que podem ser reconhecidas e ligadas por receptores específicos nas membranas celulares, direcionando sua carga lipídica para células e tecidos específicos que atualmente ingerem essas partículas de transporte de gordura. Esses receptores de superfície servem como assinaturas moleculares únicas, que ajudam a determinar a entrega da distribuição de gordura por todo o corpo.
Os quilomícrons, as moléculas de transporte de colesterol menos densas, contêm apolipoproteína B-48, apolipoproteína C e apolipoproteína E (o principal transportador de colesterol no cérebro) em suas conchas. Os quilomícrons transportam gorduras do intestino para os músculos e outros tecidos que precisam de ácidos graxos para produção de energia ou gordura. O colesterol não utilizado permanece em mais remanescentes de quilomícrons ricos em colesterol e levado daqui para a corrente sanguínea pelo fígado.
As moléculas de VLDL são produzidas pelo fígado a partir de triacilglicerol e colesterol que não foram utilizados na síntese de ácidos biliares. Essas moléculas contêm apolipoproteína B100 e apolipoproteína E em suas cascas e podem ser degradadas pela lipoproteína lipase na parede da artéria para IDL. Essa clivagem da parede arterial permite a absorção de triacilglicerol e aumenta a concentração de colesterol circulante. As moléculas de IDL são então consumidas em dois processos: metade é metabolizada pelo HTGL e captada pelo receptor de LDL nas superfícies das células do fígado, enquanto a outra metade continua a perder triacilgliceróis na corrente sanguínea até se tornarem partículas de LDL carregadas de colesterol.
As partículas de LDL são as principais transportadoras de colesterol no sangue. Cada um contém aproximadamente 1.500 moléculas de éster de colesterol. As cascas das moléculas de LDL contêm apenas uma molécula de apolipoproteína B100, reconhecida pelos receptores de LDL nos tecidos periféricos. Após a ligação da apolipoproteína B100, muitos receptores de LDL se concentram em poços revestidos de clatrina. Tanto o LDL quanto seu receptor formam vesículas dentro de uma célula por endocitose. Essas vesículas então se fundem com um lisossomo, onde a enzima lipase ácida lisossômica hidrolisa os ésteres de colesterol. O colesterol pode então ser usado para biossíntese de membrana ou esterificado e armazenado dentro da célula, de modo a não interferir com as membranas celulares.
Os receptores de LDL são consumidos durante a absorção do colesterol, e sua síntese é regulada pela SREBP, a mesma proteína que controla a síntese do colesterol de novo, de acordo com sua presença no interior da célula. Uma célula com colesterol abundante terá sua síntese de receptores de LDL bloqueada, para evitar que o novo colesterol nas moléculas de LDL seja captado. Por outro lado, a síntese do receptor de LDL ocorre quando uma célula é deficiente em colesterol.
Quando esse processo se torna desregulado, moléculas de LDL sem receptores começam a aparecer no sangue. Essas moléculas de LDL são oxidadas e captadas por macrófagos, que se tornam ingurgitadas e formam células espumosas. Essas células espumosas geralmente ficam presas nas paredes dos vasos sanguíneos e contribuem para a formação da placa aterosclerótica. As diferenças na homeostase do colesterol afetam o desenvolvimento da aterosclerose precoce (espessura da camada íntima-média da carótida). Essas placas são as principais causas de ataques cardíacos, derrames e outros problemas médicos graves, levando à associação do chamado colesterol LDL (na verdade, uma lipoproteína) com colesterol "ruim" colesterol.
Acredita-se que as partículas de HDL transportem o colesterol de volta ao fígado, seja para excreção ou para outros tecidos que sintetizam hormônios, em um processo conhecido como transporte reverso do colesterol (RCT). Um grande número de partículas de HDL se correlaciona com melhores resultados de saúde, enquanto um baixo número de partículas de HDL está associado à progressão da doença ateromatosa nas artérias.
Metabolismo, reciclagem e excreção
O colesterol é suscetível à oxidação e forma facilmente derivados oxigenados chamados oxisteróis. Três mecanismos diferentes podem formar estes: autoxidação, oxidação secundária à peroxidação lipídica e oxidação da enzima metabolizadora do colesterol. Um grande interesse nos oxisteróis surgiu quando se demonstrou que eles exerciam ações inibitórias na biossíntese do colesterol. Essa descoberta ficou conhecida como a "hipótese do oxisterol". Papéis adicionais para oxisteróis na fisiologia humana incluem sua participação na biossíntese de ácidos biliares, função como formas de transporte de colesterol e regulação da transcrição de genes.
Em experimentos bioquímicos, formas de colesterol marcadas radioativamente, como o colesterol tritiado, são usadas. Esses derivados sofrem degradação durante o armazenamento e é essencial purificar o colesterol antes do uso. O colesterol pode ser purificado usando pequenas colunas Sephadex LH-20.
O colesterol é oxidado pelo fígado em uma variedade de ácidos biliares. Estes, por sua vez, são conjugados com glicina, taurina, ácido glucurônico ou sulfato. Uma mistura de ácidos biliares conjugados e não conjugados, junto com o próprio colesterol, é excretada do fígado para a bile. Aproximadamente 95% dos ácidos biliares são reabsorvidos no intestino e o restante é perdido nas fezes. A excreção e reabsorção de ácidos biliares forma a base da circulação entero-hepática, que é essencial para a digestão e absorção de gorduras dietéticas. Em certas circunstâncias, quando mais concentrado, como na vesícula biliar, o colesterol cristaliza e é o principal constituinte da maioria dos cálculos biliares (cálculos de lecitina e bilirrubina também ocorrem, mas com menos frequência). Todos os dias, até 1 g de colesterol entra no cólon. Esse colesterol tem origem na dieta, na bile e nas células intestinais descamadas e pode ser metabolizado pelas bactérias colônicas. O colesterol é convertido principalmente em coprostanol, um esterol não absorvível que é excretado nas fezes.
Embora o colesterol seja um esteróide geralmente associado a mamíferos, o patógeno humano Mycobacterium tuberculosis é capaz de degradar completamente esta molécula e contém um grande número de genes que são regulados por sua presença. Muitos desses genes regulados pelo colesterol são homólogos dos genes da β-oxidação de ácidos graxos, mas evoluíram de forma a se ligarem a grandes substratos de esteroides como o colesterol.
Fontes alimentares
As gorduras animais são misturas complexas de triglicerídeos, com quantidades menores de fosfolipídios e moléculas de colesterol a partir das quais todas as membranas celulares animais (e humanas) são construídas. Como todas as células animais fabricam colesterol, todos os alimentos de origem animal contêm colesterol em quantidades variadas. As principais fontes dietéticas de colesterol incluem carne vermelha, gema de ovo e ovos inteiros, fígado, rim, miúdos, óleo de peixe e manteiga. O leite materno também contém quantidades significativas de colesterol.
As células vegetais sintetizam o colesterol como precursor de outros compostos, como fitoesteróis e glicoalcalóides esteróides, com o colesterol permanecendo em alimentos vegetais apenas em quantidades menores ou ausentes. Alguns alimentos vegetais, como abacate, sementes de linhaça e amendoim, contêm fitoesteróis, que competem com o colesterol pela absorção no intestino e reduzem a absorção do colesterol dietético e biliar. Uma dieta típica contribui com cerca de 0,2 grama de fitoesteróis, o que não é suficiente para ter um impacto significativo no bloqueio da absorção do colesterol. A ingestão de fitoesteróis pode ser complementada através do uso de alimentos funcionais contendo fitoesteróis ou suplementos dietéticos que são reconhecidos como tendo potencial para reduzir os níveis de colesterol LDL.
Diretrizes e recomendações médicas
Em 2015, o Comitê Consultivo de Diretrizes Dietéticas do Departamento de Agricultura dos Estados Unidos (DGAC) recomendou que os americanos comessem o mínimo possível de colesterol na dieta, porque a maioria dos alimentos ricos em colesterol também é rica em gordura saturada e, portanto, pode aumentar o risco de doença cardiovascular.
Um relatório de 2013 da American Heart Association e do American College of Cardiology recomendou o foco em padrões alimentares saudáveis, em vez de limites de colesterol específicos, pois são difíceis de serem implementados por médicos e consumidores. Eles recomendam a dieta DASH e mediterrânea, que são baixas em colesterol. Uma revisão de 2017 da American Heart Association recomenda a troca de gorduras saturadas por gorduras poliinsaturadas para reduzir o risco de doenças cardiovasculares.
Algumas diretrizes suplementares recomendaram doses de fitoesteróis na faixa de 1,6–3,0 gramas por dia (Health Canada, EFSA, ATP III, FDA). Uma meta-análise recente demonstrando uma redução de 12% no colesterol LDL em uma dose média de 2,1 gramas por dia. No entanto, os benefícios de uma dieta suplementada com fitoesteróis também têm sido questionados.
Significado clínico
Hipercolesterolemia
De acordo com a hipótese lipídica, níveis elevados de colesterol no sangue levam à aterosclerose, que pode aumentar o risco de ataque cardíaco, derrame e doença arterial periférica. Como o LDL no sangue mais alto - especialmente as concentrações mais altas de LDL e o tamanho menor das partículas de LDL - contribui para esse processo mais do que o teor de colesterol das partículas de HDL, as partículas de LDL são frequentemente denominadas "mau colesterol". Altas concentrações de HDL funcional, que podem remover o colesterol das células e ateromas, oferecem proteção e são comumente chamadas de "colesterol bom". Esses equilíbrios são determinados geneticamente, mas podem ser alterados pela composição corporal, medicamentos, dieta e outros fatores. Um estudo de 2007 demonstrou que os níveis de colesterol total no sangue têm um efeito exponencial na mortalidade cardiovascular e total, com a associação mais pronunciada em indivíduos mais jovens. Como a doença cardiovascular é relativamente rara na população mais jovem, o impacto do colesterol alto na saúde é maior nas pessoas mais velhas.
Níveis elevados das frações de lipoproteínas, LDL, IDL e VLDL, em vez do nível de colesterol total, correlacionam-se com a extensão e o progresso da aterosclerose. Por outro lado, o colesterol total pode estar dentro dos limites normais, mas ser composto principalmente de pequenas partículas de LDL e pequenas partículas de HDL, condições nas quais as taxas de crescimento de ateroma são altas. Uma análise post hoc dos estudos prospectivos IDEAL e EPIC encontrou uma associação entre altos níveis de colesterol HDL (ajustado para apolipoproteína A-I e apolipoproteína B) e aumento do risco de doença cardiovascular, lançando dúvidas sobre o papel cardioprotetor de "bom colesterol".
Cerca de um em cada 250 indivíduos pode ter uma mutação genética para o receptor de colesterol LDL que os leva a ter hipercolesterolemia familiar. O colesterol elevado hereditário também pode incluir mutações genéticas no gene PCSK9 e no gene da apolipoproteína B.
Os níveis elevados de colesterol são tratados com uma dieta rigorosa que consiste em alimentos com baixo teor de gordura saturada, sem gordura trans e com baixo colesterol, geralmente seguidos por um dos vários agentes hipolipidêmicos, como estatinas, fibratos, inibidores da absorção de colesterol, terapia com anticorpos monoclonais (inibidores de PCSK9), derivados do ácido nicotínico ou sequestrantes de ácidos biliares. Existem várias diretrizes internacionais sobre o tratamento da hipercolesterolemia.
Testes em humanos usando inibidores da HMG-CoA redutase, conhecidos como estatinas, confirmaram repetidamente que mudar os padrões de transporte de lipoproteínas de padrões não saudáveis para padrões mais saudáveis reduz significativamente as taxas de eventos de doenças cardiovasculares, mesmo para pessoas com valores de colesterol atualmente considerados baixos para adultos. Estudos mostraram que reduzir os níveis de colesterol LDL em cerca de 38,7 mg/dL com o uso de estatinas pode reduzir o risco de doenças cardiovasculares e derrames em cerca de 21%. Estudos também descobriram que as estatinas reduzem a progressão do ateroma. Como resultado, pessoas com histórico de doença cardiovascular podem se beneficiar das estatinas, independentemente de seus níveis de colesterol (colesterol total abaixo de 5,0 mmol/L [193 mg/dL]), e em homens sem doença cardiovascular, há benefício em reduzir anormalmente níveis elevados de colesterol ("prevenção primária"). A prevenção primária em mulheres foi praticada originalmente apenas como extensão dos achados em estudos com homens, uma vez que, em mulheres, nenhum dos grandes estudos com estatinas conduzidos antes de 2007 demonstrou uma redução significativa na mortalidade geral ou nos desfechos cardiovasculares. Metanálises demonstraram reduções significativas na mortalidade cardiovascular e por todas as causas, sem heterogeneidade significativa por sexo.
| Nível | Interpretação | |
|---|---|---|
| mg/dL | mmol/L | |
| < 200 | < 5.2 | Nível desejável (risco inferior) |
| 200–240 | 5.2–6.2 | Risco de alto risco |
| > 240 | > 6.2 | Risco elevado |
O relatório de 1987 do National Cholesterol Education Program, Adult Treatment Panels sugere que o nível total de colesterol no sangue deve ser: < 200 mg/dL colesterol normal no sangue, 200–239 mg/dL limítrofe-alto, > 240 mg/dL de colesterol alto. A American Heart Association fornece um conjunto semelhante de diretrizes para os níveis de colesterol total (jejum) no sangue e risco de doença cardíaca: as estatinas são eficazes na redução do colesterol LDL e amplamente utilizadas para prevenção primária em pessoas com alto risco de doença cardiovascular, bem como em prevenção secundária para aqueles que desenvolveram doença cardiovascular.
Métodos de teste mais atuais determinam o colesterol LDL ("ruim") e HDL ("bom") separadamente, permitindo que a análise do colesterol seja mais sutil. O nível desejável de LDL é considerado inferior a 100 mg/dL (2,6 mmol/L), embora um limite superior mais recente de 70 mg/dL (1,8 mmol/L) possa ser considerado em indivíduos de alto risco com base em alguns dos julgamentos acima mencionados. Uma proporção de colesterol total para HDL – outra medida útil – muito inferior a 5:1 é considerada mais saudável.
O colesterol total é definido como a soma de HDL, LDL e VLDL. Normalmente, apenas o total, HDL e triglicerídeos são medidos. Por razões de custo, o VLDL é geralmente estimado como um quinto dos triglicerídeos e o LDL é estimado usando a fórmula de Friedewald (ou uma variante): LDL estimado = [colesterol total] − [HDL total] − [VLDL estimado]. As medições diretas de LDL são usadas quando os triglicerídeos excedem 400 mg/dL. As estimativas de VLDL e LDL apresentam mais erros quando os triglicerídeos estão acima de 400 mg/dL.
No Framingham Heart Study, cada aumento de 10 mg/dL (0,6 mmol/L) nos níveis de colesterol total aumentou a mortalidade geral em 30 anos em 5% e a mortalidade por DCV em 9%. Enquanto os indivíduos com mais de 50 anos tiveram um aumento de 11% na mortalidade geral e um aumento de 14% na mortalidade por doença cardiovascular por 1 mg/dL (0,06 mmol/L) de queda anual nos níveis de colesterol total. Os pesquisadores atribuíram esse fenômeno à causalidade reversa, em que a própria doença aumenta o risco de morte, além de alterar uma miríade de fatores, como perda de peso e incapacidade de comer, que reduzem o colesterol sérico. Este efeito também foi demonstrado em homens de todas as idades e mulheres com mais de 50 anos no Programa de Promoção e Monitoramento da Saúde de Vorarlberg. Esses grupos eram mais propensos a morrer de câncer, doenças hepáticas e doenças mentais com colesterol total muito baixo, de 186 mg/dL (10,3 mmol/L) e inferior. Esse resultado indica que o efeito do colesterol baixo ocorre mesmo entre os entrevistados mais jovens, contrariando a avaliação anterior entre coortes de idosos de que esse é um marcador de fragilidade que ocorre com a idade.
Hipocolesterolemia
Níveis anormalmente baixos de colesterol são chamados de hipocolesterolemia. A pesquisa sobre as causas desse estado é relativamente limitada, mas alguns estudos sugerem uma ligação com depressão, câncer e hemorragia cerebral. Em geral, os níveis baixos de colesterol parecem ser uma consequência, e não a causa, de uma doença subjacente. Um defeito genético na síntese do colesterol causa a síndrome de Smith-Lemli-Opitz, frequentemente associada a níveis baixos de colesterol no plasma. O hipertireoidismo, ou qualquer outro distúrbio endócrino que cause regulação positiva do receptor de LDL, pode resultar em hipocolesterolemia.
Teste de colesterol
A American Heart Association recomenda testar o colesterol a cada 4 a 6 anos para pessoas com 20 anos ou mais. Um conjunto separado de diretrizes da American Heart Association emitidas em 2013 indica que as pessoas que tomam estatinas devem ter seu colesterol testado 4 a 12 semanas após a primeira dose e, a partir de então, a cada 3 a 12 meses. Para homens de 45 a 65 anos e mulheres de 55 a 65 anos, um teste de colesterol deve ser feito a cada 1-2 anos, e para idosos com mais de 65 anos, um teste anual deve ser realizado.
Uma amostra de sangue após 12 horas de jejum é coletada por um profissional de saúde de uma veia do braço para medir um perfil lipídico para a) colesterol total, b) colesterol HDL, c) colesterol LDL e d) triglicerídeos. Os resultados podem ser expressos como "calculados", indicando um cálculo de colesterol total, HDL e triglicerídeos.
O colesterol é testado para determinar o colesterol "normal" ou "desejável" níveis se uma pessoa tiver um colesterol total de 5,2 mmol/L ou menos (200 mg/dL), um valor de HDL superior a 1 mmol/L (40 mg/dL, "quanto maior, melhor"), um valor de LDL inferior a 2,6 mmol/L (100 mg/dL) e um nível de triglicerídeos inferior a 1,7 mmol/L (150 mg/dL). O colesterol sanguíneo em pessoas com estilo de vida, envelhecimento ou fatores de risco cardiovascular, como diabetes mellitus, hipertensão, história familiar de doença arterial coronariana ou angina, é avaliado em diferentes níveis.
Mapa de percurso interativo
Clique nos genes, proteínas e metabólitos abaixo para acessar os respectivos artigos.
- ^ O mapa interativo do caminho pode ser editado no WikiPathways: «Statin_Pathway_WP430» (em inglês).
Cristais líquidos colestéricos
Alguns derivados do colesterol (entre outros lipídios colestéricos simples) são conhecidos por gerar a "fase colestérica" líquida cristalina. A fase colestérica é, na verdade, uma fase nemática quiral, e muda de cor quando sua temperatura muda. Isso torna os derivados de colesterol úteis para indicar temperatura em termômetros de cristal líquido e em tintas sensíveis à temperatura.
Estereoisômeros
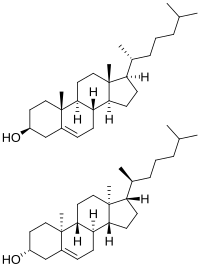
O colesterol tem 256 estereoisômeros que surgem de seus oito estereocentros, embora apenas dois dos estereoisômeros tenham significado bioquímico (nat-colesterol e ent-colesterol, para natural e enantiômero, respectivamente), e apenas um ocorre naturalmente (nat-colesterol).
Imagens adicionais
Contenido relacionado
DNA ligase
Kary Mullis
Adenilil ciclase
Eletroforese em gel
Enzima