Tumor cerebral
Un tumor cerebral ocurre cuando se forman células anormales dentro del cerebro. Hay dos tipos principales de tumores: tumores malignos y tumores benignos (no cancerosos). Estos pueden clasificarse además como tumores primarios, que comienzan dentro del cerebro, y tumores secundarios, que con mayor frecuencia se han propagado desde tumores ubicados fuera del cerebro, conocidos como tumores de metástasis cerebral. Todos los tipos de tumores cerebrales pueden producir síntomas que varían según el tamaño del tumor y la parte del cerebro afectada. Cuando existen síntomas, pueden incluir dolores de cabeza, convulsiones, problemas de visión, vómitos y cambios mentales. Otros síntomas pueden incluir dificultad para caminar, hablar, con sensaciones o pérdida del conocimiento.
Se desconoce la causa de la mayoría de los tumores cerebrales. Los factores de riesgo poco frecuentes incluyen la exposición al cloruro de vinilo, el virus de Epstein-Barr, la radiación ionizante y síndromes hereditarios como la neurofibromatosis, la esclerosis tuberosa y la enfermedad de von Hippel-Lindau. Los estudios sobre exposición a teléfonos móviles no han mostrado un riesgo claro. Los tipos más comunes de tumores primarios en adultos son los meningiomas (generalmente benignos) y los astrocitomas como los glioblastomas. En los niños, el tipo más común es un meduloblastoma maligno. El diagnóstico generalmente se realiza mediante un examen médico junto con una tomografía computarizada (TC) o una resonancia magnética nuclear (RMN). Luego, el resultado a menudo se confirma mediante una biopsia. Según los hallazgos, los tumores se dividen en diferentes grados de gravedad.
El tratamiento puede incluir alguna combinación de cirugía, radioterapia y quimioterapia. Si se producen convulsiones, es posible que se necesiten medicamentos anticonvulsivos. La dexametasona y la furosemida son medicamentos que se pueden usar para disminuir la inflamación alrededor del tumor. Algunos tumores crecen gradualmente, lo que requiere solo vigilancia y posiblemente no necesiten más intervención. Se están estudiando tratamientos que utilizan el sistema inmunitario de una persona. Los resultados de los tumores malignos varían considerablemente según el tipo de tumor y cuánto se ha propagado en el momento del diagnóstico. Aunque los tumores benignos solo crecen en un área, aún pueden ser potencialmente mortales según su tamaño y ubicación. Los glioblastomas malignos suelen tener muy malos resultados, mientras que los meningiomas benignos suelen tener buenos resultados. La tasa de supervivencia promedio a cinco años para todos los cánceres cerebrales (malignos) en los Estados Unidos es del 33 %.
Los tumores cerebrales secundarios o metastásicos son aproximadamente cuatro veces más comunes que los tumores cerebrales primarios, y aproximadamente la mitad de las metástasis provienen del cáncer de pulmón. Los tumores cerebrales primarios ocurren en alrededor de 250 000 personas al año en todo el mundo y representan menos del 2 % de los cánceres. En los niños menores de 15 años, los tumores cerebrales ocupan el segundo lugar después de la leucemia linfoblástica aguda como la forma más común de cáncer. En NSW, Australia, en 2005, el costo económico promedio de por vida de un caso de cáncer cerebral fue de 1,9 millones de dólares australianos, el mayor de cualquier tipo de cáncer.
Signos y síntomas
Los signos y síntomas de los tumores cerebrales son amplios. Las personas pueden experimentar síntomas independientemente de si el tumor es benigno (no canceroso) o canceroso. Los tumores cerebrales primarios y secundarios se presentan con síntomas similares, según la ubicación, el tamaño y la tasa de crecimiento del tumor. Por ejemplo, los tumores más grandes en el lóbulo frontal pueden provocar cambios en la capacidad de pensar. Sin embargo, un tumor más pequeño en un área como el área de Wernicke (área pequeña responsable de la comprensión del lenguaje) puede resultar en una mayor pérdida de función.
Dolor de cabeza
Los dolores de cabeza como resultado del aumento de la presión intracraneal pueden ser un síntoma temprano de cáncer cerebral. Sin embargo, el dolor de cabeza aislado sin otros síntomas es raro, y pueden presentarse otros síntomas, incluidas anomalías visuales, antes de que los dolores de cabeza se vuelvan comunes. Existen ciertas señales de advertencia de dolor de cabeza que hacen que sea más probable que el dolor de cabeza esté asociado con el cáncer cerebral. Estos son, según la definición de la Academia Estadounidense de Neurología: "examen neurológico anormal, dolor de cabeza empeorado por la maniobra de Valsalva, dolor de cabeza que causa despertar del sueño, nuevo dolor de cabeza en la población de mayor edad, dolor de cabeza que empeora progresivamente, características atípicas del dolor de cabeza o pacientes que no cumplen con la definición estricta de migraña". Otros signos asociados son dolores de cabeza que empeoran por la mañana o que desaparecen después de vomitar.
Síntomas específicos de la ubicación
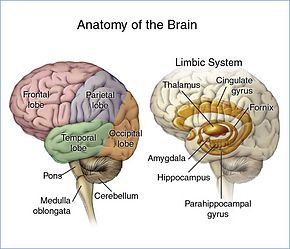
El cerebro se divide en lóbulos y cada lóbulo o área tiene su propia función. Un tumor en cualquiera de estos lóbulos puede afectar el funcionamiento de la zona. Los síntomas experimentados a menudo están relacionados con la ubicación del tumor, pero cada persona puede experimentar algo diferente.
- Lóbulo frontal: Los tumores pueden contribuir a un mal razonamiento, comportamiento social inapropiado, cambios de personalidad, mala planificación, menor inhibición y disminución de la producción de habla (zona de Broca).
- Lóbulo temporal: Los tumores en este lóbulo pueden contribuir a la mala memoria, pérdida de audición y dificultad en la comprensión del lenguaje (la zona de Wernicke está ubicada en este lóbulo).
- Lobo parietal: Los tumores aquí pueden resultar en una mala interpretación de idiomas, dificultad para hablar, escribir, dibujar, nombrar y reconocer, y mala percepción espacial y visual.
- Lóbulo occipital: El daño a este lóbulo puede resultar en una mala visión o pérdida de la visión.
- Cerebellum: Los tumores en este área pueden causar mal equilibrio, movimiento muscular y postura.
- Tallo cerebral: Los tumores en el cerebro pueden causar convulsiones, problemas endocrinos, cambios respiratorios, cambios visuales, dolores de cabeza y parálisis parcial.
Cambios de comportamiento
La personalidad de una persona puede verse alterada debido a que el tumor daña los lóbulos del cerebro. Dado que los lóbulos frontal, temporal y parietal controlan la inhibición, las emociones, el estado de ánimo, el juicio, el razonamiento y el comportamiento, un tumor en esas regiones puede causar un comportamiento social inapropiado, rabietas, reírse de cosas que no merecen la risa e incluso síntomas psicológicos como como depresión y ansiedad. Se necesita más investigación sobre la eficacia y la seguridad de los medicamentos para la depresión en personas con tumores cerebrales.
Los cambios de personalidad pueden tener efectos perjudiciales, como desempleo, relaciones inestables y falta de control.
Causa
Se requieren estudios epidemiológicos para determinar los factores de riesgo. Aparte de la exposición al cloruro de vinilo o la radiación ionizante, no se conocen factores ambientales asociados con los tumores cerebrales. Se cree que las mutaciones y deleciones de los genes supresores de tumores, como el P53, son la causa de algunas formas de tumores cerebrales. Las condiciones hereditarias, como la enfermedad de Von Hippel-Lindau, la esclerosis tuberosa, la neoplasia endocrina múltiple y la neurofibromatosis tipo 2 conllevan un alto riesgo de desarrollar tumores cerebrales. Las personas con enfermedad celíaca tienen un riesgo ligeramente mayor de desarrollar tumores cerebrales. Se ha sugerido que fumar aumenta el riesgo, pero la evidencia sigue sin estar clara.
Aunque los estudios no han demostrado ningún vínculo entre la radiación de los teléfonos móviles o los teléfonos móviles y la aparición de tumores cerebrales, la Organización Mundial de la Salud ha clasificado la radiación de los teléfonos móviles en la escala IARC en el Grupo 2B, posiblemente cancerígeno. La afirmación de que el uso de teléfonos celulares puede causar cáncer cerebral probablemente se base en estudios epidemiológicos que observaron un ligero aumento en el riesgo de glioma entre los usuarios intensivos de teléfonos inalámbricos. Cuando se realizaron esos estudios, los teléfonos GSM (2G) estaban en uso. Los teléfonos modernos de tercera generación (3G) emiten, en promedio, alrededor del 1 % de la energía emitida por los teléfonos GSM (2G) y, por lo tanto, el hallazgo de una asociación entre el uso de teléfonos celulares y un mayor riesgo de cáncer cerebral no se basa en uso actual del teléfono.
Fisiopatología
Meninges
El cerebro humano está rodeado por un sistema de membranas de tejido conectivo llamadas meninges que separan el cerebro del cráneo. Esta cubierta de tres capas está compuesta (de afuera hacia adentro) por la duramadre, la aracnoides y la piamadre. La aracnoides y la piamadre están conectadas físicamente y, por lo tanto, a menudo se las considera como una sola capa, las leptomeninges. Entre la aracnoides y la piamadre se encuentra el espacio subaracnoideo que contiene líquido cefalorraquídeo (LCR). Este líquido circula en los estrechos espacios entre las células ya través de las cavidades del cerebro llamadas ventrículos, para sostener y proteger el tejido cerebral. Los vasos sanguíneos ingresan al sistema nervioso central a través del espacio perivascular por encima de la piamadre. Las células de las paredes de los vasos sanguíneos se unen estrechamente, formando la barrera hematoencefálica que protege al cerebro de las toxinas que podrían ingresar a través de la sangre.
Los tumores de las meninges son meningiomas y suelen ser benignos. Aunque técnicamente no es un tumor del tejido cerebral, a menudo se consideran tumores cerebrales ya que sobresalen en el espacio donde se encuentra el cerebro y causan síntomas. Dado que generalmente son tumores de crecimiento lento, los meningiomas pueden ser bastante grandes cuando aparecen los síntomas.
Materia cerebral
Los cerebros de los humanos y otros vertebrados están compuestos de tejido muy suave y tienen una textura similar a la gelatina. El tejido cerebral vivo tiene un tinte rosado en el exterior (materia gris) y casi completamente blanco en el interior (materia blanca), con sutiles variaciones de color. Las tres divisiones más grandes del cerebro son:
- Corteza cerebral
- Cerebro
- Cerebellum
Estas áreas están compuestas por dos amplias clases de células: neuronas y glía. Estos dos tipos son igualmente numerosos en el cerebro como un todo, aunque las células gliales superan en número a las neuronas en aproximadamente 4 a 1 en la corteza cerebral. Glia viene en varios tipos, que realizan una serie de funciones críticas, incluido el soporte estructural, el soporte metabólico, el aislamiento y la guía del desarrollo. Los tumores primarios de las células gliales se denominan gliomas y, a menudo, son malignos en el momento del diagnóstico.
El tálamo y el hipotálamo son divisiones principales del diencéfalo, con la glándula pituitaria y la glándula pineal unidas en la parte inferior; los tumores de la glándula pituitaria y pineal a menudo son benignos.
El tronco encefálico se encuentra entre la corteza cerebral grande y la médula espinal. Se divide en mesencéfalo, protuberancia y bulbo raquídeo.
Médula espinal
La médula espinal se considera parte del sistema nervioso central. Está formado por las mismas células que el cerebro: neuronas y células gliales.
Diagnóstico
Aunque no hay un síntoma o signo específico o singular, la presencia de una combinación de síntomas y la falta de indicaciones correspondientes de otras causas puede ser un indicador para investigar la posibilidad de un tumor cerebral. Los tumores cerebrales tienen características y obstáculos similares cuando se trata de diagnóstico y terapia con tumores ubicados en otras partes del cuerpo. Sin embargo, crean problemas específicos que siguen de cerca las propiedades del órgano en el que se encuentran.
A menudo, el diagnóstico se inicia tomando una historia clínica que tenga en cuenta los antecedentes médicos y los síntomas actuales. Las investigaciones clínicas y de laboratorio servirán para descartar infecciones como causa de los síntomas. Los exámenes en esta etapa pueden incluir exámenes de la vista, otorrinolaringológicos (o ENT) y electrofisiológicos. El uso de electroencefalografía (EEG) a menudo desempeña un papel en el diagnóstico de tumores cerebrales.
Los tumores cerebrales, en comparación con los tumores en otras áreas del cuerpo, representan un desafío para el diagnóstico. Por lo general, los trazadores radiactivos se captan en grandes volúmenes en los tumores debido a la alta actividad de las células tumorales, lo que permite obtener imágenes radiactivas del tumor. Sin embargo, la mayor parte del cerebro está separada de la sangre por la barrera hematoencefálica (BBB, por sus siglas en inglés), una membrana que ejerce un control estricto sobre qué sustancias pueden pasar al cerebro. Por lo tanto, muchos marcadores que pueden llegar fácilmente a los tumores en otras áreas del cuerpo no podrían llegar a los tumores cerebrales hasta que el tumor rompa la BBB. La interrupción de la BBB se visualiza bien mediante resonancia magnética o tomografía computarizada y, por lo tanto, se considera el principal indicador de diagnóstico de gliomas malignos, meningiomas y metástasis cerebrales.
La hinchazón u obstrucción del paso del líquido cefalorraquídeo (LCR) desde el cerebro puede causar signos (precoces) de aumento de la presión intracraneal que se traduce clínicamente en dolores de cabeza, vómitos o alteración del estado de conciencia, y en niños cambios en el diámetro del cráneo y abombamiento de las fontanelas. Los síntomas más complejos, como las disfunciones endocrinas, deberían alarmar a los médicos para que no excluyan los tumores cerebrales.
Un defecto del campo visual temporal bilateral (debido a la compresión del quiasma óptico) o dilatación de la pupila, y la aparición de síntomas neurológicos focales de evolución lenta o aparición repentina, como deterioro cognitivo y conductual (incluido deterioro del juicio, pérdida de memoria, falta de reconocimiento, trastornos de la orientación espacial), cambios de personalidad o emocionales, hemiparesia, hipoestesia, afasia, ataxia, alteración del campo visual, alteración del sentido del olfato, alteración de la audición, parálisis facial, visión doble o síntomas más graves como los temblores, la parálisis en un lado del cuerpo, la hemiplejía o las convulsiones (epilépticas) en un paciente con antecedentes negativos de epilepsia deberían plantear la posibilidad de un tumor cerebral.
Imágenes
Las imágenes médicas juegan un papel central en el diagnóstico de tumores cerebrales. Los primeros métodos de diagnóstico por imágenes, invasivos y, a veces, peligrosos, como la neumoencefalografía y la angiografía cerebral, se han abandonado en favor de técnicas no invasivas de alta resolución, especialmente la resonancia magnética nuclear (RMN) y la tomografía computarizada (TC), aunque la RM suele ser la patrón de referencia utilizado. Las neoplasias a menudo se mostrarán como masas de diferentes colores (también conocidas como procesos) en los resultados de la TC o la RM.
- Los tumores cerebrales benignos a menudo aparecen como lesiones de masa hipodenses (aprendizaje que el tejido cerebral) en las tomografías computarizadas. En la resonancia magnética, aparecen hipodenses o isointenses (la misma intensidad que el tejido cerebral) en los escaneos con peso T1, o hiperintensos (más que el tejido cerebral) en la resonancia magnética con peso T2, aunque la apariencia es variable.
- La captación de agentes de contraste, a veces en patrones característicos, se puede demostrar en los escáneres de TC o RM en la mayoría de los tumores cerebrales primarios y metastásicos malignos.
- Las áreas de presión donde el tejido cerebral ha sido comprimido por un tumor también aparecen hiperintensos en los escaneos con peso T2 y pueden indicar la presencia de un neoplasia difuso debido a un esbozo poco claro. Hinchazón alrededor del tumor conocido como edema peritumoral también puede mostrar un resultado similar. Esto se debe a que estos tumores perturban el funcionamiento normal de la BBB y conducen a un aumento de su permeabilidad.
Más recientemente, se han realizado avances para aumentar la utilidad de la resonancia magnética para proporcionar datos fisiológicos que pueden ayudar a informar el diagnóstico y el pronóstico. La MRI en sí misma es suficiente para identificar la ubicación y la morfología del tumor cerebral, pero se pueden usar otros tipos de MRI además de eso, como MRA, MRS, pMRI, fMRI y DWI. Estas técnicas de imagen ayudan a los médicos y cirujanos a diagnosticar el tipo de tumor, planificar la cirugía y evaluar el tratamiento y la radiación/quimioterapia.
Diferentes tipos de resonancias magnéticas
Angiografía por resonancia magnética (ARM): examina los vasos sanguíneos del cerebro. En el diagnóstico de un tumor cerebral, las MRA generalmente se realizan antes de la cirugía para ayudar a los cirujanos a comprender mejor la vasculatura del tumor. Por ejemplo, se realizó un estudio en el que los cirujanos pudieron separar los tumores cerebrales benignos de los malignos mediante el análisis de las formas de los vasos sanguíneos que se extrajeron de la ARM. Aunque no es obligatorio, algunas ARM pueden inyectar un agente de contraste, gadolinio, en el paciente para obtener una imagen mejorada.
Espectroscopía de resonancia magnética (MRS): mide los cambios metabólicos o químicos dentro del tumor. El MRS más común es la espectroscopia de protones con su frecuencia medida en partes por millón (ppm). Los gliomas o tumores cerebrales malignos tienen espectros diferentes del tejido cerebral normal, ya que tienen mayores niveles de colina y señales más bajas de N-acetil aspartato (NAA). El uso de MRS en el diagnóstico de tumores cerebrales puede ayudar a los médicos a identificar el tipo de tumor y su agresividad. Por ejemplo, los tumores cerebrales benignos o los meningiomas tienen niveles elevados de alanina. También puede ayudar a distinguir los tumores cerebrales de los tejidos cicatriciales o muertos causados por un tratamiento de radiación anterior, que no tiene niveles elevados de colina que tienen los tumores cerebrales, y de lesiones que simulan tumores, como abscesos o infartos.
Imágenes por resonancia magnética de perfusión (pMRI): evalúe el volumen sanguíneo y el flujo sanguíneo de diferentes partes del cerebro y los tumores cerebrales. pMRI requiere la inyección de un agente de contraste, generalmente gadopentetato de dimeglumina (Gd-DTPA) en las venas para mejorar el contraste. pMRI proporciona un mapa de volumen de sangre cerebral que muestra la vascularización del tumor y la angiogénesis. Los tumores cerebrales requerirían un mayor suministro de sangre y, por lo tanto, mostrarían un alto volumen de sangre cerebral en el mapa pMRI. La morfología vascular y el grado de angiogénesis de la pMRI ayudan a determinar el grado y la malignidad de los tumores cerebrales. Para el diagnóstico de tumores cerebrales, la pMRI es útil para determinar el mejor sitio para realizar la biopsia y para ayudar a reducir el error de muestreo. La pMRI también es valiosa para después del tratamiento para determinar si el área anormal es un tumor remanente o un tejido cicatricial. Para los pacientes que se someten a una terapia contra el cáncer contra la angiogénesis, la pMRI puede brindarles a los médicos una mejor idea de la eficacia del tratamiento mediante el control del volumen sanguíneo cerebral del tumor. MRI funcional (fMRI): mide los cambios en el flujo sanguíneo en partes activas del cerebro mientras el paciente realiza tareas y proporciona ubicaciones específicas del cerebro que son responsables de ciertas funciones. Antes de realizar una cirugía de tumor cerebral en los pacientes, los neurocirujanos usarían resonancia magnética funcional para evitar daños en las estructuras del cerebro que se corresponden con funciones cerebrales importantes mientras resecaban el tumor al mismo tiempo. La fMRI preoperatoria es importante porque a menudo es difícil distinguir la anatomía cerca del tumor, ya que distorsiona las regiones circundantes. Los neurocirujanos usarían IRMf para planificar si realizar una resección en la que el tumor se extirpa quirúrgicamente tanto como sea posible, una biopsia en la que toman una cantidad de muestra quirúrgica para proporcionar un diagnóstico o no someterse a ninguna cirugía. Por ejemplo, un neurocirujano puede oponerse a la resección de un tumor cerca de la corteza motora, ya que eso afectaría los movimientos del paciente. Sin resonancia magnética funcional preoperatoria, el neurocirujano tendría que realizar una craneotomía despierto en la que el paciente tendría que interactuar durante la cirugía abierta para ver si la extirpación del tumor afectaría funciones cerebrales importantes.
Imágenes ponderadas por difusión (DWI): una forma de resonancia magnética que mide el movimiento browniano aleatorio de las moléculas de agua a lo largo de un gradiente de campo magnético. Para el diagnóstico de tumores cerebrales, la medición del coeficiente de difusión aparente (ADC) en los tumores cerebrales permite a los médicos clasificar el tipo de tumor. La mayoría de los tumores cerebrales tienen un ADC más alto que los tejidos cerebrales normales y los médicos pueden comparar el ADC observado del tumor cerebral del paciente con una lista de ADC aceptados para identificar el tipo de tumor. DWI también es útil para fines de tratamiento y terapia en los que los cambios en la difusión se pueden analizar en respuesta a fármacos, radiación o terapia génica. La respuesta exitosa da como resultado la apoptosis y el aumento de la difusión, mientras que el tratamiento fallido da como resultado valores de difusión sin cambios.
Otros tipos de técnicas de imagen
Tomografía computarizada (TC): utiliza rayos X para tomar imágenes desde diferentes ángulos y procesamiento informático para combinar las imágenes en una imagen 3D. Una tomografía computarizada generalmente sirve como una alternativa a la resonancia magnética en los casos en que el paciente no puede someterse a una resonancia magnética debido a la claustrofobia o al marcapasos. En comparación con la resonancia magnética, una tomografía computarizada muestra una imagen más detallada de las estructuras óseas cercanas al tumor y se puede usar para medir el tamaño del tumor. Al igual que una resonancia magnética, también se puede inyectar un tinte de contraste en las venas o ingerirlo por la boca antes de una tomografía computarizada para delinear mejor cualquier tumor que pueda estar presente. Las tomografías computarizadas usan materiales de contraste a base de yodo y compuestos de sulfato de bario. La desventaja de usar tomografías computarizadas en lugar de resonancias magnéticas es que algunos tumores cerebrales no se ven bien en las tomografías computarizadas porque algunas masas intraaxiales son débiles y se asemejan al tejido cerebral normal. En algunos escenarios, los tumores cerebrales en las tomografías computarizadas pueden confundirse con infarto, infección y desmielinización. Para sospechar que una masa intraaxial es un tumor cerebral en lugar de otras posibilidades, debe haber calcificaciones inexplicables en el cerebro, preservación de la corteza y efecto de masa desproporcionado.
Angiografía por TC (CTA): proporciona información sobre los vasos sanguíneos del cerebro mediante rayos X. Siempre se requiere que se inyecte un agente de contraste en el paciente en el escáner CT. CTA sirve como una alternativa a MRA.
Tomografía por emisión de positrones (PET): utiliza sustancias radiactivas, siendo la más común un azúcar conocido como FDG. Esta sustancia inyectada es absorbida por células que se están dividiendo activamente. Las células tumorales son más activas en la división, por lo que absorberían más sustancia radiactiva. Después de la inyección, se usaría un escáner para crear una imagen de las áreas radiactivas en el cerebro. Las exploraciones PET se usan con más frecuencia para tumores de alto grado que para tumores de bajo grado. Es útil después del tratamiento para ayudar a los médicos a determinar si el área anormal en una imagen de MRI es un tumor remanente o tejido cicatricial. Los tejidos cicatriciales no aparecerán en las tomografías PET mientras que los tumores sí lo harían.
Sin embargo, estas técnicas por sí solas no pueden diagnosticar gliomas de grado alto versus bajo y, por lo tanto, el diagnóstico definitivo de tumor cerebral solo debe confirmarse mediante un examen histológico de muestras de tejido tumoral obtenidas mediante biopsia cerebral o cirugía abierta. El examen histológico es fundamental para determinar el tratamiento adecuado y el pronóstico correcto. Este examen, realizado por un patólogo, generalmente tiene tres etapas: examen interoperatorio de tejido fresco, examen microscópico preliminar de tejidos preparados y examen de seguimiento de tejidos preparados después de tinción inmunohistoquímica o análisis genético.
Patología
Los tumores tienen características que permiten determinar si son malignos y cómo evolucionarán, y determinar estas características permitirá al equipo médico determinar el plan de manejo.
Anaplasia o desdiferenciación: pérdida de la diferenciación de las células y de su orientación entre sí y los vasos sanguíneos, característica del tejido tumoral anaplásico. Las células anaplásicas han perdido el control total de sus funciones normales y muchas tienen estructuras celulares deterioradas. Las células anaplásicas a menudo tienen proporciones anormalmente altas de núcleo a citoplasma y muchas son multinucleadas. Además, el núcleo de las células anaplásicas suele tener una forma poco natural o un tamaño demasiado grande. Las células pueden volverse anaplásicas de dos maneras: las células tumorales neoplásicas pueden desdiferenciarse para convertirse en anaplasias (la desdiferenciación hace que las células pierdan toda su estructura/función normal), o las células madre cancerosas pueden aumentar su capacidad de multiplicarse (es decir, crecimiento incontrolable debido a fracaso de la diferenciación).
Atipia: una indicación de anormalidad de una célula (que puede ser indicativa de malignidad). La importancia de la anomalía depende en gran medida del contexto.
Neoplasia: la división (descontrolada) de células. Como tal, la neoplasia no es problemática pero sus consecuencias sí lo son: la división descontrolada de las células hace que la masa de una neoplasia aumente de tamaño, y en un espacio confinado como la cavidad intracraneal esto rápidamente se vuelve problemático porque la masa invade el espacio de la el cerebro lo empuja a un lado, lo que lleva a la compresión del tejido cerebral y al aumento de la presión intracraneal y la destrucción del parénquima cerebral. El aumento de la presión intracraneal (PIC) puede atribuirse al efecto de masa directo del tumor, al aumento del volumen sanguíneo o al aumento del volumen del líquido cefalorraquídeo (LCR), que a su vez puede tener síntomas secundarios.
Necrosis: la muerte (prematura) de las células, causada por factores externos como infecciones, toxinas o traumatismos. Las células necróticas envían señales químicas incorrectas que impiden que los fagocitos eliminen las células muertas, lo que lleva a una acumulación de tejido muerto, desechos celulares y toxinas en el sitio de las células necróticas o cerca de él.
La hipoxia arterial y venosa, o la privación del suministro adecuado de oxígeno a ciertas áreas del cerebro, ocurre cuando un tumor utiliza los vasos sanguíneos cercanos para su suministro de sangre y la neoplasia entra en competencia por los nutrientes con el tejido cerebral circundante.. De manera más general, una neoplasia puede provocar la liberación de productos finales metabólicos (p. ej., radicales libres, electrolitos alterados, neurotransmisores) y la liberación y reclutamiento de mediadores celulares (p. ej., citocinas) que interrumpen la función parenquimatosa normal.
Clasificación
Los tumores pueden ser benignos o malignos, pueden ocurrir en diferentes partes del cerebro y pueden clasificarse como primarios o secundarios. Un tumor primario es el que ha comenzado en el cerebro, a diferencia de un tumor metastásico, que es el que se ha diseminado al cerebro desde otra zona del cuerpo. La incidencia de tumores metastásicos es aproximadamente cuatro veces mayor que la de los tumores primarios. Los tumores pueden o no ser sintomáticos: algunos tumores se descubren porque el paciente tiene síntomas, otros aparecen incidentalmente en una exploración por imágenes o en una autopsia.
La clasificación de los tumores del sistema nervioso central se realiza comúnmente en una escala de 4 puntos (I-IV) creada por la Organización Mundial de la Salud en 1993. Los tumores de grado I son los menos graves y comúnmente se asocian con una supervivencia a largo plazo. con gravedad y pronóstico empeorando a medida que aumenta el grado. Los tumores de bajo grado a menudo son benignos, mientras que los de mayor grado son agresivamente malignos y/o metastásicos. Existen otras escalas de calificación, muchas basadas en los mismos criterios que la escala de la OMS y calificadas de I-IV.
Primaria
(feminine)Los tumores cerebrales primarios más comunes son:
- Gliomas (50,4%)
- Meningiomas (20,8%)
- Adenomas pituitarios (15%)
- Tumores nerviosos (10%)
Estos tumores comunes también se pueden organizar según el tejido de origen, como se muestra a continuación:
Tissue of origin | Niños | Adultos |
|---|---|---|
| Astrocitos | Astrocitoma pilocítico (PCA) | Glioblastoma Multiforme (GBM) |
| Oligodendrocitos | Oligodendroglioma | |
| Ependyma | Ependymoma | |
| Neuronas | Medulloblastoma | |
| Meninges | Meningioma |
Secundario
Los tumores secundarios del cerebro son metastásicos y han invadido el cerebro a partir de cánceres que se originan en otros órganos. Esto significa que se ha desarrollado una neoplasia cancerosa en otro órgano en otra parte del cuerpo y que las células cancerosas se han filtrado de ese tumor primario y luego han entrado en el sistema linfático y los vasos sanguíneos. Luego circulan por el torrente sanguíneo y se depositan en el cerebro. Allí, estas células continúan creciendo y dividiéndose, convirtiéndose en otra neoplasia invasiva del tejido del cáncer primario. Los tumores secundarios del cerebro son muy comunes en las fases terminales de pacientes con un cáncer metastásico incurable; Los tipos de cáncer más comunes que provocan tumores secundarios en el cerebro son el cáncer de pulmón, el cáncer de mama, el melanoma maligno, el cáncer de riñón y el cáncer de colon (en orden decreciente de frecuencia).
Los tumores cerebrales secundarios son más comunes que los primarios; en los Estados Unidos, hay alrededor de 170.000 casos nuevos cada año. Los tumores cerebrales secundarios son la causa más común de tumores en la cavidad intracraneal. La estructura ósea del cráneo también puede estar sujeta a una neoplasia que por su propia naturaleza reduce el volumen de la cavidad intracraneal y puede dañar el cerebro.
Por comportamiento
Los tumores cerebrales o neoplasias intracraneales pueden ser cancerosos (malignos) o no cancerosos (benignos). Sin embargo, las definiciones de neoplasias malignas o benignas difieren de las comúnmente utilizadas en otros tipos de neoplasias cancerosas o no cancerosas del cuerpo. En los cánceres en otras partes del cuerpo, tres propiedades malignas diferencian los tumores benignos de las formas malignas de cáncer: los tumores benignos son autolimitados y no invaden ni metastatizan. Las características de los tumores malignos incluyen:
- mitosis incontrolada (crecimiento por división más allá de los límites normales)
- anaplasia: las células del neoplasma tienen una forma obviamente diferente (en tamaño y forma). Las células anaplásicas muestran pleomorfismo marcado. Los núcleos celulares son característicamente extremadamente hipercromáticos (husados tercamente) y ampliados; el núcleo podría tener el mismo tamaño que el citoplasma de la célula (la relación nuclear-citoplasmática puede acercarse 1:1, en lugar de la proporción normal 1:4 o 1:6). Las células gigantescas, considerablemente más grandes que sus vecinos, pueden formar y poseer un enorme núcleo o varios núcleos (syncytia). Los núcleos anaplásicos son variables y extraños en tamaño y forma.
- invasión o infiltración (la literatura médica utiliza estos términos como equivalentes sinónimos. Sin embargo, para la claridad, los artículos que siguen se adhieren a una convención que significan cosas ligeramente diferentes; esta convención no se sigue fuera de estos artículos:
- La invasión o invasividad es la expansión espacial del tumor a través de la mitosis incontrolada, en el sentido de que el neoplasma invade el espacio ocupado por el tejido adyacente, empujando el otro tejido a un lado y finalmente comprime el tejido. A menudo estos tumores se asocian con tumores claramente descritos en imágenes.
- La infiltración es el comportamiento del tumor para crecer (microscópico) tentáculos que se introducen en el tejido circundante (a menudo haciendo que el contorno del tumor no esté definido o difuso) o para tener células tumorales "sembradas" en el tejido más allá de la circunferencia de la masa tumoral; esto no significa que un tumor infiltrado no tome espacio o no comprime el tejido circundante a medida que crece, sino que un infiltrado difícil
- metástasis (spread to other locations in the body via linfo or blood).
De las características malignas anteriores, algunos elementos no se aplican a las neoplasias primarias del cerebro:
- Los tumores cerebrales primarios raramente se metástasis en otros órganos; algunas formas de tumores cerebrales primarios pueden metástasis pero no se diseminarán fuera de la cavidad intracraneal o del canal espinal central. Debido a la BBB, las células cancerosas de un neoplasia primario no pueden entrar en el torrente sanguíneo y ser llevadas a otro lugar en el cuerpo. (Los informes de casos aislados ocasionales sugieren diseminación de ciertos tumores cerebrales fuera del sistema nervioso central, por ejemplo metástasis ósea de glioblastoma multiforme.)
- Los tumores cerebrales primarios generalmente son invasivos (es decir, se expandirán espacialmente e intruden en el espacio ocupado por otros tejidos cerebrales y comprimen esos tejidos cerebrales); sin embargo, algunos de los tumores cerebrales primarios más malignos se infiltrarán en el tejido circundante.
Por genética
En 2016, la OMS reestructuró sus clasificaciones de algunas categorías de gliomas para incluir distintas mutaciones genéticas que han sido útiles para diferenciar tipos de tumores, pronósticos y respuestas al tratamiento. Las mutaciones genéticas generalmente se detectan mediante inmunohistoquímica, una técnica que visualiza la presencia o ausencia de una proteína objetivo mediante tinción.
- Las mutaciones en los genes IDH1 y IDH2 se encuentran comúnmente en gliomas de bajo grado
- La pérdida de ambos genes IDH combinados con la pérdida de brazos cromosomas 1p y 19q indica que el tumor es un oligodendroglioma
- Pérdida de TP53 y ATRX caracteriza astrocitomas
- Los genes EGFR, TERT y PTEN se alteran comúnmente en gliomas y son útiles para diferenciar el grado tumoral y la biología
Tipos específicos
Astrocitoma anaplásico, Oligodendroglioma anaplásico, Astrocitoma, Neurocitoma central, Carcinoma del plexo coroideo, Papiloma del plexo coroideo, Tumor del plexo coroideo, Quiste coloide, Tumor neuroepitelial disembrioplásico, Tumor ependimario, Astrocitoma fibrilar, Glioblastoma de células gigantes, Glioblastoma multiforme, Gliomatosis cerebri, Gliosarcoma, hemangiopericitoma, meduloblastoma, meduloepitelioma, carcinomatosis meníngea, neuroblastoma, neurocitoma, oligoastrocitoma, oligodendroglioma, meningioma de la vaina del nervio óptico, ependimoma pediátrico, astrocitoma pilocítico, pinealoblastoma, pineocitoma, neuroblastoma anaplásico pleomórfico, xantoastrocitoma pleomórfico, linfoma de ala primario del sistema nervioso central, esfenoides, Astrocitoma subependimario de células gigantes, Subependimoma, Retinoblastoma trilateral.
Tratamiento
Un equipo médico generalmente evalúa las opciones de tratamiento y las presenta a la persona afectada y su familia. Hay varios tipos de tratamiento disponibles según el tipo de tumor y la ubicación, y pueden combinarse para producir las mejores posibilidades de supervivencia:
- Cirugía: resección completa o parcial del tumor con el objetivo de eliminar tantas células tumorales como sea posible.
- Radioterapia: el tratamiento más utilizado para tumores cerebrales; el tumor se irradia con beta, rayos X o rayos gamma.
- Quimioterapia: una opción de tratamiento para el cáncer, sin embargo, no siempre se usa para tratar los tumores cerebrales, ya que la barrera de la sangre-cerebro puede impedir que algunos medicamentos lleguen a las células cancerosas.
- Una variedad de terapias experimentales están disponibles a través de ensayos clínicos.
Las tasas de supervivencia en los tumores cerebrales primarios dependen del tipo de tumor, la edad, el estado funcional del paciente, la extensión de la extirpación quirúrgica y otros factores específicos de cada caso.
La atención estándar para los oligodendrogliomas anaplásicos y los oligoastrocitomas anaplásicos es la cirugía seguida de radioterapia. Un estudio encontró un beneficio de supervivencia al agregar quimioterapia a la radioterapia después de la cirugía, en comparación con la radioterapia sola.
Cirugía
El curso de acción principal y más deseado descrito en la literatura médica es la extirpación quirúrgica (resección) mediante craneotomía. Las técnicas mínimamente invasivas se están convirtiendo en la tendencia dominante en la oncología neuroquirúrgica. El objetivo principal de la cirugía es eliminar la mayor cantidad posible de células tumorales, siendo la eliminación completa el mejor resultado y la citorreducción ("reducción de volumen") del tumor en caso contrario. Una resección total macroscópica (GTR, por sus siglas en inglés) ocurre cuando se eliminan todos los signos visibles del tumor y las exploraciones posteriores no muestran ningún tumor aparente. En algunos casos el acceso al tumor es imposible e impide o prohíbe la cirugía.
Muchos meningiomas, a excepción de algunos tumores ubicados en la base del cráneo, se pueden extirpar quirúrgicamente con éxito. La mayoría de los adenomas hipofisarios se pueden extirpar quirúrgicamente, a menudo mediante un abordaje mínimamente invasivo a través de la cavidad nasal y la base del cráneo (abordaje transnasal, transesfenoidal). Los adenomas pituitarios grandes requieren una craneotomía (apertura del cráneo) para su extirpación. La radioterapia, incluidos los enfoques estereotácticos, se reserva para los casos inoperables.
Varios estudios de investigación actuales apuntan a mejorar la extirpación quirúrgica de tumores cerebrales al marcar las células tumorales con ácido 5-aminolevulínico que hace que emitan fluorescencia. La radioterapia y la quimioterapia posoperatorias son partes integrales del estándar terapéutico para los tumores malignos.
Los tumores metastásicos múltiples generalmente se tratan con radioterapia y quimioterapia en lugar de cirugía, y el pronóstico en tales casos está determinado por el tumor primario y, por lo general, es malo.
Radioterapia
El objetivo de la radioterapia es destruir las células tumorales sin dañar el tejido cerebral normal. En la radioterapia de haz externo estándar, los tratamientos múltiples de "fracciones" de radiación se aplican al cerebro. Este proceso se repite para un total de 10 a 30 tratamientos, dependiendo del tipo de tumor. Este tratamiento adicional brinda a algunos pacientes mejores resultados y tasas de supervivencia más prolongadas.
La radiocirugía es un método de tratamiento que usa cálculos computarizados para concentrar la radiación en el sitio del tumor mientras se minimiza la dosis de radiación al cerebro circundante. La radiocirugía puede ser un complemento de otros tratamientos o puede representar la técnica de tratamiento principal para algunos tumores. Las formas utilizadas incluyen la radiocirugía estereotáctica, como la radiocirugía Gamma Knife, Cyberknife o Novalis Tx.
La radioterapia es el tratamiento más común para los tumores cerebrales secundarios. La cantidad de radioterapia depende del tamaño del área del cerebro afectada por el cáncer. "tratamiento de radioterapia de cerebro total" de haz externo convencional (WBRT) o "irradiación de todo el cerebro" puede sugerirse si existe el riesgo de que se desarrollen otros tumores secundarios en el futuro. La radioterapia estereotáctica generalmente se recomienda en casos que involucran menos de tres pequeños tumores cerebrales secundarios. La radioterapia se puede utilizar después de la resección del tumor o, en algunos casos, en lugar de la misma. Las formas de radioterapia utilizadas para el cáncer de cerebro incluyen la radioterapia de haz externo, la más común, y la braquiterapia y la terapia de protones, la última especialmente utilizada para los niños.
Las personas que reciben radiocirugía estereotáctica (SRS) y radioterapia de todo el cerebro (WBRT) para el tratamiento de tumores cerebrales metastásicos tienen más del doble de riesgo de desarrollar problemas de aprendizaje y memoria que aquellos tratados solo con SRS. Los resultados de una revisión sistemática de 2021 encontraron que cuando se usa SRS como tratamiento inicial, la supervivencia o la muerte relacionada con la metástasis cerebral no fue mayor que la SRS sola en comparación con WBRT.
La radioterapia diaria convencional posoperatoria mejora la supervivencia de los adultos con buen bienestar funcional y glioma de alto grado en comparación con la ausencia de radioterapia posoperatoria. La radioterapia hipofraccionada tiene una eficacia similar para la supervivencia en comparación con la radioterapia convencional, particularmente para personas de 60 años o más con glioblastoma.
Quimioterapia
A los pacientes que se someten a quimioterapia se les administran medicamentos diseñados para destruir las células tumorales. Aunque la quimioterapia puede mejorar la supervivencia general en pacientes con los tumores cerebrales primarios más malignos, lo hace solo en alrededor del 20 por ciento de los pacientes. La quimioterapia se usa a menudo en niños pequeños en lugar de la radiación, ya que la radiación puede tener efectos negativos en el cerebro en desarrollo. La decisión de recetar este tratamiento se basa en la salud general del paciente, el tipo de tumor y la extensión del cáncer. La toxicidad y muchos efectos secundarios de los medicamentos, y el resultado incierto de la quimioterapia en los tumores cerebrales colocan a este tratamiento más abajo en la línea de opciones de tratamiento con cirugía y radioterapia preferidas.
UCLA Neuro-Oncology publica datos de supervivencia en tiempo real para pacientes con diagnóstico de glioblastoma multiforme. Son la única institución en los Estados Unidos que muestra el desempeño de los pacientes con tumores cerebrales con las terapias actuales. También muestran una lista de los agentes de quimioterapia que se usan para tratar los tumores de glioma de alto grado.
Las mutaciones genéticas tienen efectos significativos sobre la eficacia de la quimioterapia. Los gliomas con mutaciones IDH1 o IDH2 responden mejor a la quimioterapia que los que no tienen la mutación. La pérdida de los brazos cromosómicos 1p y 19q también indica una mejor respuesta a la quimiorradiación.
Otro
Se puede usar una derivación para aliviar los síntomas causados por la presión intracraneal, al reducir la acumulación de líquido (hidrocefalia) causada por el bloqueo del flujo libre de líquido cefalorraquídeo.
Pronóstico
El pronóstico del cáncer de cerebro depende del tipo de cáncer diagnosticado. El meduloblastoma tiene un buen pronóstico con quimioterapia, radioterapia y resección quirúrgica, mientras que el glioblastoma multiforme tiene una mediana de supervivencia de solo 12 meses incluso con quimiorradioterapia agresiva y cirugía. Los gliomas de tronco encefálico tienen el peor pronóstico de cualquier forma de cáncer cerebral, y la mayoría de los pacientes mueren dentro de un año, incluso con una terapia que generalmente consiste en radiación al tumor junto con corticosteroides. Sin embargo, un tipo, los gliomas focales del tronco encefálico en niños, parece estar abierto a un pronóstico excepcional y con frecuencia se ha informado sobre la supervivencia a largo plazo.
El pronóstico también se ve afectado por la presentación de mutaciones genéticas. Ciertas mutaciones proporcionan mejor pronóstico que otras. Las mutaciones de IDH1 e IDH2 en los gliomas, así como la deleción de los brazos cromosómicos 1p y 19q, generalmente indican un mejor pronóstico. Las mutaciones de TP53, ATRX, EGFR, PTEN y TERT también son útiles para determinar el pronóstico.
Glioblastoma multiforme
El glioblastoma multiforme (GBM) es la forma más agresiva (grado IV) y más común de tumor cerebral maligno. Incluso cuando se usa una terapia multimodal agresiva que consiste en radioterapia, quimioterapia y escisión quirúrgica, la mediana de supervivencia es de solo 12 a 17 meses. La terapia estándar para el glioblastoma multiforme consiste en la resección quirúrgica máxima del tumor, seguida de radioterapia entre dos y cuatro semanas después del procedimiento quirúrgico para extirpar el cáncer, luego quimioterapia, como temozolomida. La mayoría de los pacientes con glioblastoma toman un corticosteroide, generalmente dexametasona, durante su enfermedad para aliviar los síntomas. Los tratamientos experimentales incluyen terapia dirigida, radiocirugía con bisturí gamma, terapia de captura de neutrones de boro, terapia génica e implantes de quimiooblea.
Oligodendrogliomas
Los oligodendrogliomas son tumores cerebrales malignos incurables pero de progresión lenta. Se pueden tratar con resección quirúrgica, quimioterapia, radioterapia o una combinación. Para algunos tumores sospechosos de bajo grado (grado II), solo se opta por un curso de conducta expectante y terapia sintomática. Estos tumores muestran una alta frecuencia de codeleciones de los brazos p y q del cromosoma 1 y el cromosoma 19 respectivamente (codeleción 1p19q) y se ha encontrado que son especialmente quimiosensibles con un informe que afirma que son uno de los tumores más quimiosensibles.. Se ha informado una mediana de supervivencia de hasta 16,7 años para los oligodendrogliomas de grado II.
Neuroma acústico
Los neuromas acústicos son tumores no cancerosos. Se pueden tratar con cirugía, radioterapia u observación. Se recomienda una intervención temprana con cirugía o radiación para prevenir la pérdida auditiva progresiva.
Epidemiología
Las cifras de incidencia de cánceres de cerebro muestran una diferencia significativa entre los países más y menos desarrollados (los países menos desarrollados tienen una incidencia más baja de tumores de cerebro). Esto podría explicarse por muertes relacionadas con tumores no diagnosticadas (pacientes en situaciones de extrema pobreza no son diagnosticados, simplemente porque no tienen acceso a las modernas instalaciones de diagnóstico requeridas para diagnosticar un tumor cerebral) y por muertes causadas por otras causas relacionadas con la pobreza. que se apropian de la vida de un paciente antes de que se desarrollen tumores o los tumores se conviertan en una amenaza para la vida. Sin embargo, las estadísticas sugieren que ciertas formas de tumores cerebrales primarios son más comunes entre ciertas poblaciones.
No se ha demostrado que la incidencia de astrocitoma de bajo grado varíe significativamente según la nacionalidad. Sin embargo, los estudios que examinan la incidencia de tumores malignos del sistema nervioso central (SNC) han mostrado alguna variación con el origen nacional. Dado que algunas lesiones de alto grado surgen de tumores de bajo grado, vale la pena mencionar estas tendencias. Específicamente, la incidencia de tumores del SNC en los Estados Unidos, Israel y los países nórdicos es relativamente alta, mientras que Japón y los países asiáticos tienen una incidencia más baja. Estas diferencias probablemente reflejen algunas diferencias biológicas, así como diferencias en el diagnóstico patológico y el informe. Los datos mundiales sobre la incidencia del cáncer se pueden encontrar en la OMS (Organización Mundial de la Salud) y son manejados por la IARC (Agencia Internacional para la Investigación del Cáncer) ubicada en Francia.
Estados Unidos
En los Estados Unidos, en 2015, aproximadamente 166 039 personas vivían con tumores cerebrales u otros tumores del sistema nervioso central. Durante 2018, se proyectó que habría 23 880 nuevos casos de tumores cerebrales y 16 830 muertes en 2018 como resultado, lo que representa el 1,4 % de todos los cánceres y el 2,8 % de todas las muertes por cáncer. La mediana de edad de diagnóstico fue de 58 años, mientras que la mediana de edad de muerte fue de 65. El diagnóstico fue un poco más común en los hombres, con aproximadamente 7,5 casos por cada 100 000 personas, mientras que las mujeres vieron 2 menos con 5,4. Las muertes como resultado del cáncer cerebral fueron 5,3 por 100 000 para los hombres y 3,6 por 100 000 para las mujeres, lo que convierte al cáncer cerebral en la décima causa principal de muerte por cáncer en los Estados Unidos. El riesgo general de por vida de desarrollar cáncer cerebral se aproxima al 0,6 por ciento para hombres y mujeres.
Reino Unido
Los tumores cerebrales, del SNC o intracraneales son el noveno cáncer más común en el Reino Unido (alrededor de 10 600 personas fueron diagnosticadas en 2013) y es la octava causa más común de muerte por cáncer (alrededor de 5200 personas murieron en 2012). Los pacientes británicos blancos con tumor cerebral tienen un 30 % más de probabilidades de morir en el plazo de un año desde el diagnóstico que los pacientes de otras etnias. La razón de esto es desconocida.
Niños
En los Estados Unidos, se estima que más de 28 000 personas menores de 20 años tienen un tumor cerebral. Se espera que se diagnostiquen alrededor de 3720 nuevos casos de tumores cerebrales en menores de 15 años en 2019. Se informaron tasas más altas en 1985–1994 que en 1975–1983. Existe cierto debate sobre las razones; una teoría es que la tendencia es el resultado de mejores diagnósticos e informes, ya que el salto ocurrió al mismo tiempo que las resonancias magnéticas estuvieron disponibles ampliamente, y no hubo un salto coincidente en la mortalidad. Los tumores del sistema nervioso central representan del 20 al 25 por ciento de los cánceres en niños.
La tasa de supervivencia promedio para todos los cánceres cerebrales primarios en niños es del 74 %. Los cánceres de cerebro son los más comunes en niños menores de 19 años y causan más muertes en este grupo que la leucemia. A las personas más jóvenes les va menos bien.
Los tipos de tumores cerebrales más comunes en niños (0-14) son: astrocitoma pilocítico, glioma maligno, meduloblastoma, tumores neuronales y mixtos neurogliales y ependimoma.
En niños menores de 2 años, alrededor del 70 % de los tumores cerebrales son meduloblastomas, ependimomas y gliomas de bajo grado. Con menos frecuencia, y vistos generalmente en lactantes, son los teratomas y los tumores rabdoides teratoides atípicos. Los tumores de células germinales, incluidos los teratomas, constituyen solo el 3% de los tumores cerebrales primarios pediátricos, pero la incidencia mundial varía significativamente.
En el Reino Unido, cada año se diagnostica un tumor cerebral a 429 niños menores de 14 años en promedio, y se diagnostica a 563 niños y jóvenes menores de 19 años.
Investigación
Inmunoterapia
La inmunoterapia contra el cáncer se está estudiando activamente. Para los gliomas malignos, ninguna terapia ha demostrado mejorar la esperanza de vida a partir de 2015.
Virus de la estomatitis vesicular
En el año 2000, los investigadores utilizaron el virus de la estomatitis vesicular, o VSV, para infectar y eliminar las células cancerosas sin afectar las células sanas.
Vectores replicantes retrovirales
Dirigidos por el profesor Nori Kasahara, los investigadores de la USC, que ahora se encuentran en la UCLA, informaron en 2001 del primer ejemplo exitoso de la aplicación del uso de vectores de replicación retrovirales para la transducción de líneas celulares derivadas de tumores sólidos. Sobre la base de este trabajo inicial, los investigadores aplicaron la tecnología a modelos de cáncer in vivo y en 2005 informaron un beneficio de supervivencia a largo plazo en un modelo animal de tumor cerebral experimental. Posteriormente, en preparación para los ensayos clínicos en humanos, Tocagen (una compañía farmacéutica centrada principalmente en tratamientos contra el cáncer cerebral) desarrolló aún más esta tecnología como un tratamiento combinado (Toca 511 y Toca FC). Esto ha estado bajo investigación desde 2010 en un ensayo clínico de Fase I/II para el tratamiento potencial del glioma de alto grado recurrente, incluido el glioblastoma multiforme (GBM) y el astrocitoma anaplásico. Aún no se han publicado resultados.
Detección no invasiva
Los esfuerzos para detectar y controlar el desarrollo y la respuesta al tratamiento de los tumores cerebrales mediante biopsia líquida de sangre, líquido cefalorraquídeo u orina se encuentran en las primeras etapas de desarrollo.
Contenido relacionado
Registro fósil
Fabales
Azawakh