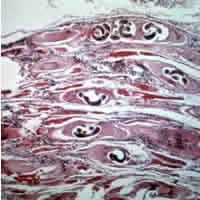
Triquinosis
La triquinosis, también conocida como triquinelosis, es una enfermedad parasitaria causada por lombrices intestinales del tipo Trichinella. Durante la infección inicial, la invasión de los intestinos puede provocar diarrea, dolor abdominal y vómitos. La migración de las larvas al músculo, que ocurre aproximadamente una semana después de la infección, puede causar hinchazón de la cara, inflamación de la parte blanca de los ojos, fiebre, dolores musculares y sarpullido. La infección menor puede no tener síntomas. Las complicaciones pueden incluir inflamación del músculo cardíaco, afectación del sistema nervioso central e inflamación de los pulmones.
La triquinosis se propaga principalmente cuando se come carne poco cocida que contiene quistes de Trichinella. En América del Norte, esto es más frecuente en osos, pero la infección también puede ocurrir a partir de la carne de cerdo, jabalí y perro. Varias especies de Trichinella pueden causar enfermedades, siendo T. spiralis la más común. Después de que se ha comido la carne infectada, las larvas se liberan de sus quistes en el estómago. Luego invaden la pared del intestino delgado, donde se convierten en gusanos adultos. Después de una semana, las hembras liberan nuevas larvas que migran hacia los músculos controlados voluntariamente, donde forman quistes. El diagnóstico generalmente se basa en los síntomas y se confirma al encontrar anticuerpos específicos en la sangre o larvas en una biopsia de tejido.
La mejor manera de prevenir la triquinosis es cocinar completamente la carne. Un termómetro para alimentos puede verificar que la temperatura dentro de la carne sea lo suficientemente alta. La infección generalmente se trata con medicamentos antiparasitarios como albendazol o mebendazol. El tratamiento rápido puede matar los gusanos adultos y, por lo tanto, detener el empeoramiento de los síntomas. Ambos medicamentos se consideran seguros, pero se han asociado con efectos secundarios como la supresión de la médula ósea. Su uso durante el embarazo o en niños menores de 2 años está poco estudiado, pero parece ser seguro. A veces también se requiere tratamiento con esteroides en casos graves. Sin tratamiento, los síntomas generalmente se resuelven dentro de los tres meses.
En todo el mundo, se producen unas 10.000 infecciones al año. Al menos 55 países, incluidos Estados Unidos, China, Argentina y Rusia, han tenido casos documentados recientemente. Si bien la enfermedad ocurre en los trópicos, es menos común allí. Las tasas de triquinosis en los Estados Unidos han disminuido de alrededor de 400 casos por año en la década de 1940 a 20 o menos por año en la década de 2000. El riesgo de muerte por infección es bajo.
Signos y síntomas
La gran mayoría de las infecciones por triquinosis tienen síntomas menores o no tienen síntomas ni complicaciones. Las dos fases principales de la infección son la enteral (que afecta a los intestinos) y la parenteral (fuera de los intestinos). Los síntomas varían según la fase, la especie de Trichinella, la cantidad de larvas enquistadas ingeridas, la edad, el sexo y la inmunidad del huésped.
Fase enteral
Una gran cantidad de gusanos adultos en los intestinos provoca síntomas como náuseas, acidez estomacal, dispepsia y diarrea de dos a siete días después de la infección, mientras que las pequeñas cantidades de gusanos generalmente son asintomáticas. La eosinofilia se presenta temprano y aumenta rápidamente.
Fase parenteral
La gravedad de los síntomas causados por la migración de las larvas desde los intestinos depende del número de larvas producidas. A medida que las larvas migran a través de tejidos y vasos, la respuesta inflamatoria del cuerpo produce edema, dolor muscular, fiebre y debilidad. Un signo clásico de triquinosis es el edema periorbitario, hinchazón alrededor de los ojos, que puede ser causado por vasculitis. La hemorragia en astillas en las uñas también es un síntoma común.
En muy raras ocasiones, pueden causar suficiente daño como para producir déficits neurológicos graves (como ataxia o parálisis respiratoria) a partir de gusanos que ingresan al sistema nervioso central (SNC), que se ve afectado por la triquinosis en el 10-24 % de los casos notificados de enfermedad venosa cerebral. trombosis sinusal, una forma muy rara de ictus (tres o cuatro casos por millón de incidencia anual en adultos). La triquinosis puede ser fatal según la gravedad de la infección; la muerte puede ocurrir de 4 a 6 semanas después de la infección y generalmente es causada por miocarditis, encefalitis o neumonía.
Causa
El agente clásico es T. spiralis (que se encuentra en todo el mundo en muchos animales carnívoros y omnívoros, tanto domésticos como selváticos (salvajes), pero ahora también se reconocen siete especies principalmente selváticas de Trichinella:
Especies y características
- T. espiralis está más adaptada a los cerdos, la mayoría patógenos en humanos, y es cosmopolita en distribución.
- T. britovi es la segunda especie común para infectar humanos; se distribuye en toda Europa, Asia y África septentrional y occidental, generalmente en carnívoros salvajes, cocodrilos, aves, jabalí salvaje y cerdos domesticados.
- T. murrelli También infecta a los humanos, especialmente de carne de oso negro; se distribuye entre carnívoros salvajes en América del Norte.
- T. nativa, que tiene una alta resistencia a la congelación, se encuentra en las regiones árticas y suárticas; los anfitriones de embalses incluyen osos polares, zorros árticos, moros y otro juego salvaje.
- T. nelsoni, encontrado en depredadores y estafadores de África Oriental, ha sido documentado para causar algunos casos humanos.
- T. papuae infecta tanto a mamíferos como a reptiles, incluyendo cocodrilos, humanos y cerdos salvajes y domésticos; esta especie, que se encuentra en Papua Nueva Guinea y Tailandia, también no está encapsulada.
- T. pseudospiralis infecta aves y mamíferos, y ha demostrado infección en humanos; es una especie no encapsulada.
- T. zimbabwensis puede infectar mamíferos, y posiblemente humanos; esta especie no encapsulada fue detectada en cocodrilos en África.
Taxonomía
- Reino: Animalia
- Phylum: Nematoda
- Clase: Adenoforea
- Orden: Trichurida
- Familia: Trichinellidae
- Genus: Trichinella
Ciclo de vida
El ciclo de vida típico de T. spiralis afecta a humanos, cerdos y roedores. Un cerdo se infecta cuando come quistes infecciosos en la carne cruda, a menudo carroña porcina o una rata (ciclo selvático). Un ser humano se infecta al consumir carne de cerdo infectada cruda o poco cocida (ciclo doméstico). En el estómago, la pepsina y el ácido clorhídrico actúan sobre los quistes de la carne mal cocida infectada, que ayudan a liberar las larvas de los quistes en el estómago. Luego, las larvas migran al intestino delgado y se entierran en la mucosa intestinal, donde mudan cuatro veces antes de convertirse en adultos.
Treinta a 34 horas después de la ingestión original de los quistes, los adultos se aparean y en cinco días producen larvas. Los gusanos adultos solo pueden reproducirse por un tiempo limitado, porque el sistema inmunitario finalmente los expulsa del intestino delgado. Luego, las larvas usan su pieza bucal perforante, llamada 'estilete', para atravesar la mucosa intestinal e ingresar a los vasos linfáticos, y luego ingresar al torrente sanguíneo.
Las larvas viajan por capilares a varios órganos, como la retina, el miocardio o los ganglios linfáticos; sin embargo, solo las larvas que migran a las células del músculo esquelético sobreviven y se enquistan. La célula huésped de la larva se convierte en una célula nodriza, en la que se encapsulará la larva, potencialmente durante la vida del huésped, a la espera de que se la coma. El desarrollo de una red capilar alrededor de la célula nodriza completa la enquistación de la larva. La triquinosis no se transmite por el suelo, ya que el parásito no pone huevos ni puede sobrevivir mucho tiempo fuera de un huésped.
Diagnóstico
El diagnóstico de triquinosis se confirma mediante una combinación de antecedentes de exposición, diagnóstico clínico y pruebas de laboratorio.
Historial de exposición
Se puede realizar una investigación epidemiológica para determinar la exposición de un paciente a carne cruda infectada. A menudo, una infección surge de la preparación casera de carne contaminada, en cuyo caso se puede usar la microscopía de la carne para determinar la infección. La determinación de la exposición no tiene que ser directamente de un animal infectado confirmado por laboratorio. Los criterios de exposición indirecta incluyen el consumo de productos de un animal infectado confirmado por laboratorio, o compartir una exposición común con un ser humano infectado confirmado por laboratorio.
Diagnóstico clínico
La presentación clínica de los síntomas comunes de la triquinosis también puede sugerir una infección. Estos síntomas incluyen hinchazón de los ojos, hemorragia en astilla, gastroenteritis inespecífica y dolor muscular. La definición de caso de triquinosis en el Centro Europeo para el Control de Enfermedades establece, "al menos tres de los siguientes seis: fiebre, dolor y dolor muscular, síntomas gastrointestinales, edema facial, eosinofilia y hemorragias subconjuntivales, subungueales y retinianas". "
Pruebas de laboratorio
Los análisis de sangre y la microscopía se pueden usar para ayudar en el diagnóstico de la triquinosis. Los análisis de sangre incluyen un hemograma completo para detectar eosinofilia, actividad de creatina fosfoquinasa y varios inmunoensayos como ELISA para antígenos larvales.
Prevención
Legislación
Las leyes y normas para los productores de alimentos pueden mejorar la seguridad alimentaria para los consumidores, como las normas establecidas por la Comisión Europea para las inspecciones, el control de roedores y la mejora de la higiene. Existe un protocolo similar en los Estados Unidos, en las pautas del USDA para las responsabilidades de las granjas y los mataderos en la inspección de la carne de cerdo.
Educación y formación
La educación pública sobre los peligros de consumir carne cruda y poco cocida, especialmente de cerdo, puede reducir las tasas de infección. Los cazadores también son una población en riesgo debido a su contacto y consumo de animales salvajes, incluido el oso. Como tal, muchos estados, como Nueva York, exigen la finalización de un curso sobre estos asuntos antes de poder obtener una licencia de caza.
Pruebas de carne
Los métodos de prueba están disponibles tanto para canales individuales como para el seguimiento de los rebaños. El método de digestión artificial generalmente se usa para la prueba de canales individuales, mientras que la prueba de anticuerpos específicos generalmente se usa para el control del rebaño.
Preparación de alimentos
Las larvas pueden morir por el calentamiento o la irradiación de la carne cruda. La congelación normalmente solo es efectiva para T. spiralis, ya que otras especies, como T. nativa, son resistentes a la congelación y pueden sobrevivir a la congelación a largo plazo.
- Toda la carne (incluyendo el cerdo) se puede preparar con seguridad cocinando a una temperatura interna de 165 °F (74 °C) o superior durante 15 segundos o más.
- Juego salvaje: La carne de juego salvaje debe cocinarse a fondo (ver la preparación de la carne arriba) Freezing salvaje juego no mata a todos los gusanos larval trichinosis, porque la especie de gusano que normalmente infesta juego salvaje puede resistir la congelación.
- Pork: Freezing cuts of pork less than 6 inches grueso for 20 days at 5 °F (−15 °C) or three days at −4 °F (−20 °C) kills T. espiralis gusanos larval; pero esto no matará a otras especies de gusano larval trichinosis, tales como T. nativa, si han infestado el suministro de alimentos de cerdo (que es poco probable, debido a la geografía).
La carne de cerdo se puede cocinar de forma segura a una temperatura ligeramente más baja, siempre que la temperatura interna de la carne sea al menos tan caliente durante al menos el tiempo que se indica en la siguiente tabla del USDA. No obstante, es prudente permitir un margen de error para la variación de la temperatura interna dentro de un corte de cerdo en particular, que puede tener huesos que afecten la uniformidad de la temperatura. Además, los termómetros de cocina tienen un error de medición que debe tenerse en cuenta. La carne de cerdo se puede cocinar durante mucho más tiempo y a una temperatura interna uniforme más alta que la que se indica a continuación para que sea segura.
| Temperatura interna | Temperatura interna | Hora mínima |
|---|---|---|
| (°F) | (°C) | (minutos) |
| 120 | 49 | 1260 |
| 122 | 50.0 | 570 |
| 124 | 51.1 | 270 |
| 126 | 52.2 | 120 |
| 128 | 53.4 | 60 |
| 130 | 54,5 | 30 |
| 132 | 55.6 | 15 |
| 134 | 56,7 | 6 |
| 136 | 57.8 | 3 |
| 138 | 58.9 | 2 |
| 140 | 60.0 | 1 |
| 142 | 61.1 | 1 |
| 144 | 62.2 | Instant Instant |
Los métodos inseguros y poco confiables para cocinar carne incluyen el uso de hornos de microondas, curado, secado y ahumado, ya que estos métodos son difíciles de estandarizar y controlar.
Cría de cerdos
La incidencia de infección se puede reducir mediante:
- Mantener cerdos en plumas limpias, con suelos que se pueden lavar (como hormigón)
- No permitir que los cerdos comen carcasas de otros animales, incluyendo ratas, que pueden infectarse con Trichinella
- Rectificadoras de carne al preparar carnes de tierra
- Control y destrucción de carne que contenga trichinae, por ejemplo, eliminación y eliminación adecuada de diafragmas porcina antes de la venta pública de carne
Los Centros para el Control y la Prevención de Enfermedades de EE. UU. hacen la siguiente recomendación: "Curar (salar), secar, ahumar o calentar la carne en el microondas no mata de manera constante los gusanos infecciosos." Sin embargo, bajo condiciones controladas de procesamiento comercial de alimentos, el USDA considera efectivos algunos de estos métodos.
El Servicio de Inspección de Sanidad Animal y Vegetal (APHIS) del USDA es responsable de las reglamentaciones relativas a la importación de cerdos de países extranjeros. La sección de Carne y Productos Cárnicos de Origen Extranjero, Porcino cubre la carne porcina (cocida, curada y seca, y fresca). APHIS desarrolló el Programa Nacional de Certificación de Triquinas; esta es una "precosecha" voluntaria; programa para productores de cerdos de EE. UU. "que proporcionará documentación de las prácticas de manejo de cerdos" para reducir la incidencia de Trichinella en cerdos. El CDC informa que el 0,013 % de los cerdos de EE. UU. están infectados con Trichinella.
Tratamiento
Como con la mayoría de las enfermedades, el tratamiento temprano es mejor y disminuye el riesgo de desarrollar la enfermedad. Si las larvas se enquistan en las células del músculo esquelético, pueden permanecer infecciosas durante meses o años.
Tratamiento primario
La administración temprana de antihelmínticos, como mebendazol o albendazol, disminuye la probabilidad de enquistamiento de larvas, particularmente si se administran dentro de los tres días posteriores a la infección. Sin embargo, la mayoría de los casos se diagnostican después de este tiempo. En humanos, se administra mebendazol (200 a 400 mg tres veces al día durante tres días) o albendazol (400 mg dos veces al día durante 8 a 14 días) para tratar la triquinosis. Estos medicamentos evitan que se desarrollen las larvas recién nacidas, pero no deben administrarse a mujeres embarazadas ni a niños menores de dos años.
Las referencias médicas de la década de 1940 no describían ningún tratamiento específico para la triquinosis en ese momento, pero se descubrió que la inyección intravenosa de sales de calcio era útil para controlar los síntomas relacionados con la toxemia grave de la infección.
Tratamiento secundario
Después de la infección, se pueden usar esteroides, como la prednisona, para aliviar el dolor muscular asociado con la migración de las larvas.
Investigación de vacunas
Los investigadores que intentan desarrollar una vacuna para Trichinella han intentado usar "extractos de larvas, antígeno excretor-secretor, ADN o proteína de antígeno recombinante". Actualmente, no hay ninguna vacuna comercial disponible para la triquinosis, pero los estudios experimentales con ratones han sugerido posibilidades.
- En un estudio, microondas Trichinella Las larvas se utilizaron para inmunizar ratones (oral o intraperitoneally), que posteriormente fueron infectados. Dependiendo de la dosis y la frecuencia de la inmunización, los resultados variaron de un recuento larval reducido a una protección completa de la triquinosis.
- Otro estudio utilizó extractos y productos secretos excretarios de larvas de primera etapa para producir una vacuna oral. Para evitar que los ácidos gástricos disolvieran los antígenos antes de llegar al intestino delgado, los científicos encapsularon los antígenos en microcápsulas. Esta vacuna aumentó significativamente los niveles de células CD4+, y aumentó el suero específico de antígeno IgGq e IgA, lo que dio lugar a una reducción estadísticamente significativa en el número promedio de gusanos adultos en los intestinos pequeños de los ratones. El significado de este enfoque es que, si los glóbulos blancos en el intestino delgado han sido expuestos a Trichinella antígenos (a través de la vacunación), cuando un individuo se infecta, el sistema inmunitario responderá para expulsar los gusanos del intestino delgado lo suficientemente rápido como para evitar que los gusanos femeninos salgan de sus larvas.
- Una vacuna de ADN probada en ratones "indujo una reducción de larvas musculares en ratones BALB/c en un 29% en respuesta a T. espiralis infección".
Epidemiología
Alrededor de 11 millones de humanos están infectados con Trichinella; T. spiralis es la especie responsable de la mayoría de estas infecciones. La infección fue una vez muy común, pero esta enfermedad ahora es rara en el mundo desarrollado, pero dos brotes conocidos ocurrieron en 2015. En el primer brote, alrededor de 40 personas se infectaron en Liguria, Italia, durante una celebración de Nochevieja.. El segundo brote en Francia se asoció con salchichas de cerdo de Córcega, que se comían crudas y afectaron a 14 personas en total. La incidencia de triquinosis en los EE. UU. ha disminuido drásticamente en el último siglo desde un promedio de 400 casos por año a mediados del siglo XX hasta un promedio anual de 20 casos por año (2008–10). El número de casos ha disminuido debido a la legislación que prohíbe alimentar a los cerdos con desechos de carne cruda, el aumento de la congelación comercial y doméstica de la carne de cerdo y la conciencia pública sobre el peligro de comer productos de carne de cerdo crudos o poco cocidos.
China notifica alrededor de 10.000 casos cada año, por lo que es el país con el mayor número de casos. En China, entre 1964 y 1998, más de 20 000 personas se infectaron con triquinosis y más de 200 personas murieron.
La triquinosis es común en los países en desarrollo donde la carne que se alimenta a los cerdos está cruda o poco cocida, pero las infecciones también surgen en los países desarrollados de Europa donde la carne de cerdo, jabalí y caballo cruda o poco cocida se puede consumir como manjares.
En el mundo en desarrollo, la mayoría de las infecciones están asociadas con carne de cerdo poco cocida. Por ejemplo, en Tailandia, se notifican anualmente entre 200 y 600 casos alrededor del Año Nuevo tailandés. Esto se atribuye principalmente a un manjar particular, larb, que requiere carne de cerdo poco cocida como parte de la receta.
En partes de Europa del Este, informa la Organización Mundial de la Salud, algunas piaras de cerdos tienen tasas de infección por triquinosis superiores al 50 %, con un gran número correspondiente de infecciones humanas.
Estados Unidos
Históricamente, se pensaba que los productos de cerdo tenían el mayor riesgo de infectar a los humanos con T. espiralis. Sin embargo, una vigilancia de triquinosis realizada entre 1997 y 2001 mostró un mayor porcentaje de casos causados por el consumo de caza silvestre (el ciclo de transmisión selvático). Se cree que esto se debe a la Ley Federal de Protección de la Salud Porcina (Ley Pública 96-468) aprobada por el Congreso en 1980. Antes de esta ley, los cerdos eran alimentados con basura que podría estar potencialmente infectada por T. spiralis. Esta ley se implementó para evitar que se administren alimentos contaminados con trichinella a los cerdos. Además, se establecieron otros requisitos, como el control de roedores, la limitación del contacto de los cerdos comerciales con la vida silvestre, el mantenimiento de una buena higiene y la eliminación inmediata de los cerdos muertos de los corrales.
Entre 2002 y 2007, se informaron a los CDC 11 casos de triquinosis cada año en promedio en los Estados Unidos, y 2008–10 promedió 20 casos por año; estos fueron principalmente el resultado de consumir animales de caza poco cocidos (transmisión selvática) o cerdos criados en casa (transmisión doméstica).
Grupos religiosos
Las leyes dietéticas kashrut y halal del judaísmo y el Islam prohíben comer carne de cerdo. En el siglo XIX, cuando se estableció por primera vez la asociación entre la triquinosis y la carne de cerdo poco cocida, se sugirió que esta asociación era el motivo de la prohibición, lo que recuerda la opinión anterior del filósofo judío medieval Maimónides de que los alimentos prohibidos por la ley judía eran " insalubres". Esta teoría fue controvertida y finalmente cayó en desgracia.
Resurgimiento
La desaparición del patógeno de los cerdos domésticos ha provocado una relajación de la legislación y los esfuerzos de control por parte de los sistemas de salud pública veterinaria. Últimamente se ha considerado a la triquinosis como una zoonosis reemergente, complementada por una mayor distribución de productos cárnicos, cambios políticos, un clima cambiante y una transmisión selvática creciente.
Grandes cambios sociopolíticos pueden producir condiciones que favorezcan el resurgimiento de infecciones por Trichinella en cerdos y, en consecuencia, en humanos. Por ejemplo, "el derrocamiento de las estructuras sociales y políticas en la década de 1990" en Rumania condujo a un aumento en la tasa de incidencia de triquinosis.
Historia
Ya en 1835, se sabía que la triquinosis había sido causada por un parásito, pero el mecanismo de infección no estaba claro en ese momento. Una década más tarde, el científico estadounidense Joseph Leidy identificó la carne poco cocida como el principal vector del parásito, y dos décadas después, esta hipótesis fue totalmente aceptada por la comunidad científica.
Parásito
Las circunstancias que rodearon la primera observación e identificación de T. spiralis son controvertidos, debido a la falta de registros. En 1835, James Paget, un estudiante de medicina de primer año, observó por primera vez la forma larvaria de T. spiralis, mientras presenciaba una autopsia en el Hospital St. Bartholomew de Londres. Paget se interesó especialmente en la presentación del músculo con motas blancas, descritas como un 'diafragma de arena'. Aunque es muy probable que Paget sea la primera persona que notó y registró estos hallazgos, el parásito fue nombrado y publicado en un informe por su profesor, Richard Owen, a quien ahora se le atribuye el descubrimiento del T. spiralis forma larvaria.
Ciclo de vida
Una serie de experimentos realizados entre 1850 y 1870 por los investigadores alemanes Rudolf Virchow, Rudolf Leuckart y Friedrich Albert von Zenker, que involucraron alimentar a un perro con carne infectada y realizar la necropsia posterior, condujo al descubrimiento del ciclo de vida de Triquina. A través de estos experimentos, Virchow pudo describir el desarrollo y la infectividad de T. espiralis.
Investigación
La Comisión Internacional sobre Triquinosis (ICT) se formó en Budapest en 1958. Su misión es intercambiar información sobre la epidemiología, biología, fisiopatología, inmunología y aspectos clínicos de la triquinosis en humanos y animales. La prevención es un objetivo primordial. Desde la creación del ICT, sus miembros (más de 110 de 46 países) se han reunido y trabajado regularmente en reuniones que se realizan cada cuatro años: la Conferencia Internacional sobre Triquinosis.
Contenido relacionado
Darbepoetina alfa
Partería
Roberto palo dorado