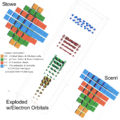
Tipos de tablas periódicas

| Alkali metal Metal de tierra alcalino Lanthanide Actinide Metal de transición | Metal post-transición Metalloide Polyatomic nonmetal Diatómico no metálico Gas noble |
Desde que Dimitri Mendeleev formuló la ley periódica en 1871 y publicó una tabla periódica de elementos químicos asociada, los autores han experimentado con distintos tipos de tablas periódicas, incluso con fines didácticos, estéticos o filosóficos.
Anteriormente, en 1869, Mendeleev había mencionado diferentes diseños, incluidas formas cortas, medianas e incluso cúbicas. Le pareció que esta última forma (tridimensional) sería el enfoque más natural, pero que "los intentos de tal construcción no han conducido a ningún resultado real". En las tablas periódicas en espiral, "Mendeleev... se negó rotundamente a representar el sistema como [tal]... Su objeción fue que no podía expresar esta función matemáticamente".
Tipología
En 1934, George Quam, profesor de química en la Universidad de Long Island, Nueva York, y Mary Quam, bibliotecaria de la Biblioteca Pública de Nueva York, compilaron y publicaron una bibliografía de 133 tablas periódicas utilizando una tipología quíntuple: I. corto; II. largo (incluido triangular); III. espiral; IV. helicoidal y V. varios.
En 1952, Moeller expresó su desdén por los numerosos tipos de tabla periódica:
La literatura está repleta de modificaciones sugeridas (y descartadas) de la tabla periódica M. De hecho, han aparecido tantas modificaciones que se siente tentado a concluir que prácticamente todo autor tiene su propio concepto de lo que debe ser un arreglo viable. Desafortunadamente, la mayoría de las tabulaciones propuestas son poco inteligentes o totalmente inútiles, y sólo se han hecho algunas sugerencias valiosas. La geometría no permite un arreglo que sea suficientemente ideal para cumplir todos los propósitos requeridos igualmente bien. Así, los numerosos modelos tridimensionales, que abarcan globos, cálices, conos, prismas, castillos, etc., son interesantes pero carecen de utilidad. En menor medida, los arreglos bidimensionales más involucrados hacen poco para resolver la dificultad, y esencialmente las únicas sugerencias sobre modificaciones que son verdaderamente constructivas son las que se centran en la reflexión de las configuraciones electrónicas.
Ciertamente la más útil de estas modificaciones, y al mismo tiempo una de las primeras que se propone, es la llamada larga o [18-column]...table.
En 1954, Tomkeieff se refirió a los tres tipos principales de tabla periódica: helicoidal, rectilínea y espiral. Añadió que "lamentablemente también hay algunos fenómenos".
En 1974, Edward Mazurs, profesor de química, publicó un estudio y análisis de unas setecientas tablas periódicas que se habían publicado en los cien años anteriores; Reconoció mesas cortas, medianas, largas, helicoidales, espirales, en serie y mesas no clasificadas.
En 1999, Mark Leach, un químico, inauguró la base de datos de Tablas Periódicas de INTERNET. Tiene más de 1200 entradas en mayo de 2023. Si bien la base de datos es una compilación cronológica, los tipos específicos de tablas periódicas que se pueden buscar son las espirales y helicoidales; 3 dimensiones; y varios.
Por conveniencia, las tablas periódicas pueden tipificarse como: 1. cortas; 2. triangular; 3. medio; 4. largo; 5. continuo (circular, espiral, lemniscata o helicoidal); 6. plegado; o 7. espacial. Las tablas que desafían una clasificación fácil se cuentan como tipo 8, sin clasificar.
Corta
(feminine)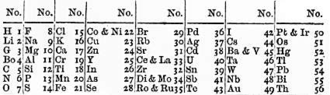


| Metales Alkali Metales de tierra alcalinos Lanthanides Actinides Metales de transición | Metales post-transición Metaloides No metálicos no reclasificados Halógenos Gases nobles |
Las tablas breves tienen alrededor de ocho columnas. Esta forma se hizo popular tras la publicación de la tabla periódica de ocho columnas de Mendeleev en 1871.
También se muestra en esta sección una versión modernizada de la misma tabla.
Mendeleev y otros que descubrieron la periodicidad química en la década de 1860 habían notado que cuando los elementos estaban ordenados por sus pesos atómicos había una repetición aproximada de las propiedades fisicoquímicas después de cada ocho elementos. En consecuencia, Mendeleev organizó los elementos conocidos en ese momento en una tabla con ocho columnas. Usó la tabla para predecir las propiedades de elementos entonces desconocidos. Si bien su tasa de acierto fue inferior al 50%, fueron sus éxitos los que impulsaron la aceptación generalizada de la idea de una tabla periódica de elementos químicos. El estilo de ocho columnas sigue siendo popular hasta el día de hoy, sobre todo en Rusia, el país de nacimiento de Mendeleev.
Un intento anterior de Newlands, un químico inglés, de presentar el meollo de la misma idea a la Sociedad Química de Londres, en 1866, no tuvo éxito; Los miembros eran poco receptivos a las ideas teóricas, como era la tendencia británica en ese momento. Se refirió a su idea como la Ley de las Octavas, y en un momento hizo una analogía con una escala musical de ocho teclas.
John Gladstone, un colega químico, objetó basándose en que la tabla de Newland suponía que no quedaban elementos por descubrir. "En los últimos años se había producido talio, indio, cesio y rubidio, y ahora el hallazgo de uno más echaría por tierra todo el sistema". Creía que había una analogía tan estrecha entre los metales nombrados en la última columna vertical como entre cualquiera de los elementos que se encontraban en la misma línea horizontal.
Su compañero químico inglés Carey Foster preguntó con humor a Newlands si alguna vez había examinado los elementos según el orden de sus letras iniciales. Foster creía que cualquier acuerdo presentaría coincidencias ocasionales, pero condenó aquel que separaba tan lejos el manganeso y el cromo, o el hierro del níquel y el cobalto.
Las ventajas de la corta forma de tabla periódica son su tamaño compacto y que muestra las relaciones entre los principales elementos de grupo y los grupos de metal de transición
Sus desventajas son que parece agrupar elementos disimilares, como cloro y manganeso, juntos; la separación de metales y no metales es difícil de discernir; hay "inconsistencias en la agrupación de elementos que dan iones incoloros y diamagnéticos con elementos que dan iones coloreados y paramagnéticos; y [una] falta de posiciones razonables para el hidrógeno, los elementos de lanthanide, y los iones.
Algunos otros cuadros breves notables incluyen:
- 1862 — Sistema de Meyer: 28 elementos en 6 columnas
- 1895 — Tabla periódica de Retger: Alojamiento intraperiodico de las tierras raras (a)
- 1902 — Mesa de Brauner: Alojamiento intraperiodico de las tierras raras (b)
- 1906 — Mesa de Mendeleev: con seis elementos supuestamente desaparecidos entre H y Él
- 1919 — tabla de Hackh, con 9 columnas en la mitad superior y 11 en la mitad inferior. La posición de un elemento en la tabla determina sus propiedades.
- 1923 — La otra mesa de Deming: Estilo Mendeleev con línea divisoria entre metales y no metales
- 1924 — Gráfico Hubbard de átomos: clásico americano
- 1935 — Mesa de Rysselberghe: bloques separados
- 1945 — mesa de Krafft: Diez grupos
- 1950 — Clasificación de Sidgwick (Mendeleeff): Lanthanides collocated; actinides fragmented
- 1960 — International Mesa de la Corporación Rectificadora: Estilo Arco Iris
- 1975 — Sistema de Shukarev: Los metales de transición se vuelven contra sí mismos
- 2011 — Mesa de Tresvyatskii: Asignación de lanthanides y actinides a grupos
Triangulares
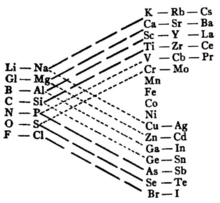

Las tablas triangulares tienen anchos de columna de 2-8-18-32 o más o menos. Bayley proporcionó un ejemplo temprano, que apareció en 1882.
Mediante el uso de líneas de conexión, estas tablas facilitan indicar propiedades análogas entre los elementos.
En cierto modo, representan una forma intermedia entre las tablas cortas y medianas, ya que el ancho promedio de la versión completamente madura (con anchos de 2+8+18+32 = 60) es de 15 columnas.
Uno de los primeros inconvenientes de esta forma fue hacer predicciones de elementos faltantes basándose en consideraciones de simetría. Bayely consideraba, por ejemplo, que los metales de tierras raras eran análogos indirectos de otros elementos como, por ejemplo, el circonio y el niobio, presunción que resultó ser en gran medida infundada.
Las ventajas de esta forma son su atractivo estético y tamaño relativamente compacto; las desventajas son su anchura, el hecho de que es más difícil dibujar, e interpretar ciertas tendencias o relaciones periódicas puede ser más difícil en comparación con el formato rectangular tradicional.
Algunas otras tablas periódicas triangulares notables incluyen:
- 1895 — El arreglo sistemático de Thomsen: Elementos electropositivos y electronegativos etiquetados
- 1911 — tabla de Adán: Separación de lantanoides (izquierda) y radioactivos (derecha)
- 1922 — Sistema de Bohr: Basado en la teoría atómica moderna
- 1935 — Mesa de Zmaczynski: Período 0 arriba H-He
- 1949 — La representación de Antropoff revisada por Fritz Scheele: Lanthanides y actinides incluidos en el cuerpo principal
- 1952 — Mesa de Coryell: Grupos de excavación limitados a 3 y 13
- 1953 — Mesa de Kapustinsky: Electron y neutrones añadidos al período 0; cada período repite una vez. Hay una relación diagonal secundaria entre el neutron (que se descompone a un protón, electron y antineutrino), e hidrógeno.
- 1967 — Mesa de Sanderson: 2-8-10-14 períodos apilados
- 1987 — Forma escalonada del gráfico periódico: Versión modernizada de 1882 Bayley
- 1989 — Mesa de concha de electrones de Seaborg: Hasta Z = 168
- 1995 — mesa de Klein: Se rompe al comienzo de cada nuevo bloque
- 2023 — La versión triangular de Marks de la tabla 1869 de Mendeleyev: El primer nivel tiene elementos sp en lugar de H y Él solo
Medio


| Metales Alkali Metales de tierra alcalinos Lanthanides Actinides Metales de transición | Metales post-transición Metaloides No metálicos no reclasificados Halógenos Gases nobles |
Las tablas medianas tienen alrededor de 18 columnas. Se cree que la popularidad de esta forma se debe a que tiene un buen equilibrio de características en términos de facilidad de construcción y tamaño, y a su representación del orden atómico y las tendencias periódicas.
A la versión de Deming de una tabla mediana, que apareció en la primera edición de su libro de texto de 1923 "General Chemistry: An Elementary Survey Emphasizing Industrial Applications of Fundamental Principles", se le atribuye la popularización de la tabla mediana. Formulario de 18 columnas.
LeRoy se refirió a la tabla de Deming, "ésta...más conocida como la 'forma de dieciocho columnas' como representa "una mejora muy marcada con respecto al tipo original de Mendeleef en lo que respecta a la presentación a las clases principiantes".
Merck and Company preparó un folleto de la tabla de Deming en 1928, que circuló ampliamente en las escuelas estadounidenses. En la década de 1930, su tabla aparecía en manuales y enciclopedias de química. También fue distribuido durante muchos años por Sargent-Welch Scientific Company.
Las ventajas de la forma mediana son que correlaciona las posiciones de los elementos con sus estructuras electrónicas, se adapta a las tendencias verticales, horizontales y diagonales que caracterizan a los elementos; y separa los metales y no metales; sus desventajas son que oscurece las relaciones entre los elementos del grupo principal y los metales de transición.
Algunas otras tablas medianas notables incluyen:
- 1893 — Mesa de 17 columnas de Rang: Forerunner de la moderna mesa de 18 columnas
- 1920 — El arreglo de Stewart: Los lantanoides alojados en sus 18 columnas
- 1945 — Mesa de Seaborg: Se sugirió una serie de actinide para complementar los lanthanides
- 1956 — Forma del período "longo" de Remy: Uranides compitiendo con las actinides de Seaborg
- 1976 — Mesa futurista de Seaborg: Elementos hasta Z = 168
- 1980 — Mesa de Jodogne: Al revés.
- 1990 - IUPAC Mesa del Libro Rojo: 15 bloques
- 2002 — Tabla de químicos inorgánicos: Patrones mayores y menores indicados.
- 2006 — Mesa de Scerri: Simétrica
Largo


Las tablas largas tienen alrededor de 32 columnas. Bassett (1892) da los primeros ejemplos, con 37 columnas dispuestas aunque verticalmente en lugar de horizontalmente; Gooch &erio; Caminante (1905), con 25 columnas; y de Werner (1905), con 33 columnas.
En la primera imagen de esta sección, de la llamada tabla de pasos izquierdo:
- Los grupos 1 y 2 (el bloque) se han trasladado al lado derecho de la tabla.
- El bloque s se desplaza hacia arriba una fila, por lo tanto todos los elementos no en el bloque s ahora son una fila inferior a la tabla estándar. Por ejemplo, la mayoría de la cuarta fila en la tabla estándar es la quinta fila en esta tabla.
- El helio se coloca en el grupo 2 (no en el grupo 18).
Los elementos permanecen posicionados en orden de número atómico (Z).
La mesa con escalón izquierdo fue desarrollada por Charles Janet en 1928, originalmente con fines estéticos. Dicho esto, muestra una correspondencia razonable con la regla de ordenación de energía de Madelung, ya que se trata de una secuencia teórica en la que se llenan las capas de electrones de los átomos neutros en sus estados fundamentales.
Se incluye una forma larga más convencional de tabla periódica para comparar.
La ventaja de la forma larga es que muestra dónde encajan los lantánidos y actínidos en la tabla periódica; su desventaja es su ancho.
Algunas otras tablas largas notables incluyen:
- 1892 — Disposición vertical de Bassett: 37 columnas laterales
- 1905 — Sistema de Gooch & Walker: 25 columnas
- 1905 — Disposición de Werner: 33 grupos
- 1927 — Mesa de LeRoy: precursor de la etapa izquierda; tres conjuntos de elementos de transición
- 1928 — Mesa de paso derecho de Corbino: No hay brechas entre elementos
- 1934 — sistema de Romanoff: Primera forma larga con actinides bajo lanthanides (incluyendo una división d-block)
- 1964 - Ternstrom Una tabla periódica: Un dibujo de mesa de triple combo sobre las ventajas del sistema de bloques completos según Werner (1905) y un sistema de línea Bohr horizontal; el resultado se asemeja a la forma de paso izquierdo de Janet (1928)
- 1982 — Formulario de sistemas de Periodiska rätta: Variación del paso izquierdo con colocación novedosa de H-He
- 2002 — Tabla Periódica de Los Elementos Químicos-Forma Armonica - Sistema A-2 (Mesa Periódica de Elementos Químicos-Forma Armónica): Variación del paso izquierdo en los grupos 1 y 2
- 2018 — Mesa de Beylkin: Mesa simétrica con lantanoides y actinides incorporadas
Continuo
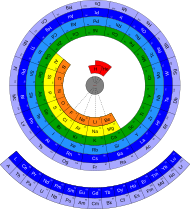
Mesas circulares, espirales, lemniscates o helicales.
La tabla periódica de lemniscatas de Crookes, que se muestra en esta sección, tiene los siguientes elementos, uno debajo del otro:
| H | Él | Li | Gl | B | C | N | O | F | Na | Mg | Al | Si | P | S |
| Cl | Ar | K | Ca | Sc | Ti | V | Cr | Mn·Fe·Ni·Co | Cu | Zn | Ga | Ge | As | Se |
| Br | Kr | Rb | Sr | Yt | Zr | Nb | Mo | Rh·Ru·Pd | Ag | Cd | In | Sn | Sb | Te |
| I | – | Cs | Ba | La | Ce | () | () | () | () | () | () | () | () | () |
| () | – | () | () | () | () | Ta | W | Ir·Pt·Os | () | () | () | () | () | () |
| – | – | – | – | – | Th | – | Ur | – | – | – | – | – | – | – |
La colocación del manganeso con hierro, níquel y cobalto se ve más tarde en la versión modernizada de la tabla de von Bichowsky de 1918, en la sección sin clasificar de este artículo.
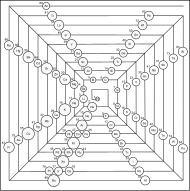 |  |  |
El geólogo francés Alexandre-Émile Béguyer de Chancourtois fue la primera persona en utilizar pesos atómicos para producir una clasificación de periodicidad. Dibujó los elementos como una espiral continua alrededor de un cilindro de metal dividido en 16 partes. El peso atómico del oxígeno se tomó como 16 y se utilizó como estándar con el que se compararon todos los demás elementos. El telurio estaba situado en el centro, lo que provocó el vis tellurique, o tornillo telúrico.
La ventaja de esta forma es que enfatiza, en mayor o menor grado, que los elementos forman una secuencia continua; Dicho esto, las tablas continuas son más difíciles de construir, leer y memorizar que la forma rectangular tradicional de la tabla periódica.
Algunas otras formas notables de tablas periódicas continuas incluyen:
- 1867 — El programa de atomecánica de Hinrichs: Captura muchas de las principales relaciones periódicas que se observan en la mesa moderna, al tiempo que no se rompe con los intentos de mostrar relaciones secundarias
- 1886 — Clasificación natural de Shepard: Forma espiral con instrucciones para convertirla en tubo
- 1905 — La serie primaria, secundaria y terciaria de Gooch & Walker: Una temprana representación de doble periodicidad entre los Ln
- 1914 — Tabla periódica de Hackh: Primera espiral para tener en cuenta los números atómicos de Mosley, y la primera para mostrar sucesivamente pares más grandes de bobinas. También es interesante ya que H se encuentra solo en el centro
- 1925 — Courtines es un modelo de la tabla periódica: Un helix con la apariencia de un submarino o un castillo
- 1939 — tabla periódica de Irwin: Extensive analysis of periodicity patterns
- 1940 — Mesa periódica de la cinta [primera] Gases nobles como grupo 0
- 1965 — Alexander disposición de elementos: Diseñado para complementar el punto en que comienza la educación sobre la disposición de los átomos en un gráfico, tanto como el globo mundial establece la realidad, y para enfatizar la naturaleza vital y conveniente de las proyecciones impresas planas o mapas
- 1999 — Mesa periódica espiral de Moran: En forma hexagonal
- 2003 - galaxia química II: Camino estrellado para unir los elementos, expresar el alcance astronómico de la química, estimular la imaginación y evocar la maravilla en el orden subyacente del universo
- 2010 — Harrison Tabla periódica espiral: La organización de los elementos sigue de cerca la tabla periódica 1923 de H. G. Deming donde se utilizó por primera vez una numeración B para corresponder los óxidos característicos de los grupos 'B' a los de los grupos 'A'.
Plegable

Este tipo de mesas, que incorporan un mecanismo de plegado, son relativamente poco comunes:
- 1895 — Un ejemplo temprano es el modelo 'Flap' de la mesa periódica de David Orme Masson.
- 1915 — William Ramsay, en su libro Los gases de la atmósfera, incluye una tabla periódica con un pliegue (o solapa) que se puede mover de la página 220 a 221.
- 1950 — McCutchon publicó una tabla corta en la que los bloques d y f fueron representados como solapas plegables colocados en la parte superior de los s- y p-blocks.
- 2015 — Tabla periódica plegada cuántica.
- 2016 — Una tabla periódica del paso izquierdo en el estilo tradicional japonés "byobu".
- 2022 — Mesa periódica de hexaflexagon.
Las ventajas de estas tablas son su novedad y que pueden representar relaciones que normalmente requieren tablas periódicas espaciales, pero conservan la portabilidad y conveniencia de las tablas bidimensionales. Una desventaja es que su construcción requiere un esfuerzo marginalmente mayor.
Espacial

Las tablas espaciales pasan por tres o más dimensiones (las tablas helicoidales se clasifican en cambio como tablas continuas). Estas mesas son relativamente específicas y no se utilizan con tanta frecuencia como las mesas tradicionales. Si bien ofrecen ventajas únicas, su complejidad y requisitos de personalización los hacen más adecuados para investigación especializada, educación avanzada o áreas de estudio específicas donde se desea una comprensión más profunda de las relaciones multidimensionales.
Las ventajas de los cuadros periódicos de tres o más dimensiones son:
- Visualización mejorada. Estas tablas proporcionan una visualización única y mejorada de los elementos y sus propiedades. Al incorporar dimensiones adicionales, como profundidad o ejes múltiples, estos cuadros ofrecen una representación más completa de las tendencias y relaciones periódicas entre los elementos. Pueden proporcionar una comprensión más rica de patrones complejos e interacciones.
- Inclusión de propiedades extra: Las tablas periódicas tradicionales suelen centrarse en algunas propiedades clave, como el número atómico y el peso atómico. Sin embargo, las tablas periódicas de tres o más dimensiones tienen el potencial de incluir propiedades adicionales, como electronegatividad, energía de ionización, afinidad de electrones, o propiedades físicas como punto de ebullición o punto de fusión. Esta información ampliada puede ofrecer una imagen más completa de los elementos y sus características.
- Exploración de las tendencias de alto nivel: Tales tablas pueden facilitar la exploración de tendencias y relaciones de alto nivel que pueden no ser aparentes en tablas bidimensionales tradicionales. Permiten la visualización de patrones complejos que emergen cuando se consideran simultáneamente múltiples propiedades o variables. Esto puede ayudar a descubrir conexiones ocultas y correlaciones entre los elementos.
- Flexibilidad y personalización: Tablas periódicas de tres o más dimensiones ofrecen flexibilidad en términos de su diseño y personalización. Los investigadores, educadores o científicos pueden adaptar las dimensiones y propiedades representadas en función de sus necesidades y objetivos específicos. Esta adaptabilidad permite adaptar la tabla para centrarse en áreas específicas de interés o investigación.
Las desventajas son:
- Complexity: A medida que aumenta el número de dimensiones, aumenta la complejidad de interpretar y comprender la tabla. Puede ser más difícil para los individuos captar y visualizar las relaciones entre elementos, especialmente cuando se incorporan múltiples propiedades. La naturaleza intrincada de estos cuadros puede requerir esfuerzos adicionales y familiaridad para navegar e interpretar eficazmente.
- Dificultad en la representación: La detección de tendencias y relaciones periódicas en tres o más dimensiones puede ser técnicamente difícil. Diseñar y visualizar la tabla de manera clara y coherente puede requerir software o herramientas especializadas. La complejidad de estas tablas puede hacerlas menos accesibles para personas que no están familiarizadas con las técnicas específicas de representación o visualización utilizadas.
- Sobrecarga de información: La inclusión de múltiples dimensiones y propiedades puede llevar a la sobrecarga de información, especialmente si la tabla no está diseñada de manera fácil y organizada. Se vuelve crucial para organizar y presentar eficazmente los datos para evitar usuarios abrumadores con detalles excesivos. El equilibrio entre la información completa y la claridad puede ser un reto importante.
- Falta de estandarización: Las tablas periódicas de tres o más dimensiones no son tan estandarizadas o ampliamente reconocidas como tablas bidimensionales tradicionales. Esta falta de estandarización puede crear confusión e inconsistencia en diferentes representaciones. También puede hacer más difícil comparar y comunicar información entre diferentes formatos de tablas periódicas.
Algunas otras tablas periódicas espaciales notables incluyen:
- 1920 — Sistema de Kohlweiler: Primer sistema espacial: Planos paralelos conectados por pilares de grupo de transición y elemento lantanoide
- 1925 — La esfera periódica del amigo: Primera forma esférica
- 1945 — Clasificación gnomónica de Talpain de los elementos: Diagrama en el espacio con la forma de una doble pirámide
- 1949 — Sistema Laminado de Wringley: Primer híbrido 2D/3D
- 1954 — Modelo volumétrico de Sabo & Lakatosh de la tabla periódica: Forma compleja de construcción de apartamentos modulares
- 1965 — Mesa periódica de Giguère: Forma de la furgoneta meteorológica
- 1972 — Mesa periódica octogonal prismática
- 1982 — Cement chemist's periodic cube
- 1983 - pirámide periódica
- 1989 - Stowe's Tabla periódica de un físico: 4-dimensional
- 1990 — Árbol periódico de Dufour
- 1992 — Tabla periódica tridimensional de Magarshak " Malinsky: Tabla de mecánica cuántica con el grupo 3 como Sc-Y-La-Ac
- 2003 - Representaciones gráficas del sistema periódico: Como edificio
- 2003 — Mesa periódica de la pirámide de dos hilos
- 2011 — Aldersley 3D mesa periódica: Como cuatro apartamentos
- 2014 — ADOMAH Cubo de vidrio de mesa periódica: Una mesa separada dentro de un tetraedro dentro de un cubo
- 2019 — La periodicidad elemental de Grainger con la formulación "esferas concéntricas que intersectan planos ortogonales": Una mesa en o en la esquina de una habitación o mesa
Sin clasificar

Las tablas periódicas sin clasificar desafían la clasificación fácil:
- 1891 — Wendt's generation-tree of the elements
- 1893 - Los conos truncados de Nechaev
- 1907 — Agrupación de los elementos para ilustrar la reactividad: Corridas del grupo 12 a la izquierda al grupo 13 a la derecha
- 1918 — Cherkesov: Dos cuadros periódicos: Mn en el grupo 8 en lugar del grupo 7
- 1920 — El arreglo de Stewart de los elementos: Con 14 lantanoides incorporados
- 1934 — sistema de Romanoff: Combinado espiral-lemniscate
- 1944 — Sistema de árboles de Müller
- 1950 — Tabla periódica actualizada de Clark: Sistema de arena
- 1971 — Clark, John O.E. periodic table
- 2005 — El gráfico periódico de Rich expone las relaciones diagonales: No metales de la izquierda; metales a la derecha
- 2018 — Mesa periódica de Beylkin de los elementos:4n2 períodos, donde n = 2,3... y muestra simetría, regularidad y elegancia, más que la tabla de paso izquierda de Janet
- 2019 — Alexander arreglo desenrollado... y reelaborado: p, d y f bloques que se alejan del bloque s en espacio tridimensional
- 2023 — Tabla periódica de Deming 1923, actualizada: 25 columnas de ancho
- 2023 — Yin Yang periodic table: Fusión de la mesa redonda izquierda y la mesa tradicional
Galería
- ADOMAH (long)
- Cinta curvada (continua)
- Cuatro bucles (continua)
- Distorsión parcial (no clasificada)
- Columnas cortas (9/11)
- Notas cortas (9/11 columnas)
- Spiral
- Ziggurat (sin clasificar)
- Notas de Ziggurat
- 4D Stowe-Scerri (espacial)