Syn y anti adición
En química orgánica, sin y antiadición son formas diferentes en las que se pueden agregar moléculas sustituyentes a un alqueno ( R2C=CR2) o alquino (RC≡CR). Los conceptos de sin y anti adición se utilizan para caracterizar las diferentes reacciones de la química orgánica al reflejar la estereoquímica de los productos en una reacción.

El tipo de adición que ocurre depende de múltiples factores diferentes de una reacción y se define por la orientación final de los sustituyentes en la molécula original. La adición syn y anti están relacionadas con la regla de Markovnikov para la orientación de una reacción, que se refiere a la preferencia de enlace de diferentes sustituyentes por diferentes carbonos en un alqueno o alquino. Para que una reacción siga la regla de Markovnikov, el carbocatión intermedio del mecanismo de una reacción debe estar en el carbono más sustituido, permitiendo que el sustituyente se enlace al carbocatión más estable y al carbono más sustituido.

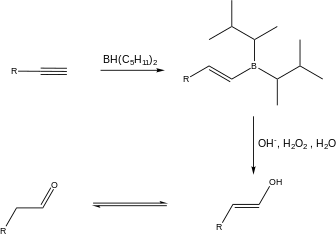
La adición syn es la adición de dos sustituyentes al mismo lado (o cara) de un doble enlace o triple enlace, lo que da como resultado una disminución en el orden de los enlaces pero un aumento en el número de sustituyentes. Generalmente el sustrato será un alqueno o alquino. Un ejemplo de adición sintética sería la oxidación de un alqueno a un diol mediante un agente oxidante adecuado como el tetróxido de osmio, OsO4 , o permanganato de potasio, KMnO4.
La antiadición contrasta directamente con la adición syn. Además, se agregan dos sustituyentes a lados (o caras) opuestos de un doble enlace o triple enlace, lo que nuevamente resulta en una disminución en el orden de los enlaces y un aumento en el número de sustituyentes. El ejemplo clásico de esto es la bromación (cualquier halogenación) de alquenos. Una reacción antiadición da como resultado un isómero trans de los productos, ya que los sustituyentes están en caras opuestas del enlace.
Dependiendo del doble enlace del sustrato, la adición puede tener diferentes efectos en la molécula. Después de la adición a un alqueno de cadena lineal como el eteno (C2H4), el alcano resultante rotará rápida y libremente alrededor de su enlace sigma único en condiciones normales (es decir, temperatura ambiente). Por lo tanto, si los sustituyentes se agregan al mismo lado (syn) o a los lados opuestos (anti) de un doble, generalmente se puede ignorar debido a la libre rotación. Sin embargo, si es necesario tener en cuenta la quiralidad o la orientación absoluta específica de los sustituyentes, es importante conocer el tipo de adición. A diferencia de los alquenos de cadena lineal, la adición sintética de cicloalqueno permite la adición estable de sustituyentes al mismo lado del anillo, donde permanecen juntos. La estructura de anillo bloqueado cíclico evita la rotación libre.
Laeliminación de syn y la antieliminación son los procesos inversos de la adición de syn y anti. Estos dan como resultado un nuevo doble enlace, como en la eliminación de Ei.