Suelo alcalino
Los suelos alcalinos o alcalinos son suelos arcillosos con un pH elevado (superior a 8,5), una estructura pobre y una capacidad de infiltración baja. A menudo tienen una capa calcárea dura a una profundidad de 0,5 a 1 metro. Los suelos alcalinos deben sus propiedades físico-químicas desfavorables principalmente a la presencia dominante de carbonato de sodio, que hace que el suelo se hinche y sea difícil de clarificar/asentar. Su nombre deriva del grupo de elementos metálicos alcalinos, al que pertenece el sodio, y que puede inducir basicidad. A veces, estos suelos también se denominan suelos sódicos alcalinos. Los suelos alcalinos son básicos, pero no todos los suelos básicos son alcalinos.
Causas
Las causas de la alcalinidad del suelo pueden ser naturales o provocadas por el hombre:
- La causa natural es la presencia de minerales de suelo que producen carbonato de sodio (Na2CO3) y bicarbonato de sodio (NaHCO)3Con el tiempo.
- Calderas de carbón / centrales eléctricas, al usar carbón o lignito rico en piedra caliza, producen ceniza que contiene óxido de calcio. CaO se disuelve fácilmente en el agua para formar lima azotada, Ca(OH)2, y llevado por agua de lluvia a ríos / agua de riego. El proceso de suavidad de limón precipita Ca2+ and Mg2+ iones / elimina la dureza en el agua y también convierte bicarbonatos de sodio en agua del río en carbonato de sodio. Carbonatos de sodio (lavado de soda) reacciona con el Ca restante2+ and Mg2+ en el agua para eliminar / precipitar la dureza total. También las sales de sodio solubles en agua presentes en la ceniza aumentan el contenido de sodio en el agua. El consumo mundial de carbón en el mundo fue de 7.700 millones de toneladas en el año 2011. Así el agua del río se hace desprovista de Ca2+ and Mg2+ iones y Na mejorado+ por calderas de carbón.
- Muchas sales de sodio se utilizan en aplicaciones industriales y domésticas como carbonato de sodio, bicarbonato de sodio (sodio de sodio), sulfato de sodio, hidróxido de sodio (sodio caótico), hipoclorito de sodio (polvo de blanqueamiento), etc. en cantidades enormes. Estas sales se producen principalmente con cloruro de sodio (sal común). Todo el sodio en estas sales entra en el río / agua subterránea durante su proceso de producción o consumo mejorando la sodicidad del agua. El consumo mundial total de cloruro de sodio es de 270 millones de toneladas en el año 2010. Esto es casi igual a la carga de sal en el poderoso río Amazonas. La contribución de las sales de sodio es casi el 7% de la carga total de sal de todos los ríos. El problema de la carga salada de sodio se agrava en la corriente baja de cuencas fluviales intensamente cultivadas ubicadas en China, India, Egipto, Pakistán, Asia occidental, Australia, Estados Unidos occidental, etc. debido a la acumulación de sales en el agua restante después de haber encontrado varias pérdidas de transpiración y evaporación.
- Otra fuente de sal de sodio hecha por el hombre además de los campos agrícolas / masa terrestre está en las proximidades de las torres de refrigeración húmeda utilizando agua de mar para disipar el calor de desecho generado en diversas industrias situadas cerca de la costa del mar. En las refinerías de petróleo, los complejos petroquímicos, las plantas de fertilizantes, las plantas químicas, las centrales nucleares y térmicas, los sistemas centralizados de HVAC, etc. Las gotas de deriva / finas emitidas de las torres de refrigeración contienen casi el 6% de cloruro de sodio que se depositaría en las zonas circundantes. Este problema agrava cuando las normas nacionales de control de la contaminación no se imponen o no se aplican para minimizar las emisiones de deriva a la mejor norma industrial para las torres de refrigeración húmeda basadas en el agua marina.
- La causa hecha por el hombre es la aplicación de agua suavizada en riego (agua superficial o subterránea) que contiene una proporción relativamente alta de bicarbonatos de sodio y menos calcio y magnesio.
Problemas agrícolas
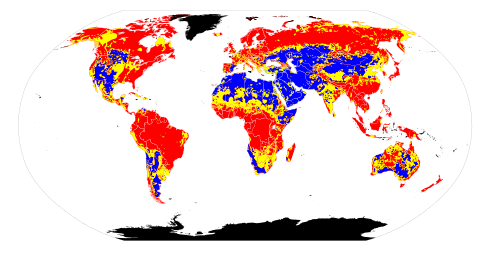
Los suelos alcalinos son difíciles de incorporar a la producción agrícola. Debido a su baja capacidad de infiltración, el agua de lluvia se estanca fácilmente en el suelo y, en épocas secas, el cultivo es prácticamente imposible sin abundante agua de riego y un buen drenaje. La agricultura se limita a cultivos tolerantes al encharcamiento superficial (por ejemplo, arroz, pasto) y la productividad es menor.
Química
La alcalinidad del suelo está asociada con la presencia de carbonato de sodio (Na2CO3) o bicarbonato de sodio (NaHCO3) en el suelo, ya sea como resultado de la erosión natural de las partículas del suelo o traída por el riego y/o el agua de inundación.
Esta sal es extremadamente soluble, cuando sufre hidratación se disocia en:
- Na
2CO
3 → 2 Na+
+ CO2 - 2
3
El anión carbonato CO2−
3, es una base débil que acepta un protón, por lo que se hidroliza en agua para dar el ion bicarbonato y un ion hidroxilo:
- CO2 - 2
3 + H
2O → HCO−
3 + Oh.−
que a su vez da ácido carbónico e hidroxilo:
- HCO−
3 + H
2O → H
2CO
3 + Oh.−
Véase carbonato para el equilibrio de carbonato-bicarbonato-dióxido de carbono.
Las reacciones anteriores son similares a la disolución del carbonato de calcio, siendo la solubilidad de las dos sales la única diferencia. El Na2CO3 es aproximadamente 78000 veces más soluble que el CaCO3, por lo que puede disolver cantidades mucho mayores de CO2−
3, aumentando así el pH a valores superiores a 8,5, que está por encima del pH máximo alcanzable cuando el equilibrio entre el carbonato de calcio y el dióxido de carbono disuelto está en equilibrio en la solución del suelo.
- Notas:
- Agua (H2O) se disocia parcialmente en H3O+ (hidronio) y OH– iones. El ion H3O+ tiene una carga eléctrica positiva (+) y su concentración se escribe generalmente como [H+]. El hidroxil ion OH– tiene una carga negativa (−) y su concentración se escribe como [OH−].
- En agua pura, a 25 °C, la constante de disociación del agua (Kw) es 10−14.
Desde Kw [H]+[OH]–], entonces ambos la concentración de H3O+ y OH– iones iguales 10−7 M (una concentración muy pequeña). - En el agua neutral, el pH, siendo el logaritmo decimal negativo del H3O+ concentración, es 7. Del mismo modo, el pOH es también 7. Cada unidad de disminución en pH indica un aumento diez veces mayor del H3O+ concentración. Del mismo modo, cada aumento del pH indica un aumento diez veces mayor de la OH– concentración.
- En el agua con sales disueltas, las concentraciones de H3O+ y la OH– iones pueden cambiar, pero su suma permanece constante, es decir, 7 + 7 = 14. Por lo tanto, un pH de 7 corresponde a un pOH de 7, y un pH de 9 con un pOH de 5.
- Formalmente se prefiere expresar las concentraciones de iones en términos de actividad química, pero esto apenas afecta el valor del pH.
- Agua con exceso de H3O+ iones se llama ácido (pH), y agua con exceso OH– iones se llama alcalino o más bien básico (pH Ø 7). Humedad de suelo con pH se llama muy ácido y con pH Ø 10 muy alcalino (básico).
No todo el carbonato de sodio disuelto experimenta la reacción química mencionada anteriormente. El carbonato de sodio restante, y por lo tanto la presencia de iones CO2−
3, hace que el CaCO3 (que es solo ligeramente soluble) precipite como carbonato de calcio sólido (caliza), porque el producto de los iones CO2−
3 y la concentración de Ca2+ excede el límite permitido. Por lo tanto, los iones de calcio Ca2+ quedan inmovilizados.

La presencia de abundantes iones Na+ en la solución del suelo y la precipitación de iones Ca2+ como mineral sólido hace que las partículas de arcilla, que tienen cargas eléctricas negativas a lo largo de sus superficies, adsorban más Na+ en la zona de adsorción difusa (ZAD, también llamada más comúnmente doble capa difusa (DDL), o doble capa eléctrica (EDL), ver figura correspondiente) y, a cambio, liberen Ca2+ previamente adsorbido, con lo que aumenta su porcentaje de sodio intercambiable (PSI) como se ilustra en la misma figura.
El Na+ es más móvil y tiene una carga eléctrica menor que el Ca2+, por lo que el espesor de la capa DDL aumenta a medida que más iones de sodio la ocupan. El espesor de la capa DDL también está influenciado por la concentración total de iones en la humedad del suelo, en el sentido de que concentraciones más altas hacen que la zona DDL se encoja.Las partículas de arcilla con un ESP considerable (> 16), en contacto con la humedad del suelo no salino, presentan una zona DDL expandida y el suelo se hincha (dispersa). El fenómeno produce un deterioro de la estructura del suelo y, especialmente, la formación de una costra y compactación de la capa superior. Por lo tanto, se reduce la capacidad de infiltración del suelo y la disponibilidad de agua en el suelo, mientras que aumenta el anegamiento o la escorrentía superficial. La emergencia de las plántulas y la producción de cultivos se ven gravemente afectadas.
- Nota:
- En condiciones salinas, los muchos iones de la solución del suelo contrarrestan la hinchazón del suelo, por lo que los suelos salinos generalmente no tienen propiedades físicas desfavorables. Los suelos alcalinos, en principio, no son salinos ya que el problema de la alcalinidad es peor ya que la salinidad es menor.
Los problemas de alcalinidad son más pronunciados en los suelos arcillosos que en los francos, limosos o arenosos. Los suelos arcillosos que contienen montmorillonita o esmectita (arcillas expansivas) están más sujetos a problemas de alcalinidad que los suelos arcillosos de illita o caolinita. La razón es que los primeros tipos de arcilla tienen mayores áreas superficiales específicas (es decir, el área superficial de las partículas del suelo dividida por su volumen) y una mayor capacidad de intercambio catiónico (CIC).
- Nota:
- Ciertos minerales de arcilla con casi el 100% ESP (es decir, casi totalmente saturados de sodio) se llaman bentonita, que se utiliza en la ingeniería civil para colocar cortinas impermeables en el suelo, por ejemplo debajo de las presas, para prevenir la véase el agua.
La calidad del agua de riego en relación con el riesgo de alcalinidad se expresa mediante los dos índices siguientes:
- The sodium adsorption ratio (SAR,)
La fórmula para calcular la relación de adsorción de sodio es:
- SAR = [Na+]/√[Caso]2+/2 + Mg2+/2] = #Na+/23}/√{Ca2+/40 + Mg2+/24}
- El carbonato de sodio residual (RSC, meq/L):
La fórmula para calcular el carbonato residual de sodio es:
RSC =HCO−
3 + CO2 - 2
3[Ca]2+ + Mg2+]=HCO−
3/61 + CO2 - 2
3/30} - {Ca2+/20 + Mg2+/12}que no debe ser mucho más alto que 1 y preferiblemente menos de 0.5.
La expresión anterior reconoce la presencia de bicarbonatos (HCO−
3), la forma en que la mayoría de carbonatos se disuelven.
Al calcular el SAR y el RSC, se debe tener en cuenta la calidad del agua presente en la zona de la raíz del cultivo, lo que tendría en cuenta el factor de lixiviación en el campo. La presión parcial de CO2 disuelto en la zona de la raíz de las plantas también determina el calcio presente en forma disuelta en el agua del campo. El USDA sigue el SAR ajustado para calcular la sodicidad del agua.
Mejora del suelo
Los suelos alcalinos con CaCO3 sólido se pueden recuperar con cultivos de pasto, abono orgánico, restos de pelos y plumas, basura orgánica, papel usado, limones y naranjas desechados, etc., lo que garantiza la incorporación de mucho material acidificante (material inorgánico u orgánico) al suelo y mejora el Ca disuelto en el agua del campo mediante la liberación de gas CO2. También ayuda el arado profundo y la incorporación del subsuelo calcáreo a la capa superior del suelo.
Muchas veces, la migración de sales a la capa superior del suelo se produce desde fuentes de agua subterráneas en lugar de fuentes superficiales. Cuando el nivel freático es alto y la tierra está expuesta a una alta radiación solar, el agua subterránea rezuma a la superficie de la tierra debido a la acción capilar y se evapora dejando las sales disueltas en la capa superior del suelo. Cuando el agua subterránea contiene mucha sal, se produce un problema agudo de salinidad. Este problema se puede reducir aplicando mantillo a la tierra. También se recomienda el uso de invernaderos o redes de sombra durante el verano para cultivar verduras/cultivos para mitigar la salinidad del suelo y conservar el agua/humedad del suelo. Los invernaderos filtran la intensa radiación solar del verano en los países tropicales para proteger a las plantas del estrés hídrico y las quemaduras de las hojas.
Cuando la calidad del agua subterránea no es alcalina/salina y el nivel freático es alto, la acumulación de sales en el suelo se puede evitar utilizando la tierra durante todo el año para el cultivo de árboles o cultivos permanentes con la ayuda del riego por aspersión. Cuando el agua subterránea se utiliza con el factor de lixiviación requerido, las sales en el suelo no se acumulan.
También se aconseja arar el campo poco después de cortar el cultivo para evitar la migración de sales a la capa superior del suelo y conservar la humedad del mismo durante los intensos meses de verano. Esto se hace para romper los poros capilares del suelo y evitar que el agua llegue a la superficie del mismo.
Los suelos arcillosos en áreas con una alta precipitación anual (más de 100 cm) no suelen sufrir de alta alcalinidad, ya que la escorrentía del agua de lluvia puede reducir/lixiviar las sales del suelo a niveles confortables si se siguen los métodos adecuados de recolección de agua de lluvia. En algunas áreas agrícolas, se utilizan "líneas de tejas" subterráneas para facilitar el drenaje y lixiviar las sales. El riego por goteo continuo conduciría a la formación de suelos alcalinos en ausencia de agua de lixiviación/drenaje del campo.
También es posible recuperar suelos alcalinos añadiendo minerales acidificantes como pirita o alumbre o sulfato de aluminio, que son más económicos.
Alternativamente, yeso (sulfato de calcio, CaSO
4 · 2 H
2O) también se puede aplicar como una fuente de iones Ca2+ para reemplazar el sodio en el complejo de intercambio. El yeso también reacciona con el carbonato de sodio para convertirse en sulfato de sodio, que es una sal neutra y no contribuye al pH alto. Debe haber suficiente drenaje natural hacia el subsuelo, o bien debe estar presente un sistema de drenaje subterráneo artificial, para permitir la lixiviación del exceso de sodio por percolación de la lluvia y/o agua de riego a través del perfil del suelo.
El cloruro de calcio también se utiliza para recuperar suelos alcalinos. El CaCl2 convierte el Na2CO3 en NaCl, precipitando CaCO3. El NaCl se drena mediante el agua de lixiviación. El nitrato de calcio tiene un efecto similar, con NaNO3 en el lixiviado. El ácido usado (HCl, H2SO4, etc.) también se puede utilizar para reducir el exceso de Na2CO3 en el suelo o el agua.
Cuando la urea está disponible a bajo precio para los agricultores, también se utiliza principalmente para reducir la alcalinidad/salinidad del suelo. El catión amonio (NH+
4) producido por la hidrólisis de la urea, que es un catión fuertemente adsorbente, intercambia con el catión Na+ débilmente adsorbente de la estructura del suelo y el Na+ se libera al agua. Por lo tanto, los suelos alcalinos adsorben/consumen más urea en comparación con otros suelos.
Para recuperar completamente los suelos se necesitan dosis prohibitivamente altas de enmiendas. Por lo tanto, la mayoría de los esfuerzos se dirigen a mejorar solo la capa superior (por ejemplo, los primeros 10 cm de los suelos), ya que la capa superior es la más sensible al deterioro de la estructura del suelo. Sin embargo, los tratamientos deben repetirse en unos pocos años (por ejemplo, 5). Los árboles / plantas siguen el gravitropismo. Es difícil sobrevivir en suelos alcalinos para los árboles con un sistema de raíces más profundo, que puede tener más de 60 metros de profundidad en buenos suelos no alcalinos.
Será importante evitar el riego (subterráneo o superficial) con agua de mala calidad. En viticultura, se ha sugerido añadir al agua de riego agentes quelantes naturales como el ácido tartárico para solubilizar los carbonatos de calcio y magnesio en suelos sódicos.
Una forma de reducir el carbonato de sodio es cultivar plantas de salicornia, salicornia o barrilla. Estas plantas secuestran el carbonato de sodio que absorben del suelo alcalino en sus tejidos. La ceniza de estas plantas contiene una buena cantidad de carbonato de sodio que se puede extraer comercialmente y utilizar en lugar del carbonato de sodio derivado de la sal común, que es un proceso que consume mucha energía. De este modo, el deterioro de las tierras alcalinas se puede controlar cultivando plantas de barrilla que pueden servir como fuente de alimento, combustible de biomasa y materia prima para carbonato de sodio y potasa, etc.
Principales suelos sódicos salinos
Los suelos salinos son en su mayoría también sódicos (la sal predominante es el cloruro de sodio), pero no tienen un pH muy alto ni una tasa de infiltración deficiente. Al lixiviarse, por lo general no se convierten en un suelo alcalino (sódico), ya que los iones Na+ se eliminan fácilmente. Por lo tanto, los suelos salinos (sódicos) en su mayoría no necesitan aplicaciones de yeso para su recuperación.
Remediación y utilización a través de la acuicultura
Desde la década de 1990, se han llevado a cabo investigaciones y experimentos en China y otros lugares para la recuperación y utilización de tierras alcalinas mediante prácticas combinadas de agricultura y acuicultura, con un éxito considerable y un aumento de la experiencia. La tecnología de acuicultura que utiliza aguas salinas y alcalinas continentales para la producción de mariscos está madurando y abarca una amplia gama de especies de mariscos, incluidos camarones, cangrejos, mariscos y peces como la lubina y el mero.
En los últimos años, el Ministerio de Agricultura y Asuntos Rurales de China ha recomendado la acuicultura (o acuicultura en tierras salinas y alcalinas) como un modelo exitoso para la transformación y utilización de tierras salinas y alcalinas. La FAO señaló en un boletín reciente que las tierras alcalinas son un área en la que existen formas innovadoras y oportunidades para la expansión de la acuicultura.
Véase también
- Amoníaco volatilización de urea
- Agreti verde vegetal
- Barilla
- Biosalinidad
- Capacidad de intercambio
- riego por goteo
- Impacto ambiental del riego
- Fertilizante
- Halotolerance
- Índice de artículos relacionados con el suelo
- Manura orgánica rica en fosfato
- Phosphogypsum
- Lodo rojo
- Índice de carbonato sódico residual
- Sajji Khar
- Lago Soda
- fertilidad del suelo
- PH de suelo
- Salinidad del suelo
- Control de salinidad del suelo
Referencias
- ^ a b Gestión de la calidad del agua de riego, Universidad Estatal de Oregon, EE.UU., Consultado el 2012-10-04.
- ^ "Ablandamiento de la preparación, GE Power & Water". Archivado desde el original el 24 de enero de 2013. Retrieved 11 de octubre 2012.
- ^ J. Keller, A. Keller y G. Davids. "Fases de desarrollo de cuencas y implicaciones de cierre" (PDF). Archivado desde el original (PDF) el 19 de octubre de 2013. Retrieved 25 de agosto 2012.
- ^ "Guía de torre de refrigeración húmeda para materia de partículas, Medio Ambiente Canadá". 25 noviembre 2008. Retrieved 2013-01-29.
- ^ a b c Manual del laboratorio de salinidad de EE.UU. 60
- ^ a b G.H. Bolt (ed.), 1981. Química del suelo: A. elementos básicos. Vol 5a, Elsevier, Amsterdam, Holanda
- ^ "Capítulo 11: Calidad del agua". Manual de gestión de la salinidad (Informe). Gobierno de Queensland. 19 de diciembre de 2013. p. 85.
- ^ Lesch S. M. y SuárezD. L. "Una nota corta para calcular el índice SAR ajustado". Archivado desde el original el 8 de abril de 2013. Retrieved 5 de octubre 2012.
- ^ a b c Chhabra, R. 1996. Soil Salinity and Water Quality. 284 pp. Oxford & IBH Publishing Co. Pvt. Ltd., New Delhi (South Asian edition) and A.A. Balkema Uitgevers BC, Rotterdam (edition elsewhere). ISBN 81-204-1049-1.
- ^ "Evaluación del riesgo de salinidad para la Región Queensland Murray-Darling (véase el apéndice-2), Departamento de Medio Ambiente y Gestión de Recursos de Queensland" (PDF). Archivado desde el original (PDF) on 2013-04-10. Retrieved 29 de octubre 2012.
- ^ I.P. Abrol, J.S.P. Yadav y F.I. Massoud. "Salt-Affected Soils and their Management, refer para 4.7". Retrieved 23 de diciembre 2012.
- ^ Ashworth, J. 2007. El efecto de los agentes chelativos en la sodicidad del suelo. Contaminación del suelo y del sedimento 16: 301-312.
- ^ Farooq Ahmad. "Crecimiento de hierba de Karnal / Kallar en suelos alcalinos sódicos en Pakistán" (PDF). Retrieved 22 de enero 2013.
- ^ Estudio de caso Chacupe
- ^ a b "conseguir" ################################################################################################################################################################################################################################################################. 2023-06-29. Retrieved 2024-01-20.
- ^ a b "Pond Aquaculture in Waterlogged Salt-Alkali Land". Springer2023-04-05.
- ^ "La Estrategia de Estado y Desarrollo actual para la Pesca Saline-Alkaline de China". Estudio estratégico de CAE (en chino). 2016. doi:10.15302/J-SSCAE-2016.03.012. ISSN 1009-1742. Wikidata Q124547052.
- ^ ⋅春 (2023-09-26). "justificador". Retrieved 2024-02-14.
- ^ "actualizar." China News Service. 2023-12-04. Retrieved 2024-02-16.
- ^ "justo de la píldora 2022." 中文 parecía haber conseguido. 2023-02-14. Retrieved 2024-01-16.
- ^ "China: Utilizando recursos hídricos en tierras salinas-alcalinas para la agricultura y la pesca". tridge.com. 2021-12-18. Retrieved 2024-01-21.
- ^ "FAO Aquaculture News, 2023 de junio" (PDF). FAO. 2023-06-01. Retrieved 2024-01-21.
