Sitio CPG
Los sitios CpG o sitios CG son regiones de ADN donde un nucleótido de citosina es seguido por un nucleótido de guanina en la secuencia lineal de bases a lo largo de su 5' → 3' dirección. Los sitios CpG ocurren con alta frecuencia en regiones genómicas llamadas islas CpG (o islas CG).
Las citosinas en los dinucleótidos CpG se pueden metilar para formar 5-metilcitosinas. Las enzimas que agregan un grupo metilo se llaman ADN metiltransferasas. En los mamíferos, del 70% al 80% de las citosinas CpG están metiladas. La metilación de la citosina dentro de un gen puede cambiar su expresión, un mecanismo que forma parte de un campo más amplio de la ciencia que estudia la regulación génica que se llama epigenética. Las citosinas metiladas a menudo mutan a timinas.
En humanos, aproximadamente el 70 % de los promotores ubicados cerca del sitio de inicio de la transcripción de un gen (promotores proximales) contienen una isla CpG.
Características de CpG
Definición
CpG es la abreviatura de 5'—C—fosfato—G—3' , es decir, citosina y guanina separadas por un solo grupo fosfato; el fosfato une dos nucleósidos cualesquiera en el ADN. La notación CpG se utiliza para distinguir esta secuencia lineal monocatenaria del apareamiento de bases CG de citosina y guanina para secuencias de doble cadena. Por lo tanto, la notación CpG debe interpretarse como que la citosina es 5 prima con respecto a la base de guanina. CpG no debe confundirse con GpC, lo último significa que una guanina es seguida por una citosina en el 5' → 3' dirección de una secuencia monocatenaria.
Subrepresentación causada por una alta tasa de mutación
Durante mucho tiempo se han observado dinucleótidos de CpG que ocurren con una frecuencia mucho menor en la secuencia de genomas vertebrados de lo que se esperaría debido a posibilidades aleatorias. Por ejemplo, en el genoma humano, que tiene un contenido de 42% GC, se espera que ocurra un par de nucleótidos compuestos de citosina seguida de guanina. 0.21× × 0.21=4.41% % {displaystyle 0.21times 0.21=4.41%} de la época. La frecuencia de los dinucleótidos CpG en los genomas humanos es inferior a la quinta parte de la frecuencia esperada.
Esta subrepresentación es una consecuencia de la alta tasa de mutación de los sitios CpG metilados: la desaminación espontánea de una citosina metilada da como resultado una timina, y las bases incompatibles G:T resultantes a menudo se resuelven incorrectamente en A:T; mientras que la desaminación de la citosina no metilada da como resultado un uracilo, que como base extraña se reemplaza rápidamente por una citosina mediante el mecanismo de reparación por escisión de la base. La tasa de transición de C a T en los sitios CpG metilados es aproximadamente 10 veces mayor que en los sitios no metilados.
Distribución genómica
Los dinucleótidos CpG se encuentran con frecuencia en islas CpG (consulte la definición de islas CpG, a continuación). Hay 28.890 islas CpG en el genoma humano (50.267 si se incluyen islas CpG en secuencias repetidas). Esto está de acuerdo con las 28.519 islas CpG encontradas por Venter et al. desde Venter et al. La secuencia del genoma no incluía los interiores de elementos repetitivos muy similares y las regiones repetidas extremadamente densas cerca de los centrómeros. Dado que las islas CpG contienen múltiples secuencias de dinucleótidos CpG, parece haber más de 20 millones de dinucleótidos CpG en el genoma humano.
Islas CpG
Las islas CpG (o islas CG) son regiones con una alta frecuencia de sitios CpG. Aunque las definiciones objetivas para las islas CpG son limitadas, la definición formal habitual es una región con al menos 200 bp, un porcentaje de GC superior al 50%, y una proporción de CpG observada a expansión superior al 60%. La relación de CpG observada puede derivarse cuando se calcula que: ()Número deCpGs){displaystyle ({text{number of }CpGs)} y las expectativas ()Número deCAlternativa Alternativa Número deG)/longitud de la secuencia{displaystyle ({text{number of }}C*{text{number of }G)/{text{length of sequence}}}} o ()()Número deC+Número deG)/2)2/longitud de la secuencia{displaystyle ({text{number of }}C+{text{number of }G)/2)^{2}/{text{length of sequence}}}}.
Muchos genes en los genomas de los mamíferos tienen islas CpG asociadas con el inicio del gen (regiones promotoras). Debido a esto, la presencia de una isla CpG se usa para ayudar en la predicción y anotación de genes.
En los genomas de los mamíferos, las islas CpG suelen tener entre 300 y 3000 pares de bases de longitud y se han encontrado en o cerca de aproximadamente el 40 % de los promotores de genes de mamíferos. Más del 60% de los genes humanos y casi todos los genes domésticos tienen sus promotores incrustados en islas CpG. Dada la frecuencia de las secuencias de dos nucleótidos de GC, el número de dinucleótidos de CpG es mucho menor de lo esperado.
Un estudio de 2002 revisó las reglas de predicción de islas CpG para excluir otras secuencias genómicas ricas en GC, como las repeticiones Alu. Con base en una búsqueda exhaustiva de las secuencias completas de los cromosomas humanos 21 y 22, se encontró que las regiones de ADN de más de 500 pb tenían más probabilidades de ser el 'verdadero'. Islas CpG asociadas con el 5' regiones de genes si tenían un contenido de GC superior al 55 % y una proporción de CpG observada a esperada del 65 %.
Las islas CpG se caracterizan por un contenido de dinucleótidos CpG de al menos el 60 % de lo que se esperaría estadísticamente (~4–6 %), mientras que el resto del genoma tiene una frecuencia CpG mucho más baja (~1 %), un fenómeno llamada supresión de CG. A diferencia de los sitios CpG en la región codificante de un gen, en la mayoría de los casos, los sitios CpG en las islas CpG de los promotores no están metilados si se expresan los genes. Esta observación condujo a la especulación de que la metilación de los sitios CpG en el promotor de un gen puede inhibir la expresión génica. La metilación, junto con la modificación de histonas, es fundamental para la impresión. La mayoría de las diferencias de metilación entre tejidos, o entre muestras normales y de cáncer, se producen a poca distancia de las islas CpG (en las "costas de las islas CpG") y no en las propias islas.
Las islas CpG normalmente ocurren en o cerca del sitio de inicio de la transcripción de los genes, particularmente los genes domésticos, en los vertebrados. Una base C (citosina) seguida inmediatamente por una base G (guanina) (una CpG) es rara en el ADN de los vertebrados porque las citosinas en tal disposición tienden a estar metiladas. Esta metilación ayuda a distinguir la hebra de ADN recién sintetizada de la hebra original, lo que ayuda en las etapas finales de la corrección del ADN después de la duplicación. Sin embargo, con el tiempo, las citosinas metiladas tienden a convertirse en timinas debido a la desaminación espontánea. Hay una enzima especial en humanos (Timina-ADN glicosilasa, o TDG) que reemplaza específicamente a los T de los desajustes T/G. Sin embargo, debido a la rareza de los CpG, se teoriza que no es lo suficientemente efectivo para prevenir una mutación posiblemente rápida de los dinucleótidos. La existencia de islas CpG suele explicarse por la existencia de fuerzas selectivas para un contenido relativamente alto de CpG, o niveles bajos de metilación en esa área genómica, quizás relacionado con la regulación de la expresión génica. Un estudio de 2011 mostró que la mayoría de las islas CpG son el resultado de fuerzas no selectivas.
Metilación, silenciamiento, cáncer y envejecimiento
Islas CpG en promotores
En humanos, aproximadamente el 70 % de los promotores ubicados cerca del sitio de inicio de la transcripción de un gen (promotores proximales) contienen una isla CpG.
Los elementos del promotor distal también suelen contener islas CpG. Un ejemplo es el gen de reparación del ADN ERCC1, en el que el elemento que contiene la isla CpG se encuentra unos 5400 nucleótidos aguas arriba del sitio de inicio de la transcripción del gen ERCC1. Las islas CpG también ocurren con frecuencia en promotores de ARN no codificantes funcionales, como los microARN.
La metilación de islas CpG silencia genes de forma estable
En humanos, la metilación del ADN ocurre en la posición 5 del anillo de pirimidina de los residuos de citosina dentro de los sitios CpG para formar 5-metilcitosinas. La presencia de múltiples sitios CpG metilados en islas CpG de promotores provoca un silenciamiento estable de genes. El silenciamiento de un gen puede ser iniciado por otros mecanismos, pero esto a menudo es seguido por la metilación de los sitios CpG en la isla promotora CpG para provocar el silenciamiento estable del gen.
Promotora CpG hiper / hipometilación en cáncer
(feminine)En los cánceres, la pérdida de la expresión de los genes se produce con una frecuencia diez veces mayor debido a la hipermetilación de las islas CpG del promotor que a las mutaciones. Por ejemplo, en un cáncer colorrectal suele haber de 3 a 6 mutaciones de conductor y de 33 a 66 mutaciones de autoestopista o pasajero. Por el contrario, en un estudio de tumores de colon en comparación con la mucosa colónica adyacente de apariencia normal, 1.734 islas CpG estaban muy metiladas en los tumores, mientras que estas islas CpG no estaban metiladas en la mucosa adyacente. La mitad de las islas CpG estaban en promotores de genes codificadores de proteínas anotados, lo que sugiere que alrededor de 867 genes en un tumor de colon han perdido expresión debido a la metilación de la isla CpG. Un estudio separado encontró un promedio de 1549 regiones diferencialmente metiladas (hipermetiladas o hipometiladas) en los genomas de seis cánceres de colon (en comparación con la mucosa adyacente), de las cuales 629 estaban en regiones promotoras conocidas de genes. Un tercer estudio encontró más de 2000 genes diferencialmente metilados entre los cánceres de colon y la mucosa adyacente. Usando el análisis de enriquecimiento de conjuntos de genes, 569 de 938 conjuntos de genes estaban hipermetilados y 369 estaban hipometilados en cánceres. La hipometilación de las islas CpG en los promotores da como resultado la sobreexpresión de los genes o conjuntos de genes afectados.
Un estudio de 2012 enumeró 147 genes específicos con promotores hipermetilados asociados con el cáncer de colon, junto con la frecuencia con la que se encontraron estas hipermetilaciones en los cánceres de colon. Al menos 10 de esos genes tenían promotores hipermetilados en casi el 100 % de los cánceres de colon. También indicaron 11 microARN cuyos promotores estaban hipermetilados en cánceres de colon a frecuencias entre el 50% y el 100% de los cánceres. Los microARN (miARN) son pequeños ARN endógenos que se emparejan con secuencias en los ARN mensajeros para dirigir la represión postranscripcional. En promedio, cada microARN reprime varios cientos de genes diana. Por lo tanto, los microARN con promotores hipermetilados pueden permitir la sobreexpresión de cientos a miles de genes en un cáncer.
La información anterior muestra que, en los cánceres, la hiper/hipometilación del promotor CpG de los genes y de los microARN provoca la pérdida de la expresión (o, a veces, el aumento de la expresión) de muchos más genes que la mutación.
Genes de reparación de ADN con promotores hiper/hipometilados en cánceres
Los genes de reparación del ADN se reprimen con frecuencia en los cánceres debido a la hipermetilación de las islas CpG dentro de sus promotores. En los carcinomas de células escamosas de cabeza y cuello, al menos 15 genes de reparación del ADN tienen promotores frecuentemente hipermetilados; estos genes son XRCC1, MLH3, PMS1, RAD51B, XRCC3, RAD54B, BRCA1, SHFM1, GEN1, FANCE, FAAP20, SPRTN, SETMAR, HUS1, y PER1. Alrededor de diecisiete tipos de cáncer son frecuentemente deficientes en uno o más genes de reparación del ADN debido a la hipermetilación de sus promotores. Por ejemplo, la hipermetilación del promotor del gen de reparación del ADN MGMT ocurre en el 93 % de los cánceres de vejiga, el 88 % de los cánceres de estómago, el 74 % de los cánceres de tiroides, el 40 %-90 % de los cánceres colorrectales y el 50 % de cánceres cerebrales. La hipermetilación del promotor de LIG4 ocurre en el 82 % de los cánceres colorrectales. La hipermetilación del promotor de NEIL1 ocurre en el 62 % de los cánceres de cabeza y cuello y en el 42 % de los cánceres de pulmón de células no pequeñas. La hipermetilación del promotor de ATM ocurre en el 47 % de los cánceres de pulmón de células no pequeñas. La hipermetilación del promotor de MLH1 ocurre en el 48% de los carcinomas de células escamosas de cáncer de pulmón de células no pequeñas. La hipermetilación del promotor de FANCB ocurre en el 46 % de los cánceres de cabeza y cuello.
Por otro lado, los promotores de dos genes, PARP1 y FEN1, estaban hipometilados y estos genes estaban sobreexpresados en numerosos cánceres. PARP1 y FEN1 son genes esenciales en la unión de extremos mediada por microhomología de la vía de reparación del ADN mutagénica y propensa a errores. Si esta vía se sobreexpresa, el exceso de mutaciones que provoca puede provocar cáncer. PARP1 se sobreexpresa en leucemias activadas por tirosina quinasa, en neuroblastoma, en testículos y otros tumores de células germinales, y en el sarcoma de Ewing, FEN1 se sobreexpresa en la mayoría de los cánceres de mama, próstata, estómago, neuroblastomas, páncreas y pulmón.
El daño en el ADN parece ser la principal causa subyacente del cáncer. Si la reparación precisa del ADN es deficiente, los daños en el ADN tienden a acumularse. Tal exceso de daño en el ADN puede aumentar los errores mutacionales durante la replicación del ADN debido a la síntesis de translesión propensa a errores. El exceso de daño en el ADN también puede aumentar las alteraciones epigenéticas debido a errores durante la reparación del ADN. Tales mutaciones y alteraciones epigenéticas pueden dar lugar al cáncer (ver neoplasias malignas). Por lo tanto, la hiper/hipometilación de la isla CpG en los promotores de los genes de reparación del ADN es probablemente fundamental para la progresión del cáncer.
Metilación de sitios CpG con la edad
Dado que la edad tiene un fuerte efecto en los niveles de metilación del ADN en decenas de miles de sitios CpG, se puede definir un reloj biológico de alta precisión (denominado reloj epigenético o edad de metilación del ADN) en humanos y chimpancés.
Sitios no metilados
Los sitios de dinucleótidos CpG no metilados pueden detectarse mediante el receptor tipo Toll 9 (TLR 9) en células dendríticas plasmocitoides, monocitos, células asesinas naturales (NK) y células B en humanos. Esto se utiliza para detectar la infección viral intracelular.
Papel de los sitios CpG en la memoria
En los mamíferos, las ADN metiltransferasas (que agregan grupos metilo a las bases del ADN) exhiben una preferencia de secuencia por las citosinas dentro de los sitios CpG. En el cerebro del ratón, el 4,2% de todas las citosinas están metiladas, principalmente en el contexto de los sitios CpG, formando 5mCpG. La mayoría de los sitios 5mCpG hipermetilados aumentan la represión de los genes asociados.
Como revisaron Duke et al., la actividad neuronal altera la metilación del ADN neuronal (represión de la expresión de genes particulares). La metilación del ADN neuronal es necesaria para la plasticidad sináptica; es modificado por experiencias; y se requiere la metilación y desmetilación activa del ADN para la formación y el mantenimiento de la memoria.
En 2016 Halder et al. usando ratones, y en 2017 Duke et al. usando ratas, sometió a los roedores a un condicionamiento de miedo contextual, causando que se formara una memoria a largo plazo especialmente fuerte. A las 24 horas después del condicionamiento, en la región del cerebro del hipocampo de las ratas, la expresión de 1048 genes se reguló a la baja (generalmente asociada con 5mCpG en los promotores de genes) y la expresión de 564 genes se reguló al alza (a menudo asociada con la hipometilación de CpG). sitios en los promotores de genes). A las 24 horas después del entrenamiento, el 9,2% de los genes en el genoma de rata de las neuronas del hipocampo se metilaron diferencialmente. Sin embargo, aunque el hipocampo es esencial para aprender nueva información, no almacena información por sí mismo. En los experimentos con ratones de Halder, se observaron 1.206 genes diferencialmente metilados en el hipocampo una hora después del condicionamiento del miedo contextual, pero estas metilaciones alteradas se revirtieron y no se observaron después de cuatro semanas. En contraste con la ausencia de cambios de metilación de CpG a largo plazo en el hipocampo, se pudo detectar una metilación de CpG diferencial sustancial en las neuronas corticales durante el mantenimiento de la memoria. Hubo 1.223 genes diferencialmente metilados en la corteza cingulada anterior de ratones cuatro semanas después del condicionamiento del miedo contextual.
La desmetilación en los sitios CpG requiere actividad de ROS
En las células somáticas adultas, la metilación del ADN suele ocurrir en el contexto de los dinucleótidos CpG (sitios CpG), formando 5-metilcitosina-pG o 5mCpG. Las especies reactivas de oxígeno (ROS) pueden atacar a la guanina en el sitio del dinucleótido, formando 8-hidroxi-2'-desoxiguanosina (8-OHdG) y dando como resultado un sitio de dinucleótido 5mCp-8-OHdG. La enzima de reparación por escisión de base OGG1 se dirige a 8-OHdG y se une a la lesión sin escisión inmediata. OGG1, presente en un sitio 5mCp-8-OHdG recluta a TET1 y TET1 oxida los 5mC adyacentes al 8-OHdG. Esto inicia la desmetilación de 5mC.
Como se revisó en 2018, en las neuronas cerebrales, la familia de dioxigenasas (TET1, TET2, TET3) de translocación diez-once (TET) oxida 5mC para generar 5-hidroximetilcitosina (5hmC). En pasos sucesivos, las enzimas TET hidroxilan más 5hmC para generar 5-formilcitosina (5fC) y 5-carboxilcitosina (5caC). La timina-ADN glicosilasa (TDG) reconoce las bases intermedias 5fC y 5caC y escinde el enlace glucosídico dando como resultado un sitio apirimidínico (sitio AP). En una vía alternativa de desaminación oxidativa, 5hmC puede ser desaminado oxidativamente por desaminasas del complejo de edición de ARNm de citidina desaminasa/apolipoproteína B inducida por actividad (AID/APOBEC) para formar 5-hidroximetiluracilo (5hmU) o 5mC puede convertirse en timina (Thy). 5hmU puede ser escindido por TDG, uracil-DNA glicosilasa 1 monofuncional selectiva de cadena única (SMUG1), Nei-Like DNA Glycosylase 1 (NEIL1) o proteína de unión a metil-CpG 4 (MBD4). Los sitios AP y los desajustes T:G luego se reparan mediante enzimas de reparación por escisión de base (BER) para producir citosina (Cyt).
Dos revisiones resumen la gran cantidad de evidencia sobre el papel crítico y esencial de ROS en la formación de la memoria. La desmetilación del ADN de miles de sitios CpG durante la formación de la memoria depende del inicio de ROS. En 2016, Zhou et al. demostraron que las ROS tienen un papel central en la desmetilación del ADN.
TET1 es una enzima clave involucrada en la desmetilación de 5mCpG. Sin embargo, TET1 solo puede actuar sobre 5mCpG si una ROS ha actuado primero sobre la guanina para formar 8-hidroxi-2'-desoxiguanosina (8-OHdG), lo que da como resultado un dinucleótido 5mCp-8-OHdG (ver la primera figura). en esta sección). Después de la formación de 5mCp-8-OHdG, la enzima de reparación por escisión de base OGG1 se une a la lesión de 8-OHdG sin escisión inmediata. La adherencia de OGG1 al sitio 5mCp-8-OHdG recluta a TET1, lo que permite que TET1 oxide los 5mC adyacentes a 8-OHdG, como se muestra en la primera figura de esta sección. Esto inicia la vía de desmetilación que se muestra en la segunda figura de esta sección.
La expresión alterada de proteínas en las neuronas, controlada por la desmetilación dependiente de ROS de los sitios CpG en los promotores de genes dentro del ADN de las neuronas, es fundamental para la formación de la memoria.
Pérdida de CpG
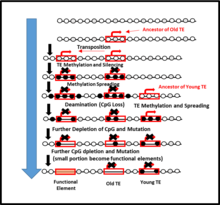
El agotamiento de CpG se ha observado en el proceso de metilación del ADN de elementos transponibles (TE), donde los TE no solo son responsables de la expansión del genoma, sino también de la pérdida de CpG en el ADN del huésped. Los TE pueden conocerse como "centros de metilación" mediante el proceso de metilación, los TE se propagan al ADN flanqueante una vez en el ADN huésped. Esta propagación podría resultar posteriormente en la pérdida de CpG a lo largo del tiempo evolutivo. Los tiempos evolutivos más antiguos muestran una mayor pérdida de CpG en el ADN flanqueante, en comparación con los tiempos evolutivos más jóvenes. Por lo tanto, la metilación del ADN puede conducir eventualmente a una pérdida notable de sitios CpG en el ADN vecino.
El tamaño del genoma y la relación CpG están negativamente correlacionados
Estudios anteriores han confirmado la variedad de tamaños de genomas en las especies, donde los invertebrados y los vertebrados tienen genomas pequeños y grandes en comparación con los humanos. El tamaño del genoma está fuertemente relacionado con el número de elementos transponibles. Sin embargo, existe una correlación entre el número de metilaciones de TE frente a la cantidad de CpG. En consecuencia, esta correlación negativa provoca el agotamiento de CpG debido a la metilación del ADN intergénico que se atribuye principalmente a la metilación de los TE. En general, esto contribuye a una cantidad notable de pérdida de CpG en diferentes especies de genomas.
Elementos Alu como promotores de la pérdida de CpG
Los elementos Alu se conocen como el tipo más abundante de elementos transponibles. Algunos estudios han utilizado elementos Alu como una forma de estudiar la idea de qué factor es responsable de la expansión del genoma. Los elementos Alu son ricos en CpG en una secuencia más larga, a diferencia de los LINE y los ERV. Alus puede funcionar como un centro de metilación, y la inserción en el ADN del huésped puede producir la metilación del ADN y provocar una propagación en el área del ADN flanqueante. Esta propagación es la razón por la cual hay una pérdida considerable de CpG y un aumento considerable en la expansión del genoma. Sin embargo, este es un resultado que se analiza con el tiempo porque los elementos Alus más antiguos muestran una mayor pérdida de CpG en sitios de ADN vecinos en comparación con los más jóvenes.
Contenido relacionado
Dogma central de la biología molecular
Polimorfismo (biología)
Wilhelm Johansen
Diversidad genética
Adenovirus










