Síndrome del corazón izquierdo hipoplásico
Síndrome del corazón izquierdo hipoplásico (HLHS) es un defecto cardíaco congénito poco común en el que el lado izquierdo del corazón está muy subdesarrollado y es incapaz de soportar la circulación sistémica. Se estima que representa del 2 al 3% de todas las cardiopatías congénitas. Los primeros signos y síntomas incluyen mala alimentación, cianosis y disminución del pulso en las extremidades. Se cree que la etiología es multifactorial y resulta de una combinación de mutaciones genéticas y defectos que provocan una alteración del flujo sanguíneo en el corazón. Varias estructuras pueden verse afectadas, incluido el ventrículo izquierdo, la aorta, la válvula aórtica o la válvula mitral, lo que resulta en una disminución del flujo sanguíneo sistémico.
El diagnóstico puede ocurrir prenatalmente mediante ultrasonido o poco después del nacimiento mediante ecocardiografía. El tratamiento inicial está orientado a mantener la permeabilidad del conducto arterioso, una conexión entre la arteria pulmonar y la aorta que se cierra poco después del nacimiento. Posteriormente, el paciente se somete a una reparación paliativa en tres etapas durante los siguientes años de vida. El procedimiento de Norwood generalmente se realiza a los pocos días del nacimiento. El procedimiento de Glenn generalmente se realiza entre los tres y los seis meses de edad. Finalmente, el procedimiento de Fontan se realiza en algún momento entre los dos y los cinco años de edad.
Si no se tratan, los pacientes con HLHS mueren dentro de las primeras semanas de vida, mientras que el 70% de los que se someten a cirugía paliativa en tres etapas llegan a la edad adulta. Después de la cirugía, los niños con HLHS generalmente experimentan retraso en el desarrollo neurológico y motor y tienen un mayor riesgo de insuficiencia cardíaca en la edad adulta.
Epidemiología
El HLHS se produce aproximadamente en 1 de cada 3841 nacimientos vivos en los Estados Unidos, o en un total estimado de 1025 nacimientos vivos por año en los EE. UU. En general, se estima que representa entre el 2 y el 3 % de todos los casos de cardiopatía congénita y es el defecto de un solo ventrículo más común. Se cree que es más común en los bebés varones, 1,5 veces más común que en las niñas. Una revisión sistemática reciente encontró una ligera disminución en la prevalencia del HLHS de 0,689/1000 en 1995 -1999 a 0,475/1000 en 2010 - 2017. Se cree que esto se debe a mejoras en la detección prenatal y el asesoramiento prenatal y el embarazo posterior.
Signos y síntomas
El cierre del conducto arterioso en un corazón que está muy subdesarrollado en el lado izquierdo produce cianosis y dificultad respiratoria que pueden progresar a un shock cardiogénico y la muerte. Los primeros síntomas pueden incluir mala alimentación o cianosis que no responde a la administración de oxígeno. Los pulsos periféricos pueden ser débiles y las extremidades frías al tacto.
El SHLHS suele coexistir con bajo peso al nacer y nacimiento prematuro.
En los recién nacidos con una comunicación interauricular pequeña, denominada "restrictiva", hay una mezcla inadecuada de sangre oxigenada y desoxigenada. Estos recién nacidos se descompensan rápidamente y desarrollan acidosis y cianosis.
En el ECG, la desviación del eje hacia la derecha y la hipertrofia del ventrículo derecho son comunes, pero no son indicativos de HLHS. La radiografía de tórax puede mostrar un corazón grande (cardiomegalia) o un aumento de la vasculatura pulmonar. Los recién nacidos con HLHS no suelen tener un soplo cardíaco, pero en algunos casos, puede ser audible un soplo de flujo pulmonar o un soplo de regurgitación tricuspídea.
La insuficiencia tricuspídea o la disfunción ventricular derecha concurrentes pueden provocar el desarrollo de hepatomegalia.
Patogenia
La mayoría de los casos de HLHS son esporádicos, lo que significa que surgen en pacientes sin antecedentes familiares de HLHS. Algunos casos pueden tener un componente genético, ya que se ha demostrado que el HLHS es hereditario y está asociado con mutaciones genéticas específicas. Los posibles factores contribuyentes pueden incluir infarto intrauterino, cambios infecciosos y una miocardiopatía selectiva del ventrículo izquierdo.
Genética
Los loci genéticos asociados con HLHS incluyen GJA1 (conexina 43), HAND1, NKX2.5, 10q22 y 6q23. Existe un ligero riesgo de recurrencia en futuros embarazos, estimado en un 2-4%, que aumenta al 25% en familias con dos hijos afectados. Se cree que esto está mediado por mutaciones genéticas con penetrancia incompleta.
El HLHS también se asocia con varios síndromes genéticos, incluida la trisomía 13 (síndrome de Patau), la trisomía 18 (síndrome de Edwards), la trisomía parcial 9, el síndrome de Turner (XO), el síndrome de Jacobsen (síndrome de deleción 11q), el síndrome de Holt -Síndrome de Oram y síndrome de Smith-Lemli-Opitz.
Flujo sanguíneo alterado
Una teoría popular denominada "sin flujo, no crece" La hipótesis sugiere que los defectos anatómicos primarios de las válvulas aórtica y mitral conducen a malformaciones del ventrículo izquierdo y su tracto de salida. Estos defectos primarios se pueden dividir en aquellos que conducen a una obstrucción del tracto de salida o a una reducción del llenado del ventrículo izquierdo. La obstrucción del tracto de salida provoca hipertrofia del ventrículo izquierdo y reducción de la luz del ventrículo izquierdo. Un ejemplo de esto sería el caso de la estenosis aórtica. La estenosis aórtica que se produce durante el desarrollo fetal provoca una tensión adicional en el ventrículo izquierdo en el útero. Con el tiempo, esto puede provocar una disminución de la perfusión a través del ventrículo izquierdo, lo que se cree que inhibe el crecimiento ventricular.
Fisiopatología
Al nacer, el conducto arterioso todavía está abierto y hay una resistencia mayor de lo normal al flujo sanguíneo en los pulmones. Esto permite una oxigenación adecuada mediante la mezcla entre las aurículas y una apariencia normal al nacer. Cuando el conducto comienza a cerrarse y la resistencia vascular pulmonar disminuye, el flujo sanguíneo a través del conducto se restringe y aumenta el flujo a los pulmones.
En la anatomía típica, el lado izquierdo del corazón recibe sangre rica en oxígeno de los pulmones y la bombea al resto del cuerpo. Los pacientes con HLHS pueden tener una serie de malformaciones cardíacas que, en última instancia, conducen a un ventrículo izquierdo diminuto que no puede suministrar suficiente flujo sanguíneo al resto del cuerpo. Hay tres variantes anatómicas principales de la enfermedad que se diferencian por estenosis o atresia de la válvula aórtica y mitral.
El subtipo de atresia mitral y atresia aórtica (MA-AA) es la forma más grave de HLHS, lo que provoca que no entre ningún flujo sanguíneo al ventrículo izquierdo, lo que impide la posibilidad de salida del ventrículo izquierdo. En el subtipo de estenosis mitral y atresia aórtica (EM-AA), la sangre puede llenar el ventrículo izquierdo, pero no puede llegar a la circulación sistémica a través de la aorta ascendente hipoplásica. Por último, la forma más leve es el subtipo de estenosis mitral y estenosis aórtica (EM-AS). En estos pacientes, aunque el ventrículo izquierdo es capaz de suministrar algo de flujo sanguíneo al resto del cuerpo, el gasto sistémico general del ventrículo izquierdo sigue siendo inadecuado.
En todos estos casos, el ventrículo izquierdo no puede bombear la sangre al resto del cuerpo. El recién nacido depende de la sangre que fluye a través de una comunicación interauricular para mezclar la sangre oxigenada y desoxigenada, y de un conducto arterioso permeable para permitir que la sangre llegue a la aorta y la circulación sistémica a través del ventrículo derecho. Esto es lo que define al HLHS como un "ventrículo único" defecto.
Debido al subdesarrollo del lado izquierdo del corazón en el útero, el aumento de la poscarga provoca hipertensión de la aurícula izquierda, edema pulmonar y, por tanto, daño pulmonar al feto antes del nacimiento.
Diagnóstico
El síndrome del corazón izquierdo hipoplásico se puede diagnosticar antes del nacimiento o después del nacimiento mediante ecocardiografía. Los hallazgos típicos incluyen un ventrículo izquierdo y una aorta pequeños, anomalías de las válvulas mitral y aórtica, flujo retrógrado en el arco transversal de la aorta y flujo de izquierda a derecha entre las aurículas. A menudo se reconoce durante el segundo trimestre del embarazo, entre las semanas 18 y 24. gestación.
Gestión
Médica
(feminine)Sin intervenciones que prolonguen la vida, el HLHS es fatal, pero con intervención, un bebé puede sobrevivir. Un cirujano cardiotorácico puede realizar una serie de operaciones o un trasplante de corazón completo. Si bien la intervención quirúrgica se ha convertido en el estándar de atención en los Estados Unidos, otros sistemas nacionales de salud, especialmente en Francia, abordan el diagnóstico del HLHS de una manera más conservadora, con énfasis en la interrupción del embarazo o la atención compasiva después del parto.
Antes de la cirugía, el conducto debe mantenerse abierto para permitir el flujo sanguíneo utilizando medicamentos que contengan prostaglandinas. En los bebés con síndrome del corazón izquierdo hipoplásico se utiliza aire con menos oxígeno de lo normal. Estos bajos niveles de oxígeno aumentan la resistencia vascular pulmonar (PVR) y así mejoran el flujo sanguíneo al resto del cuerpo debido a la mayor diferencia de presión entre los pulmones y el cuerpo. Lograr niveles de oxígeno por debajo de la atmósfera requiere el uso de nitrógeno inhalado. El óxido nítrico es un potente vasodilatador pulmonar y, por tanto, reduce la RVP y mejora el retorno venoso. Cualquier factor que aumente la PVR impedirá el flujo del lado derecho.
Quirúrgico
Las operaciones quirúrgicas para ayudar con el corazón izquierdo hipoplásico son complejas y deben individualizarse para cada paciente. Un cardiólogo debe evaluar todas las opciones médicas y quirúrgicas caso por caso.
Actualmente, los bebés se someten a cirugía reconstructiva por etapas (procedimiento de Norwood o Sano a los pocos días de nacer, procedimiento de Glenn o procedimiento de Hemi-Fontan entre los 3 y 6 meses de edad, y el procedimiento de Fontan a los 1 1/2 a 5 años de edad) o trasplante cardíaco. Las expectativas actuales son que el 70% de las personas con HLHS puedan llegar a la edad adulta. Muchos estudios muestran que cuanto mayor es el volumen (número de cirugías realizadas) en un hospital, menor es la tasa de mortalidad (muerte). Los factores que aumentan el riesgo de un bebé incluyen un menor peso al nacer, anomalías congénitas adicionales, un síndrome genético o aquellos con un tabique auricular altamente restrictivo. Para los pacientes sin estos factores de riesgo adicionales, la supervivencia a 5 años ahora se acerca al 80%. Los estudios muestran que alrededor del 75% de los niños que sobreviven a la cirugía muestran retrasos en el desarrollo en una o más áreas, como deficiencias motoras, cognitivas o del lenguaje, y aproximadamente un tercio de los niños con un solo ventrículo sin síndrome genético tienen deficiencias significativas. La investigación actual se centra en trazar las conexiones entre las lesiones del desarrollo neurológico, los procedimientos quirúrgicos y de cuidados intensivos y la susceptibilidad genética con el objetivo de modificar las intervenciones que perjudican los resultados psicosociales y del desarrollo neurológico. Una alternativa al tradicional Norwood es el procedimiento híbrido.
Algunos médicos ofrecen atención compasiva, en lugar de cirugías, lo que provoca la muerte del niño, generalmente dentro de las 2 semanas posteriores al nacimiento. La atención compasiva está supervisada por un médico y puede llevarse a cabo en el hospital o en el hogar. Sin embargo, debido a la gran mejora de la intervención quirúrgica, con muchos hospitales logrando una supervivencia superior al 90%, existe un debate sobre si aún se debe ofrecer atención compasiva a las familias. Un estudio realizado en 2003 concluyó que una selección de médicos expertos en el cuidado de niños con HLHS se dividió equitativamente cuando se les preguntó qué harían si sus propios hijos nacieran con HLHS: 1/3 respondió que elegiría la cirugía, 1 /3 afirman que elegirían un tratamiento paliativo (compasivo) sin cirugía, y 1/3 afirman que no están seguros de qué elección harían.
El procedimiento de tres etapas es un procedimiento paliativo (no una cura), ya que la circulación del niño se hace funcionar con sólo dos de las cuatro cámaras del corazón.

Procedimiento de Norwood
El primer paso es el procedimiento de Norwood. En este procedimiento, se utiliza el ventrículo derecho para bombear sangre a la circulación sistémica. Dado que el ventrículo derecho ya no bombea sangre directamente a los pulmones, se requiere una derivación para hacer pasar sangre desoxigenada a través de los pulmones. O la arteria subclavia se puede conectar a la circulación pulmonar (derivación de Blalock-Taussig) o se realiza una derivación directamente desde el ventrículo derecho a la circulación pulmonar (derivación de Sano). La aorta estrecha se agranda usando un parche para mejorar el flujo sanguíneo al cuerpo.
Durante este tiempo, el bebé puede estar médicamente frágil y tener problemas de alimentación porque el corazón está trabajando muy duro. Existe un grado considerable de mezcla venosa en el ventrículo derecho, lo que conduce a una menor saturación de oxigenación. Además, tanto la derivación de Blalock-Taussig como la de Sano exponen los pulmones a presiones arteriales sistémicas, lo que provoca hipertensión pulmonar a largo plazo y, finalmente, insuficiencia cardíaca.
Procedimiento híbrido
Se puede utilizar el procedimiento híbrido en lugar del Norwood. El procedimiento híbrido no requiere el uso de circulación extracorpórea ni la realización de una esternotomía. En lugar de una cirugía de seis horas, el híbrido suele tardar entre una y dos horas. En este procedimiento, se coloca un stent en el conducto arterioso para mantener su permeabilidad y se colocan bandas sobre las ramas de la arteria pulmonar izquierda y derecha para limitar la presión y la circulación excesiva en los pulmones. Los resultados con el enfoque híbrido son comparables a los del Norwood.
Procedimiento de Glenn
La segunda etapa, el Glenn bidireccional o Hemi-Fontan (ver también el procedimiento de Kawashima), alivia algunos de los problemas introducidos por la paliación de la Etapa I. En esta operación, se liga la vena cava superior del corazón y se conecta a la circulación pulmonar. En este momento, se retira la derivación Blalock-Taussig o Sano. Los pulmones ya no están expuestos a presiones arteriales sistémicas, sino a presiones venosas mucho más bajas. Aunque la sangre venosa de la mitad superior del cuerpo ya no se mezcla con la sangre oxigenada en el ventrículo derecho, todavía hay mezcla venosa de la mitad inferior del cuerpo, lo que provoca cierto grado de desaturación de oxígeno.
Procedimiento de Fontan
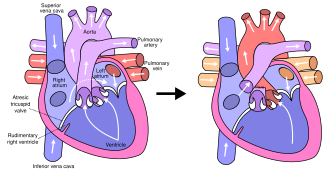
El procedimiento final, el procedimiento de Fontan, completa la reparación del corazón izquierdo hipoplásico. Aunque existen varias variaciones, el efecto funcional es redirigir la sangre venosa desde la parte inferior del cuerpo (a través de la vena cava inferior) lejos de la aurícula derecha hacia la arteria pulmonar. Esto debería eliminar cualquier mezcla de sangre oxigenada y desoxigenada en el ventrículo derecho. El ventrículo derecho realiza el trabajo tradicional del izquierdo, suministrando al cuerpo sangre oxigenada, mientras que la presión venosa sistémica pasiva realiza el trabajo tradicional del derecho, pasando sangre desoxigenada a los pulmones.
Cirugía fetal
Se están investigando las intervenciones realizadas durante el desarrollo fetal. Cuando los signos de HLHS se detectan prenatalmente mediante ecografía, un procedimiento percutáneo que implica la inserción de un catéter con balón puede abrir la comunicación interauricular para prevenir la hipertensión auricular izquierda y promover un mejor desarrollo del corazón.
Pronóstico
El 95% de los bebés con HLHS que no reciben tratamiento mueren en las primeras semanas de vida.
La supervivencia temprana ha mejorado desde la introducción del procedimiento Norwood. Dado que no existen estudios a largo plazo en adultos con HLHS, las estadísticas generalmente se derivan de pacientes post-Fontan; se estima que el 70% de los pacientes con HLHS pueden llegar a la edad adulta.
El pronóstico depende de la salud del niño, ya que existe una mayor demanda de frecuencia respiratoria y cardíaca en los bebés durante enfermedades infantiles comunes. Esta frágil población tiene poca reserva cardíaca para adaptarse a estas demandas y proporcionar estabilidad hemodinámica durante las enfermedades.
Los niños con HLHS y otras afecciones comparables de un solo ventrículo, como grupo, tienen peores resultados de desarrollo neurológico que sus pares sanos. Se han demostrado déficits en el lenguaje, el funcionamiento ejecutivo y tasas más altas de trastornos de ansiedad y depresión. Algunos de estos resultados pueden ser consecuencia de factores genéticos asociados con el HLHS y otros pueden ser modificables mediante cambios en los procedimientos y en el entorno sanitario. Existe un consenso clínico emergente sobre la importancia de la vigilancia continua del desarrollo neurológico desde los primeros años hasta la edad adulta. Además, un metanálisis reciente que comparó veintidós estudios mostró que el 64,7% de los estudios informaron un retraso en el desarrollo motor en niños con fisiologías de ventrículo único, como el síndrome del corazón izquierdo hipoplásico.
Al igual que ocurre con otros tipos de defectos cardíacos que involucran válvulas malformadas, los pacientes con HLHS corren un alto riesgo de endocarditis y deben ser monitoreados por un cardiólogo por el resto de sus vidas para controlar su función cardíaca.
El trasplante cardíaco puede indicarse, típicamente después de la terminación de Fontan. Un estudio multicéntrico (de pacientes sometidos al Fontan de 1993 a 2001) reportó una tasa de supervivencia del 76% en pacientes que sobrevivieron al trasplante.
Futuro de las terapias con células madre
Una revisión sistemática encontró 23 artículos, publicados desde 2010, así como nueve ensayos clínicos relevantes relacionados con enfermedades cardíacas congénitas y avances recientes en terapias de células madre. La investigación preclínica se ha centrado en varios tipos de células madre incluyendo: células madre mesenquimales (MSCs), células sanguíneas de cordón umbilical autólogo, células madre cardiacas de c-kit+ y células madre mesenquimales de timo neonatal. Estos tipos de células han demostrado la capacidad de diferenciar en el tejido cardíaco haciéndolos ideales para la terapia regenerativa cardíaca. El primer uso de células sanguíneas de cordón umbilical autólogo se hizo en la Clínica Mayo en 2015 y se encontró que aumentó la función ventricular derecha en el paciente después de su procedimiento. El primer uso de células progenitoras cardíacas ocurrió en la Infusión Transcoronaria de Células Progenitoras Cardiacas en Pacientes con Fisiología Única-Ventrículo (TICAP) Trail de 2011.
Ensayos en curso
Hay varios estudios en curso que prueban la viabilidad y eficacia de las terapias con células madre para enfermedades de ventrículo único como el HLHS. Estos ensayos se centran en cuáles son las células madre más eficaces, cuál es el mejor momento para la reparación en tres etapas y cuál es el método de administración óptimo.
- Prueba Fase IIb prueba la eficacia de las inyecciones intramioárdicas de los glóbulos de cordón umbilical durante la reparación de estadio II (Glenn).
- Prueba de fase I prueba la eficacia de la infusión de glóbulos de cordón autólogo durante la etapa 1 (Norwood) reparación dentro de dos a tres días de nacimiento.
- El ensayo ELPIS es un piloto abierto de fase I/IIb que prueba la eficacia y seguridad de las inyecciones de células madre mesenquimales de donante intramiocardio en pacientes durante la etapa 2 (Glenn) y la etapa 3 (Fontan).
- Prueba de fase I prueba la eficacia de las inyecciones intramiocardiales de sangre cordón umbilical durante la reparación de estadio 2 (Glenn).
- El estudio PERSEUS es un ensayo de fase II que prueba la eficacia de las infusiones intracoronarias de células progenitoras cardíacas y evalúa la función post-tratamiento de 3 meses.
- El estudio APOLLON es un ensayo clínico de fase III que prueba la eficacia y seguridad de las inyecciones intracoronarias de células madre cardiacas autólogas durante la etapa 2 (Glenn) o la etapa 3 (Fontan).
- NIÑO El estudio es un ensayo clínico de fase I que prueba la viabilidad y seguridad de las inyecciones intramiocardiales de células c-kit+ durante la reparación de estadio 2 (Glenn).
Es importante tener en cuenta que los pacientes con HLHS tienen un mayor riesgo de desarrollar insuficiencia cardíaca en la edad adulta. Aún se desconoce si estas posibles terapias reducirían el riesgo futuro de insuficiencia cardíaca en estos pacientes.