Síndrome de Waardenburg
síndrome de Waardenburg es un grupo de enfermedades genéticas raras caracterizadas por al menos cierto grado de pérdida auditiva congénita y deficiencias de pigmentación, que pueden incluir ojos azules brillantes (o un ojo azul y otro marrón), un mechón blanco o parches de piel clara. Estas características básicas constituyen el tipo 2 de la condición; en el tipo 1, también hay un espacio más amplio entre las esquinas internas de los ojos llamado telecanto o distopía cantorum. En el tipo 3, que es raro, los brazos y las manos también están malformados, con contracturas permanentes de los dedos o dedos fusionados, mientras que en el tipo 4, la persona también padece la enfermedad de Hirschsprung. También existen al menos dos tipos (2E y PCWH) que pueden provocar síntomas del sistema nervioso central (SNC), como retraso en el desarrollo y anomalías del tono muscular.
El síndrome es causado por mutaciones en cualquiera de varios genes que afectan la división y migración de las células de la cresta neural durante el desarrollo embrionario (aunque algunos de los genes involucrados también afectan el tubo neural). Las células de la cresta neural son células madre que quedan después del cierre del tubo neural y que pasan a formar diversas células no pertenecientes al SNC en diferentes partes del cuerpo, incluidos los melanocitos, varios huesos y cartílagos de la cara y el oído interno y los nervios periféricos del cerebro. los intestinos. El tipo 1 es causado por una mutación en el gen PAX3, mientras que el gen que con mayor frecuencia causa el tipo 2 cuando muta es el MITF. El tipo 3 es una presentación más grave del tipo 1 y está causado por una mutación en el mismo gen, mientras que el tipo 4 es causado con mayor frecuencia por una mutación en SOX10. Las mutaciones en otros genes también pueden causar los diferentes tipos, y a algunos de ellos se les han asignado sus propios subtipos con letras. La mayoría de los tipos son autosómicos dominantes.
La prevalencia estimada del síndrome de Waardenburg es de 1 en 42.000. Los tipos 1 y 2 son los más comunes, comprendiendo aproximadamente la mitad y un tercio de los casos, respectivamente, mientras que el tipo 4 comprende una quinta parte y el tipo 3 menos del 2% de los casos. Se estima que entre el 2% y el 5% de las personas con sordera congénita tienen síndrome de Waardenburg. Las descripciones del síndrome se remontan al menos a la primera mitad del siglo XX, sin embargo, lleva el nombre del oftalmólogo y genetista holandés Petrus Johannes Waardenburg, quien lo describió en 1951. Sus subtipos se descubrieron progresivamente en las décadas siguientes y tenían genes atribuidos a principalmente en las décadas de 1990 y 2000.
Signos y síntomas
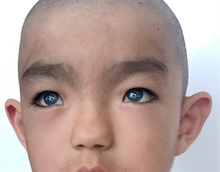
El síndrome de Waardenburg tiene múltiples tipos diferentes con algunas variaciones en los síntomas, y los síntomas pueden variar entre personas con el mismo tipo. Las dos características consistentes en todos los tipos de síndrome de Waardenburg son cierto grado de pérdida auditiva neurosensorial congénita y cierto grado de deficiencias de pigmentación, más consistentemente en los ojos.
Tipo 1
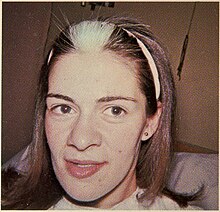
El tipo 1 se caracteriza por pérdida auditiva neurosensorial congénita, deficiencias pigmentarias del cabello, como un mechón de cabello blanco (poliosis) en el centro frontal de la cabeza o encanecimiento prematuro, deficiencias pigmentarias de los ojos, como ojos de diferentes colores. ojos (heterocromía iridum completa), múltiples colores en un ojo (heterocromía iridum sectorial) u ojos azules brillantes, parches de despigmentación de la piel y un espacio más amplio entre las esquinas internas de los ojos llamado telecanto o distopía cantorum. Otros rasgos faciales asociados con el tipo 1 pueden incluir un puente nasal alto, una punta de la nariz plana, una uniceja (synophrys), bordes más pequeños de las fosas nasales (alae) o un filtrum liso.
Tipo 2
La diferencia que define el tipo 2 del tipo 1 es que los pacientes no tienen un espacio más amplio entre las esquinas internas de los ojos (telecanthus/dystopia canthorum). La pérdida auditiva neurosensorial tiende a ser más común y más grave en este tipo. Con diferencia, el gen más común que causa este tipo cuando está mutado es el MITF (clasificado como tipo 2A). Si dos individuos con una mutación en este gen (heterocigotos) tienen un hijo portador de ambas mutaciones (homocigotos), para lo cual existe un 25% de posibilidades, se presentarán síntomas adicionales en el niño, como un agujero en el iris (coloboma), ojos pequeños (microftalmia), huesos endurecidos (osteopetrosis), macrocefalia, albinismo y sordera.
Se han identificado dos pacientes conocidos con mutaciones en ambas copias de SNAI2 (clasificadas como tipo 2D); Estos individuos presentaban síndrome de Waardenburg tipo 2 pero no tenían deficiencias de pigmentación del cabello.
Cuando el síndrome de Waardenburg tipo 2 está causado por una mutación en SOX10 (clasificada como tipo 2E), en algunas ocasiones puede presentarse con múltiples síntomas neurológicos. Estos pueden incluir retraso en el desarrollo, nistagmo en la primera infancia, aumento del tono muscular, anomalías de la sustancia blanca o hipomielinización en el cerebro, comportamiento similar al autista y el subdesarrollo o la ausencia total de muchas estructuras del oído interno, como el sistema vestibular o la cóclea. También puede haber falta del sentido del olfato (anosmia) debido a la falta de un bulbo olfatorio en el cerebro.
Tipo 3
También conocido como síndrome de Klein-Waardenburg o síndrome de Waardenburg-Klein, el tipo 3 tiene los mismos síntomas que el tipo 1 (y es causado por mutaciones en el mismo gen), pero tiene síntomas adicionales que afectan los brazos y las manos. Estos pueden incluir contracturas articulares de los dedos (camptodactilia), debido a músculos poco desarrollados, así como dedos fusionados (sindactilia) o escápulas aladas. También son posibles la microcefalia y el retraso en el desarrollo.
Tipo 4
También conocido como síndrome de Shah-Waardenburg o síndrome de Waardenburg-Shah, el tipo 4 tiene la mayoría de las mismas características que el tipo 2 (es decir, sin telecanto o un espacio ocular aparentemente más amplio), pero con la Además de la enfermedad de Hirschsprung, que es una falta congénita de nervios en los intestinos que conduce a una disfunción intestinal. Además, la pérdida de audición no es tan común como en el tipo 2. En raras ocasiones, se ha informado de labio hendido en esta forma de síndrome de Waardenburg.
El tipo 4 también puede ser causado por una mutación en SOX10 (el mismo gen que en el tipo 2E), en el que se conoce como tipo 4C; La pérdida de audición es muy común y grave en este tipo.
PCWH
Una mutación en SOX10, el gen implicado en el tipo 2E y el tipo 4C, a veces puede provocar síntomas de ambos tipos (síntomas neurológicos, como a veces se observa en el tipo 2E, y síntomas de Hirschsprung' s enfermedad, como se ve en el tipo 4). Cuando esto sucede, se denomina neuropatía desmielinizante periférica-leucodistrofia dismielinizante central-síndrome de Waardenburg-enfermedad de Hirschsprung (PCWH).
Causa


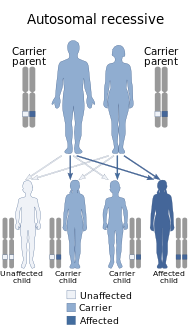
El síndrome de Waardenburg es causado por mutaciones en cualquiera de varios genes que afectan el funcionamiento de las células de la cresta neural en el desarrollo embrionario. La mayoría de los tipos de síndrome de Waardenburg son causados por mutaciones autosómicas dominantes. Los pocos que son autosómicos recesivos son raros. En la mayoría de los casos, una persona afectada lo ha heredado de uno de los padres con una de las formas dominantes de la afección. Un pequeño porcentaje de casos resulta de nuevas mutaciones espontáneas en el gen, cuando no existen antecedentes familiares de la afección.
La cresta neural es un grupo de células migratorias temporales que quedan después del cierre del tubo neural (neurulación), alrededor de la cuarta semana de desarrollo embrionario. Se encargan de diferenciarse en un grupo diverso de células que llegan a diferentes zonas del cuerpo. El tubo neural y la cresta neural se derivan del ectodermo; el tubo neural pasa a formar el cerebro y la médula espinal, mientras que las células de la cresta neural eventualmente forman varios huesos y cartílagos del cráneo y la cara al migrar a través de los arcos faríngeos. También se diferencian en la estría vascular de la cóclea, los nervios y la glía de los intestinos (plexo mientérico), las células de Schwann, que mielinizan el sistema nervioso periférico para permitir una conductividad suficiente, los odontoblastos, que producen dentina en lo profundo de los dientes, algunas células neuroendocrinas., tejido conectivo alrededor de las glándulas salival, lagrimal, pituitaria, timo y tiroides, tejido conectivo del ojo, como el estroma del iris y la córnea y la red trabecular, y melanocitos, incluidos los del estroma del iris que dan origen al color de ojos marrón a través de la melanina. Las células de la cresta neural también desempeñan un papel en la formación de músculos, incluido el músculo de la pared de ciertas arterias cardíacas.
Causas de los subtipos
- El tipo 1 es causado por una mutación dominante autosómica en el gen PAX3. PAX3, o cuadro pareado 3, es un factor de transcripción que tiene un papel en mantener una ventana abierta de tiempo para ciertas células de cresta neuronal (como las de la cabeza y los ojos) para dividir y migrar antes de su diferenciación terminal (es decir, mantenerlas en el estado de células madre). Por lo tanto, las mutaciones en este gen detienen prematuramente su división y migración, lo que da lugar a una menor falta de desarrollo de ciertos cartílagos y huesos faciales, así como a estructuras subdesarrolladas y a una falta de melanocitos en el aroma iris. Algunas evidencias muestran que PAX3 también regula las células de antes de las formas de cresta neural, es decir, el tubo neural, ya que ratones con mutaciones de pérdida de funcionamiento en una de las copias de PAX3 tienen defectos de tubo neural como espina bífida o exencefalia.
- El tipo 2 es causado por una mutación en cualquiera de una gama de genes, el ser más común MITF, cuando se clasifica como tipo 2A.
- Tipo 2A es causada por una mutación dominante autosómica en el gen MITF. MITF, o factor de transcripción asociada a microftalmia, tiene un papel más especializado en la cresta neural y está más estrictamente involucrado después de que se han encontrado las formas de cresta neural (PAX3 y SOX10 para activar MITF). Se sabe que permite dividir y migrar melanocitos, osteoclastos, células mástiles y células epiteliales pigmentarias retinas. La implicación en osteoclastos explica por qué mutaciones en ambas copias de MITF puede llevar al endurecimiento óseo (osteopetrosis), ya que los osteoclastos son responsables de descomponer el hueso. MITF También activa la transcripción de la tirosinasa, la enzima que realiza el primer paso en la creación de melanina (oxidising tyrosine). Una mutación en una copia MITF también puede conducir al síndrome de Tietz, que se distingue del síndrome de Waardenburg por albinismo uniforme en lugar de despigmentación parche.
- El tipo 2B es causado por una mutación dominante autosómica en un gen desconocido en el cromosoma 1 en el rango de locus de 1p21-1p13.3. El gen ha sido llamado provisionalmente WS2B.
- El tipo 2C es causado por una mutación autosómica dominante en un gen desconocido en el cromosoma 8 en el locus de 8p23. El gen ha sido llamado provisionalmente WS2C.
- Tipo 2D es causada por una mutación recesiva autosómica en ambas copias del gen SNAI2. El estudio que descubrió esta asociación encontró que SNAI2 se activa por MITF como parte del desarrollo de la cresta neural, y esto explicó por qué mutaciones MITF causa síndrome de Waardenburg, ya que resulta en una falta de activación SNAI2. Mutaciones en una sola copia SNAI2 también se han encontrado para causar parches de depigmentación del cabello (piebaldismo) sin otros síntomas.
- Tipo 2E es causada por una mutación dominante autosómica en el gen SOX10.
- Raramente, una mutación en un gen que no sea el conocido actualmente puede ser responsable de un síndrome de Waardenburg con características de tipo 2. Esto generalmente se clasifica inicialmente como simplemente tipo 2 pero se puede dar su propio subtipo una vez que se identifica y establece un gen o locus.
- Tipo 3 es causado por una mutación en el gen PAX3, el mismo gen que en tipo 1. Se puede heredar de forma autosómica dominante o autosómica recesiva; es posible que dos padres con síndrome de Waardenburg tipo 1 tengan un hijo que lleve ambas copias mutadas del PAX3 gen (25% de probabilidad) y presente con el tipo de síndrome de Waardenburg 3. Se ha documentado una mutación por error para tener este efecto. Sin embargo, también es posible que el síndrome de Waardenburg tipo 3 presente espontáneamente con sólo una copia mutada de PAX3. Se ha documentado la eliminación de la región de dominio pareado del gen para tener este efecto. Sin embargo, no se ha encontrado ninguna correlación importante entre tipo de mutación y gravedad de la enfermedad. La severidad tiende a ser dictada por mutaciones en otros genes (epistasis), como lo demuestran los patrones familiares distintos en gravedad no ligados al tipo de mutación de Waardenburg. Mutaciones en ambas copias PAX3 a veces han llevado a la muerte antes o poco después del nacimiento, y ratones con mutaciones de pérdida de funciones en ambas copias del gen no sobreviven.
- El tipo 4 es causado por una mutación en cualquiera de una gama de genes, el ser más común SOX10, cuando se clasifica como tipo 4C.
- Tipo 4A es causada por una mutación autosómica dominante o autosómica recesiva en el gen EDNRB.
- Tipo 4B es causada por una mutación autosómica dominante o autosómica recesiva en el gen EDN3.
- Tipo 4C es causada por una mutación autosómica dominante o autosómica recesiva en el gen SOX10, el mismo gen que en el tipo 2E.
Se realizó un estudio en un caso raro de un niño doblemente heterocigoto en el que cada padre tenía solo mutaciones únicas en MITF o PAX3. El efecto de mutaciones dobles heterocigotas en los genes MITF y PAX3 en WS1 y WS2 puede aumentar los síntomas afectados por la pigmentación. Se lleva a la conclusión de que la doble mutación de MITF está asociada con la extremidad del síndrome de Waardenburg y puede afectar los fenotipos o síntomas del síndrome.
Tabla de clasificación
| Tipo | OMIM | Gene | Locus | Herencia |
|---|---|---|---|---|
| Tipo 1 (WS1) | 193500 | PAX3 | 2q36.1 | Autosómica dominante |
| Tipo 2A (WS2A, originalmente WS2) | 193510 | MITF | 3p14.1–p12.3 | Autosómica dominante |
| Tipo 2B (WS2B) | 600193 | WS2B | 1p21–p13.3 | Autosómica dominante |
| Tipo 2C (WS2C) | 606662 | WS2C | 8p23 | Autosómica dominante |
| Tipo 2D (WS2D) | 608890 | SNAI2 | 8q11 | Receptivo autosómico |
| Tipo 2E (WS2E) | 611584 | SOX10 | 22q13.1 | Autosómica dominante |
| Tipo 3 (WS3) | 148820 | PAX3 | 2q36.1 | Recesivo autosómico dominante o autosómico |
| Tipo 4A (WS4A) | 277580 | EDNRB | 13q22 | Recesivo autosómico dominante o autosómico |
| Tipo 4B (WS4B) | 613265 | EDN3 | 20q13 | Recesivo autosómico dominante o autosómico |
| Tipo 4C (WS4C) | 613266 | SOX10 | 22q13.1 | Autosómica dominante |
Tratamiento
Actualmente no existe tratamiento ni cura para el síndrome de Waardenburg. El síntoma que con mayor probabilidad tiene importancia práctica es la sordera, y ésta se trata como cualquier otra sordera irreversible. En casos marcados, puede haber problemas estéticos. Otras anomalías (neurológicas, estructurales, enfermedad de Hirschsprung) asociadas con el síndrome se tratan sintomáticamente.
Epidemiología
La prevalencia de todos los tipos de síndrome de Waardenburg se estima en alrededor de 1 en 42.000. Los tipos 1 y 2 son, con diferencia, los más comunes, aunque el tipo 1 parece ser un poco más común. En una revisión de 2015 que analizó a 417 pacientes, se encontró que el tipo 1 era el tipo más común, abarcando alrededor de la mitad de todos los casos (47%), mientras que el tipo 2 fue el segundo tipo más común, abarcando alrededor de un tercio (33%).. La gran mayoría (alrededor del 85%) de los casos de tipo 2 son de tipo 2A. Se desconoce la prevalencia del tipo 2B, ya que sólo se informó en un estudio de 1996. Hasta ahora, el tipo 2C solo se ha encontrado en una familia italiana, y el tipo 2D solo se había encontrado en 2 pacientes no relacionados en 2018. Se informó que el número de casos conocidos de tipo 2E que involucraban anomalías neurológicas era 23 en 2017, mientras que el número del resto se desconoce. El tipo 3 es más raro que los tipos 1, 2 y 4 y comprende menos del 2% de los casos. El tipo 4 parece abarcar alrededor de una quinta parte de los casos (19%). De sus subtipos, el tipo 4C es con diferencia el más común (alrededor del 71% del tipo 4), seguido por el tipo 4A (19%) y el tipo 4B (10%).
Se estima que el síndrome de Waardenburg está presente en entre el 2% y el 5% de las personas con sordera congénita. La sordera congénita representa aproximadamente la mitad de la sordera en su conjunto. Aproximadamente 1 de cada 30 estudiantes de escuelas para sordos tiene el síndrome de Waardenburg. La presentación variable del síndrome dificulta llegar a cifras precisas sobre su prevalencia.
Historia
Descripciones tempranas
En 1916, el oftalmólogo holandés Jan van der Hoeve (1878–1952) describió a un par de niñas gemelas con sordera y un tipo particular de blefarofimosis, que se cree que es la distopía cantorum que se encuentra en el síndrome de Waardenburg tipos 1 y 3. La blefarofimosis describe los párpados. que están tan poco desarrollados que cubren permanentemente parte de los ojos.
En 1926, la médica alemana Irmgard Mende describió una familia de cuatro generaciones en la que cinco niños tenían síntomas de despigmentación del cabello, la piel y los ojos, sordera y un síndrome "mongoloide" apariencia. (Waardenburg atribuyó más tarde esta descripción a la distopía cantorum). Esto llevó más tarde a que se registrara el sinónimo síndrome de Mende en algunas bases de datos.
En 1929, el médico holandés K. T. A. Halbertsma describió un patrón familiar de distopía canthorum, y en 1930, el médico italiano Vincenzo Gualdi (1891-1976) también confirmó un patrón hereditario de distopía canthorum. Esto llevó más tarde a que en algunas bases de datos se registrara el sinónimo síndrome de Van der Hoeve-Halbertsma-Waardenburg-Gualdi.
En 1947, el oftalmólogo suizo David Klein (1908-1993) informó por primera vez de un paciente con sordera bilateral, deficiencias de pigmentación, rasgos faciales característicos y malformación de los brazos. Aunque esta fue la primera descripción completa de un paciente con síndrome de Waardenburg tipo 3, los médicos contemporáneos no consideraron que el síndrome que describió fuera el mismo que el descrito por Waardenburg cuatro años después, en parte debido a la gravedad de las malformaciones del brazo en su paciente.
El síndrome fue formalizado y descrito completamente por primera vez por el oftalmólogo y genetista holandés Petrus Johannes Waardenburg (1886-1979) en 1951. La afección que describió ahora se clasifica como síndrome de Waardenburg tipo 1.
Descripciones de subtipos
El tipo 2 se estableció por primera vez en 1971 cuando un estudio observó que algunos pacientes con síndrome de Waardenburg no tenían distopía cantorum. Un estudio de 1977 confirmó un patrón familiar en esta otra presentación. Dos estudios de 1994 confirmaron por primera vez un vínculo entre este tipo de síndrome de Waardenburg y mutaciones en el gen MITF (ahora clasificado como tipo 2A), ubicado en el cromosoma 3 en el locus 3p14.1–p12.3.
El tipo 2B se estableció por primera vez en 1994 cuando el mismo estudio que encontró mutaciones en MITF en pacientes con síndrome de Waardenburg tipo 2 también encontró que algunos pacientes no tenían ninguna mutación en esta región. Un segundo estudio de 1994 encontró un vínculo con el cromosoma 1 en el locus 1p21-p13.3. Esto se conoció como tipo 2B de la afección (con el gen denominado WS2B), sin embargo, no se ha documentado desde entonces y el gen responsable sigue siendo desconocido.
El tipo 2C se estableció en 2001 cuando un estudio de una familia italiana con características del síndrome de Waardenburg tipo 2 encontró que se debían a un gen desconocido en el cromosoma 8 en el locus 8q23 que había sido roto por una translocación cromosómica. El estudio estableció un nombre provisional para el gen, WS2C. Sin embargo, desde entonces no se han encontrado mutaciones en esta región en pacientes con síndrome de Waardenburg.
El tipo 2D se estableció en 2002 cuando un estudio que buscaba encontrar mutaciones en la versión humana del gen SNAI2, conocido por causar despigmentación en ratones, encontró deleciones de ambas copias de este gen en dos no relacionados. individuos con síndrome de Waardenburg tipo 2. Desde entonces, no se han encontrado mutaciones en ambas copias de este gen en personas con síndrome de Waardenburg tipo 2.
El tipo 2E se estableció por primera vez en 1996 cuando un estudio identificó a una niña con síntomas del síndrome de Waardenburg tipo 2 pero con un subdesarrollo adicional de la parte frontal del ojo, lo que provocaba ceguera. En 1999 se descubrió que tenía una mutación en su gen SOX10 y estudios posteriores confirmaron la asociación entre las mutaciones en este gen y este fenotipo, así como síntomas neurológicos como el retraso en el desarrollo.
El nombre del tipo 3 fue dado por primera vez por Goodman et al. en 1981, en colaboración con Klein, en el que establecieron la asociación con anomalías del brazo reportadas por primera vez por Klein en 1947. Mutaciones en PAX3 se vincularon por primera vez a este fenotipo en 1992.
La comorbilidad con la enfermedad de Hirschsprung, que más tarde constituiría el tipo 4, se observó por primera vez en varios estudios en la década de 1970. El pediatra indio Krishnakumar Shah y sus asociados describieron por primera vez el síndrome como una posible variante del síndrome de Waardenburg en 1981. La variante se atribuyó por primera vez a una mutación en EDNRB en 1994 (ahora clasificada como tipo 4A). El tipo 4B se estableció en 1996 cuando se descubrió que las mutaciones en EDN3 conducían a este tipo de síndrome de Waardenburg, y el tipo 4C se estableció por primera vez en 1998 cuando también se encontraron mutaciones en SOX10. para conducir a este tipo.
Sociedad y cultura
Cultura popular
- La novela de 2001 Shock por Robin Cook menciona un personaje con el trastorno.
- Enzo MacLeod, protagonista de la serie de libros 2006-2017 de Peter May Los archivos EnzoTiene síndrome de Waardenburg. Sus ojos son diferentes colores, y tiene una mancha blanca en su pelo.
- En la temporada 2011 episodio de Bones "Los signos en el silencio", el equipo debe resolver un caso en el que el sospechoso asesino tiene síndrome de Waardenburg.
- El libro 2013 Reconstrucción de Amelia por Kimberly McCreight presenta varios caracteres con síntomas de Waardenburg.
- El libro 2014 Más cerca de ti Piensa por Karen Rose cuenta con tres personajes, hermanos, con síndrome de Waardenburg.
- El libro 2017 Asesinato en el Templo Maya por M.J. Mandrake presenta varios caracteres con síndrome de Waardenburg.
- La novela 2019 The Whisper Network por Chandler Baker utiliza el síndrome como punto de trama.
personas notables
- Canadian YouTube vlogger Stef Sanjati tiene tipo de síndrome de Waardenburg 1.
otros animales

Los gatos domesticados con ojos azules y abrigos blancos a menudo son completamente sordos. La sordera es mucho más común en los gatos blancos que en aquellos con otros colores de abrigo. Según la Guía completa de ASPCA para los gatos , " 17 a 20 por ciento de los gatos blancos con ojos no azules son sordos; 40 por ciento de " Odd Eyer " Los gatos blancos con un ojo azul son sordos; y del 65 al 85 por ciento de los gatos blancos de ojos azules son sordos. " Aunque se han realizado pocos estudios para vincular esto con los genes que se sabe que están involucrados en el síndrome humano de Waardenburg, una interrupción genética con el desarrollo de la cresta neural también conduciría a esta presentación en gatos. Se ha encontrado que uno de los genes que conduce a la sordera y una bata blanca en los gatos cuando kit aumenta la expresión mitf .
El síndrome de blanco letal es un síndrome en caballos causados por mutaciones en ambas copias de ednrb . Conduce a la muerte por pseudo-obstrucción intestinal debido a la enfermedad de Hirschsprung. Sin embargo, una mutación en una sola copia de EDNRB , como en el síndrome de Waardenburg, tipo 4a, produce la capa blanca irregular con sordera.
hurones con el síndrome de Waardenburg tiene una pequeña franja blanca a lo largo de la parte superior o posterior de la cabeza y, a veces, en la parte posterior del cuello (conocido como A " Blaze " Patrón de abrigo), o una cabeza de color blanco sólido. Desde la nariz hasta los hombros (conocido como A " Panda " patrón de abrigo). Los hurones afectados a menudo tienen un cráneo ligeramente más plano y ojos más anchos que los hurones sanos. Como los hurones sanos tienen una mala audición, la sordera solo puede detectarse por falta de reacción a los ruidos fuertes. Como este es un trastorno heredado, los animales afectados no deben usarse para la reproducción. Un estudio de la correlación entre las variaciones de la capa y la sordera en los hurones europeos encontrados, " todos (n = 27) panda, panda americana y hurones de incendio eran sordos. "