Ritmo circadiano
Un ritmo circadiano (), o ciclo circadiano, es un proceso interno natural que regula el ciclo de sueño-vigilia y se repite aproximadamente cada 24 horas. Puede referirse a cualquier proceso que se origina dentro de un organismo (es decir, endógeno) y responde al medio ambiente (arrastrado por el medio ambiente). Estos ritmos de 24 horas son impulsados por un reloj circadiano y se han observado ampliamente en animales, plantas, hongos y cianobacterias.
El término circadiano proviene del latín circa, que significa "aproximadamente", y muere, que significa "día". Los procesos con ciclos de 24 horas se denominan más generalmente ritmos diurnos; los ritmos diurnos no deben llamarse ritmos circadianos a menos que se pueda confirmar que son endógenos y no ambientales.
Aunque los ritmos circadianos son endógenos, se ajustan al entorno local mediante señales externas llamadas zeitgebers (del alemán Zeitgeber (alemán: [ˈtsaɪtˌɡeːbɐ]; lit. 'time giver')), que incluyen luz, Temperatura y ciclos redox. En entornos clínicos, un ritmo circadiano anormal en humanos se conoce como trastorno del sueño del ritmo circadiano.
Historia
Si bien hay múltiples menciones de "ciclo corporal natural" en las culturas orientales y nativas americanas, el relato occidental más antiguo registrado de un proceso circadiano se le atribuye a Teofrasto, que data del siglo IV a. En su libro 'Περὶ φυτῶν ἱστορία', o 'Investigación sobre las plantas', Teofrasto describe un "árbol con muchas hojas como la rosa, y que se cierra por la noche, pero se abre al amanecer y al mediodía está completamente desplegado; y al anochecer vuelve a cerrarse por grados y queda cerrada de noche, y dicen los naturales que se va a dormir." El árbol mencionado por él fue identificado mucho más tarde como el árbol de tamarindo por el botánico H Bretzl, en su libro sobre los hallazgos botánicos de las campañas de Alejandría.
La observación de un proceso circadiano o diurno en humanos se menciona en textos médicos chinos que datan de alrededor del siglo XIII, incluido el Manual del mediodía y la medianoche y la Mnemonic Rhyme to Aid in the Selección de puntos de acupuntura según el ciclo diurno, el día del mes y la estación del año.
En 1729, el científico francés Jean-Jacques d'Ortous de Mairan realizó el primer experimento diseñado para distinguir un reloj endógeno de las respuestas a los estímulos diarios. Observó que persistían patrones de 24 horas en el movimiento de las hojas de la planta Mimosa pudica, incluso cuando las plantas se mantenían en oscuridad constante.
En 1896, Patrick y Gilbert observaron que durante un período prolongado de privación del sueño, la somnolencia aumenta y disminuye con un período de aproximadamente 24 horas. En 1918, J. S. Szymanski demostró que los animales son capaces de mantener patrones de actividad de 24 horas en ausencia de señales externas como la luz y los cambios de temperatura.
A principios del siglo XX, se observaron ritmos circadianos en los tiempos de alimentación rítmicos de las abejas. Auguste Forel, Ingeborg Beling y Oskar Wahl realizaron numerosos experimentos para determinar si este ritmo era atribuible a un reloj endógeno. La existencia del ritmo circadiano fue descubierta de forma independiente en las moscas de la fruta en 1935 por dos zoólogos alemanes, Hans Kalmus y Erwin Bünning.
En 1954, un importante experimento informado por Colin Pittendrigh demostró que la eclosión (el proceso de pupa que se convierte en adulto) en Drosophila pseudoobscura era un comportamiento circadiano. Demostró que, si bien la temperatura desempeñaba un papel vital en el ritmo de eclosión, el período de eclosión se retrasaba pero no se detenía cuando se disminuía la temperatura.
El término circadiano fue acuñado por Franz Halberg en 1959. Según la definición original de Halberg:
El término "circadiano" se deriva de circa (sobre) y muere (día); puede servir para implicar que ciertos períodos fisiológicos están cerca de 24 horas, si no exactamente esa longitud. En este caso, "circadiano" se puede aplicar a todos los ritmos "24 horas", ya sea o no sus períodos, individualmente o en promedio, son diferentes de 24 horas, más largas o más cortas, en unos minutos o horas.
En 1977, el Comité Internacional de Nomenclatura de la Sociedad Internacional de Cronobiología adoptó formalmente la definición:
Circadian: relacionado con variaciones biológicas o ritmos con una frecuencia de 1 ciclo en 24 ± 4 h; circa (alrededor, aproximadamente) y muere (día o 24 h). Nota: el término describe los ritmos con una longitud de ciclo de 24h, ya sean sincronizados con frecuencia (aceptables) o están desincronizados o libres de la escala de tiempo ambiental local, con períodos de ligeramente pero consistentemente diferentes de 24-h.
Ron Konopka y Seymour Benzer identificaron la primera mutación del reloj en Drosophila en 1971, llamando al gen "período" (per), el primer determinante genético descubierto de la ritmicidad del comportamiento. El gen per fue aislado en 1984 por dos equipos de investigadores. Konopka, Jeffrey Hall, Michael Roshbash y su equipo demostraron que el locus per es el centro del ritmo circadiano, y que la pérdida de per detiene la actividad circadiana. Al mismo tiempo, el equipo de Michael W. Young informó efectos similares de per, y que el gen cubre un intervalo de 7,1 kilobases (kb) en el cromosoma X y codifica un poli de 4,5 kb. (A)+ ARN. Continuaron descubriendo los genes y las neuronas clave en el sistema circadiano de Drosophila, por el cual Hall, Rosbash y Young recibieron el Premio Nobel de Fisiología o Medicina 2017.
Joseph Takahashi descubrió la primera mutación del reloj circadiano de mamíferos (relojΔ19) usando ratones en 1994. Sin embargo, estudios recientes muestran que la eliminación de reloj no conduce a un fenotipo conductual (los animales aún tienen ritmos circadianos normales), lo que cuestiona su importancia en la generación de ritmos.
La primera mutación del reloj humano fue identificada en una familia extendida de Utah por Chris Jones y caracterizada genéticamente por Ying-Hui Fu y Louis Ptacek. Los individuos afectados son 'alondras mañaneras' extremas. con sueño avanzado de 4 horas y otros ritmos. Esta forma de síndrome familiar de la fase avanzada del sueño está causada por un único cambio de aminoácido, S662➔G, en la proteína PER2 humana.
Criterios
Para ser llamado circadiano, un ritmo biológico debe cumplir con estos tres criterios generales:
- El ritmo tiene un período de libre funcionamiento endógeno que dura aproximadamente 24 horas. El ritmo persiste en condiciones constantes, es decir, oscuridad constante, con un período de alrededor de 24 horas. El período del ritmo en condiciones constantes se llama el período de libre funcionamiento y es denotado por la letra griega τ (tau). La racionalidad de este criterio es distinguir los ritmos circadianos de respuestas simples a los dados externos diarios. No se puede decir que un ritmo sea endógeno a menos que haya sido probado y persista en condiciones sin entrada periódica externa. En los animales diurnos (activos durante las horas de la luz del día), en general τ es ligeramente superior a 24 horas, mientras que en los animales nocturnos (activos por la noche), en general τ es más corto que 24 horas.
- Los ritmos son encadenables. El ritmo se puede restablecer por exposición a estímulos externos (como la luz y el calor), un proceso llamado enentrenamiento. El estímulo externo utilizado para entrenar un ritmo se llama el zeitgeber, o "Dactor de tiempo". El viaje a través de las zonas de tiempo ilustra la capacidad del reloj biológico humano para ajustarse a la hora local; una persona por lo general experimentará retrasos antes de la formación de su reloj circadiano lo ha hecho sincronizar con el tiempo local.
- Los ritmos muestran compensación de temperatura. En otras palabras, mantienen la periodicidad circadiana sobre una gama de temperaturas fisiológicas. Muchos organismos viven a una amplia gama de temperaturas, y las diferencias en la energía térmica afectarán a los cines de todos los procesos moleculares en sus células. Para hacer un seguimiento del tiempo, el reloj circadiano del organismo debe mantener aproximadamente una periodicidad de 24 horas a pesar de los kinetics cambiantes, una propiedad conocida como compensación de temperatura. El coeficiente de temperatura Q10 es una medida de este efecto compensatorio. Si el Q10 el coeficiente permanece aproximadamente 1 a medida que aumenta la temperatura, el ritmo se considera compensado por la temperatura.
Origen
Los ritmos circadianos permiten a los organismos anticipar y prepararse para cambios ambientales precisos y regulares. Por lo tanto, permiten a los organismos hacer un mejor uso de los recursos ambientales (por ejemplo, luz y alimentos) en comparación con aquellos que no pueden predecir dicha disponibilidad. Por lo tanto, se ha sugerido que los ritmos circadianos dan a los organismos una ventaja selectiva en términos evolutivos. Sin embargo, la ritmicidad parece ser tan importante en la regulación y coordinación de los procesos metabólicos internos como en la coordinación con el ambiente. Esto es sugerido por el mantenimiento (heredabilidad) de los ritmos circadianos en moscas de la fruta después de varios cientos de generaciones en condiciones constantes de laboratorio, así como en criaturas en constante oscuridad en la naturaleza, y por la eliminación experimental de los ritmos circadianos conductuales, pero no fisiológicos. en codorniz
Lo que impulsó la evolución de los ritmos circadianos ha sido una pregunta enigmática. Las hipótesis previas enfatizaron que las proteínas fotosensibles y los ritmos circadianos pueden haberse originado juntos en las primeras células, con el propósito de proteger el ADN replicado de los altos niveles de radiación ultravioleta dañina durante el día. Como resultado, la replicación quedó relegada a la oscuridad. Sin embargo, falta evidencia de esto: de hecho, los organismos más simples con un ritmo circadiano, las cianobacterias, hacen lo contrario: se dividen más durante el día. En cambio, estudios recientes destacan la importancia de la coevolución de las proteínas redox con los osciladores circadianos en los tres dominios de la vida después del Gran Evento de Oxidación hace aproximadamente 2300 millones de años. La opinión actual es que es probable que los cambios circadianos en los niveles de oxígeno ambiental y la producción de especies reactivas de oxígeno (ROS) en presencia de la luz del día hayan impulsado la necesidad de evolucionar los ritmos circadianos para adelantarse y, por lo tanto, contrarrestar las reacciones redox dañinas a diario. base.
Los relojes circadianos conocidos más simples son los ritmos circadianos bacterianos, ejemplificados por las cianobacterias procariotas. Investigaciones recientes han demostrado que el reloj circadiano de Synechococcus elongatus se puede reconstituir in vitro con solo las tres proteínas (KaiA, KaiB, KaiC) de su oscilador central. Se ha demostrado que este reloj mantiene un ritmo de 22 horas durante varios días con la adición de ATP. Las explicaciones previas del cronometrador circadiano procariótico dependían de un mecanismo de retroalimentación de transcripción/traducción de ADN.
Un defecto en el homólogo humano de Drosophila "período" El gen fue identificado como una causa del trastorno del sueño FASPS (síndrome de la fase avanzada del sueño familiar), lo que subraya la naturaleza conservada del reloj circadiano molecular a lo largo de la evolución. Ahora se conocen muchos más componentes genéticos del reloj biológico. Sus interacciones dan como resultado un circuito de retroalimentación entrelazado de productos genéticos que genera fluctuaciones periódicas que las células del cuerpo interpretan como un momento específico del día.
Ahora se sabe que el reloj circadiano molecular puede funcionar dentro de una sola célula. Es decir, es celular autónomo. Esto fue demostrado por Gene Block en neuronas retinianas basales (BRN) de moluscos aislados. Al mismo tiempo, diferentes celdas pueden comunicarse entre sí dando como resultado una salida sincronizada de señalización eléctrica. Estos pueden interactuar con las glándulas endocrinas del cerebro para dar lugar a la liberación periódica de hormonas. Los receptores de estas hormonas pueden estar ubicados a lo largo del cuerpo y sincronizar los relojes periféricos de varios órganos. Por lo tanto, la información de la hora del día transmitida por los ojos viaja al reloj en el cerebro y, a través de eso, los relojes en el resto del cuerpo pueden sincronizarse. Así es como el reloj biológico controla de forma coordinada el tiempo de, por ejemplo, el sueño/vigilia, la temperatura corporal, la sed y el apetito.
Importancia en animales
La ritmicidad circadiana está presente en los patrones de sueño y alimentación de los animales, incluidos los seres humanos. También hay patrones claros de temperatura corporal central, actividad de ondas cerebrales, producción de hormonas, regeneración celular y otras actividades biológicas. Además, el fotoperiodismo, la reacción fisiológica de los organismos a la duración del día o de la noche, es vital tanto para las plantas como para los animales, y el sistema circadiano juega un papel en la medición e interpretación de la duración del día. La predicción oportuna de los períodos estacionales de las condiciones climáticas, la disponibilidad de alimentos o la actividad de los depredadores es crucial para la supervivencia de muchas especies. Aunque no es el único parámetro, la duración cambiante del fotoperíodo (duración del día) es la señal ambiental más predictiva para la sincronización estacional de la fisiología y el comportamiento, sobre todo para la sincronización de la migración, la hibernación y la reproducción.
Efecto de la interrupción circadiana
Las mutaciones o deleciones de los genes del reloj en ratones han demostrado la importancia de los relojes corporales para garantizar el momento adecuado de los eventos celulares/metabólicos; los ratones con reloj mutante son hiperfágicos y obesos, y tienen un metabolismo de la glucosa alterado. En ratones, la eliminación del gen del reloj alfa Rev-ErbA puede provocar obesidad inducida por la dieta y cambiar el equilibrio entre la utilización de glucosa y lípidos, lo que predispone a la diabetes. Sin embargo, no está claro si existe una fuerte asociación entre los polimorfismos del gen reloj en humanos y la susceptibilidad a desarrollar el síndrome metabólico.
Efecto del ciclo luz-oscuridad
El ritmo está vinculado al ciclo de luz-oscuridad. Los animales, incluidos los humanos, que se mantienen en la oscuridad total durante períodos prolongados finalmente funcionan con un ritmo de carrera libre. Su ciclo de sueño es retrasado o adelantado cada 'día', dependiendo de si su 'día', su período endógeno, es más corto o más largo que 24 horas. Las señales ambientales que restablecen los ritmos cada día se llaman zeitgebers. Los mamíferos subterráneos totalmente ciegos (por ejemplo, la rata topo ciega Spalax sp.) son capaces de mantener sus relojes endógenos en la aparente ausencia de estímulos externos. Aunque carecen de ojos que formen imágenes, sus fotorreceptores (que detectan la luz) siguen funcionando; también salen a la superficie periódicamente.
Los organismos que corren libremente y que normalmente tienen uno o dos episodios de sueño consolidados aún los tendrán cuando estén en un ambiente protegido de señales externas, pero el ritmo no está sincronizado con el ciclo de luz-oscuridad de 24 horas en la naturaleza. El ritmo de sueño-vigilia puede, en estas circunstancias, perder la fase con otros ritmos circadianos o ultradianos, como los ritmos metabólicos, hormonales, eléctricos del SNC o de neurotransmisores.
Las investigaciones recientes han influido en el diseño de los entornos de las naves espaciales, ya que se ha descubierto que los sistemas que imitan el ciclo de luz y oscuridad son muy beneficiosos para los astronautas. La fototerapia se ha probado como tratamiento para los trastornos del sueño.
Animales del Ártico
Investigadores noruegos de la Universidad de Tromsø han demostrado que algunos animales del Ártico (por ejemplo, la perdiz nival, el reno) muestran ritmos circadianos solo en las partes del año en las que el amanecer y el atardecer son diarios. En un estudio de renos, los animales a 70 grados norte mostraron ritmos circadianos en otoño, invierno y primavera, pero no en verano. Los renos en Svalbard a 78 grados norte mostraron tales ritmos solo en otoño y primavera. Los investigadores sospechan que otros animales del Ártico tampoco pueden mostrar ritmos circadianos en la luz constante del verano y la oscuridad constante del invierno.
Un estudio de 2006 en el norte de Alaska descubrió que las ardillas terrestres y los puercoespines nocturnos mantienen estrictamente sus ritmos circadianos durante 82 días y noches de sol. Los investigadores especulan que estos dos roedores notan que la distancia aparente entre el sol y el horizonte es más corta una vez al día y, por lo tanto, tienen una señal suficiente para seguir (ajustarse).
Mariposa y polilla
La navegación de la migración otoñal de la mariposa monarca del este de América del Norte (Danaus plexippus) a sus áreas de hibernación en el centro de México utiliza una brújula solar con compensación de tiempo que depende de un reloj circadiano en sus antenas.. También se sabe que el ritmo circadiano controla el comportamiento de apareamiento en ciertas especies de polillas como Spodoptera littoralis, donde las hembras producen una feromona específica que atrae y restablece el ritmo circadiano del macho para inducir el apareamiento nocturno.
En plantas
Los ritmos circadianos de la planta le indican en qué estación se encuentra y cuándo florecer para tener la mejor oportunidad de atraer polinizadores. Los comportamientos que muestran ritmos incluyen el movimiento de las hojas, el crecimiento, la germinación, el intercambio de gases/estomas, la actividad enzimática, la actividad fotosintética y la emisión de fragancias, entre otros. Los ritmos circadianos se producen cuando una planta avanza para sincronizarse con el ciclo de luz del entorno que la rodea. Estos ritmos se generan endógenamente, son autosuficientes y relativamente constantes en un rango de temperaturas ambientales. Las características importantes incluyen dos bucles de retroalimentación de transcripción-traducción que interactúan: proteínas que contienen dominios PAS, que facilitan las interacciones proteína-proteína; y varios fotorreceptores que ajustan el reloj a diferentes condiciones de luz. La anticipación de cambios en el ambiente permite cambios apropiados en el estado fisiológico de una planta, confiriendo una ventaja adaptativa. Una mejor comprensión de los ritmos circadianos de las plantas tiene aplicaciones en la agricultura, como ayudar a los agricultores a escalonar las cosechas de cultivos para ampliar la disponibilidad de cultivos y protegerse contra pérdidas masivas debido al clima.
La luz es la señal mediante la cual las plantas sincronizan sus relojes internos con su entorno y es detectada por una amplia variedad de fotorreceptores. La luz roja y azul se absorben a través de varios fitocromos y criptocromos. Un fitocromo, phyA, es el fitocromo principal en las plántulas que crecen en la oscuridad, pero se degrada rápidamente con la luz para producir Cry1. Los fitocromos B–E son más estables con phyB, el fitocromo principal en plántulas cultivadas a la luz. El gen del criptocromo (llanto) también es un componente sensible a la luz del reloj circadiano y se cree que está involucrado como fotorreceptor y como parte del mecanismo de marcapasos endógeno del reloj. Los criptocromos 1–2 (involucrados en azul-UVA) ayudan a mantener la duración del período en el reloj a través de una amplia gama de condiciones de luz.
El oscilador central genera un ritmo autosostenido y es impulsado por dos bucles de retroalimentación que interactúan y están activos en diferentes momentos del día. El ciclo de la mañana consta de CCA1 (circadian and clock-associated 1) y LHY (Late Elongated Hypocotyl), que codifican factores de transcripción MYB estrechamente relacionados que regulan los ritmos circadianos en Arabidopsis, así como PRR 7 y 9 (Reguladores de Pseudo-Respuesta.) El ciclo vespertino consta de GI (Gigantea) y ELF4, ambos involucrados en la regulación de los genes del tiempo de floración. Cuando CCA1 y LHY se sobreexpresan (en condiciones de luz u oscuridad constantes), las plantas se vuelven arrítmicas y las señales de ARNm se reducen, lo que contribuye a un ciclo de retroalimentación negativa. La expresión génica de CCA1 y LHY oscila y alcanza su punto máximo temprano en la mañana, mientras que la expresión génica de TOC1 oscila y alcanza su punto máximo temprano en la noche. Si bien anteriormente se planteó la hipótesis de que estos tres genes modelan un ciclo de retroalimentación negativa en el que CCA1 y LHY sobreexpresados reprimen TOC1 y TOC1 sobreexpresado es un regulador positivo de CCA1 y LHY, Andrew Millar y otros demostraron en 2012 que TOC1, de hecho, sirve como represor no solo de CCA1, LHY y PRR7 y 9 en el bucle de la mañana, sino también de GI y ELF4 en el bucle de la tarde. Este hallazgo y el modelado computacional adicional de las funciones e interacciones del gen TOC1 sugieren una reformulación del reloj circadiano de la planta como un modelo represor de triple componente negativo en lugar del ciclo de retroalimentación de elemento positivo/negativo que caracteriza el reloj en los mamíferos.
En 2018, los investigadores descubrieron que la expresión de los transcritos nacientes de ARNhn de PRR5 y TOC1 sigue el mismo patrón oscilatorio que los transcritos de ARNm procesados rítmicamente en A.thaliana. Los LNK se unen a la región 5 de PRR5 y TOC1 e interactúan con RNAP II y otros factores de transcripción. Además, la interacción RVE8-LNK permite modificar un patrón permisivo de metilación de histonas (H3K4me3) y la modificación de histonas en sí es paralela a la oscilación de la expresión del gen del reloj.
Se ha descubierto anteriormente que hacer coincidir el ritmo circadiano de una planta con los ciclos de luz y oscuridad de su entorno externo tiene el potencial de afectar positivamente a la planta. Los investigadores llegaron a esta conclusión al realizar experimentos en tres variedades diferentes de Arabidopsis thaliana. Una de estas variedades tenía un ciclo circadiano normal de 24 horas. Las otras dos variedades estaban mutadas, una para tener un ciclo circadiano de más de 27 horas y otra para tener un ciclo circadiano más corto de lo normal de 20 horas.
La Arabidopsis con ciclo circadiano de 24 horas se cultivó en tres ambientes diferentes. Uno de estos ambientes tenía un ciclo de luz y oscuridad de 20 horas (10 horas de luz y 10 horas de oscuridad), el otro tenía un ciclo de luz y oscuridad de 24 horas (12 horas de luz y 12 horas de oscuridad), y el el ambiente final tuvo un ciclo de luz y oscuridad de 28 horas (14 horas de luz y 14 horas de oscuridad). Las dos plantas mutadas se cultivaron tanto en un entorno que tenía un ciclo de luz y oscuridad de 20 horas como en un entorno que tenía un ciclo de luz y oscuridad de 28 horas. Se encontró que la variedad de Arabidopsis con un ciclo de ritmo circadiano de 24 horas creció mejor en un entorno que también tenía un ciclo de luz y oscuridad de 24 horas. En general, se encontró que todas las variedades de Arabidopsis thaliana tenían mayores niveles de clorofila y un mayor crecimiento en ambientes cuyos ciclos de luz y oscuridad coincidían con su ritmo circadiano.
Los investigadores sugirieron que una razón para esto podría ser la coincidencia de una Arabidopsis's ritmo circadiano a su entorno podría permitir que la planta esté mejor preparada para el amanecer y el anochecer, y así poder sincronizar mejor sus procesos. En este estudio, también se encontró que los genes que ayudan a controlar la clorofila alcanzaron su punto máximo unas horas después del amanecer. Esto parece ser consistente con el fenómeno propuesto conocido como amanecer metabólico.
Según la hipótesis del amanecer metabólico, los azúcares producidos por la fotosíntesis tienen el potencial de ayudar a regular el ritmo circadiano y ciertas vías fotosintéticas y metabólicas. A medida que sale el sol, hay más luz disponible, lo que normalmente permite que se produzca más fotosíntesis. Los azúcares producidos por la fotosíntesis reprimen PRR7. Esta represión de PRR7 luego conduce a una mayor expresión de CCA1. Por otro lado, la disminución de los niveles de azúcar fotosintético aumenta la expresión de PRR7 y disminuye la expresión de CCA1. Este ciclo de retroalimentación entre CCA1 y PRR7 es lo que se propone para causar el amanecer metabólico.
En Drosófila
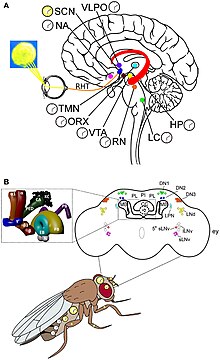
El mecanismo molecular del ritmo circadiano y la percepción de la luz se comprenden mejor en Drosophila. Los genes reloj se descubren a partir de Drosophila, y actúan junto con las neuronas reloj. Hay dos ritmos únicos, uno durante el proceso de eclosión (llamado eclosión) de la pupa y el otro durante el apareamiento. Las neuronas del reloj están ubicadas en distintos grupos en el cerebro central. Las neuronas reloj mejor entendidas son las neuronas ventrales laterales grandes y pequeñas (l-LNvs y s-LNvs) del lóbulo óptico. Estas neuronas producen factor de dispersión de pigmento (PDF), un neuropéptido que actúa como neuromodulador circadiano entre diferentes neuronas reloj.
El ritmo circadiano de Drosophila es a través de un ciclo de retroalimentación de transcripción-traducción. El mecanismo central del reloj consta de dos bucles de retroalimentación interdependientes, a saber, el bucle PER/TIM y el bucle CLK/CYC. El bucle CLK/CYC se produce durante el día e inicia la transcripción de los genes per y tim. Pero sus niveles de proteínas se mantienen bajos hasta el anochecer, ya que durante el día también se activa el gen doubletime (dbt). La proteína DBT provoca la fosforilación y el recambio de proteínas PER monoméricas. TIM también es fosforilado por Shaggy hasta el atardecer. Después de la puesta del sol, DBT desaparece, por lo que las moléculas PER se unen de manera estable a TIM. El dímero PER/TIM ingresa al núcleo varias veces por la noche y se une a los dímeros CLK/CYC. El PER unido detiene por completo la actividad transcripcional de CLK y CYC.A primera hora de la mañana, la luz activa el gen cry y su proteína CRY provoca la descomposición de TIM. Por lo tanto, el dímero PER/TIM se disocia y el PER no unido se vuelve inestable. PER sufre una fosforilación progresiva y finalmente una degradación. La ausencia de PER y TIM permite la activación de los genes clk y cyc. Por lo tanto, el reloj se reinicia para comenzar el siguiente ciclo circadiano.
Modelo POR TIEMPO
Este modelo de proteína fue desarrollado en base a las oscilaciones de las proteínas PER y TIM en la Drosophila. Se basa en su antecesor, el modelo PER donde se explicaba cómo el gen PER y su proteína influyen en el reloj biológico. El modelo incluye la formación de un complejo nuclear PER-TIM que influye en la transcripción de los genes PER y TIM (proporcionando retroalimentación negativa) y la fosforilación múltiple de estas dos proteínas. Las oscilaciones circadianas de estas dos proteínas parecen sincronizarse con el ciclo de luz-oscuridad aunque no dependan necesariamente de él. Tanto las proteínas PER como las TIM se fosforilan y, después de formar el complejo nuclear PER-TIM, regresan al interior del núcleo para detener la expresión del ARNm de PER y TIM. Esta inhibición dura mientras la proteína o el ARNm no se degrade. Cuando esto sucede, el complejo libera la inhibición. Aquí también se puede mencionar que la degradación de la proteína TIM se acelera por la luz.
En mamíferos
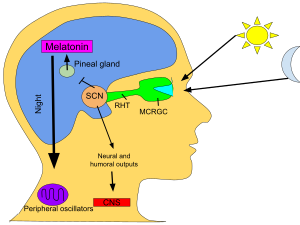
El reloj circadiano primario en los mamíferos se encuentra en el núcleo (o núcleos) supraquiasmático (SCN), un par de grupos distintos de células ubicados en el hipotálamo. La destrucción del SCN da como resultado la ausencia total de un ritmo regular de sueño y vigilia. El SCN recibe información sobre la iluminación a través de los ojos. La retina del ojo contiene "clásico" fotorreceptores ("bastones" y "conos"), que se utilizan para la visión convencional. Pero la retina también contiene células ganglionares especializadas que son directamente fotosensibles y se proyectan directamente al SCN, donde ayudan en el arrastre (sincronización) de este reloj circadiano maestro. Las proteínas involucradas en el reloj SCN son homólogas a las que se encuentran en la mosca de la fruta.
Estas células contienen el fotopigmento melanopsina y sus señales siguen una vía llamada tracto retinohipotalámico, que conduce al SCN. Si se extraen y cultivan células del SCN, mantienen su propio ritmo en ausencia de señales externas.
El SCN toma la información sobre la duración del día y la noche de la retina, la interpreta y la pasa a la glándula pineal, una estructura diminuta con forma de piña y ubicada en el epitálamo. En respuesta, la pineal secreta la hormona melatonina. La secreción de melatonina tiene picos durante la noche y reflujos durante el día y su presencia proporciona información sobre la duración de la noche.
Varios estudios han indicado que la melatonina pineal retroalimenta la ritmicidad del SCN para modular los patrones circadianos de actividad y otros procesos. Sin embargo, se desconoce la naturaleza y la importancia a nivel del sistema de esta retroalimentación.
Los ritmos circadianos de los humanos pueden ajustarse a períodos ligeramente más cortos y más largos que las 24 horas de la Tierra. Investigadores de Harvard han demostrado que los sujetos humanos pueden al menos entrenarse en un ciclo de 23,5 horas y un ciclo de 24,65 horas.
Humanos
Las primeras investigaciones sobre los ritmos circadianos sugirieron que la mayoría de las personas preferían un día más cercano a las 25 horas cuando estaban aisladas de estímulos externos como la luz del día y el cronometraje. Sin embargo, esta investigación fue defectuosa porque no logró proteger a los participantes de la luz artificial. Aunque los sujetos estaban protegidos de las señales de tiempo (como los relojes) y la luz del día, los investigadores no estaban al tanto de los efectos de retraso de fase de las luces eléctricas interiores. A los sujetos se les permitió encender la luz cuando estaban despiertos y apagarla cuando querían dormir. La luz eléctrica de la tarde retrasó su fase circadiana. Un estudio más estricto realizado en 1999 por la Universidad de Harvard estimó que el ritmo humano natural está más cerca de 24 horas y 11 minutos: mucho más cerca del día solar. De acuerdo con esta investigación, un estudio más reciente de 2010 también identificó diferencias de sexo, siendo el período circadiano ligeramente más corto para las mujeres (24,09 horas) que para los hombres (24,19 horas). En este estudio, las mujeres tendían a despertarse más temprano que los hombres y mostraban una mayor preferencia por las actividades matutinas que los hombres, aunque se desconocen los mecanismos biológicos subyacentes de estas diferencias.
Marcadores y efectos biológicos
Los marcadores de fase clásicos para medir la sincronización del ritmo circadiano de un mamífero son:
- secreción de melatonina por la glándula pineal,
- temperatura corporal mínima, y
- Nivel de plasma de cortisol.
Para los estudios de temperatura, los sujetos deben permanecer despiertos pero tranquilos y semi-reclinados en la oscuridad cercana mientras se les toma la temperatura rectal de forma continua. Aunque la variación es grande entre los cronotipos normales, la temperatura promedio de un adulto humano alcanza su mínimo alrededor de las 5:00 am, unas dos horas antes de la hora habitual de despertar. Baehr et al. encontraron que, en adultos jóvenes, la temperatura corporal mínima diaria se producía alrededor de las 04:00 (4 a. m.) para los tipos matutinos, pero alrededor de las 06:00 (6 a. m.) para los tipos vespertinos. Este mínimo ocurrió aproximadamente a la mitad del período de sueño de ocho horas para los tipos matutinos, pero más cerca del despertar en los tipos vespertinos.
La melatonina está ausente del sistema o es indetectablemente baja durante el día. Su inicio en luz tenue, inicio de melatonina en luz tenue (DLMO), aproximadamente a las 21:00 (9:00 p. m.) se puede medir en la sangre o la saliva. Su principal metabolito también se puede medir en la orina de la mañana. Tanto el DLMO como el punto medio (en el tiempo) de la presencia de la hormona en la sangre o la saliva se han utilizado como marcadores circadianos. Sin embargo, investigaciones más recientes indican que la compensación de melatonina puede ser el marcador más confiable. Benloucif et al. encontraron que los marcadores de fase de melatonina eran más estables y estaban más altamente correlacionados con el momento del sueño que con la temperatura central mínima. Descubrieron que tanto la compensación del sueño como la compensación de la melatonina están más fuertemente correlacionadas con los marcadores de fase que con el inicio del sueño. Además, la fase de declinación de los niveles de melatonina es más confiable y estable que la terminación de la síntesis de melatonina.
Otros cambios fisiológicos que ocurren de acuerdo con un ritmo circadiano incluyen la frecuencia cardíaca y muchos procesos celulares, incluido el estrés oxidativo, el metabolismo celular, las respuestas inmunitarias e inflamatorias, la modificación epigenética, las vías de respuesta a la hipoxia/hiperoxia, el estrés reticular endoplásmico, la autofagia. y regulación del entorno de las células madre." En un estudio de hombres jóvenes, se encontró que el ritmo cardíaco alcanza su ritmo promedio más bajo durante el sueño y su ritmo promedio más alto poco después de despertarse.
En contradicción con estudios previos, se ha encontrado que no hay efecto de la temperatura corporal sobre el rendimiento en las pruebas psicológicas. Esto probablemente se deba a presiones evolutivas para una función cognitiva superior en comparación con las otras áreas de función examinadas en estudios anteriores.
Fuera del "reloj maestro"
Los ritmos circadianos más o menos independientes se encuentran en muchos órganos y células del cuerpo fuera de los núcleos supraquiasmáticos (SCN), el "reloj maestro". De hecho, el neurocientífico Joseph Takahashi y sus colegas afirmaron en un artículo de 2013 que "casi todas las células del cuerpo contienen un reloj circadiano". Por ejemplo, estos relojes, llamados osciladores periféricos, se han encontrado en la glándula suprarrenal, el esófago, los pulmones, el hígado, el páncreas, el bazo, el timo y la piel. También hay alguna evidencia de que el bulbo olfatorio y la próstata pueden experimentar oscilaciones, al menos cuando se cultivan.
Aunque los osciladores de la piel responden a la luz, no se ha demostrado una influencia sistémica. Además, se ha demostrado que muchos osciladores, como las células del hígado, por ejemplo, responden a entradas distintas de la luz, como la alimentación.
La luz y el reloj biológico
La luz restablece el reloj biológico de acuerdo con la curva de respuesta de fase (PRC). Dependiendo del momento, la luz puede adelantar o retrasar el ritmo circadiano. Tanto el PRC como la iluminancia requerida varían de una especie a otra, y se requieren niveles de luz más bajos para restablecer los relojes en roedores nocturnos que en humanos.
Ciclos obligatorios más largos o más cortos
Diversos estudios en humanos han hecho uso de ciclos forzados de sueño/vigilia muy diferentes de 24 horas, como los realizados por Nathaniel Kleitman en 1938 (28 horas) y Derk-Jan Dijk y Charles Czeisler en la década de 1990 (20 horas). Debido a que las personas con un reloj circadiano normal (típico) no pueden adaptarse a ritmos diurnos/nocturnos tan anormales, esto se denomina protocolo de desincronización forzada. Según dicho protocolo, los episodios de sueño y vigilia se desacoplan del período circadiano endógeno del cuerpo, lo que permite a los investigadores evaluar los efectos de la fase circadiana (es decir, el momento relativo del ciclo circadiano) en aspectos del sueño y la vigilia, incluidos latencia del sueño y otras funciones, tanto fisiológicas, conductuales y cognitivas.
Los estudios también muestran que Cyclosa turbinata es única en el sentido de que su actividad locomotora y de construcción de redes hace que tenga un reloj circadiano de período excepcionalmente corto, alrededor de 19 horas. Cuando C. turbinata se colocan en cámaras con períodos de 19, 24 o 29 horas de luz y oscuridad divididas uniformemente, ninguna de las arañas exhibió una disminución de la longevidad en su propio reloj circadiano. Estos hallazgos sugieren que C. turbinata no tienen los mismos costos de desincronización extrema que tienen otras especies de animales.
Salud humana
Fundamentos de la medicina circadiana
La vanguardia de la investigación en biología circadiana es la traducción de los mecanismos básicos del reloj corporal en herramientas clínicas, y esto es especialmente relevante para el tratamiento de enfermedades cardiovasculares. Esto está conduciendo al desarrollo de un campo de la medicina completamente nuevo, denominado medicina circadiana. Una investigación pionera revela que la medicina circadiana puede conducir a una vida más larga y saludable. Por ejemplo: 1) "Iluminación circadiana" o la reducción de la luz adversa durante la noche en los hospitales puede mejorar los resultados de los pacientes después de un infarto de miocardio (ataque cardíaco). 2) "Cronoterapia circadiana" o la sincronización de los medicamentos puede reducir la remodelación cardíaca adversa en pacientes con enfermedades cardíacas. El momento del tratamiento médico en coordinación con el reloj biológico, la cronoterapia, también puede beneficiar a los pacientes con hipertensión (presión arterial alta) al aumentar significativamente la eficacia y reducir la toxicidad del fármaco o las reacciones adversas. 3) "Farmacología circadiana" o Se ha demostrado experimentalmente en modelos de roedores que los fármacos dirigidos al mecanismo del reloj circadiano reducen significativamente el daño debido a los ataques cardíacos y previenen la insuficiencia cardíaca. Es importante destacar que, para la traducción racional de las terapias de medicina circadiana más prometedoras a la práctica clínica, es imperativo que entendamos cómo ayuda a tratar la enfermedad en ambos sexos biológicos.
Relación con la enfermedad cardiovascular
Uno de los primeros estudios para determinar cómo la interrupción de los ritmos circadianos causa enfermedades cardiovasculares se realizó en los hámsters Tau, que tienen un defecto genético en su mecanismo de reloj circadiano. Cuando se mantuvo en un ciclo de luz-oscuridad de 24 horas que estaba "desincronizado" con su mecanismo circadiano normal 22 desarrollaron enfermedad cardiovascular y renal profunda; sin embargo, cuando los animales Tau fueron criados durante toda su vida en un ciclo diario de luz y oscuridad de 22 horas, tenían un sistema cardiovascular saludable. Los efectos adversos de la desalineación circadiana en la fisiología humana se han estudiado en el laboratorio utilizando un protocolo de desalineación y estudiando a los trabajadores por turnos.
Desincronía circadiana
Estudios posteriores han demostrado que mantener el sueño y los ritmos circadianos normales es importante para muchos aspectos del cerebro y la salud. Varios estudios también han indicado que una siesta reparadora, un breve período de sueño durante el día, puede reducir el estrés y mejorar la productividad sin ningún efecto medible en los ritmos circadianos normales. Los ritmos circadianos también juegan un papel en el sistema de activación reticular, que es crucial para mantener un estado de conciencia. Una inversión en el ciclo sueño-vigilia puede ser un signo o complicación de uremia, azotemia o lesión renal aguda. Los estudios también han ayudado a dilucidar cómo la luz tiene un efecto directo en la salud humana a través de su influencia en la biología circadiana.
Iluminación interior
Los requisitos de iluminación para la regulación circadiana no son simplemente los mismos que para la visión; la planificación de la iluminación interior en oficinas e instituciones está empezando a tener esto en cuenta. Los estudios en animales sobre los efectos de la luz en condiciones de laboratorio han considerado hasta hace poco la intensidad de la luz (irradiación), pero no el color, que se puede demostrar que "actúa como un regulador esencial del tiempo biológico en entornos más naturales".
Obesidad y diabetes
La obesidad y la diabetes están asociadas con el estilo de vida y factores genéticos. Entre esos factores, la interrupción del reloj circadiano y/o la desalineación del sistema de tiempo circadiano con el entorno externo (p. ej., el ciclo de luz y oscuridad) podrían desempeñar un papel en el desarrollo de trastornos metabólicos.
El trabajo por turnos o el desfase horario crónico tienen profundas consecuencias para los eventos metabólicos y circadianos del cuerpo. Los animales que se ven obligados a comer durante su período de descanso muestran un aumento de la masa corporal y una expresión alterada de los genes metabólicos y del reloj. En los seres humanos, el trabajo por turnos que favorece horarios irregulares para comer se asocia con una sensibilidad alterada a la insulina y una mayor masa corporal. El trabajo por turnos también conduce a mayores riesgos metabólicos de síndrome cardiometabólico, hipertensión e inflamación.
Pilotos de líneas aéreas y tripulantes de cabina
Debido a la naturaleza del trabajo de los pilotos de líneas aéreas, que a menudo cruzan varias zonas horarias y regiones de luz solar y oscuridad en un día, y pasan muchas horas despiertos tanto de día como de noche, a menudo no pueden mantener patrones de sueño que se correspondan con los ritmo circadiano humano natural; esta situación puede conducir fácilmente a la fatiga. La NTSB menciona que esto contribuye a muchos accidentes y ha realizado varios estudios de investigación para encontrar métodos para combatir la fatiga en los pilotos.
Interrupción
La interrupción de los ritmos suele tener un efecto negativo. Muchos viajeros han experimentado la condición conocida como jet lag, con sus síntomas asociados de fatiga, desorientación e insomnio.
Otros trastornos, como el trastorno bipolar y algunos trastornos del sueño, como el trastorno de la fase retrasada del sueño (DSPD), están asociados con el funcionamiento irregular o patológico de los ritmos circadianos.
Se cree que la interrupción de los ritmos a largo plazo tiene importantes consecuencias adversas para la salud de los órganos periféricos fuera del cerebro, en particular en el desarrollo o la exacerbación de enfermedades cardiovasculares. La iluminación LED azul suprime la producción de melatonina cinco veces más que la luz de sodio de alta presión (HPS) de color amarillo anaranjado; una lámpara de haluro metálico, que es luz blanca, suprime la melatonina a un ritmo más de tres veces mayor que HPS. Los síntomas de depresión de la exposición prolongada a la luz nocturna se pueden deshacer volviendo a un ciclo normal.
Efecto de las drogas
Los estudios realizados en animales y humanos muestran importantes relaciones bidireccionales entre el sistema circadiano y las drogas de abuso. Se indica que estas drogas abusivas afectan el marcapasos circadiano central. Las personas con trastorno por uso de sustancias muestran ritmos interrumpidos. Estos ritmos interrumpidos pueden aumentar el riesgo de abuso de sustancias y recaídas. Es posible que las alteraciones genéticas y/o ambientales del ciclo normal de sueño y vigilia puedan aumentar la susceptibilidad a la adicción.
Es difícil determinar si una alteración en el ritmo circadiano es la causa del aumento en la prevalencia del abuso de sustancias, o si la culpa es de otros factores ambientales, como el estrés. Los cambios en el ritmo circadiano y el sueño ocurren una vez que una persona comienza a abusar de las drogas y el alcohol. Una vez que una persona decide dejar de consumir drogas y alcohol, el ritmo circadiano continúa interrumpiéndose.
La estabilización del sueño y el ritmo circadiano posiblemente podría ayudar a reducir la vulnerabilidad a la adicción y reducir las posibilidades de recaída.
Los ritmos circadianos y los genes del reloj expresados en regiones del cerebro fuera del núcleo supraquiasmático pueden influir significativamente en los efectos producidos por drogas como la cocaína. Además, las manipulaciones genéticas de los genes del reloj afectan profundamente las acciones de la cocaína.
Sociedad y cultura
En 2017, Jeffrey C. Hall, Michael W. Young y Michael Rosbash recibieron el Premio Nobel de Fisiología o Medicina "por sus descubrimientos de los mecanismos moleculares que controlan el ritmo circadiano".
Los ritmos circadianos se tomaron como un ejemplo de transferencia del conocimiento científico a la esfera pública.
Contenido relacionado
Dilatación y extracción intactas
Ericáceas
Muerte negra