Rifampicina
Rifampicina, también conocida como rifampicina, es un antibiótico ansamicina que se usa para tratar varios tipos de infecciones bacterianas, incluida la tuberculosis (TB), el complejo Mycobacterium avium, la lepra y Legionarios' enfermedad. Casi siempre se utiliza junto con otros antibióticos, con dos excepciones notables: cuando se administra como "tratamiento preferido y fuertemente recomendado" para infección de tuberculosis latente; y cuando se usa como profilaxis post-exposición para prevenir Haemophilus influenzae tipo b y la enfermedad meningocócica en personas que han estado expuestas a esas bacterias. Antes de tratar a una persona durante un período prolongado, se recomiendan mediciones de enzimas hepáticas y recuentos sanguíneos. La rifampicina se puede administrar por vía oral o intravenosa.
Los efectos secundarios comunes incluyen náuseas, vómitos, diarrea y pérdida de apetito. A menudo la orina, el sudor y las lágrimas adquieren un color rojo o naranja. Pueden producirse problemas hepáticos o reacciones alérgicas. Forma parte del tratamiento recomendado de la tuberculosis activa durante el embarazo, aunque se desconoce su seguridad durante el embarazo. La rifampicina pertenece al grupo de antibióticos de la rifamicina. Actúa disminuyendo la producción de ARN por parte de las bacterias.
La rifampicina se descubrió en 1965, se comercializó en Italia en 1968 y se aprobó en los Estados Unidos en 1971. Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud. La Organización Mundial de la Salud clasifica la rifampicina como de importancia crítica para la medicina humana. Está disponible como medicamento genérico. La rifampicina es producida por la bacteria del suelo Amycolatopsis rifamycinica.
Usos médicos

Mycobacteria
La rifampicina se usa para el tratamiento de la tuberculosis en combinación con otros antibióticos, como pirazinamida, isoniazida y etambutol. Para el tratamiento de la tuberculosis se administra diariamente durante al menos seis meses. La terapia combinada se utiliza para prevenir el desarrollo de resistencia y acortar la duración del tratamiento. La resistencia de Mycobacterium tuberculosis a la rifampicina se desarrolla rápidamente cuando se usa sin otro antibiótico, con estimaciones de laboratorio de tasas de resistencia de 10−7 a 10−10 por bacteria de tuberculosis por generación.
La rifampicina se puede utilizar sola en pacientes con infecciones tuberculosas latentes para prevenir o retrasar el desarrollo de la enfermedad activa porque sólo hay una pequeña cantidad de bacterias presentes. Una revisión Cochrane no encontró diferencias en la eficacia entre un régimen de rifampicina de 3 a 4 meses y un régimen de isoniazida de 6 meses para prevenir la tuberculosis activa en pacientes no infectados con VIH, y los pacientes que recibieron rifampicina tuvieron una tasa más baja de hepatotoxicidad. Sin embargo, la calidad de la evidencia se consideró baja. Anteriormente se había recomendado un ciclo más corto de dos meses con rifampicina y pirazinamida, pero ya no se recomienda debido a las altas tasas de hepatotoxicidad.
La rifampicina debe tomarse con el estómago vacío y con un vaso de agua. Generalmente se toma al menos una hora antes de las comidas o dos horas después de las comidas.
La rifampicina también se usa para tratar infecciones por micobacterias no tuberculosas, incluida la lepra (enfermedad de Hansen) y Mycobacterium kansasii.
Con la terapia multimedicamentosa utilizada como tratamiento estándar de la enfermedad de Hansen, la rifampicina siempre se usa en combinación con dapsona y clofazimina para evitar causar resistencia a los medicamentos.
También se utiliza en el tratamiento de infecciones por Mycobacterium ulcerans asociadas con la úlcera de Buruli, generalmente en combinación con claritromicina u otros antibióticos.
Otras bacterias y protozoos
En 2008, pruebas provisionales demostraron que la rifampicina puede ser útil en el tratamiento del Staphylococcus aureus (MRSA) resistente a la meticilina en combinación con otros antibióticos, incluso en infecciones difíciles de tratar como la osteomielitis y Infecciones de prótesis articulares. En 2012, no estaba claro si la terapia combinada con rifampicina era útil para la osteomielitis vertebral piógena. Un metanálisis concluyó que agregar rifampicina como complemento a un β-lactámico o vancomicina puede mejorar los resultados en la bacteriemia por estafilococo aureus. Sin embargo, un ensayo más reciente no encontró ningún beneficio con la rifampicina como complemento.
También se utiliza como tratamiento preventivo contra las infecciones por Neisseria meningitidis (meningocócicas). La rifampicina también se recomienda como tratamiento alternativo para las infecciones por los patógenos transmitidos por garrapatas Borrelia burgdorferi y Anaplasma phagocytophilum cuando el tratamiento con doxiciclina está contraindicado, como en mujeres embarazadas o en pacientes. con antecedentes de alergia a los antibióticos de tetraciclina.
A veces también se utiliza para tratar infecciones por especies de Listeria, Neisseria gonorrhoeae, Haemophilus influenzae y Legionella pneumophila. yo>. Para estas indicaciones no estándar, se deben realizar pruebas de susceptibilidad a los antimicrobianos (si es posible) antes de iniciar el tratamiento con rifampicina.
Las especies Enterobacteriaceae, Acinetobacter y Pseudomonas son intrínsecamente resistentes a la rifampicina.
Se ha utilizado con anfotericina B en intentos en gran medida infructuosos de tratar la meningoencefalitis amebiana primaria causada por Naegleria fowleri.
La rifampicina se puede utilizar en monoterapia durante unos días como profilaxis contra la meningitis, pero la resistencia se desarrolla rápidamente durante el tratamiento a largo plazo de infecciones activas, por lo que el fármaco siempre se utiliza contra infecciones activas en combinación con otros antibióticos.
La rifampicina es relativamente ineficaz contra las espiroquetas, lo que ha llevado a su uso como agente selectivo capaz de aislarlas en materiales que se cultivan en laboratorios.
Virus
La rifampicina tiene cierta eficacia contra el virus vaccinia.
Susceptibilidad a patógenos
Las concentraciones inhibidoras mínimas de rifampicina para varios patógenos médicamente importantes son:
- Mycobacterium tuberculosis 0,002 – 64 μg/m L
- Mycobacterium bovis 0.125 μg/m L
- Staphylococcus aureus (resistente a la methicilina) — ≤ 0,006–256 μg/mL
- Chlamydia pneumoniae — 0.005 μg/m L
Colangitis biliar primaria
La rifampicina se usa para tratar la picazón causada por la colangitis biliar primaria. Los efectos adversos relacionados con el tratamiento incluyen hepatotoxicidad, nefrotoxicidad, hemólisis e interacciones con otros fármacos. Por esas razones, así como por algunas preocupaciones éticas con respecto al uso no autorizado de antibióticos, la rifampicina, como antibiótico preventivo muy eficaz para la meningitis, no se considera apropiada para la picazón.
Hidradenitis supurativa
La rifampicina con clindamicina se ha utilizado para tratar la enfermedad de la piel hidradenitis supurativa.
Efectos adversos
El efecto adverso más grave es la hepatotoxicidad, y las personas que la reciben a menudo experimentan pruebas de base y frecuentes funciones hepáticas para detectar daño hepático temprano.
Los efectos secundarios más comunes incluyen fiebre, trastornos gastrointestinales, erupciones cutáneas y reacciones inmunológicas. La toma de rifampicina suele provocar que ciertos fluidos corporales, como la orina, el sudor y las lágrimas, adquieran un color rojo anaranjado, un efecto secundario benigno que, sin embargo, puede resultar aterrador si no se espera. Esto también se puede utilizar para controlar la absorción efectiva del fármaco (si no se observa el color del fármaco en la orina, es posible que el paciente desee alejar la dosis del fármaco en el tiempo de la ingesta de alimentos o leche). La decoloración del sudor y las lágrimas no se nota directamente, pero el sudor puede manchar la ropa clara de naranja y las lágrimas pueden manchar permanentemente los lentes de contacto blandos. Dado que la rifampicina puede excretarse en la leche materna, se debe evitar la lactancia mientras se esté tomando.
Otros efectos adversos incluyen:
- Toxicidad del hígado: hepatitis, insuficiencia hepática en casos graves
- Insuficiencia respiratoria
- Corriente: fluir, pruritus, erupción, hiperpigmentación, enrojecimiento y riego de los ojos
- Abdominal — náuseas, vómitos, calambres abdominales, diarrea
- Síntomas parecidos a la gripe: enfermedades, fiebre, dolor de cabeza, arthralgia y malestar. Rifampicin tiene buena penetración en el cerebro, y esto puede explicar directamente algún malestar y disforia en una minoría de usuarios.
- Reacción alérgica: sarpullidos, picazón, inflamación de la lengua o garganta, mareos severos y dificultad para respirar
Estructura química
La rifampicina es un policétido que pertenece a la clase química de compuestos denominados ansamicinas, llamados así debido a su estructura heterocíclica que contiene un núcleo de naftoquinona atravesado por una cadena alifática ansa. El cromóforo naftoquinónico confiere a la rifampicina su característico color cristalino rojo anaranjado.
Los grupos funcionales críticos de la rifampicina en su unión inhibidora de la ARN polimerasa bacteriana son los cuatro grupos hidroxilo críticos del puente ansa y el anillo naftol, que forman enlaces de hidrógeno con residuos de aminoácidos en la proteína.
La rifampicina es el derivado 3-(4-metil-1-piperazinil)-iminometilo de la rifamicina SV.
Interacciones
La rifampicina es el inductor más potente conocido del sistema enzimático citocromo P450 hepático, incluidas las isoenzimas CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP3A4, CYP3A5 y CYP3A7. Aumenta el metabolismo de muchos fármacos y, como consecuencia, puede hacerlos menos eficaces, o incluso ineficaces, al disminuir sus niveles. Por ejemplo, los pacientes sometidos a terapia anticoagulante a largo plazo con warfarina deben aumentar su dosis de warfarina y controlar su tiempo de coagulación con frecuencia porque no hacerlo podría conducir a una anticoagulación inadecuada, lo que tendría consecuencias graves de tromboembolismo.
La rifampicina puede reducir la eficacia de las píldoras anticonceptivas u otros anticonceptivos hormonales mediante la inducción del sistema citocromo P450, hasta el punto de que se han producido embarazos no deseados en mujeres que usan anticonceptivos orales y tomaron rifampicina incluso en ciclos muy cortos (por ejemplo, , como profilaxis contra la exposición a meningitis bacteriana).
Otras interacciones incluyen niveles reducidos y menor eficacia de los agentes antirretrovirales, everolimus, atorvastatina, rosiglitazona, pioglitazona, celecoxib, claritromicina, caspofungina, voriconazol y lorazepam.
La rifampicina es antagonista de los efectos microbiológicos de los antibióticos gentamicina y amikacina. La actividad de la rifampicina contra algunas especies de micobacterias puede potenciarse con la isoniazida (mediante la inhibición de la síntesis de micolato) y el ambroxol (mediante efectos dirigidos por el huésped en la autofagia y la farmacocinética).
Farmacología
Mecanismo de acción
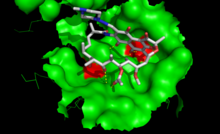
La rifampicina inhibe la síntesis de ARN dependiente de ADN bacteriano al inhibir la ARN polimerasa dependiente de ADN bacteriana.
Los datos de la estructura cristalina y los datos bioquímicos sugieren que la rifampicina se une al bolsillo de la subunidad β de la ARN polimerasa dentro del canal de ADN/ARN, pero lejos del sitio activo. El inhibidor previene la síntesis de ARN bloqueando físicamente el alargamiento y evitando así la síntesis de proteínas bacterianas del huésped. Mediante esta "oclusión estérica" mecanismo, la rifampicina bloquea la síntesis del segundo o tercer enlace fosfodiéster entre los nucleótidos en la columna vertebral del ARN, impidiendo el alargamiento del enlace 5' El extremo de la transcripción de ARN pasa más de 2 o 3 nucleótidos.
En un estudio reciente, se demostró que la rifampicina se une a la citocromo P450 reductasa y altera su conformación, así como su actividad para apoyar el metabolismo de la progesterona a través de CYP21A2.
Mecanismo de resistencia
La resistencia a la rifampicina surge de mutaciones que alteran los residuos del sitio de unión de la rifampicina en la ARN polimerasa, lo que resulta en una disminución de la afinidad por la rifampicina. Las mutaciones de resistencia se asignan al gen rpoB, que codifica la subunidad beta de la ARN polimerasa. La mayoría de las mutaciones de resistencia en E. coli se encuentran en 3 grupos en rpoB. El grupo I son los aminoácidos 509 a 533, el grupo II son los aminoácidos 563 a 572 y el grupo III es el aminoácido 687.
Al describir mutaciones en rpoB en otras especies, el número de aminoácidos correspondiente en E. coli se suele utilizar. En Mycobacterium tuberculosis, la mayoría de las mutaciones que conducen a la resistencia a la rifampicina se encuentran en el grupo I, en una región central de 81 pb llamada RRDR para “región determinante de la resistencia a la rifampcina”. La mutación más común es un cambio en el aminoácido 531 de serina a leucina que surge de un cambio en la secuencia de ADN de TCG a TTG. También se ha producido resistencia a la tuberculosis debido a mutaciones en la región N-terminal de rpoB y el grupo III.
Un mecanismo alternativo de resistencia es a través de la ribosilación ADP de rifampicina catalizada por Arr. Con la ayuda de la enzima Arr producida por el patógeno Mycobacterium smegmatis, se añade ADP-ribosa a la rifampicina en uno de sus grupos hidroxi de la cadena ansa, inactivando así el fármaco.
Resistencia en la tuberculosis
La resistencia de las micobacterias a la rifampicina puede ocurrir sola o junto con la resistencia a otros fármacos antituberculosos de primera línea. La detección temprana de esta tuberculosis multirresistente o extremadamente resistente a los medicamentos es fundamental para mejorar los resultados de los pacientes mediante el establecimiento de tratamientos apropiados de segunda línea y para disminuir la transmisión de la tuberculosis resistente a los medicamentos. Los métodos tradicionales para detectar resistencia implican cultivos de micobacterias y pruebas de susceptibilidad a fármacos, cuyos resultados pueden tardar hasta seis semanas. El ensayo Xpert MTB/RIF es una prueba automatizada que puede detectar la resistencia a la rifampicina y también diagnosticar la tuberculosis. Una revisión Cochrane actualizada en 2014 y 2021 concluyó que para la detección de resistencia a la rifampicina, Xpert MTB/RIF fue preciso, es decir, (95%) sensible y (98%) específico.
Farmacocinética
La rifampicina administrada por vía oral produce concentraciones plasmáticas máximas en aproximadamente 2 a 4 horas. El ácido 4-aminosalicílico (otro fármaco antituberculoso) reduce significativamente la absorción de rifampicina y las concentraciones máximas pueden ser menores. Si estos dos medicamentos deben usarse simultáneamente, deben administrarse por separado, con un intervalo de 8 a 12 horas entre administraciones.
La rifampicina se absorbe fácilmente en el tracto gastrointestinal (GI); su grupo funcional éster se hidroliza rápidamente en la bilis y está catalizado por un pH alto y esterasas específicas de sustrato. Después de aproximadamente 6 horas, casi todo el fármaco se desacetila. Incluso en esta forma desacetilada, la rifampicina sigue siendo un antibiótico potente; sin embargo, ya no puede ser reabsorbido por los intestinos y se elimina del cuerpo. Sólo alrededor del 7% del fármaco administrado se excreta sin cambios en la orina, aunque la eliminación urinaria representa sólo alrededor del 30% de la excreción del fármaco. Alrededor del 60% al 65% se excreta a través de las heces.
La vida media de la rifampicina oscila entre 1,5 y 5,0 horas, aunque la insuficiencia hepática la aumenta significativamente. El consumo de alimentos inhibe su absorción en el tracto gastrointestinal y el fármaco se elimina más rápidamente. Cuando la rifampicina se toma con las comidas, su concentración sanguínea máxima cae un 36%. Los antiácidos no afectan su absorción. La disminución en la absorción de rifampicina con los alimentos a veces es suficiente para afectar notablemente el color de la orina, que puede usarse como marcador de si una dosis del medicamento se ha absorbido efectivamente o no.
La distribución del fármaco es alta en todo el cuerpo y alcanza concentraciones efectivas en muchos órganos y fluidos corporales, incluido el líquido cefalorraquídeo. Dado que la sustancia en sí es roja, esta alta distribución es la causa del color rojo anaranjado de la saliva, las lágrimas, el sudor, la orina y las heces. Alrededor del 60% al 90% del fármaco se une a las proteínas plasmáticas.
Uso en biotecnología
La rifampicina inhibe la ARN polimerasa bacteriana y se usa comúnmente para inhibir la síntesis de proteínas bacterianas del huésped durante la expresión de proteínas recombinantes en bacterias. El ARN que codifica el gen recombinante generalmente se transcribe a partir del ADN mediante una ARN polimerasa viral T7, que no se ve afectada por la rifampicina.
Historia
En 1957, una muestra de suelo de un bosque de pinos en la Riviera francesa fue llevada para su análisis al laboratorio de investigación de Lepetit Pharmaceuticals en Milán, Italia. Allí, un grupo de investigación encabezado por Piero Sensi y María Teresa Timbal descubrió una nueva bacteria. Esta nueva especie produjo una nueva clase de moléculas con actividad antibiótica. Como a Sensi, Timbal y los investigadores les gustó especialmente la historia criminal francesa Rififi (sobre un robo de joyas y bandas rivales), decidieron llamar a estos compuestos rifamicinas. Después de dos años de intentos por obtener productos semisintéticos más estables, en 1965 se produjo una nueva molécula con alta eficacia y buena tolerabilidad y se llamó rifampicina.
La rifampicina se vendió por primera vez en Italia en 1968 y fue aprobada por la FDA en 1971.
Sociedad y cultura
Impurezas cancerígenas
En agosto de 2020, la Administración de Alimentos y Medicamentos de EE. UU. (FDA) se dio cuenta de impurezas de nitrosamina en ciertas muestras de rifampicina. La FDA y los fabricantes están investigando el origen de estas impurezas en la rifampicina, y la agencia está desarrollando métodos de prueba para que los reguladores y la industria detecten la 1-metil-4-nitrosopiperazina (MNP). MNP pertenece a la clase de compuestos de nitrosamina, algunos de los cuales están clasificados como probables o posibles carcinógenos humanos (sustancias que podrían causar cáncer), según pruebas de laboratorio como estudios de carcinogenicidad en roedores. Aunque no hay datos disponibles para evaluar directamente el potencial carcinogénico de las MNP, se utilizó la información disponible sobre compuestos de nitrosamina estrechamente relacionados para calcular los límites de exposición de por vida a las MNP.
A partir de enero de 2021, la FDA continúa investigando la presencia de 1-metil-4-nitrosopiperazina (MNP) en la rifampicina o 1-ciclopentil-4-nitrosopiperazina (CPNP) en la rifapentina aprobada para su venta en los EE. UU.
Nombres
La rifampicina es la posada y la prohibición, mientras que la rifampicina es la USAN. La rifampicina puede abreviarse R, RMP, RA, RF o RIF (EE. UU.).
La rifampicina también se conoce como rifaldazina, rofact y rifampicina en los Estados Unidos, también como rifamicina SV.
Su nombre químico es 5,6,9,17,19,21-hexahidroxi-23-metoxi-2,4,12,16,18,20,22-heptametil-8-[N-(4-metilo 21-acetato de -1-piperazinil)formimidoil]-2,7-(epoxipentadeca[1,11,13]trienimino)-nafto[2,1-b]furan-1,11(2H)-diona.
La rifampicina está disponible bajo muchas marcas en todo el mundo.