Riboflavina
La riboflavina, también conocida como vitamina B2, es una vitamina que se encuentra en los alimentos y se vende como suplemento dietético. Es esencial para la formación de dos coenzimas principales, el mononucleótido de flavina y el dinucleótido de flavina y adenina. Estas coenzimas están implicadas en el metabolismo energético, la respiración celular y la producción de anticuerpos, así como en el crecimiento y desarrollo normales. Las coenzimas también son necesarias para el metabolismo de la niacina, la vitamina B6 y el folato. La riboflavina se prescribe para tratar el adelgazamiento de la córnea y, si se toma por vía oral, puede reducir la incidencia de migrañas en adultos.
La deficiencia de riboflavina es rara y suele ir acompañada de deficiencias de otras vitaminas y nutrientes. Puede prevenirse o tratarse con suplementos orales o inyecciones. Como vitamina soluble en agua, cualquier riboflavina consumida en exceso de los requisitos nutricionales no se almacena; no se absorbe o se absorbe y se excreta rápidamente en la orina, lo que hace que la orina tenga un tinte amarillo brillante. Las fuentes naturales de riboflavina incluyen carne, pescado y aves, huevos, productos lácteos, verduras, champiñones y almendras. Algunos países exigen su adición a los cereales.
La riboflavina se descubrió en 1920, se aisló en 1933 y se sintetizó por primera vez en 1935. En su forma sólida purificada, es un polvo cristalino de color amarillo anaranjado soluble en agua. Además de su función como vitamina, se utiliza como colorante alimentario. La biosíntesis tiene lugar en bacterias, hongos y plantas, pero no en animales. La síntesis industrial de riboflavina se logró inicialmente mediante un proceso químico, pero la fabricación comercial actual se basa en métodos de fermentación que utilizan cepas de hongos y bacterias modificadas genéticamente.
Definición
La riboflavina, también conocida como vitamina B2, es una vitamina soluble en agua y es una de las vitaminas B. A diferencia del folato y la vitamina B6, que se presentan en varias formas relacionadas químicamente conocidas como vitámeros, la riboflavina es solo un compuesto químico. Es un compuesto inicial en la síntesis de las coenzimas flavina mononucleótido (FMN, también conocida como riboflavina-5'-fosfato) y flavina adenina dinucleótido (FAD). FAD es la forma más abundante de flavina, se informa que se une al 75 % de la cantidad de genes codificados por proteínas dependientes de flavina en el genoma de todas las especies (el flavoproteoma) y sirve como coenzima para el 84 % de las flavoproteínas codificadas por humanos.
En su forma sólida y purificada, la riboflavina es un polvo cristalino de color amarillo anaranjado con un ligero olor y sabor amargo. Es soluble en solventes polares, como agua y soluciones acuosas de cloruro de sodio, y ligeramente soluble en alcoholes. No es soluble en disolventes orgánicos no polares o débilmente polares como cloroformo, benceno o acetona. En solución o durante el almacenamiento en seco como polvo, la riboflavina es termoestable si no se expone a la luz. Cuando se calienta para descomponerse, libera humos tóxicos que contienen óxido nítrico.
Funciones
La riboflavina es esencial para la formación de dos coenzimas principales, FMN y FAD. Estas coenzimas están involucradas en el metabolismo energético, la respiración celular, la producción de anticuerpos, el crecimiento y el desarrollo. La riboflavina es esencial para el metabolismo de carbohidratos, proteínas y grasas. FAD contribuye a la conversión de triptófano en niacina (vitamina B3) y la conversión de vitamina B6 en la coenzima piridoxal 5'-fosfato requiere FMN. La riboflavina participa en el mantenimiento de niveles circulantes normales de homocisteína; en la deficiencia de riboflavina, los niveles de homocisteína aumentan, elevando el riesgo de enfermedades cardiovasculares.
Reacciones redox
Las reacciones redox son procesos que implican la transferencia de electrones. Las coenzimas flavinas respaldan la función de aproximadamente 70-80 flavoenzimas en humanos (y cientos más en todos los organismos, incluidas las codificadas por genomas de arqueas, bacterias y hongos) que son responsables de reacciones redox de uno o dos electrones que capitalizan la capacidad de flavinas para ser convertidas entre formas oxidadas, medio reducidas y completamente reducidas. FAD también es necesario para la actividad de la glutatión reductasa, una enzima esencial en la formación del antioxidante endógeno glutatión.
Metabolismo de micronutrientes
La riboflavina, FMN y FAD participan en el metabolismo de la niacina, la vitamina B6 y el folato. La síntesis de las coenzimas que contienen niacina, NAD y NADP, a partir del triptófano implica la enzima dependiente de FAD, la quinurenina 3-monooxigenasa. La deficiencia dietética de riboflavina puede disminuir la producción de NAD y NADP, lo que promueve la deficiencia de niacina. La conversión de la vitamina B6 a su coenzima, piridoxal 5'-fosfato sintasa, involucra a la enzima piridoxina 5'-fosfato oxidasa, que requiere FMN. Una enzima involucrada en el metabolismo del folato, la 5,10-metilenetetrahidrofolato reductasa, requiere FAD para formar el aminoácido metionina a partir de la homocisteína.
La deficiencia de riboflavina parece afectar el metabolismo del mineral de la dieta, el hierro, que es esencial para la producción de hemoglobina y glóbulos rojos. Aliviar la deficiencia de riboflavina en personas que tienen deficiencia tanto de riboflavina como de hierro mejora la eficacia de los suplementos de hierro para tratar la anemia por deficiencia de hierro.
Síntesis
Biosíntesis
La biosíntesis tiene lugar en bacterias, hongos y plantas, pero no en animales. Los precursores biosintéticos de la riboflavina son la ribulosa 5-fosfato y el trifosfato de guanosina. El primero se convierte en L-3,4-dihidroxi-2-butanona-4-fosfato, mientras que el segundo se transforma en una serie de reacciones que conducen al 5-amino-6-(D-ribitilamino)uracilo. Estos dos compuestos son entonces los sustratos para el penúltimo paso de la ruta, catalizado por la enzima lumazina sintasa en la reacción EC 2.5.1.78.
En el paso final de la biosíntesis, la enzima riboflavina sintasa combina dos moléculas de 6,7-dimetil-8-ribitillumazina en una reacción de dismutación. Esto genera una molécula de riboflavina y una de 5-amino-6-(D-ribitylamino) uracilo. Este último se recicla a la reacción anterior en la secuencia.
Las conversiones de riboflavina en los cofactores FMN y FAD se llevan a cabo mediante la acción secuencial de las enzimas riboflavina quinasa y FAD sintetasa.
Síntesis industrial
La producción a escala industrial de riboflavina utiliza diversos microorganismos, entre ellos hongos filamentosos como Ashbya gossypii, Candida famata y Candida flaveri, como así como las bacterias Corynebacterium ammoniagenes y Bacillus subtilis. B. subtilis que se ha modificado genéticamente para aumentar la producción de riboflavina y para introducir un marcador de resistencia a los antibióticos (ampicilina), se emplea a escala comercial para producir riboflavina para la fortificación de piensos y alimentos. Para 2012, se produjeron más de 4.000 toneladas por año mediante dichos procesos de fermentación.
En presencia de altas concentraciones de hidrocarburos o compuestos aromáticos, algunas bacterias sobreproducen riboflavina, posiblemente como mecanismo de protección. Uno de estos organismos es Micrococcus luteus (número de cepa de la American Type Culture Collection ATCC 49442), que desarrolla un color amarillo debido a la producción de riboflavina mientras crece en piridina, pero no cuando crece en otros sustratos, como succínico ácido.
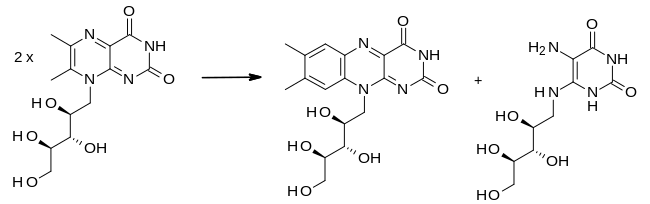
Síntesis de laboratorio
La primera síntesis total de riboflavina fue realizada por el grupo de Richard Kuhn. Una anilina sustituida, producida por aminación reductora utilizando D-ribosa, se condensó con aloxano en el paso final:
Usos
Tratamiento del adelgazamiento corneal
El queratocono es la forma más común de ectasia corneal, un adelgazamiento progresivo de la córnea. La afección se trata mediante la reticulación del colágeno corneal, lo que aumenta la rigidez de la córnea. El entrecruzamiento se logra aplicando una solución tópica de riboflavina a la córnea, que luego se expone a la luz ultravioleta A.
Prevención de la migraña
En sus directrices de 2012, la Academia Estadounidense de Neurología afirmó que la riboflavina en dosis altas (400 mg) es "probablemente eficaz y debe considerarse para la prevención de la migraña" una recomendación también proporcionada por el Centro Nacional de Migraña del Reino Unido. Una revisión de 2017 informó que la riboflavina diaria tomada a 400 mg por día durante al menos tres meses puede reducir la frecuencia de las migrañas en adultos. La investigación sobre dosis altas de riboflavina para la prevención o el tratamiento de la migraña en niños y adolescentes no es concluyente, por lo que no se recomiendan los suplementos.
Colorante alimentario
La riboflavina se utiliza como colorante alimentario (polvo cristalino de color amarillo anaranjado) y se designa con el número E, E101, en Europa para su uso como aditivo alimentario.
Recomendaciones dietéticas
La Academia Nacional de Medicina actualizó los requisitos promedio estimados (EAR) y las cantidades diarias recomendadas (RDA) de riboflavina en 1998. Los EAR de riboflavina para mujeres y hombres mayores de 14 años son 0,9 mg/día y 1,1 mg/día, respectivamente; las RDA son 1,1 y 1,3 mg/día, respectivamente. Las RDA son más altas que las EAR para proporcionar niveles de ingesta adecuados para personas con requisitos superiores al promedio. La dosis diaria recomendada durante el embarazo es de 1,4 mg/día y la dosis diaria recomendada para mujeres lactantes es de 1,6 mg/día. Para bebés de hasta 12 meses, la ingesta adecuada (IA) es de 0,3 a 0,4 mg/día y para niños de 1 a 13 años, la RDA aumenta con la edad de 0,5 a 0,9 mg/día. En cuanto a la seguridad, el IOM establece niveles máximos de ingesta tolerable (UL) para vitaminas y minerales cuando la evidencia es suficiente. En el caso de la riboflavina no hay UL, ya que no hay datos en humanos sobre los efectos adversos de dosis altas. En conjunto, las EAR, RDA, AI y UL se denominan ingestas dietéticas de referencia (DRI).
La Autoridad Europea de Seguridad Alimentaria (EFSA) se refiere al conjunto colectivo de información como Valores dietéticos de referencia, con Ingesta de referencia de la población (PRI) en lugar de RDA y Requerimiento promedio en lugar de EAR. AI y UL se definen igual que en Estados Unidos. Para mujeres y hombres mayores de 15 años, el PRI se establece en 1,6 mg/día. El PRI durante el embarazo es de 1,9 mg/día y el PRI para hembras lactantes es de 2,0 mg/día. Para niños de 1 a 14 años, los PRI aumentan con la edad de 0,6 a 1,4 mg/día. Estos PRI son más altos que los RDA de EE. UU. La EFSA también consideró la ingesta máxima segura y, al igual que la Academia Nacional de Medicina de EE. UU., decidió que no había suficiente información para establecer un UL.
| Subvenciones dietéticas recomendadas Estados Unidos | |
| Grupo de edad (años) | RDA para riboflavina (mg/d) |
|---|---|
| 0 a 6 meses | 0.3* |
| 6 a 12 meses | 0.4* |
| 1–3 | 0.5 |
| 4 a 8 | 0.6 |
| 9 a 13 | 0.9 |
| Mujeres 14-18 | 1.0 |
| Hombres 14 a 18 | 1.3 |
| Mujeres 19+ | 1.1 |
| Hombres 19+ | 1.3 |
| Mujeres embarazadas | 1.4 |
| Mujeres de lactancia | 1.6 |
| * Adquisición adecuada para los lactantes, aún no se ha establecido RDA/RDI | |
| Ingestas de referencia de población Unión Europea | |
| Grupo de edad (años) | PRI para riboflavina (mg/d) |
| 7 a 11 meses | 0,4 |
| 1–3 | 0.6 |
| 4 a 6 | 0.7 |
| 7 a 10 | 1.0 |
| 11 a 14 | 1.4 |
| 15 adulto | 1.6 |
| Mujeres embarazadas | 1.9 |
| Mujeres de lactancia | 2.0 |
Seguridad
En humanos, no hay evidencia de toxicidad de riboflavina producida por ingestas excesivas y la absorción se vuelve menos eficiente a medida que aumenta la dosis. Cualquier exceso de riboflavina se excreta a través de los riñones en la orina, lo que da como resultado un color amarillo brillante conocido como flavinuria. Durante un ensayo clínico sobre la eficacia de la riboflavina para tratar la frecuencia y la gravedad de las migrañas, los sujetos recibieron hasta 400 mg de riboflavina por vía oral al día durante períodos de 3 a 12 meses. Los dolores abdominales y la diarrea se encontraban entre los efectos secundarios informados.
Etiquetado
Para fines de etiquetado de alimentos y suplementos dietéticos de EE. UU., la cantidad en una porción se expresa como un porcentaje del valor diario (%DV). Para fines de etiquetado de riboflavina, el 100 % del valor diario era 1,7 mg, pero a partir del 27 de mayo de 2016, se revisó a 1,3 mg para que coincidiera con la RDA. Se proporciona una tabla de los valores diarios para adultos antiguos y nuevos en la Ingesta diaria de referencia.
Absorción, metabolismo, excreción
Más del 90 % de la riboflavina en la dieta se encuentra en forma de FMN y FAD unidos a proteínas. La exposición al ácido gástrico en el estómago libera las coenzimas, que posteriormente se hidrolizan enzimáticamente en el intestino delgado proximal para liberar riboflavina libre.
Deficiencia
Prevalencia
Historia
El nombre "riboflavina" proviene de "ribosa" (el azúcar cuya forma reducida, ribitol, forma parte de su estructura) y "flavin", la fracción anular que imparte el color amarillo a la molécula oxidada (del latín flavus, "amarillo"). La forma reducida, que ocurre en el metabolismo junto con la forma oxidada, aparece como agujas o cristales de color amarillo anaranjado. La primera identificación reportada, anterior a cualquier concepto de vitaminas como nutrientes esenciales, fue realizada por Alexander Wynter Blyth. En 1879, Blyth aisló un componente soluble en agua de las vacas. suero de leche, al que llamó "lactocromo", que emitía una fluorescencia de color amarillo verdoso cuando se exponía a la luz.
Contenido relacionado
Olmo
Marrubium vulgare
Gimnosfaérido