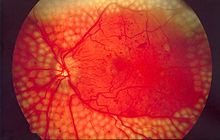
Retinopatía diabética
La retinopatía diabética (también conocida como enfermedad diabética del ojo), es una condición médica en la que se produce un daño en la retina debido a la diabetes mellitus. Es una de las principales causas de ceguera en los países desarrollados.
La retinopatía diabética afecta hasta al 80 % de las personas que han tenido diabetes tipo 1 y tipo 2 durante 20 años o más. En al menos el 90% de los casos nuevos, la progresión a formas más agresivas de retinopatía y maculopatía que amenazan la vista podría reducirse con el tratamiento adecuado y el control de los ojos. Cuanto más tiempo tenga diabetes una persona, mayores serán sus posibilidades de desarrollar retinopatía diabética. Cada año en los Estados Unidos, la retinopatía diabética representa el 12% de todos los nuevos casos de ceguera. También es la principal causa de ceguera en personas de 20 a 64 años.
Signos y síntomas
Casi todas las personas con diabetes desarrollan algún grado de daño en la retina ("retinopatía") durante varias décadas con la enfermedad. Para muchos, ese daño solo puede detectarse mediante un examen de la retina y no tiene un efecto notable en la visión. Con el tiempo, puede aparecer daño retinal progresivo en un examen de la retina, primero con pequeños bultos en los vasos sanguíneos de la retina llamados microaneurismas. Luego, anomalías más grandes en los vasos de la retina: manchas algodonosas, hemorragias, depósitos de lípidos llamados "exudados duros", anomalías microvasculares intrarretinianas y venas retinianas de apariencia anormal. Eventualmente, muchos progresan a una etapa en la que crecen nuevos vasos sanguíneos en toda la retina. Estos nuevos vasos sanguíneos a menudo se rompen y sangran. El sangrado menor puede causar puntos oscuros flotantes que obstruyen la visión; el sangrado mayor puede bloquear completamente la visión.
Alrededor de la mitad de las personas con retinopatía diabética desarrollan inflamación de la mácula, llamada edema macular, que puede comenzar en cualquier momento. Si la hinchazón ocurre cerca del centro de la mácula, puede causar alteraciones de la visión que van desde una visión levemente borrosa hasta una pérdida grave del centro del campo visual de la persona afectada. Si no se tratan, alrededor del 30 % de las personas con tal hinchazón experimentan una alteración de la visión en los próximos 3 a 5 años. El edema macular es la causa más común de pérdida de visión en personas con retinopatía diabética.
Los procesos repetidos de crecimiento, inflamación y cicatrización de los vasos sanguíneos pueden eventualmente causar un desprendimiento de retina, que se manifiesta como la aparición repentina de manchas oscuras flotantes, destellos de luz o visión borrosa.
Diagnóstico y clasificación
La retinopatía diabética generalmente se diagnostica mediante observaciones del examen de la retina mediante oftalmoscopia. La Academia Estadounidense de Oftalmología divide la retinopatía diabética en cinco categorías de gravedad progresiva. La primera categoría, "sin retinopatía aparente", describe a aquellos con un examen de retina saludable. Las siguientes tres categorías: retinopatía diabética no proliferativa (NPDR) leve, moderada y grave describen niveles crecientes de daño a la retina. Las personas con NPDR leve tienen microaneurismas en la retina, pero ningún otro daño. Aquellos con NPDR severa tienen más de 20 hemorragias retinianas en cada cuadrante de la retina, un patrón distintivo de daño en las venas de la retina llamado "perlas venosas" en al menos dos cuadrantes de la retina y anomalías microvasculares intrarretinianas evidentes en cualquier parte de la retina. La NPDR moderada se define como más grave que la NPDR leve, pero que aún no cumple los criterios para la NPDR grave. La quinta etapa, la retinopatía diabética proliferativa, es para aquellos con nuevos vasos sanguíneos que se forman en toda la retina ("neovascularización retinal"), o sangre que se filtra hacia el humor vítreo ("hemorragia vítrea") o entre la membrana vítrea y la retina ("hemorragia prerretiniana").
Las mismas pautas dividen por separado el edema macular en dos categorías: "edema macular aparentemente ausente" y "edema macular aparentemente presente". Este último se subdivide en "leve": engrosamiento de la retina o depósitos de lípidos lejos del centro de la mácula; "moderado"— engrosamiento o depósitos cerca del centro; y "grave": engrosamiento o depósitos en el centro de la mácula. La tomografía de coherencia óptica se utiliza con frecuencia para evaluar el edema macular.
Los especialistas en retina utilizan la angiografía con fluoresceína para evaluar más a fondo la gravedad de la retinopatía diabética y determinar los sitios de daño macular.
Proyección
Debido a la falta de síntomas, la mayoría de las personas con retinopatía diabética no saben que tienen la afección hasta que visitan a un oftalmólogo.
Tanto la Asociación Estadounidense de Diabetes (ADA) como el Consejo Internacional de Oftalmología (ICO) recomiendan exámenes oculares regulares para las personas con diabetes para detectar la retinopatía diabética (excepto aquellas con diabetes gestacional). La ADA recomienda un examen ocular completo en el momento del diagnóstico de diabetes tipo 2 y dentro de los cinco años posteriores al inicio de la diabetes tipo 1. Para las mujeres con diabetes que quedan embarazadas, la ADA recomienda un examen de la vista antes del embarazo, en cada trimestre y durante un año después del parto.
El ICO recomienda que los exámenes oculares para las personas con diabetes incluyan un examen de la agudeza visual y un examen de la retina mediante oftalmoscopia o fotografía de la retina.
Islandia, Irlanda y el Reino Unido son los únicos países con programas nacionales completos de detección de retinopatía diabética, mientras que se han implementado programas de detección regionales sustanciales en partes de Europa continental, partes de Asia y Botswana. En el Reino Unido, la detección de la retinopatía diabética es parte del estándar de atención para las personas con diabetes. Después de una prueba de detección normal en personas con diabetes, se recomiendan pruebas adicionales cada año. La teleoftalmología se ha empleado en estos programas.
Causas
La retinopatía diabética es causada por un nivel alto prolongado de glucosa en la sangre que daña los pequeños vasos sanguíneos de la retina.
Factores de riesgo
Los principales factores de riesgo para desarrollar retinopatía diabética son la duración de la diabetes, el control deficiente del azúcar en la sangre y, en menor medida, la presión arterial alta. Cinco años después del diagnóstico de diabetes, alrededor del 25 % de las personas con diabetes tipo 1 tienen algún grado de retinopatía diabética, mientras que el 2 % tiene retinopatía diabética proliferativa. A los 15 años del diagnóstico, aumenta al 80 % con alguna retinopatía y al 25 % con enfermedad proliferativa. Los niños son una excepción: independientemente de la duración de la diabetes, los niños rara vez experimentan retinopatía que amenaza la vista; sin embargo, la pubertad puede acelerar la progresión de la retinopatía.
Del mismo modo, el embarazo puede acelerar la progresión de la retinopatía diabética (aunque las mujeres con diabetes gestacional no corren riesgo).
Tanto el azúcar en sangre crónicamente alto (medido por una HbA1c alta) como el azúcar en sangre altamente variable están asociados con el desarrollo de retinopatía diabética. Varios factores de riesgo menores más también exacerban la retinopatía diabética, a saber, enfermedad renal, lípidos sanguíneos anormales, índice de masa corporal alto y tabaquismo.
La predisposición genética a la retinopatía diabética en la diabetes tipo 2 consta de muchas variantes genéticas en todo el genoma que se asocian colectivamente con la retinopatía diabética (riesgo poligénico) y se superponen con el riesgo genético de glucosa, colesterol de lipoproteínas de baja densidad y presión arterial sistólica. Varias variaciones en el gen VEGFC también se han asociado con un mayor riesgo de desarrollar edema macular.
Las personas con síndrome de Down, que tienen material adicional del cromosoma 21, casi nunca adquieren retinopatía diabética. Esta protección parece deberse a los niveles elevados de endostatina, una proteína antiangiogénica, derivada del colágeno XVIII. El gen del colágeno XVIII se encuentra en el cromosoma 21.
Se ha observado que la incidencia de la retinosis pigmentaria produce menos lesiones microvasculares y menos graves tanto en humanos como en ratones. La retinosis pigmentaria da como resultado la pérdida de receptores de varilla en el campo periférico medio, lo que reduce el consumo de oxígeno que está relacionado con la liberación de VEGF y el crecimiento de vasos sanguíneos no deseados en la retina.
La apnea obstructiva del sueño (AOS) se ha asociado con una mayor incidencia de enfermedad ocular diabética debido a la desaturación de la sangre causada por obstrucciones intermitentes de las vías respiratorias superiores. El tratamiento para la AOS puede ayudar a reducir el riesgo de complicaciones diabéticas.
Patogénesis
La retinopatía diabética es el resultado del daño a los vasos sanguíneos pequeños y las neuronas de la retina. Los cambios más tempranos que conducen a la retinopatía diabética incluyen el estrechamiento de las arterias retinianas asociado con un flujo sanguíneo retiniano reducido; disfunción de las neuronas de la retina interna, seguida en etapas posteriores por cambios en la función de la retina externa, asociada con cambios sutiles en la función visual; Disfunción de la barrera hematorretiniana, que protege la retina de muchas sustancias en la sangre (incluidas las toxinas y las células inmunitarias), lo que provoca la fuga de constituyentes de la sangre hacia la neuropila retiniana. Posteriormente, la membrana basal de los vasos sanguíneos de la retina se espesa, los capilares se degeneran y pierden células, en particular pericitos y células del músculo liso vascular. Esto conduce a la pérdida del flujo sanguíneo e isquemia progresiva, y aneurismas microscópicos que aparecen como estructuras en forma de globo que sobresalen de las paredes capilares, que reclutan células inflamatorias; y disfunción avanzada y degeneración de las neuronas y células gliales de la retina. La afección generalmente se desarrolla alrededor de 10 a 15 años después de recibir el diagnóstico de diabetes mellitus.
Un estudio experimental sugiere que la muerte de los pericitos es causada por la activación persistente de la proteína quinasa C y la proteína quinasa activada por mitógenos (MAPK) de glucosa en sangre que, a través de una serie de intermediarios, inhibe la señalización a través de los receptores del factor de crecimiento derivado de plaquetas, lo que indica que apoya la supervivencia celular, la proliferación y el crecimiento. La retirada resultante de esta señalización conduce a la muerte celular programada (apoptosis) de las células en este modelo experimental.
Además, el exceso de sorbitol en los diabéticos se deposita en el tejido de la retina y también se propone que desempeñe un papel en la retinopatía diabética.
Un estudio genético mostró que la retinopatía diabética comparte una predisposición genética similar con los niveles de glucosa, el colesterol de lipoproteínas de baja densidad y la presión arterial sistólica, lo que indica que el control glucémico y los factores cardiometabólicos pueden ser importantes en el desarrollo de la retinopatía diabética.
Administración
Existen cuatro tratamientos comunes para la retinopatía diabética: inyecciones anti-VEGF, inyecciones de esteroides, fotocoagulación con láser panretiniano y vitrectomía. Los regímenes de tratamiento actuales pueden prevenir el 90 % de la pérdida grave de la visión.
Aunque estos tratamientos son muy exitosos (para ralentizar o detener la pérdida adicional de la visión), no curan la retinopatía diabética. Se debe tener precaución en el tratamiento con cirugía láser ya que provoca una pérdida de tejido retiniano. A menudo es más prudente inyectar triamcinolona o fármacos anti-VEGF. En algunos pacientes resulta en un marcado aumento de la visión, especialmente si hay un edema de la mácula.
Además, el tratamiento estándar para la retinopatía diabética incluye mejorar el control del azúcar en la sangre, la presión arterial y el colesterol en la sangre, todo lo cual puede reducir la progresión de la retinopatía diabética.
Retinopatía diabética no proliferativa
La inyección de esteroides o medicamentos anti-VEGF puede reducir la progresión de la retinopatía diabética en alrededor de la mitad de los ojos tratados; sin embargo, aún no se sabe si esto resulta en una mejor visión a largo plazo. Para aquellos con retinopatía diabética no proliferativa de leve a moderada, la Academia Estadounidense de Oftalmología recomienda exámenes de retina más frecuentes, cada seis a doce meses, ya que estas personas tienen un mayor riesgo de desarrollar retinopatía proliferativa o edema macular.
Fotocoagulación láser
La fotocoagulación con láser se puede utilizar en dos escenarios para el tratamiento de la retinopatía diabética. En primer lugar, se puede usar para tratar el edema macular que era común antes de que se introdujeran las inyecciones oculares. y en segundo lugar, puede usarse para tratar la retina completa (fotocoagulación panretiniana) para controlar la neovascularización. Es ampliamente utilizado para las primeras etapas de la retinopatía proliferativa. Existen diferentes tipos de láseres y existe evidencia disponible sobre sus beneficios para tratar la retinopatía diabética proliferativa.
Fotocoagulación láser panretinal
Para las personas con retinopatía diabética proliferativa o no proliferativa grave, la pérdida de la visión se puede prevenir mediante el tratamiento con fotocoagulación con láser panretiniano.
El objetivo es crear entre 1600 y 2000 quemaduras en la retina con la esperanza de reducir la demanda de oxígeno de la retina y, por lo tanto, la posibilidad de isquemia. Se realiza en múltiples sesiones.
En el tratamiento de la retinopatía diabética avanzada, las quemaduras se usan para destruir los nuevos vasos sanguíneos anormales que se forman en la retina. Se ha demostrado que esto reduce el riesgo de pérdida severa de la visión para los ojos en riesgo en un 50 %.
Antes de usar el láser, el oftalmólogo dilata la pupila y aplica gotas anestésicas para adormecer el ojo. En algunos casos, el médico también puede adormecer el área detrás del ojo para reducir la incomodidad. El paciente se sienta frente a la máquina láser mientras el médico sostiene una lente especial en el ojo. El médico puede utilizar un láser de un solo punto, un láser de exploración de patrones para patrones bidimensionales, como cuadrados, anillos y arcos, o un láser navegado que funciona mediante el seguimiento de los movimientos oculares de la retina en tiempo real. Durante el procedimiento, el paciente verá destellos de luz. Estos destellos a menudo crean una sensación de escozor incómoda para el paciente. Después del tratamiento con láser, se debe recomendar a los pacientes que no conduzcan durante algunas horas mientras las pupilas aún estén dilatadas. Lo más probable es que la visión permanezca borrosa durante el resto del día. Aunque no debería haber mucho dolor en el ojo en sí, un dolor de cabeza como el helado puede durar horas después.
Los pacientes perderán parte de su visión periférica después de esta cirugía, aunque es posible que el paciente apenas lo note. Sin embargo, el procedimiento salva el centro de la vista del paciente. La cirugía con láser también puede reducir ligeramente el color y la visión nocturna.
Una persona con retinopatía proliferativa siempre estará en riesgo de sangrado nuevo, así como de glaucoma, una complicación de los vasos sanguíneos nuevos. Esto significa que se pueden requerir múltiples tratamientos para proteger la visión.
Medicamentos
Acetónido de triamcinolona intravítreo
La triamcinolona es una preparación de esteroides de acción prolongada. El tratamiento de personas con EMD con inyecciones intravítreas de triamcinolona puede conducir a cierto grado de mejora en la agudeza visual en comparación con los ojos tratados con inyecciones de placebo. Cuando se inyecta en la cavidad vítrea, el esteroide disminuye el edema macular (engrosamiento de la retina en la mácula) causado por la maculopatía diabética, y eso puede resultar en un aumento de la agudeza visual. El efecto de la triamcinolona no es permanente y puede durar hasta tres meses, lo que requiere inyecciones repetidas para mantener el efecto beneficioso. Los mejores resultados de la Triamcinolona intravítrea se han encontrado en ojos que ya han sido operados de cataratas. Las complicaciones de la inyección intravítrea de triamcinolona pueden incluir cataratas, glaucoma inducido por esteroides y endoftalmitis.
Anti-VEGF intravítreo
Las personas con edema macular diabético se benefician de las inyecciones periódicas de anticuerpos anti-VEGF como ranibizumab, bevacizumab y aflibercept. No existe un programa de dosificación ampliamente aceptado, aunque las personas suelen recibir inyecciones más frecuentes durante el primer año de tratamiento, y las inyecciones menos frecuentes en los años siguientes son suficientes para mantener la remisión.
Una actualización de revisión sistemática de 2017 encontró evidencia moderada de que aflibercept puede tener ventajas en la mejora de los resultados visuales sobre bevacizumab y ranibizumab, después de un año. Sin embargo, en los casos de hemorragia vítrea, las inyecciones de anti-VEGF demostraron ser menos efectivas para restaurar la agudeza visual que la vitrectomía combinada con fotocoagulación con láser panretiniano. Actualmente, el tratamiento recomendado para el edema macular diabético consiste en inyecciones múltiples de fármacos anti-VEGF, a veces combinadas con fotocoagulación con láser de rejilla modificada. Los sistemas de administración sostenida para medicamentos anti-VEGF pueden reducir las posibilidades de desarrollo de endoftalmitis al reducir la cantidad de inyecciones intravítreas necesarias para el tratamiento. Los hidrogeles se han mostrado muy prometedores para esta plataforma.
Medicamentos tópicos
Existen pocas pruebas sobre la función de los medicamentos tópicos en el tratamiento del edema macular, por ejemplo, los agentes antiinflamatorios no esteroideos tópicos.
Cirugía
En lugar de la cirugía con láser, algunas personas requieren una vitrectomía para restaurar la visión. Una vitrectomía se realiza cuando hay mucha sangre en el vítreo. Se trata de eliminar el vítreo turbio y reemplazarlo con una solución salina.
Los estudios muestran que las personas que se someten a una vitrectomía poco después de una hemorragia importante tienen más probabilidades de proteger su visión que las personas que esperan para someterse a la operación. La vitrectomía temprana es especialmente eficaz en personas con diabetes insulinodependiente, que pueden correr un mayor riesgo de ceguera por una hemorragia en el ojo.
La vitrectomía se puede realizar con anestesia general o local. El médico hace una pequeña incisión en la esclerótica o parte blanca del ojo. Luego, se coloca un pequeño instrumento en el ojo para extraer el vítreo e insertar la solución salina en el ojo.
Es posible que los pacientes puedan regresar a casa poco después de la vitrectomía, o se les puede pedir que pasen la noche en el hospital. Después de la operación, el ojo estará rojo y sensible, y los pacientes generalmente necesitan usar un parche en el ojo durante unos días o semanas para proteger el ojo. También se prescriben gotas para los ojos medicadas para proteger contra infecciones. Existe evidencia que sugiere que los fármacos anti-VEGF administrados antes o durante la vitrectomía pueden reducir el riesgo de hemorragia en la cavidad vítrea posterior. La vitrectomía se combina frecuentemente con otras modalidades de tratamiento.
Epidemiología
Alrededor del 34,6 % de las personas con diabetes tienen algún tipo de retinopatía diabética, con alrededor del 7 % experimentando retinopatía diabética proliferativa, el 7 % edema macular diabético y el 10 % experimentando pérdida de visión a causa de la retinopatía diabética. La retinopatía diabética es la principal causa de pérdida de visión en personas de 20 a 74 años.
La carga global de la retinopatía diabética aumentó drásticamente de 1990 a 2015: de 1,4 millones a 2,6 millones de personas con discapacidad visual; de 0,2 millones a 0,4 millones cegados, debido en gran parte a la creciente carga de diabetes tipo 2 en países de ingresos bajos y medianos.
La retinopatía diabética es más común en las personas con diabetes tipo 1 que en las personas con diabetes tipo 2.
Investigación
Se han realizado varios ensayos clínicos aleatorizados multicéntricos grandes para evaluar los protocolos de tratamiento para las personas con retinopatía diabética, a saber, el Estudio de tratamiento temprano para la retinopatía diabética, el Estudio de vitrectomía de la retinopatía diabética, el Estudio de retinopatía diabética, el Ensayo de control y complicaciones de la diabetes, el Estudio prospectivo de diabetes del Reino Unido., y los Protocolos I, S y T de la Red de Investigación Clínica de la Retinopatía Diabética.
Tratamiento de luz
En 2016 se estaba desarrollando un dispositivo médico que consta de una máscara que emite luz verde a través de los párpados mientras una persona duerme. La luz de la máscara evita que los bastones de la retina se adapten a la oscuridad, lo que se cree que reduce su requerimiento de oxígeno. lo que a su vez disminuye la formación de nuevos vasos sanguíneos y, por lo tanto, previene la retinopatía diabética. A partir de 2016, se estaba realizando un gran ensayo clínico. A partir de 2018, los resultados del ensayo clínico no mostraron ningún beneficio terapéutico a largo plazo del uso de la máscara en pacientes con retinopatía diabética.
Péptido C
El péptido C ha mostrado resultados prometedores en el tratamiento de las complicaciones diabéticas secundarias a la degeneración vascular. Creative Peptides, Eli Lilly y Cebix tenían programas de desarrollo de fármacos para un producto de péptido C. Cebix tenía el único programa en curso hasta que completó un ensayo de Fase IIb en diciembre de 2014 que no mostró ninguna diferencia entre el péptido C y el placebo, y terminó su programa y cerró.
Terapia con células madre
Los ensayos clínicos están en marcha o se están poblando en preparación para el estudio en centros médicos de Brasil, Irán y Estados Unidos. Los ensayos actuales implican el uso de los pacientes & # 39; propias células madre derivadas de la médula ósea e inyectadas en las áreas degeneradas en un esfuerzo por regenerar el sistema vascular.
Control de la presión arterial
Una revisión Cochrane examinó 15 ensayos controlados aleatorios para determinar si las intervenciones que buscaban controlar o reducir la presión arterial en los diabéticos tenían algún efecto sobre la retinopatía diabética. Si bien los resultados mostraron que las intervenciones para controlar o reducir la presión arterial previnieron la retinopatía diabética durante un máximo de 4 a 5 años en los diabéticos, no hubo evidencia de ningún efecto de estas intervenciones sobre la progresión de la retinopatía diabética, la preservación de la agudeza visual, los eventos adversos, la calidad de vida y costos.
Análisis de imágenes de fondo de ojo
La retinopatía diabética se diagnostica completamente mediante el reconocimiento de anomalías en las imágenes de la retina tomadas por fundoscopia. La fotografía de fondo de ojo en color se utiliza principalmente para la estadificación de la enfermedad. La angiografía con fluoresceína se usa para evaluar el alcance de la retinopatía que ayuda en el desarrollo del plan de tratamiento. La tomografía de coherencia óptica (OCT) se utiliza para determinar la gravedad del edema y la respuesta al tratamiento.
Debido a que las imágenes fundoscópicas son las fuentes principales para el diagnóstico de la retinopatía diabética, el análisis manual de esas imágenes puede llevar mucho tiempo y ser poco confiable, ya que la capacidad de detectar anomalías varía según los años de experiencia. Por lo tanto, los científicos han explorado el desarrollo de enfoques de diagnóstico asistidos por computadora para automatizar el proceso, lo que implica extraer información sobre los vasos sanguíneos y cualquier patrón anormal del resto de la imagen fundoscópica y analizarlos.
Contenido relacionado
Insomnio fatal
PCHP
Cabeza (desambiguación)