Receptor de vitamina D
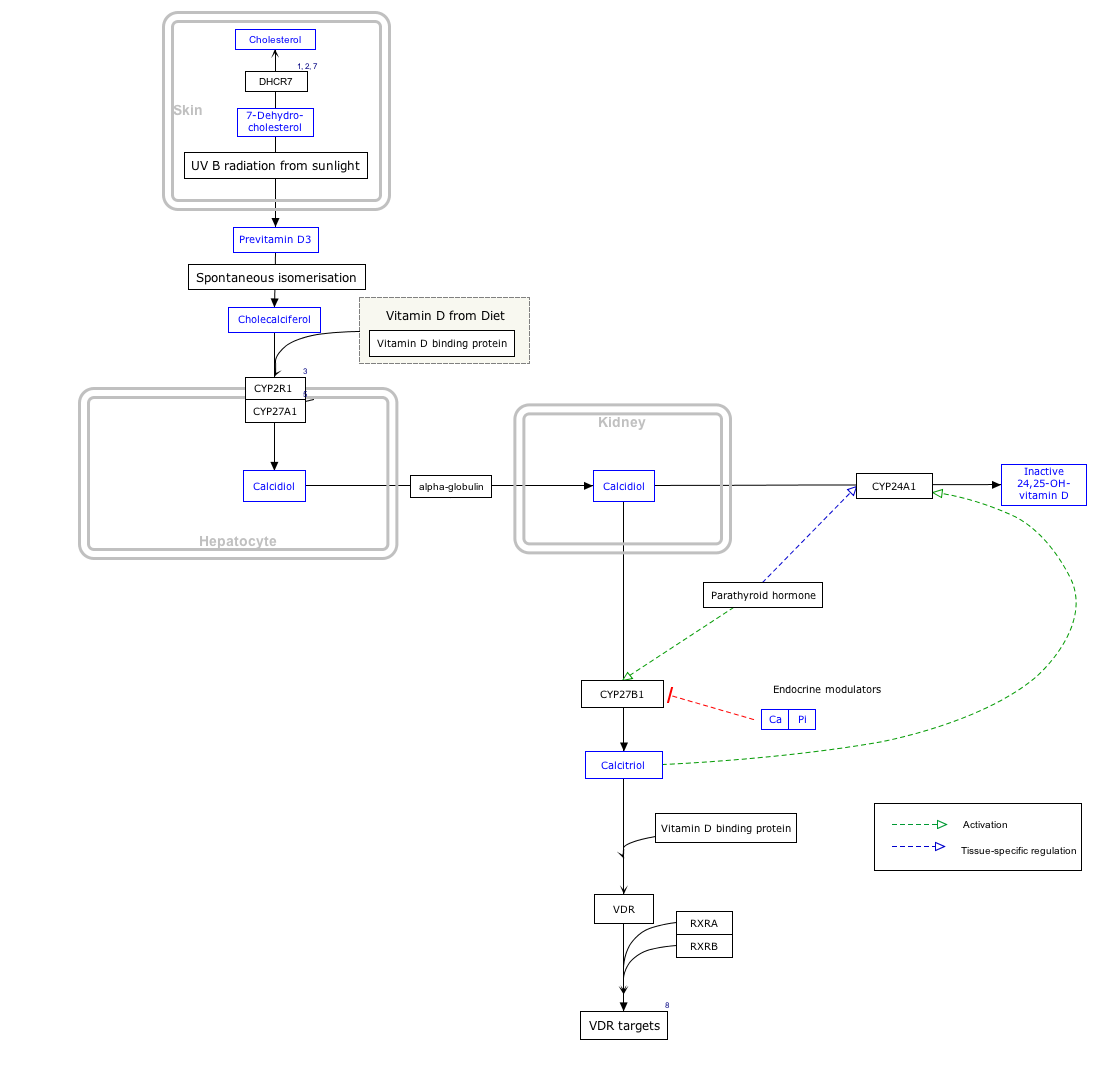
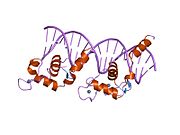
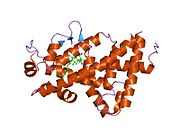
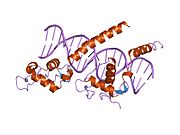
El receptor de vitamina D (VDR, también conocido como receptor de calcitriol) es un miembro de la familia de receptores nucleares de factores de transcripción. El calcitriol (la forma activa de la vitamina D, 1,25-(OH)2 vitamina D3) se une al VDR, que luego forma un heterodímero con el receptor de retinoides X. El heterodímero del VDR luego ingresa al núcleo y se une a los elementos sensibles a la vitamina D (VDRE, por sus siglas en inglés) en el ADN genómico. La unión del VDR da como resultado la expresión o transrepresión de muchos productos genéticos específicos. El VDR también está involucrado en mecanismos postranscripcionales dirigidos por microARN. En los humanos, el receptor de vitamina D está codificado por el gen VDR ubicado en el cromosoma 12q13.11.
El VDR se expresa en la mayoría de los tejidos del cuerpo y regula la transcripción de genes implicados en el transporte intestinal y renal de calcio y otros minerales. Los glucocorticoides disminuyen la expresión del VDR. Muchos tipos de células inmunitarias también expresan el VDR.
Función
El gen VDR codifica el receptor nuclear de la hormona vitamina D. El agonista natural más potente es el calcitriol (1,25-dihidroxicolecalciferol) y el homólogo de la vitamina D2, el ercalcitriol (1-alfa,25-dihidroergocalciferol), también es un activador potente. Otras formas de vitamina D se unen con menor afinidad, al igual que el ácido litocólico, un ácido biliar secundario. El receptor pertenece a la familia de factores reguladores de la transcripción que actúan en trans y muestra una secuencia similar a la de los receptores de esteroides y hormonas tiroideas.
Entre los objetivos posteriores de este receptor nuclear de hormonas se incluyen muchos genes implicados en el metabolismo mineral. El receptor regula una variedad de otras vías metabólicas, como las implicadas en la respuesta inmunitaria y el cáncer. Las variantes del VDR que refuerzan la acción de la vitamina D y que están directamente correlacionadas con las tasas de progresión del SIDA y la asociación del VDR con la progresión al SIDA sigue un modelo aditivo. El polimorfismo FokI es un factor de riesgo para la infección por virus envueltos, como se reveló en un metanálisis. La importancia de este gen también se ha observado en el proceso natural de envejecimiento, donde los haplotipos 3'UTR del gen mostraron una asociación con la longevidad.
Importancia clínica
Las mutaciones en este gen están asociadas con el raquitismo resistente a la vitamina D de tipo II. Un polimorfismo de un solo nucleótido en el codón de iniciación da como resultado un sitio de inicio de traducción alternativo tres codones más abajo. El empalme alternativo da como resultado múltiples variantes de transcripción que codifican la misma proteína. Las variantes del gen VDR parecen influir en muchos puntos finales biológicos, incluidos los relacionados con la osteoporosis.
El receptor de vitamina D desempeña un papel importante en la regulación del ciclo del cabello. La pérdida de VDR está asociada con la pérdida de cabello en animales de experimentación. Estudios experimentales han demostrado que el VDR no ligado interactúa con regiones reguladoras en cWnt (vía de señalización de WNT) y genes diana de Sonic Hedgehog y es necesario para la inducción de estas vías durante el ciclo del cabello postnatal. Estos estudios han revelado acciones novedosas del VDR no ligado en la regulación del ciclo del cabello postmorfogénico.
Los investigadores han centrado sus esfuerzos en dilucidar el papel de los polimorfismos del VDR en diferentes enfermedades y fenotipos normales, como la susceptibilidad y progresión de la infección por VIH-1 o el proceso natural de envejecimiento. Los hallazgos más destacados incluyen el informe de variantes del VDR que refuerzan la acción de la vitamina D y que están directamente correlacionadas con las tasas de progresión del SIDA, que la asociación del VDR con la progresión al SIDA sigue un modelo aditivo y el papel del polimorfismo FokI como factor de riesgo para la infección por virus envueltos, como se reveló en un metaanálisis.
Interacciones
Se ha demostrado que el receptor de vitamina D interactúa con muchos otros factores que afectan la activación de la transcripción:
- BAG1,
- CAV3,
- MED12,
- MED24,
- NCOR1,
- NCOR2,
- NCOA2
- RXRA,
- RUNX1,
- RUNX1T1,
- SNW1,
- STAT1, y
- ZBTB16.
Mapa de la ruta interactiva
Haga clic en genes, proteínas y metabolitos a continuación para vincular a los artículos respectivos.
- ^ El mapa interactivo se puede editar en WikiPathways: "VitaminDSynthesis_WP1531".
Referencias
- ^ a b c GRCh38: Ensembl release 89: ENSG00000111424 – Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00022479 – Ensembl, May 2017
- ^ "Human PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Referencia:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Moore DD, Kato S, Xie W, Mangelsdorf DJ, Schmidt DR, Xiao R, Kliewer SA (diciembre de 2006). "Unión Internacional de Farmacología. LXII. Los receptores NR1H y NR1I: receptor constitutivo de androstane, receptor pregneno X, alfa del receptor de farnesoide X, beta del receptor X de farnesoide, alfa del receptor del hígado X, beta del receptor del hígado y receptor de vitamina D". Pharmacol. Rev. 58 (4): 742–59. doi:10.1124/pr.58.4.6. PMID 17132852. S2CID 85996383.
- ^ Lisse TS, Chun RF, Rieger S, Adams JS, Hewison M (junio de 2013). "Vitamin D activation of functionally distinct regulatory miRNAs in primary human osteoblasts". J Bone Miner Res. 28 (6): 1478–14788. doi:10.1002/jbmr.1882. 3663893. PMID 23362149.
- ^ Szpirer J, Szpirer C, Riviere M, Levan G, Marynen P, Cassiman JJ, Wiese R, DeLuca HF (septiembre de 1991). "El gen del factor de transcripción Sp1 (SP1) y el gen de receptor de 1,25-dihidroxivitamina D3 (VDR) se colocan en el brazo cromosoma humano 12q y cromosoma de rata 7". Genómica. 11 (1): 168–73. doi:10.1016/0888-7543(91)90114-T. PMID 1662663.
- ^ a b c Fleet JC, Schoch RD (agosto de 2010). "Mecanismos moleculares para la regulación de la absorción intestinal de calcio por vitamina D y otros factores". Crit Rev Clin Lab Sci. 47 (4): 181–195. doi:10.3109/10408363.2010.536429. PMC 3235806. PMID 21182397.
- ^ a b Adorini L, Daniel KC, Penna G (2006). "Agonistas de receptores Vitamin D, cáncer y sistema inmunitario: una relación intrincada". Curr Top Med Chem. 6 (12): 1297–301. doi:10.2174/156802606777864890. PMID 16848743.
- ^ Germain P, Staels B, Dacquet C, Spedding M, Laudet V (diciembre de 2006). "Overview of nomenclature of nuclear recipients". Pharmacol. Rev. 58 (4): 685–704. doi:10.1124/pr.58.4.2. PMID 17132848. S2CID 1190488.
- ^ a b Laplana M, Sánchez-de-la- Torre M, Puig T, Caruz A, Fibla J (julio de 2014). "Vitamin-D pathway genes and HIV-1 disease progression in injection drug users". Gene. 545 (1): 163–9. doi:10.1016/j.gene.2014.04.035. Hdl:10459.1/67999. PMID 24768180.
- ^ a b Laplana M, Royo L, Fibla J (diciembre de 2018). "Polimorfismos de receptor de vitamina D y riesgo de infección de virus envoltura: metaanálisis". Gene. 678: 384-94. doi:10.1016/j.gene.2018.08.017. Hdl:10459.1/68000PMID 30092343. S2CID 51955566.
- ^ Laplana M, Sánchez-de-la- Torre M, Aguiló A, Casado I, Flores M, Sánchez-Pellicer R, Fibla J (abril de 2010). "Tomar individuos de larga vida a través de haplotipos del receptor de vitamina D (VDR). Biogerontología. 11 (4): 437-46. doi:10.1007/s10522-010-9273-8. hdl:10459.1/67920. PMID 20407924. S2CID 34809120.
- ^ "Entrez Gene: VDR vitamina D (1,25- dihidroxivitamina D3) receptor".
- ^ Abouzid M, Karazniewicz-Lada M, Glowka F (2018-10-19). "Los Determinantes Genéticos de los Trastornos Relacionados con la Vitamina D; Centrarse en el Receptor de la Vitamina D". Metabolismo actual de drogas. 19 (12): 1042-1052. doi:10.2174/1389200219666180723143552. PMID 30039758. S2CID 51710351.
- ^ Luderer HF, Demay MB (Julio 2010). "El receptor de vitamina D, la piel y las células madre". J. Steroid Biochem. Mol. Biol. 121 (1–2): 314–6. doi:10.1016/j.jsbmb.2010.01.015. PMID 20138991. S2CID 23876206.
- ^ Lisse TS, Saini V, Zhao H, Luderer HF, Gori F, Demay MB (septiembre de 2014). "El receptor de vitamina D es necesario para la activación de cWnt y Hedgehog señalización en Keratinocitos". Mol. Endocrinol. 28 (10): 1698–1706. doi:10.1210/me.2014-1043. PMC 4179637. PMID 25180455.
- ^ Guzey M, Takayama S, Reed JC (diciembre de 2000). "BAG1L mejora la función de transactivación del receptor de vitamina D". J. Biol. Chem. 275 (52): 40749-56. doi:10.1074/jbc.M004977200. PMID 10967105.
- ^ Zhao G, Simpson RU (2010). "Membrane Localization, Caveolin-3 Association and Rapid Actions of Vitamin D Receptor in Cardiac Myocytes". esteroides. 75 (8–9): 555–9. doi:10.1016/j.steroids.2009.12.001. PMC 2885558. PMID 20015453.
- ^ a b Ito M, Yuan CX, Malik S, Gu W, Fondell JD, Yamamura S, Fu ZY, Zhang X, Qin J, Roeder RG (marzo de 1999). "La identidad entre los complejos TRAP y SMCC indica caminos novedosos para la función de los receptores nucleares y los diversos activadores mamíferos". Mol. Celular. 3 (3): 361–70. doi:10.1016/S1097-2765(00)80463-3. PMID 10198638.
- ^ a b Tagami T, Lutz WH, Kumar R, Jameson JL (diciembre de 1998). "La interacción del receptor de vitamina D con los corepresores y coactivadores del receptor nuclear". Biochem. Biofias. Res. Commun. 253 (2): 358–63. doi:10.1006/bbrc.1998.9799. PMID 9878542.
- ^ a b c d Puccetti E, Obradovic D, Beissert T, Bianchini A, Washburn B, Chiaradonna F, Boehrer S, Hoelzer D, Ottmann OG, Pelicci PG, Nervi C, Ruthardt M (diciembre de 2002). Los productos de translocación asociados con el AML bloquean la diferenciación inducida por la vitamina D(3) mediante el secuestro del receptor de vitamina D(3). Rescate del cáncer. 62 (23): 7050-8. PMID 12460926.
- ^ Herdick M, Steinmeyer A, Carlberg C (junio de 2000). "La acción antagónica de un ester analógico de 25 carboxílicos de 1alpha, 25-dihidroxivitamina D3 es mediada por una falta de interacción de receptores de vitamina D inducida por ligand con coactivadores". J. Biol. Chem. 275 (22): 16506–12. doi:10.1074/jbc.M910000199. PMID 10748178.
- ^ a b c Zhang C, Baudino TA, Dowd DR, Tokumaru H, Wang W, MacDonald PN (noviembre de 2001). "Ternary complexes and cooperative interplay between NCoA-62/Ski-interacting protein and esteroides receptor coactivators in Vitamin D-mediated transcription". J. Biol. Chem. 276 (44): 40614–20. doi:10.1074/jbc.M106263200. PMID 11514567.
- ^ He B, Wilson EM (marzo de 2003). "La Modulación Electrotática en Receptor Esteroide de Reclutamiento de LXXLL y FXXLF Motifs". Mol. Biol. 23 (6): 2135–50. doi:10.1128/MCB.23.6.2135-2150.2003. PMC 149467. PMID 12612084.
- ^ a b Baudino TA, Kraichely DM, Jefcoat SC, Winchester SK, Partridge NC, MacDonald PN (junio de 1998). "Isolación y caracterización de una nueva proteína coactivadora, NCoA-62, implicada en la transcripción mediada por vitamina D". J. Biol. Chem. 273 (26): 16434–41. doi:10.1074/jbc.273.26.16434. PMID 9632709.
- ^ Vidal M, Ramana CV, Dusso AS (abril de 2002). "Stat1-Vitamin D Receptor Interactions Antagonize 1,25-Dihidroxyvitamin D Transcripción y Enhance Stat1-Mediated Transcripción". Mol. Biol. 22 (8): 2777–87. doi:10.1128/MCB.22.8.2777-2787.2002. PMC 133712. PMID 11909970.
- ^ Ward JO, McConnell MJ, Carlile GW, Pandolfi PP, Licht JD, Freedman LP (diciembre de 2001). "La proteína aguda promielocítica asociada a la leucemia, la leucemia promielocítica del dedo de zinc, regula 1,25-dihidroxivitamina D(3)-diducida diferenciación monocítica de células U937 a través de una interacción física con el receptor de vitamina D(3)". Sangre. 98 (12): 3290–300. doi:10.1182/blood.V98.12.3290. PMID 11719366.
Más lectura
- Hosoi T (2002). "[Polymorfismos del gen del receptor de vitamina D]". Nippon Rinsho. 60 (Supl 3): 106-10. PMID 11979895.
- Uitterlinden AG, Fang Y, Van Meurs JB, Pols HA, Van Leeuwen JP (2004). "Genética y biología de los polimorfismos del receptor de vitamina D". Gene. 338 (2): 143–56. doi:10.1016/j.gene.2004.05.014. Hdl:1765/73442. PMID 15315818. S2CID 11023870.
- Norman AW (2007). "Minireview: receptor de vitamina D: nuevas asignaciones para un receptor ya ocupado". Endocrinología. 147 (12): 5542-8. doi:10.1210/es.2006-0946. PMID 16946007.
- Bollag WB (2007). "La diferenciación de queratinocitos humanos requiere el receptor de vitamina d y sus coactivadores". J. Invest. Dermatol. 127 (4): 748–50. doi:10.1038/sj.jid.5700692. PMID 17363957.
- Bugge TH, Pohl J, Lonnoy O, Stunenberg HG (1992). "RXR alpha, un socio promiscuo de ácido retinoico y receptores de hormona tiroidea". EMBO J. 11 (4): 1409–18. doi:10.1002/j.1460-2075.1992.tb05186.x. PMC 556590. PMID 1314167.
- Goto H, Chen KS, Prahl JM, DeLuca HF (1992). "Un único receptor idéntico al de células intestina/T47D media la acción de 1,25-dihidroxivitamina D-3 en células HL-60". Biochim. Biofias. Acta. 1132 (1): 103–8. doi:10.1016/0167-4781(92)90063-6. PMID 1324736.
- Saijo T, Ito M, Takeda E, Huq AH, Naito E, Yokota I, Sone T, Pike JW, Kuroda Y (1991). "Una mutación única en el gen del receptor de vitamina D en tres pacientes japoneses con rickets dependientes de vitamina D tipo II: utilidad del análisis de polimorfismo de conformación de un solo tramo para la detección del portador heterocigoo". Am. J. Hum. Genet. 49 (3): 668–73. PMC 1683124. PMID 1652893.
- Szpirer J, Szpirer C, Riviere M, Levan G, Marynen P, Cassiman JJ, Wiese R, DeLuca HF (1992). "El gen del factor de transcripción Sp1 (SP1) y el gen de receptor de 1,25-dihidroxivitamina D3 (VDR) se colocan en el brazo cromosoma humano 12q y cromosoma de rata 7". Genómica. 11 (1): 168–73. doi:10.1016/0888-7543(91)90114-T. PMID 1662663.
- Yu XP, Mocharla H, Hustmyer FG, Manolagas SC (1991). "Expresión del receptor Vitamin D en linfocitos humanos. Requisitos de señalización y caracterización por lotes occidentales y secuenciación de ADN". J. Biol. Chem. 266 (12): 7588–95. doi:10.1016/S0021-9258(20)89488-5. PMID 1850412.
- Malloy PJ, Hochberg Z, Tiosano D, Pike JW, Hughes MR, Feldman D (1991). "La base molecular de los grillos hereditarios resistentes a 1,25-dihidroxivitamina D3 en siete familias relacionadas". J. Clin. Invest. 86 (6): 2071–9. doi:10.1172/JCI114944. PMC 329846. PMID 2174914.
- Sone T, Marx SJ, Liberman UA, Pike JW (1991). "Una mutación puntual única en el gen cromosómico del receptor de vitamina D humano confiere resistencia hereditaria a 1,25-dihidroxivitamina D3". Mol. Endocrinol. 4 (4): 623–31. doi:10.1210/mend-4-4-623. PMID 2177843.
- Baker AR, McDonnell DP, Hughes M, Crisp TM, Mangelsdorf DJ, Haussler MR, Pike JW, Shine J, O'Malley BW (1988). "Cloning and expression of full-length cDNA encoding human vitamina D receptor". Proc. Natl. Acad. Sci. USA. 85 (10): 3294-8. Código: 1988PNAS...85.3294B. doi:10.1073/pnas.85.10.3294. PMC 280195. PMID 2835767.
- Hughes MR, Malloy PJ, Kieback DG, Kesterson RA, Pike JW, Feldman D, O'Malley BW (1989). "Point mutaciones en el gen del receptor de vitamina D humano asociado con raquitismo hipocalcémico". Ciencia. 242 (4886): 1702-5. doi:10.1126/science.2849209. PMID 2849209.
- Rut AR, Hewison M, Kristjansson K, Luisi B, Hughes MR, O'Riordan JL (1995). "Dos mutaciones que causan raquitismos resistentes a la vitamina D: modelado sobre la base de estructuras de cristal de dominio de ADN de receptores de hormonas esteroideas". Clin. Endocrinol. 41 (5): 581–90. doi:10.1111/j.1365-2265.1994.tb01822.x. PMID 7828346. S2CID 40851942.
- Malloy PJ, Weisman Y, Feldman D (1994). "Hereditary 1 alpha,25-dihidroxivitamin Riquetes resistentes a la D resultantes de una mutación en el dominio de unión de ácidos del receptor de vitamina D". Endocrinol. Metab. 78 (2): 313-6. doi:10.1210/jcem.78.2.8106618. PMID 8106618.
- Maruyama K, Sugano S (1994). "Oligo-capping: un método simple para reemplazar la estructura de capa de mRNAs eucariotas con oligoribonucleótidos". Gene. 138 (1–2): 171–4. doi:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Yagi H, Ozono K, Miyake H, Nagashima K, Kuroume T, Pike JW (1993). "Una nueva mutación de puntos en el dominio desoxiribonucleico de unión de ácido del receptor de vitamina D en una especie con grillos hereditarios 1,25-dihidroxivitamina D resistentes". Endocrinol. Metab. 76 (2): 509–12. doi:10.1210/jcem.76.2.8381803. PMID 8381803.
- Kristjansson K, Rut AR, Hewison M, O'Riordan JL, Hughes MR (1993). "Dos mutaciones en el dominio de unión hormonal del receptor de vitamina D causan resistencia al tejido a 1,25 dihidroxivitamina D3". J. Clin. Invest. 92 (1): 12–6. doi:10.1172/JCI116539. PMC 293517. PMID 8392085.
- Jurutka PW, Hsieh JC, Nakajima S, Haussler CA, Whitfield GK, Haussler MR (1996). "Fosforilación del receptor de vitamina D humana por cinase de caseína II en Ser-208 potencia la activación transcripcional". Proc. Natl. Acad. Sci. USA. 93 (8): 3519–24. Código:1996PNAS...93.3519J. doi:10.1073/pnas.93.8.3519. PMC 39642. PMID 8622969.
- Lin NU, Malloy PJ, Sakati N, al-Ashwal A, Feldman D (1996). "Una mutación novedosa en el dominio de unión de ácidos desoxiribonucleicos del receptor de vitamina D causa rickets hereditarios 1,25-dihidroxivitamina D resistentes". Endocrinol. Metab. 81 (7): 2564–9. doi:10.1210/jcem.81.7.8675579PMID 8675579. S2CID 46366654.
Enlaces externos
- Calcitriol+Receptors at the U.S. National Library of Medicine Medical Subject Headings (MeSH)
- Receptor nuclear
- Receptor de vitamina D: Molécula del Mes Archivado 2015-10-16 en la Máquina Wayback
- IUPHAR: Receptor de vitamina D
- Reseña de toda la información estructural disponible en el PDB para UniProt: P11473 (Receptor Vitamin D3) en el PDBe-KB.
Este artículo incorpora texto de la Biblioteca Nacional de Medicina de los Estados Unidos, que es de dominio público.