Reacción de Nef
En química orgánica, la reacción Nef es una reacción orgánica que describe la hidrólisis ácida de una sal de un nitroalcano primario o secundario (R−NO2) a un aldehído (R−CH=O) o una cetona (R2C=O) y óxido nitroso (N2O). La reacción ha sido objeto de varias revisiones bibliográficas.

1. Sal de un nitroalkano
3. Ketone
4. Óxido nitroso
La reacción fue descrita en 1894 por el químico John Ulric Nef, quien trató la sal de sodio del nitroetano con ácido sulfúrico, lo que dio como resultado un rendimiento de óxido nitroso del 85-89% y al menos un rendimiento del 70% de acetaldehído. Sin embargo, la reacción fue iniciada un año antes, en 1893, por Konovalov, quien convirtió la sal de potasio del 1-fenilnitroetano con ácido sulfúrico en acetofenona.
Mecanismo de reacción
El mecanismo de reacción a partir de la sal de nitronato como estructuras de resonancia 1a y 1b se muestra a continuación:
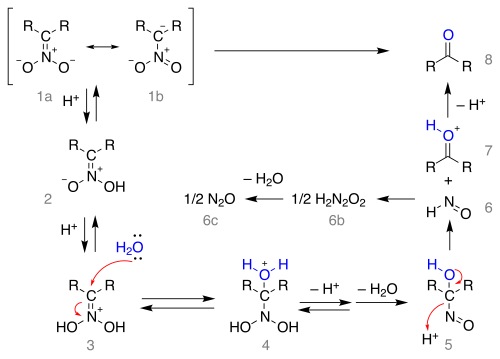
La sal se protona formando el ácido nitroso 2 (en algunos casos se han aislado estos nitronatos) y una vez más el ion iminio 3. Este intermediario es atacado por agua en una adición nucleofílica formando 4 que pierde un protón y luego agua al 1-nitroso-alcanol 5 que se cree que es responsable del color azul oscuro de la mezcla de reacción en muchas reacciones de Nef. Este intermediario se reorganiza en ácido hiponitroso 6 (formando óxido nitroso 6c a 6b) y el ion oxonio 7 que pierde un protón para formar el compuesto carbonílico.
Tenga en cuenta que la formación de la sal de nitronato a partir del compuesto nitro requiere un átomo de hidrógeno alfa y, por lo tanto, la reacción falla con los compuestos nitro terciarios.
Ámbito
Las reacciones de tipo Nef se encuentran con frecuencia en la síntesis orgánica, porque convierten la reacción de Henry en un método conveniente para la funcionalización en las posiciones β y γ. Así, por ejemplo, la reacción se combina con la reacción de Michael en la síntesis del metil 3-acetil-5-oxohexanoato de γ-ceto-carbonilo, un intermediario de la ciclopentenona:
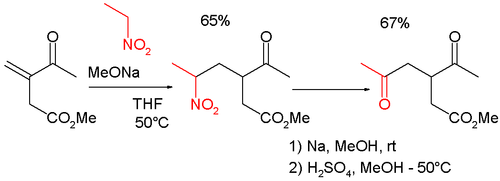
En la química de los carbohidratos, son un método de extensión de cadena para las aldosas, como en el marcaje isotópico de C14-D-manosa y C14-D-glucosa a partir de D-arabinosa y C14-nitrometano (el primer paso aquí es una reacción de Henry):

La reacción opuesta es la degradación de Wohl.
Variantes
El protocolo original de Nef, que utiliza ácido sulfúrico concentrado, ha sido descrito como "violento". La hidrólisis con ácidos fuertes sin la etapa de sal intermedia da como resultado la formación de ácidos carboxílicos y sales de hidroxilamina, pero los ácidos de Lewis, como el cloruro de estaño (IV) y el cloruro de hierro (III), dan lugar a una hidrólisis limpia. Alternativamente, los agentes oxidantes fuertes, como la oxona, el ozono o los permanganatos, escindirán el tautómero nitronato en el doble enlace para formar un carbonilo y un nitrato. Los reductores oxófilos, como las sales de titanio, reducirán el nitronato a una imina susceptible a la hidrólisis, pero los reductores menos selectivos dan lugar a la amina.
Referencias
- ^ Noland, Wayland E. (1955). "La reacción NEF". Reseñas químicas. 55 (1): 137–155. doi:10.1021/cr50001a003.
- ^ Pinnick, Harold W. (1990). "La reacción negativa". En Paquette, Leo A. (ed.). Reacciones orgánicas Volumen 38 (1a edición). Nueva York: Wiley. pp. 655–792. doi:10.1002/0471264180.or038.03. ISBN 97804715944.
- ^ Grierson, David S.; Husson, Henri-Philippe (1991). "4.7 – Polonovski- y Reacciones tipo Pummerer y Nef Reaction". En Trost, Barry; Fleming, Ian (eds.). Síntesis orgánica integral: selectividad, estrategia y eficiencia en la síntesis orgánica moderna, Volumen 6 (1a edición). Nueva York: Pergamon. pp. 909-947. doi:10.1016/B978-0-08-052349-1.00175-X. ISBN 9780080359298.
- ^ Nef, John Ulric (1894). "Ueber die Constitution der Salze der Nitroparaffine". Justus Liebigs Annalen der Chemie. 280 (2–3): 263–291. doi:10.1002/jlac.18942800209.
- ^ Konovalov, J. Russ. Phys. Soc. 2 1893, 6(I)509.
- ^ Warren & Wyatt 2008, pág. 161.
- ^ Una síntesis conveniente de ciclopentenones funcionalizados por γ Nour Lahmar, Taïcir Ben Ayed, Moncef Bellassoued y Hassen Amri Beilstein Journal of Organic Chemistry 2005, 1:11 doi:10.1186/1860-5397-1-11
- ^ McMurry, John E.; Melton, Jack (1977). "Conversión de Nitro al Carbonilo por Ozonolisis de Nitronatos: 2,5-Heptandione". Sintetías orgánicas. 56: 36. doi:10.15227/orgsyn.056.0036.
- ^ a b Warren, Stuart; Wyatt, Paul (2008). Sintesis orgánica: el enfoque de desconexión (2a edición). Wiley. págs. 161 a 164.
- ^ Miyashita, Masaaki; Yanami, Tetsuji; Yoshikoshi, Akira (1981). "Sintesis de 1,4-Diketones de Silyl Enol Ethers y Nitroolefins: 2-(2-Oxopropyl)cyclohexanone". Sintetías orgánicas. 60: 117. doi:10.15227/orgsyn.060.0117.
- ^ Heinzelman, R. V. (1955). "o-Methoxyphenylacetone". Sintetías orgánicas. 35: 74. doi:10.15227/orgsyn.035.0074.
- ^ Ceccherelli, Paolo; Curinia, Massimo; Marcotullioa, Maria Carla; Epifanoa, Francesco; Rosatia, Ornelio (1998). "Oxone promovió Nef Reaction. Conversión sencilla de Nitro Group en Carbonyl". Comunicaciones sintéticas. 28 (16): 3057–3064. doi:10.1080/00397919808004885.