Reacción de Horner-Wadsworth-Emmons
La reacción de Horner-Wadsworth-Emmons (HWE) es una reacción química utilizada en química orgánica de carbaniones fosfonato estabilizados con aldehídos (o cetonas) para producir predominantemente E-alquenos.
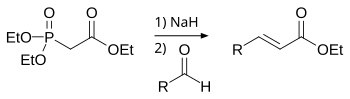
En 1958, Leopold Horner publicó una reacción de Wittig modificada utilizando carbaniones estabilizados con fosfonato. William S. Wadsworth y William D. Emmons definieron con más detalle la reacción.
A diferencia de los iluros de fosfonio utilizados en la reacción de Wittig, los carbaniones estabilizados con fosfonato son más nucleofílicos pero menos básicos. Asimismo, se pueden alquilar carbaniones estabilizados con fosfonato. A diferencia de los iluros de fosfonio, el subproducto de la sal de dialquilfosfato se elimina fácilmente mediante extracción acuosa.
Se han publicado varias reseñas.
Mecanismo de reacción

La reacción de Horner-Wadsworth-Emmons comienza con la desprotonación del fosfonato para dar el carbanión fosfonato 1. La adición nucleófila del carbanión al aldehído 2 (o cetona) produciendo 3a o 3b es el paso limitante de la velocidad. Si R2 = H, entonces los intermedios 3a y 4a y los intermedios 3b y 4b pueden interconvertirse entre sí. La eliminación final de los oxafosfetanos 4a y 4b produce (E)-alqueno 5 y (Z)-alqueno 6, siendo el subproducto un dialquilfosfato.

La relación de los isómeros alkenianos 5 y 6 no depende del resultado estereoquímico de la adición de carbanion inicial y de la capacidad de los intermediarios para equilibrar.
El grupo aceptor de electrones (EWG) alfa del fosfonato es necesario para que se produzca la eliminación final. En ausencia de un grupo aceptor de electrones, el producto final es el β-hidroxifosfonato 3a y 3b. Sin embargo, estos β-hidroxifosfonatos pueden transformarse en alquenos mediante reacción con diisopropilcarbodiimida.
Estereoselectividad
La reacción de Horner-Wadsworth-Emmons favorece la formación de (E)-alquenos. En general, cuanto mayor sea el equilibrio entre los intermedios, mayor será la selectividad para la formación de (E)-alqueno.
Alquenos disustituidos
Thompson y Heathcock han realizado un estudio sistemático de la reacción del 2-(dimetilfosfono)acetato de metilo con varios aldehídos. Si bien cada efecto fue pequeño, tuvieron un efecto acumulativo que permitió modificar el resultado estereoquímico sin modificar la estructura del fosfonato. Encontraron una mayor estereoselectividad (E) con las siguientes condiciones:
- Aumento de la masa esterática del aldehído
- Temperaturas de reacción superior (23 °C sobre −78 °C)
- Li √≥ Na َ K saless
En un estudio separado, se encontró que el fosfonato voluminoso y los grupos aceptores de electrones voluminosos mejoran la selectividad del E-alqueno.
Alquenos trisustituidos
La masa estérica de los grupos fosfonato y aceptores de electrones juega un papel crítico en la reacción de los fosfonatos ramificados en α con aldehídos alifáticos.
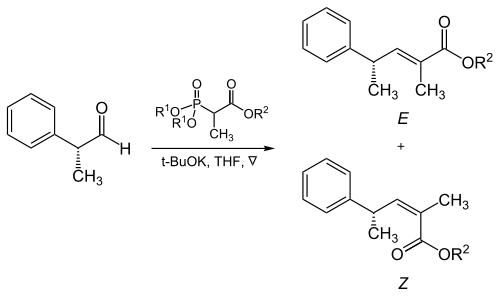
| R1 | R2 | Ratio de alkenes (E: Z) |
|---|---|---|
| Metil | Metil | 5: 95 |
| Metil | Ethyl | 10: 90 |
| Ethyl | Ethyl | 40: 60 |
| Isopropyl | Ethyl | 90: 10 |
| Isopropyl | Isopropyl | 95: 5 |
Los aldehídos aromáticos producen casi exclusivamente (E)-alquenos. En caso de que se necesiten (Z)-alquenos de aldehídos aromáticos, se puede utilizar la modificación Still-Gennari (ver más abajo).
Olefinación de cetonas
La estereoselectividad de la reacción de las cetonas de Horner-Wadsworth-Emmons es de pobre a modesta.
Variaciones
Sustratos sensibles a la base
Dado que muchos sustratos no son estables al hidruro de sodio, se han desarrollado varios procedimientos utilizando bases más suaves. Masamune y Roush han desarrollado condiciones leves utilizando cloruro de litio y DBU. Rathke amplió esto a los haluros de litio o magnesio con trietilamina. Varias otras bases han resultado eficaces.
Modificación fija
W. Clark Still y C. Gennari han desarrollado condiciones que dan a los alquenos Z una estereoselectividad excelente. Utilizando fosfonatos con grupos aceptores de electrones (trifluoroetilo) junto con condiciones de fuerte disociación (KHMDS y 18-corona-6 en THF) se puede lograr una producción casi exclusiva de Z-alqueno.
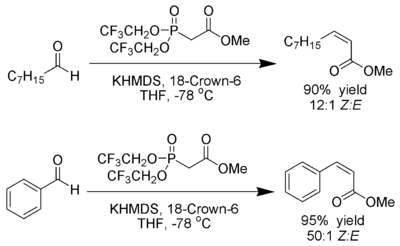
Ando ha sugerido que el uso de fosfonatos deficientes en electrones acelera la eliminación de los intermedios de oxafosfetano.