Reacción de Gattermann
La reacción de Gattermann (también conocida como formilación de Gattermann y síntesis de salicilaldehído de Gattermann) es una reacción química en la que los compuestos aromáticos se formilan mediante una mezcla de cianuro de hidrógeno (HCN) y cloruro de hidrógeno (HCl) en presencia de un catalizador de ácido de Lewis como el cloruro de aluminio (AlCl3). Recibe su nombre del químico alemán Ludwig Gattermann y es similar a la reacción de Friedel-Crafts.
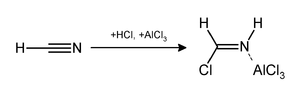

Las modificaciones han demostrado que es posible utilizar cianuro de sodio o bromuro de cianógeno en lugar de cianuro de hidrógeno.
La reacción se puede simplificar reemplazando la combinación HCN/AlCl3 por cianuro de cinc. Aunque también es muy tóxico, el Zn(CN)2 es un sólido, por lo que es más seguro trabajar con él que el HCN gaseoso. El Zn(CN)2 reacciona con el HCl para formar el reactivo clave HCN y el Zn(Cl)2 que sirve como catalizador de ácido de Lewis in situ. Un ejemplo del método Zn(CN)2 es la síntesis de mesitaldehído a partir de mesitileno.
Reacción Gattermann-Koch
La reacción de Gattermann-Koch, llamada así en honor a los químicos alemanes Ludwig Gattermann y Julius Arnold Koch, es una variante de la reacción de Gattermann en la que se utiliza monóxido de carbono (CO) en lugar de cianuro de hidrógeno.
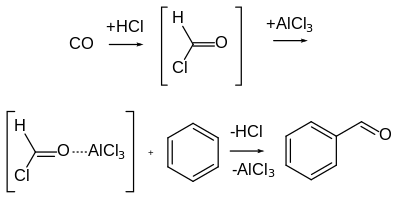
A diferencia de la reacción de Gattermann, esta reacción no es aplicable a sustratos de fenol y éter de fenol. Aunque inicialmente se postuló que el cloruro de formilo, altamente inestable, era un intermediario, ahora se piensa que el catión formilo (es decir, monóxido de carbono protonado), [HCO]+, reacciona directamente con el areno sin la formación inicial de cloruro de formilo. Además, cuando se utiliza cloruro de cinc como ácido de Lewis en lugar de cloruro de aluminio, por ejemplo, o cuando el monóxido de carbono no se utiliza a alta presión, a menudo es necesaria la presencia de trazas de cocatalizador de cloruro de cobre(I) o cloruro de níquel(II). El cocatalizador de metal de transición puede servir como "transportador" al reaccionar primero con CO para formar un complejo carbonílico, que luego se transforma en el electrófilo activo.
Véase también
- Reacción Houben-Hoesch
- Stephen aldehyde síntesis
Referencias
- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th ed.), New York: Wiley-Interscience, p. 725, ISBN 978-0-471-72091-1
- ^ Gattermann, L.; Berchelmann, W. (1898). "Synthese aromatischer Oxyaldehyde". Berichte der deutschen chemischen Gesellschaft. 31 (2): 1765-1769. doi:10.1002/cber.18980310281.
- ^ Karrer, P. (1919). "Über Oxycarbonylverbindungen I. Eine neue Synthese von" [Hydroxycarbonyl compounds. I. Nueva síntesis de hidroxialdehídos]. Helvetica Chimica Acta (en alemán). 2 (1): 89–94. doi:10.1002/hlca.19190020109.
- ^ Adams R.; Levine, I. (1923). "Simplificación de la Síntesis Gattermann de Aldehídos Hidroxi". J. Am. Chem. Soc. 45 (10): 2373–77. doi:10.1021/ja01663a020.
- ^ a b Adams, Roger (1957). Reacciones orgánicas, Volumen 9. Nueva York: John Wiley ' Sons, Inc. págs. 38 y 53 a 54. doi:10.1002/0471264180.o009.02. ISBN 9780471007265.
- ^ Fuson, R. C.; Horning, E. C.; Rowland, S. P.; Ward, M. L. (1955). "Mesitaldehyde". Sintetías orgánicas. doi:10.15227/orgsyn.023.0057; Volumenes recogidos, vol. 3, pág. 549.
- ^ Gattermann, L.; Koch, J. A. (1897). "Eine Synthese aromatischer Aldehyde". Chemische Berichte. 30 (2): 1622-1624. doi:10.1002/cber.18970300288.
- ^ Li, Jie Jack (2003). Reacciones de nombre: Una colección de mecanismos de reacción detallados (disponible en Google Books) (2a edición). Springer. p. 157. ISBN 3-540-40203-9.
- ^ Kurti, Laszlo. (2005). Aplicaciones Estratégicas de reacciones nombradas en síntesis orgánica: fondo y mecanismos detallados. Czako, Barbara. Burlington: Elsevier Science. ISBN 978-0-08-057541-4. OCLC 850164343.
- ^ Dilke, M. H.; Eley, D. D. (1949). "550. La reacción Gattermann-Koch. Parte II. Kinetics de reacción". J. Chem. Soc.: 2613–2620. doi:10.1039/JR9490002613. ISSN 0368-1769.