Química organometálica
La química organometálica es el estudio de los compuestos organometálicos, compuestos químicos que contienen al menos un enlace químico entre un átomo de carbono de una molécula orgánica y un metal, incluidos los metales alcalinos, alcalinotérreos y de transición, y en ocasiones se amplía para incluir metaloides como boro, silicio, y selenio, también.Además de los enlaces con fragmentos de organilo o moléculas, los enlaces con carbono 'inorgánico', como el monóxido de carbono (carbonilos metálicos), el cianuro o el carburo, generalmente también se consideran organometálicos. Algunos compuestos relacionados, como los hidruros de metales de transición y los complejos de fosfina metálica, a menudo se incluyen en las discusiones sobre compuestos organometálicos, aunque estrictamente hablando, no son necesariamente organometálicos. El término relacionado pero distinto "compuesto metalorgánico" se refiere a compuestos que contienen metales que carecen de enlaces metal-carbono directos pero que contienen ligandos orgánicos. Los β-dicetonatos metálicos, los alcóxidos, las dialquilamidas y los complejos de fosfina metálica son miembros representativos de esta clase. El campo de la química organometálica combina aspectos de la química orgánica e inorgánica tradicional.
Los compuestos organometálicos se usan ampliamente tanto estequiométricamente en reacciones químicas industriales y de investigación, así como en el papel de catalizadores para aumentar las velocidades de tales reacciones (p. ej., como en los usos de catálisis homogénea), donde las moléculas objetivo incluyen polímeros, productos farmacéuticos y muchos otros. otros tipos de productos prácticos.
Compuestos organometálicos
Los compuestos organometálicos se distinguen por el prefijo "organo-" (p. ej., compuestos de organopaladio) e incluyen todos los compuestos que contienen un enlace entre un átomo de metal y un átomo de carbono de un grupo organilo. Además de los metales tradicionales (metales alcalinos, metales alcalinotérreos, metales de transición y metales de postransición), se considera que los lantánidos, actínidos, semimetales y los elementos boro, silicio, arsénico y selenio forman compuestos organometálicos. Los ejemplos de compuestos organometálicos incluyen los reactivos de Gilman, que contienen litio y cobre, y los reactivos de Grignard, que contienen magnesio. El tetracarbonil níquel y el ferroceno son ejemplos de compuestos organometálicos que contienen metales de transición. Otros ejemplos de compuestos organometálicos incluyen compuestos de organolitio como n-butillitio (n-BuLi), compuestos de organocinc como el dietilzinc (Et 2 Zn), compuestos de organoestaño como el hidruro de tributilestaño (Bu 3 SnH), compuestos de organoborano como el trietilborano (Et 3 B) y compuestos de organoaluminio como el trimetilaluminio (Me 3Al).
Un complejo organometálico natural es la metilcobalamina (una forma de vitamina B 12), que contiene un enlace cobalto-metilo. Este complejo, junto con otros complejos biológicamente relevantes, se discuten a menudo dentro del subcampo de la química bioorganometálica.
- Compuestos organometálicos representativos
 El ferroceno es un complejo de organohierro arquetípico. Es un compuesto sublimable, estable al aire.
El ferroceno es un complejo de organohierro arquetípico. Es un compuesto sublimable, estable al aire. El cobaltoceno es un análogo estructural del ferroceno, pero es muy reactivo con el aire.
El cobaltoceno es un análogo estructural del ferroceno, pero es muy reactivo con el aire. El hidruro de carbonilo de tris (trifenilfosfina) rodio se utiliza en la producción comercial de muchas fragancias a base de aldehído.
El hidruro de carbonilo de tris (trifenilfosfina) rodio se utiliza en la producción comercial de muchas fragancias a base de aldehído. La sal de Zeise es un ejemplo de un complejo de alqueno de metal de transición.
La sal de Zeise es un ejemplo de un complejo de alqueno de metal de transición. El trimetilaluminio es un compuesto organometálico con un grupo metilo puente. Se utiliza en la producción industrial de algunos alcoholes.
El trimetilaluminio es un compuesto organometálico con un grupo metilo puente. Se utiliza en la producción industrial de algunos alcoholes. El dimetilzinc tiene una coordinación lineal. Es un líquido pirofórico volátil que se utiliza en la preparación de películas semiconductoras.
El dimetilzinc tiene una coordinación lineal. Es un líquido pirofórico volátil que se utiliza en la preparación de películas semiconductoras.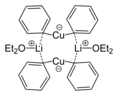 El bis(dietil eterato) de difenilcuprato de litio es un ejemplo de un reactivo de Gilman, un tipo de complejo de organocobre empleado con frecuencia en la síntesis orgánica.
El bis(dietil eterato) de difenilcuprato de litio es un ejemplo de un reactivo de Gilman, un tipo de complejo de organocobre empleado con frecuencia en la síntesis orgánica.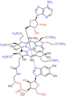 La adenosilcobalamina es un cofactor requerido por varias reacciones enzimáticas cruciales que tienen lugar en el cuerpo humano. Es un raro ejemplo de un alquilo de metal (cobalto) en biología.
La adenosilcobalamina es un cofactor requerido por varias reacciones enzimáticas cruciales que tienen lugar en el cuerpo humano. Es un raro ejemplo de un alquilo de metal (cobalto) en biología. El pentacarbonilo de hierro (0) es un líquido de color rojo anaranjado que se prepara directamente a partir de la unión de hierro finamente dividido y gas monóxido de carbono bajo presión.
El pentacarbonilo de hierro (0) es un líquido de color rojo anaranjado que se prepara directamente a partir de la unión de hierro finamente dividido y gas monóxido de carbono bajo presión.![El tecnecio [99mTc] sestamibi se utiliza para obtener imágenes del músculo cardíaco en medicina nuclear.](https://upload.wikimedia.org/wikipedia/commons/thumb/1/17/Tc99_sestamibi_2D_structure.svg/100px-Tc99_sestamibi_2D_structure.svg.png) El tecnecio [Tc] sestamibi se utiliza para obtener imágenes del músculo cardíaco en medicina nuclear.
El tecnecio [Tc] sestamibi se utiliza para obtener imágenes del músculo cardíaco en medicina nuclear.
Distinción de compuestos de coordinación con ligandos orgánicos.
Muchos complejos presentan enlaces de coordinación entre un metal y ligandos orgánicos. Los complejos en los que los ligandos orgánicos se unen al metal a través de un heteroátomo como el oxígeno o el nitrógeno se consideran compuestos de coordinación (p. ej., hemo A y Fe(acac) 3). Sin embargo, si alguno de los ligandos forma un enlace directo metal-carbono (MC), entonces el complejo se considera organometálico. Aunque la IUPAC no ha definido formalmente el término, algunos químicos usan el término "metalorgánico" para describir cualquier compuesto de coordinación que contenga un ligando orgánico independientemente de la presencia de un enlace MC directo.
El estado de los compuestos en los que el anión canónico tiene una carga negativa que se comparte entre un átomo de carbono (deslocalizado) y un átomo más electronegativo que el carbono (por ejemplo, enolatos) puede variar con la naturaleza del resto aniónico, el ion metálico y posiblemente la médium. En ausencia de evidencia estructural directa de un enlace carbono-metal, estos compuestos no se consideran organometálicos. Por ejemplo, los enolatos de litio a menudo contienen solo enlaces Li-O y no son organometálicos, mientras que los enolatos de zinc (reactivos de Reformatsky) contienen enlaces Zn-O y Zn-C y son de naturaleza organometálica.
Estructura y propiedades
El enlace metal-carbono en los compuestos organometálicos es generalmente altamente covalente. Para elementos altamente electropositivos, como el litio y el sodio, el ligando de carbono exhibe un carácter carbaniónico, pero los aniones libres basados en carbono son extremadamente raros, un ejemplo es el cianuro.
La mayoría de los compuestos organometálicos son sólidos a temperatura ambiente, sin embargo, algunos son líquidos como el metilciclopentadienil manganeso tricarbonilo o incluso líquidos volátiles como el níquel tetracarbonilo. Muchos compuestos organometálicos son sensibles al aire (reactivos con el oxígeno y la humedad) y, por lo tanto, deben manipularse en una atmósfera inerte. Algunos compuestos organometálicos como el trietilaluminio son pirofóricos y se encenderán al contacto con el aire.
Conceptos y técnicas
Como en otras áreas de la química, el conteo de electrones es útil para organizar la química organometálica. La regla de los 18 electrones es útil para predecir la estabilidad de los complejos organometálicos, por ejemplo, los carbonilos metálicos y los hidruros metálicos. La regla 18e tiene dos modelos representativos de conteo de electrones, modelos de ligando iónico y neutro (también conocido como covalente), respectivamente. La hapticidad de un complejo metal-ligando puede influir en el conteo de electrones. Hapticidad (η, minúscula griega eta), describe el número de ligandos contiguos coordinados a un metal. Por ejemplo, el ferroceno, [(η -C 5 H 5) 2 Fe], tiene dos ligandos de ciclopentadienilo que dan una hapticidad de 5, donde los cinco átomos de carbono del C 5 H5 ligando aportan un electrón al centro de hierro. Los ligandos que se unen a átomos no contiguos se denotan con la letra griega kappa, κ. Quelante κ2-acetato es un ejemplo. El método de clasificación de enlaces covalentes identifica tres clases de ligandos, X, L y Z; que se basan en las interacciones donadoras de electrones del ligando. Muchos compuestos organometálicos no siguen la regla 18e. Los átomos de metal en los compuestos organometálicos se describen con frecuencia por su número de electrones d y su estado de oxidación. Estos conceptos se pueden utilizar para ayudar a predecir su reactividad y geometría preferida. El enlace químico y la reactividad en compuestos organometálicos se discuten a menudo desde la perspectiva del principio isolobal.
Se utiliza una amplia variedad de técnicas físicas para determinar la estructura, composición y propiedades de los compuestos organometálicos. La difracción de rayos X es una técnica particularmente importante que puede ubicar las posiciones de los átomos dentro de un compuesto sólido, brindando una descripción detallada de su estructura. Otras técnicas como la espectroscopia infrarroja y la espectroscopia de resonancia magnética nuclear también se utilizan con frecuencia para obtener información sobre la estructura y la unión de compuestos organometálicos. La espectroscopia ultravioleta-visible es una técnica común utilizada para obtener información sobre la estructura electrónica de los compuestos organometálicos. También se utiliza para monitorear el progreso de las reacciones organometálicas, así como para determinar su cinética.La dinámica de los compuestos organometálicos se puede estudiar mediante espectroscopia de RMN dinámica. Otras técnicas notables incluyen la espectroscopia de absorción de rayos X, la espectroscopia de resonancia paramagnética de electrones y el análisis elemental.
Debido a su alta reactividad frente al oxígeno y la humedad, los compuestos organometálicos a menudo deben manipularse utilizando técnicas sin aire. El manejo sin aire de compuestos organometálicos generalmente requiere el uso de aparatos de laboratorio como una caja de guantes o una línea Schlenk.
Historia
Los primeros desarrollos en química organometálica incluyen la síntesis de Louis Claude Cadet de compuestos de arsénico metílico relacionados con el cacodilo, el complejo de platino-etileno de William Christopher Zeise, el descubrimiento de dietil y dimetilzinc de Edward Frankland, el descubrimiento de Ni (CO) 4 de Ludwig Mond y los compuestos de organomagnesio de Victor Grignard.. (Aunque no siempre se reconoce como un compuesto organometálico, el azul de Prusia, un complejo de cianuro de hierro de valencia mixta, fue preparado por primera vez en 1706 por el fabricante de pinturas Johann Jacob Diesbach como el primer polímero de coordinación y material sintético que contiene un enlace metal-carbono). abundantes y diversos productos del carbón y el petróleo llevaron a Ziegler-Natta, Fischer-Tropsch, catálisis de hidroformilación que emplean CO, H 2y alquenos como materias primas y ligandos.
El reconocimiento de la química organometálica como un subcampo distinto culminó con los Premios Nobel a Ernst Fischer y Geoffrey Wilkinson por su trabajo en metalocenos. En 2005, Yves Chauvin, Robert H. Grubbs y Richard R. Schrock compartieron el Premio Nobel por la metátesis de olefinas catalizada por metales.
Cronología de la química organometálica.
- 1760 Louis Claude Cadet de Gassicourt investiga tintas a base de sales de cobalto y aísla el cacodilo del mineral de cobalto que contiene arsénico.
- 1827 William Christopher Zeise produce la sal de Zeise; el primer complejo platino/olefina
- 1848 Edward Frankland descubre el dietilzinc
- 1863 Charles Friedel y James Crafts preparan organoclorosilanos
- 1890 Ludwig Mond descubre el carbonilo de níquel
- 1899 Introducción de la reacción de Grignard
- 1899 John Ulric Nef descubre la alquinilación utilizando acetiluros de sodio.
- 1900 Paul Sabatier trabaja en la hidrogenación de compuestos orgánicos con catalizadores metálicos. La hidrogenación de grasas da inicio a los avances en la industria alimentaria, véase margarina
- 1909 Paul Ehrlich presenta Salvarsan para el tratamiento de la sífilis, uno de los primeros compuestos organometálicos a base de arsénico.
- 1912 Premio Nobel Víctor Grignard y Paul Sabatier
- 1930 Henry Gilman trabaja en cupratos de litio, ver reactivo de Gilman
- 1951 Walter Hieber recibió el premio Alfred Stock por su trabajo con la química del carbonilo metálico.
- 1951 Se descubre el Ferroceno
- 1956 Dorothy Crawfoot Hodgkin determina la estructura de la vitamina B 12, la primera biomolécula encontrada que contiene un enlace metal-carbono, ver química bioorganometálica
- Premio Nobel de 1963 para Karl Ziegler y Giulio Natta sobre el catalizador Ziegler-Natta
- 1965 Descubrimiento del ciclobutadieneiron tricarbonilo
- 1968 Se desarrolla la reacción de Heck
- 1973 Premio Nobel Geoffrey Wilkinson y Ernst Otto Fischer sobre compuestos sándwich
- 1981 Premio Nobel Roald Hoffmann y Kenichi Fukui por la creación de las Reglas Woodward-Hoffman
- Premio Nobel 2001 WS Knowles, R. Noyori y Karl Barry Sharpless por hidrogenación asimétrica
- Premio Nobel de 2005 Yves Chauvin, Robert Grubbs y Richard Schrock sobre la metátesis de alquenos catalizada por metales
- Premio Nobel 2010 Richard F. Heck, Ei-ichi Negishi, Akira Suzuki por reacciones de acoplamiento cruzado catalizadas por paladio
Alcance
Las áreas de subespecialidad de la química organometálica incluyen:
- Elementos del período 2: química de organolitio, química de organoberilio, química de organoborano
- Elementos del período 3: química de organosodio, química de organomagnesio, química de organoaluminio, química de organosilicio
- Elementos del período 4: química organocálcica, química organoscandio, química organotitanio, química organovanadio, química organocromo, química organomanganeso, química organohierro, química organocobalto, química organoníquel, química organocobre, química organocinc, química organogallio, química organogermanio, química organoarsénico, química organoselenio
- Elementos del período 5: química de organoitrio, química de organozirconio, química de organoniobio, química de organomolibdeno, química de organorutenio, química de organorodio, química de organopaladio, química de organoplata, química de organocadmio, química de organoindio, química de organoestaño, química de organoantimonio, química de organotelurio
- Elementos del período 6: química de organolantánidos, química de organocerio, química de organotantalio, química de organorrenio, química de organoosmio, química de organoiridio, química de organoplatino, química de organooro, química de organomercurio, química de organotalio, química de organoplomo, química de organobismuto, química de organopolonio
- Elementos del período 7: química de organoactínidos, química de organouranio, química de organoneptunio
Aplicaciones industriales
Los compuestos organometálicos encuentran un amplio uso en reacciones comerciales, tanto como catalizadores homogéneos como reactivos estequiométricos. Por ejemplo, los compuestos de organolitio, organomagnesio y organoaluminio, cuyos ejemplos son muy básicos y muy reductores, son útiles estequiométricamente pero también catalizan muchas reacciones de polimerización.
Casi todos los procesos que involucran monóxido de carbono se basan en catalizadores, y los ejemplos notables se describen como carbonilaciones. La producción de ácido acético a partir de metanol y monóxido de carbono se cataliza mediante complejos de carbonilo metálico en el proceso Monsanto y el proceso Cativa. La mayoría de los aldehídos sintéticos se producen mediante hidroformilación. La mayor parte de los alcoholes sintéticos, al menos los más grandes que el etanol, se producen por hidrogenación de aldehídos derivados de la hidroformilación. De manera similar, el proceso Wacker se usa en la oxidación de etileno a acetaldehído.
Casi todos los procesos industriales que involucran polímeros derivados de alquenos se basan en catalizadores organometálicos. El polietileno y el polipropileno del mundo se producen tanto de forma heterogénea mediante catálisis Ziegler-Natta como de forma homogénea, por ejemplo, mediante catalizadores de geometría restringida.
La mayoría de los procesos que involucran hidrógeno se basan en catalizadores a base de metales. Mientras que las hidrogenaciones a granel (por ejemplo, la producción de margarina) se basan en catalizadores heterogéneos, para la producción de productos químicos finos tales hidrogenaciones se basan en complejos organometálicos solubles (homogéneos) o involucran intermediarios organometálicos. Los complejos organometálicos permiten que estas hidrogenaciones se realicen de forma asimétrica.
Muchos semiconductores se producen a partir de trimetilgalio, trimetilindio, trimetilaluminio y trimetilantimonio. Estos compuestos volátiles se descomponen junto con el amoníaco, la arsina, la fosfina y los hidruros relacionados en un sustrato calentado mediante el proceso de epitaxia en fase vapor metalorgánica (MOVPE) en la producción de diodos emisores de luz (LED).
Reacciones organometálicas
Los compuestos organometálicos experimentan varias reacciones importantes:
- sustitución asociativa y disociativa
- adición oxidativa y eliminación reductora
- transmetalación
- inserción migratoria
- eliminación de β-hidruro
- transferencia de electrones
- activación del enlace carbono-hidrógeno
- carbometalación
- hidrometalación
- ciclometalación
- abstracción nucleofílica
Los complejos organometálicos facilitan la síntesis de muchas moléculas orgánicas. La metátesis de enlaces sigma es un método sintético para formar nuevos enlaces sigma carbono-carbono. La metátesis de enlace sigma se usa típicamente con complejos de metales de transición tempranos que se encuentran en su estado de oxidación más alto. El uso de metales de transición que se encuentran en su estado de oxidación más alto evita que ocurran otras reacciones, como la adición oxidativa. Además de la metátesis de enlaces sigma, la metátesis de olefinas se utiliza para sintetizar varios enlaces pi carbono-carbono. Ni la metátesis del enlace sigma ni la metátesis de la olefina cambian el estado de oxidación del metal. Se utilizan muchos otros métodos para formar nuevos enlaces carbono-carbono, incluidas las reacciones de eliminación e inserción de beta-hidruro.
Catálisis
Los complejos organometálicos se utilizan comúnmente en catálisis. Los principales procesos industriales incluyen hidrogenación, hidrosililación, hidrocianación, metátesis de olefinas, polimerización de alquenos, oligomerización de alquenos, hidrocarboxilación, carbonilación de metanol e hidroformilación. Los intermedios organometálicos también se invocan en muchos procesos de catálisis heterogéneos, análogos a los enumerados anteriormente. Además, se suponen intermediarios organometálicos para el proceso Fischer-Tropsch.
Los complejos organometálicos también se utilizan comúnmente en la síntesis química fina a pequeña escala, especialmente en las reacciones de acoplamiento cruzado que forman enlaces carbono-carbono, por ejemplo, el acoplamiento Suzuki-Miyaura, la aminación Buchwald-Hartwig para producir arilaminas a partir de haluros de arilo y el acoplamiento Sonogashira. etc.
Preocupaciones ambientales
En el medio ambiente se encuentran compuestos organometálicos naturales y contaminantes. Algunos que son remanentes del uso humano, como los compuestos de organoplomo y organomercurio, son riesgos de toxicidad. El tetraetilo de plomo se preparó para su uso como aditivo de gasolina, pero ha caído en desuso debido a la toxicidad del plomo. Sus sustitutos son otros compuestos organometálicos, como el ferroceno y el metilciclopentadienil manganeso tricarbonilo (MMT). El compuesto organoarsénico roxarsona es un aditivo alimentario controvertido. En 2006, se produjeron aproximadamente un millón de kilogramos solo en los EE. UU. Los compuestos de organoestaño alguna vez se usaron ampliamente en pinturas antiincrustantes, pero desde entonces se prohibieron debido a preocupaciones ambientales.
Contenido relacionado
Microfluidos
Hexoquinasa
Cuasicristal