Punto de ebullición
El punto de ebullición de una sustancia es la temperatura a la cual la presión de vapor de un líquido es igual a la presión que rodea al líquido y el líquido se convierte en vapor.
El punto de ebullición de un líquido varía dependiendo de la presión ambiental circundante. Un líquido en un vacío parcial tiene un punto de ebullición más bajo que cuando ese líquido está a presión atmosférica. Un líquido a alta presión tiene un punto de ebullición más alto que cuando ese líquido está a presión atmosférica. Por ejemplo, el agua hierve a 100 °C (212 °F) al nivel del mar, pero a 93,4 °C (200,1 °F) a 1905 metros (6250 pies) de altitud. Para una presión dada, diferentes líquidos hervirán a diferentes temperaturas.
El punto de ebullición normal (también llamado punto de ebullición atmosférico o punto de ebullición a presión atmosférica) de un líquido es el caso especial en el que la presión de vapor del líquido es igual a la presión atmosférica definida al nivel del mar, una atmósfera. A esa temperatura, la presión de vapor del líquido llega a ser suficiente para superar la presión atmosférica y permitir que se formen burbujas de vapor dentro de la mayor parte del líquido. El punto de ebullición estándar ha sido definido por la IUPAC desde 1982 como la temperatura a la que se produce la ebullición bajo una presión de un bar.
El calor de vaporización es la energía requerida para transformar una cantidad dada (un mol, kg, libra, etc.) de una sustancia de líquido a gas a una presión dada (a menudo presión atmosférica).
Los líquidos pueden cambiar a vapor a temperaturas por debajo de sus puntos de ebullición a través del proceso de evaporación. La evaporación es un fenómeno superficial en el que las moléculas ubicadas cerca del borde del líquido, que no están contenidas por suficiente presión del líquido en ese lado, escapan al entorno en forma de vapor. Por otro lado, la ebullición es un proceso en el que se escapan moléculas de cualquier parte del líquido, lo que da como resultado la formación de burbujas de vapor dentro del líquido.
Temperatura y presión de saturación
Un líquido saturado contiene tanta energía térmica como puede sin hervir (o, por el contrario, un vapor saturado contiene tan poca energía térmica como puede sin condensarse).
Temperatura de saturación significa punto de ebullición. La temperatura de saturación es la temperatura para una presión de saturación correspondiente a la cual un líquido hierve en su fase de vapor. Se puede decir que el líquido está saturado de energía térmica. Cualquier adición de energía térmica da como resultado una transición de fase.
Si la presión en un sistema permanece constante (isobárica), un vapor a la temperatura de saturación comenzará a condensarse en su fase líquida a medida que se elimina la energía térmica (calor). De manera similar, un líquido a temperatura y presión de saturación hervirá en su fase de vapor a medida que se aplique energía térmica adicional.
El punto de ebullición corresponde a la temperatura a la cual la presión de vapor del líquido es igual a la presión ambiental circundante. Por lo tanto, el punto de ebullición depende de la presión. Los puntos de ebullición pueden publicarse con respecto al NIST, la presión estándar de EE. UU. de 101,325 kPa (o 1 atm), o la presión estándar de la IUPAC de 100,000 kPa. En elevaciones más altas, donde la presión atmosférica es mucho más baja, el punto de ebullición también es más bajo. El punto de ebullición aumenta con el aumento de la presión hasta el punto crítico, donde las propiedades del gas y del líquido se vuelven idénticas. El punto de ebullición no se puede aumentar más allá del punto crítico. Asimismo, el punto de ebullición disminuye al disminuir la presión hasta alcanzar el punto triple. El punto de ebullición no puede reducirse por debajo del punto triple.
Si se conocen el calor de vaporización y la presión de vapor de un líquido a cierta temperatura, el punto de ebullición se puede calcular utilizando la ecuación de Clausius-Clapeyron, así:
donde: 







La presión de saturación es la presión para una temperatura de saturación correspondiente a la cual un líquido hierve en su fase de vapor. La presión de saturación y la temperatura de saturación tienen una relación directa: a medida que aumenta la presión de saturación, también lo hace la temperatura de saturación.
Si la temperatura en un sistema permanece constante (un sistema isotérmico), el vapor a presión y temperatura de saturación comenzará a condensarse en su fase líquida a medida que aumenta la presión del sistema. De manera similar, un líquido a la presión y temperatura de saturación tenderá a pasar rápidamente a su fase de vapor a medida que disminuye la presión del sistema.
Hay dos convenciones con respecto al punto de ebullición estándar del agua: El punto de ebullición normal es 99,97 °C (211,9 °F) a una presión de 1 atm (es decir, 101,325 kPa). El punto de ebullición estándar del agua recomendado por la IUPAC a una presión estándar de 100 kPa (1 bar) es de 99,61 °C (211,3 °F). A modo de comparación, en la cima del Monte Everest, a una altura de 8848 m (29 029 pies), la presión es de aproximadamente 34 kPa (255 Torr) y el punto de ebullición del agua es de 71 °C (160 °F). La escala de temperatura Celsius estuvo definida hasta 1954 por dos puntos: 0 °C definido por el punto de congelación del agua y 100 °C definido por el punto de ebullición del agua a la presión atmosférica estándar.
Relación entre el punto de ebullición normal y la presión de vapor de los líquidos
Cuanto mayor sea la presión de vapor de un líquido a una temperatura determinada, menor será el punto de ebullición normal (es decir, el punto de ebullición a presión atmosférica) del líquido.
El gráfico de presión de vapor a la derecha tiene gráficos de las presiones de vapor versus temperaturas para una variedad de líquidos. Como puede verse en el gráfico, los líquidos con las presiones de vapor más altas tienen los puntos de ebullición normales más bajos.
Por ejemplo, a cualquier temperatura dada, el cloruro de metilo tiene la presión de vapor más alta de todos los líquidos de la tabla. También tiene el punto de ebullición normal más bajo (−24,2 °C), que es donde la curva de presión de vapor del cloruro de metilo (la línea azul) se cruza con la línea de presión horizontal de una atmósfera (atm) de presión de vapor absoluta.
El punto crítico de un líquido es la temperatura (y presión) más alta a la que realmente hervirá.
Véase también Presión de vapor del agua.
Propiedades de los elementos
El elemento con el punto de ebullición más bajo es el helio. Tanto el punto de ebullición del renio como el del tungsteno superan los 5000 K a presión estándar; Debido a que es difícil medir las temperaturas extremas con precisión y sin sesgo, ambos han sido citados en la literatura por tener el punto de ebullición más alto.
Punto de ebullición como propiedad de referencia de un compuesto puro
Como se puede ver en el gráfico anterior del logaritmo de la presión de vapor frente a la temperatura de cualquier compuesto químico puro dado, su punto de ebullición normal puede servir como indicación de la volatilidad general de ese compuesto. Un compuesto puro dado tiene solo un punto de ebullición normal, si lo tiene, y el punto de ebullición y el punto de fusión normales de un compuesto pueden servir como propiedades físicas características para ese compuesto, enumeradas en los libros de referencia. Cuanto más alto es el punto de ebullición normal de un compuesto, menos volátil es ese compuesto en general y, a la inversa, cuanto más bajo es el punto de ebullición normal de un compuesto, más volátil es ese compuesto en general. Algunos compuestos se descomponen a temperaturas más altas antes de alcanzar su punto de ebullición normal o, a veces, incluso su punto de fusión. Para un compuesto estable, el punto de ebullición varía desde su punto triple hasta su punto crítico, dependiendo de la presión externa. Más allá de su punto triple, el punto de ebullición normal de un compuesto, si lo hay, es más alto que su punto de fusión. Más allá del punto crítico, las fases líquida y de vapor de un compuesto se fusionan en una fase, que puede llamarse gas sobrecalentado. A cualquier temperatura dada, si el punto de ebullición normal de un compuesto es más bajo, ese compuesto generalmente existirá como un gas a la presión atmosférica externa. Si el punto de ebullición normal del compuesto es más alto, entonces ese compuesto puede existir como líquido o sólido a esa temperatura dada a la presión atmosférica externa, y existirá en equilibrio con su vapor (si es volátil) si sus vapores están contenidos. Si los vapores de un compuesto no están contenidos,
En general, los compuestos con enlaces iónicos tienen puntos de ebullición normales altos, si no se descomponen antes de alcanzar temperaturas tan altas. Muchos metales tienen puntos de ebullición elevados, pero no todos. Muy generalmente, con otros factores iguales, en compuestos con moléculas unidas covalentemente, a medida que aumenta el tamaño de la molécula (o masa molecular), aumenta el punto de ebullición normal. Cuando el tamaño molecular se vuelve muy grande, el de una macromolécula, polímero o de otro modo, el compuesto a menudo se descompone a alta temperatura antes de alcanzar el punto de ebullición. Otro factor que afecta el punto de ebullición normal de un compuesto es la polaridad de sus moléculas. A medida que aumenta la polaridad de las moléculas de un compuesto, aumenta su punto de ebullición normal, siendo iguales los demás factores. Estrechamente relacionado está la capacidad de una molécula para formar enlaces de hidrógeno (en estado líquido), lo que dificulta que las moléculas abandonen el estado líquido y, por lo tanto, aumenta el punto de ebullición normal del compuesto. Los ácidos carboxílicos simples se dimerizan formando enlaces de hidrógeno entre las moléculas. Un factor menor que afecta los puntos de ebullición es la forma de una molécula. Hacer que la forma de una molécula sea más compacta tiende a reducir ligeramente el punto de ebullición normal en comparación con una molécula equivalente con más área de superficie.
| Nombre común | n -butano | isobutano |
|---|---|---|
| nombre de la IUPAC | butano | 2-metilpropano |
| forma molecular | 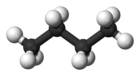 | 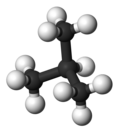 |
| Punto de ebullición(°C) | −0,5 | −11,7 |
| Nombre común | n -pentano | isopentano | neopentano |
|---|---|---|---|
| nombre de la IUPAC | pentano | 2-metilbutano | 2,2-dimetilpropano |
| forma molecular |  |  |  |
| Punto de ebullición(°C) | 36,0 | 27.7 | 9.5 |
La mayoría de los compuestos volátiles (en cualquier lugar cerca de la temperatura ambiente) pasan por una fase líquida intermedia mientras se calientan desde una fase sólida para finalmente transformarse en una fase de vapor. En comparación con la ebullición, una sublimación es una transformación física en la que un sólido se convierte directamente en vapor, lo que ocurre en algunos casos seleccionados, como con dióxido de carbono a presión atmosférica. Para tales compuestos, un punto de sublimación es una temperatura a la cual un sólido que se convierte directamente en vapor tiene una presión de vapor igual a la presión externa.
Impurezas y mezclas
En la sección anterior, se cubrieron los puntos de ebullición de los compuestos puros. Las presiones de vapor y los puntos de ebullición de las sustancias pueden verse afectados por la presencia de impurezas disueltas (solutos) u otros compuestos miscibles, dependiendo el grado del efecto de la concentración de las impurezas u otros compuestos. La presencia de impurezas no volátiles como sales o compuestos de una volatilidad muy inferior a la del componente principal disminuye su fracción molar y la volatilidad de la solución y, por tanto, eleva el punto de ebullición normal en proporción a la concentración de los solutos. Este efecto se llama elevación del punto de ebullición. Como ejemplo común, el agua salada hierve a una temperatura más alta que el agua pura.
En otras mezclas de compuestos miscibles (componentes), puede haber dos o más componentes de volatilidad variable, cada uno con su propio punto de ebullición de componente puro a cualquier presión dada. La presencia de otros componentes volátiles en una mezcla afecta las presiones de vapor y, por lo tanto, los puntos de ebullición y de rocío de todos los componentes de la mezcla. El punto de rocío es una temperatura a la cual un vapor se condensa en un líquido. Además, a cualquier temperatura dada, la composición del vapor es diferente de la composición del líquido en la mayoría de estos casos. Para ilustrar estos efectos entre los componentes volátiles en una mezcla, un diagrama de punto de ebulliciónse usa comúnmente. La destilación es un proceso de ebullición y [generalmente] condensación que aprovecha estas diferencias en la composición entre las fases líquida y vapor.
Contenido relacionado
Metal alcalino
Constante gravitacional
Solvente
