Pseudoobstrucción intestinal
La pseudoobstrucción intestinal (IPO) es un síndrome clínico causado por un deterioro grave en la capacidad de los intestinos para impulsar los alimentos. Se caracteriza por signos y síntomas de obstrucción intestinal sin lesión alguna en la luz intestinal. Las características clínicas imitan las observadas con obstrucciones intestinales mecánicas y pueden incluir dolor abdominal, náuseas, distensión abdominal, vómitos, disfagia y estreñimiento, según la parte del tracto gastrointestinal involucrada.
Es una afección difícil de diagnosticar y requiere la exclusión de cualquier otra causa mecánica de obstrucción. A muchos pacientes se les diagnostica tarde en el curso de la enfermedad después de que se observan síntomas adicionales. La mortalidad también es difícil de determinar con precisión. Un estudio retrospectivo estimó que la mortalidad por pseudoobstrucción intestinal crónica (CIPO) está entre el 10 y el 25% y varía mucho según la etiología de la afección. Cuando está presente durante menos de seis meses, se diagnostica como IPO aguda o síndrome de Ogilvie. Más tiempo que esto se considera crónico. Debido a la dificultad del diagnóstico, se dispone de pocos estudios que hayan intentado estimar su prevalencia.
La afección puede comenzar a cualquier edad. La mayoría de los estudios que describen la CIPO se realizan en poblaciones pediátricas. Puede ser una afección primaria (idiopática o hereditaria) o causada por otra enfermedad (secundaria). Puede ser el resultado de innumerables etiologías, incluidas patologías infecciosas, parasitarias, autoinmunes, genéticas, congénitas, neurológicas, tóxicas, endocrinológicas o anatómicas.
El tratamiento se centra en el apoyo nutricional, la mejora de la motilidad intestinal y la minimización de la intervención quirúrgica. El crecimiento excesivo de bacterias en el intestino delgado puede ocurrir en casos crónicos (que se presentan como malabsorción, diarrea y deficiencias de nutrientes) que pueden requerir el uso de antibióticos.
Presentación
Las características clínicas de la IPO pueden incluir dolor abdominal, náuseas, distensión abdominal, vómitos, disfagia y estreñimiento. Los síntomas dependen de la porción del tracto gastrointestinal afectada y de la duración de los síntomas. Los síntomas pueden ocurrir de forma intermitente y durante un período prolongado de tiempo. No es raro que los pacientes se presenten varias veces debido a la naturaleza inespecífica de los síntomas. Las condiciones y el inicio variarán si la enfermedad es primaria o secundaria y la enfermedad subyacente (si es una manifestación secundaria) y su tratamiento.
Los síntomas indicativos de enfermedad avanzada y posible insuficiencia intestinal incluyen diarrea, pérdida de apetito, sepsis, hinchazón, fatiga, signos de bajo volumen y malabsorción, incluidas deficiencias nutricionales y heces con mal olor.
Causas
En la CIPO primaria (la mayoría de los casos crónicos), la afección se debe a la alteración de la capacidad del intestino para mover los alimentos. Estos pueden clasificarse en términos generales como miopáticos (que afectan al músculo liso), mesenquimopáticos (que afectan a las células intersticiales de Cajal) o neuropáticos (del sistema nervioso) del tracto gastrointestinal.
En algunos casos parece haber una asociación genética. Una forma se ha asociado con DXYS154, otras con el gen ACTG2 defectuoso
La pseudoobstrucción intestinal crónica secundaria puede ocurrir como consecuencia de una serie de otras condiciones que incluyen:
- Enfermedad de Hirschsprung – ausencia de células nerviosas colonizadas
- Enfermedad de Chagas – una infección parasitaria crónica del colon que conduce a la pérdida de los nervios finales
- Enfermedad de Kawasaki - una presentación rara para este trastorno autoinmune particular de la vasculatura
- Enfermedad de Parkinson - relacionada con la neurodegeneración del tracto gastrointestinal
- Condiciones autoinmunes: condiciones que incluyen el lupus eritematoso sistémico y el escleroderma conducen a la deposición vascular de colágeno y la perturbación de la motilidad gastrointestinal
- Enfermedad mitocondrial - IPO es una presentación conocida para la enfermedad mitocondrial
- Trastornos endocrinos
- Ciertos medicamentos.
El término puede usarse como sinónimo de neuropatía entérica si se sospecha una causa neurológica.
Diagnosis
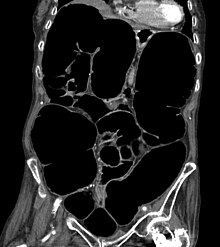
Los síntomas de la IPO no son específicos. No es raro que los pacientes se presenten repetidamente y se sometan a numerosas pruebas. Se deben excluir las causas mecánicas de la obstrucción intestinal para llegar al diagnóstico de pseudoobstrucción. También se debe intentar determinar si la IPO es el resultado de una condición primaria o secundaria. Un estudio de diagnóstico puede incluir:
- Estudios de motilidad gástrica
- Estudios de imágenes:
- Pruebas de sangre
- Endoscopias superiores e inferiores
- Manometría – utilizada para medir la presión del esófago y el estómago
Clasificación
Los síndromes de pseudoobstrucción se clasifican en agudos o crónicos según su apariencia clínica. La pseudoobstrucción colónica aguda (ACPO; a veces conocida como síndrome de Ogilvie) hace que el colon se dilate mucho; si no se descomprime, el individuo corre el riesgo de sufrir perforación, peritonitis y muerte. La pseudoobstrucción intestinal crónica es un trastorno crónico.
Tratamiento
El tratamiento para la IPO (aguda o crónica) tiene como objetivo eliminar el proceso de la enfermedad y/o controlar las complicaciones presentes. La atención se centra en el tratamiento del dolor, los síntomas gastrointestinales, las deficiencias nutricionales, el estado de los líquidos, el control de infecciones y la mejora de la calidad de vida. Cuando la CIPO es secundaria a otra enfermedad, el tratamiento se dirige a la afección subyacente. A veces se requiere cirugía en casos graves de CIPO.
Tratamiento médico
La prucaloprida, la piridostigmina, la metoclopramida, la cisaprida, la eritromicina y la octreotida son medicamentos que tienen como objetivo mejorar la motilidad intestinal.
La estasis intestinal, que puede provocar un crecimiento excesivo de bacterias y posteriormente diarrea o mala absorción, se trata con antibióticos.
Las deficiencias nutricionales se tratan alentando a los pacientes a evitar alimentos que aumentan la distensión y son difíciles de digerir (por ejemplo, aquellos con alto contenido de grasa y fibra), consumiendo comidas pequeñas y frecuentes (5 a 6 por día), centrándose en líquidos y alimentos blandos. Puede ser beneficioso reducir la ingesta de alcoholes de azúcar que se absorben mal. Se recomienda derivar a un dietista acreditado. Si los cambios en la dieta no logran satisfacer los requerimientos nutricionales y energéticos, se utiliza la nutrición enteral. Muchos pacientes eventualmente requieren nutrición parenteral.
La nutrición parenteral total (NPT) es una forma de tratamiento nutricional a largo plazo reservada para pacientes con pseudoobstrucción grave. Los pacientes dependientes de NPT requieren controles frecuentes para controlar la función del catéter, controlar los niveles de enzimas hepáticas y evaluar signos de infecciones sanguíneas. El formato de la NPT generalmente se cambia según la pérdida/aumento de peso y los resultados de los análisis de sangre, y está especialmente formulado para satisfacer las necesidades de cada paciente individual.
Procedimientos
La descompresión intestinal mediante la colocación de un tubo en un estoma pequeño también se puede utilizar para reducir la distensión y la presión dentro del intestino. El estoma puede ser una gastrostomía, yeyunostomía, ileostomía o cecostomía. Estos pueden usarse para alimentar (por ejemplo, gastrostomía y yeyunostomía) o para lavar los intestinos.
La colostomía o ileostomía pueden evitar las partes afectadas si están distales (después) del estoma. Por ejemplo, si sólo está afectado el colon, una ileostomía puede ser útil. Cualquiera de estas ostomías generalmente se coloca en el ombligo del paciente o unos pocos centímetros por debajo según la recomendación del médico según el área afectada de los intestinos, así como las preocupaciones por la comodidad del paciente y el crecimiento físico futuro de los niños.
La extirpación total del colon, llamada colectomía o resección de las partes afectadas del colon, puede ser necesaria si parte del intestino muere (por ejemplo, megacolon tóxico) o si hay un área localizada de dismotilidad.
Se han probado marcapasos gástricos y colónicos. Se trata de tiras que se colocan a lo largo del colon o del estómago y que crean una descarga eléctrica destinada a provocar que el músculo se contraiga de forma controlada.
Una solución potencial, aunque radical, es el trasplante intestinal. Esto sólo es apropiado en caso de insuficiencia intestinal. Estos procedimientos se describen con mayor frecuencia en casos pediátricos de CIPO. Una operación que implicó un trasplante de múltiples órganos de páncreas, estómago, duodeno, intestino delgado e hígado, y fue realizada por el doctor Kareem Abu-Elmagd en Gretchen Miller.
Tratamientos potenciales
Es necesario realizar más investigaciones sobre otros tratamientos que puedan aliviar los síntomas. Estos incluyen el trasplante de células madre y el trasplante de microbiota fecal. El cannabis no ha sido estudiado con respecto a CIPO. Cualquier afirmación sobre su eficacia para su uso en CIPO es especulativa.
Trastornos relacionados
- Síndrome de Ogilvie: pseudoobstrucción aguda del colon en pacientes gravemente debilitados.
- Enfermedad de Hirschsprung: ampliación del colon por falta de desarrollo de ganglios autonómicos.
- Displasia neuronal intestinal: una enfermedad de las neuronas motoras que conduce a los intestinos.
- Obstrucción intestinal: obstrucción mecánica o funcional del intestino, más comúnmente debido a las adhesiones, hernias o neoplasias.
- Neuropatía ventricular: nombre alternativo utilizado a veces para el diagnóstico en Reino Unido
Referencias
- ^ Stanghellini V, Cogliandro RF, De Giorgio R, et al. (mayo de 2005). "Historia natural de pseudo-obstrucción intestinal crónica idiopática en adultos: un estudio de un solo centro". Gastroenterología Clínica y Hepatología. 3 (5): 449–58. doi:10.1016/S1542-3565(04)00675-5. PMID 15880314. S2CID 32605317.
- ^ a b De Giorgio R, Sarnelli G, Corinaldesi R, Stanghellini V (noviembre de 2004). "Avances en nuestra comprensión de la patología de la pseudo-obstrucción intestinal crónica". Gut. 53 11): 1549–52. doi:10.1136/gut.2004.043968. PMC 1774265. PMID 15479666.
- ^ Robbins patología básica. Vinay Kumar, Abul K. Abbas, Jon C. Aster, James A. Perkins (10th ed.). Philadelphia, Pa.: Elsevier. 2018. pp. Capítulo 5: obstrucción intestinal. ISBN 978-0-323-39413-0 OCLC 972900144.
{{cite book}}: CS1 maint: others (link) - ^ a b c d e f g El-Chammas, Khalil; Sood, Manu R. (Marzo 2018). "Obstrucción del intestino Crónico". Clínicas en Cirugía Colon y Rectal. 31 (2): 99-107. doi:10.1055/s-0037-1609024. ISSN 1531-0043. PMC 5825855. PMID 29487492.
- ^ Ko, Dayoung; Yang, Hee-Beom; Youn, Joong; Kim, Hyun-Young (2021-05-28). "Resultados clínicos de Pseudo-obstrucción crónica pediátrica". Journal of Clinical Medicine. 10 11): 2376. doi:10.3390/jcm10112376. ISSN 2077-0383. PMC 8198288. PMID 34071279.
- ^ Saunders MD (octubre de 2004). "Acute colonic pseudoobstruction". Gastroenterología actual Informes. 6 (5): 410–6. doi:10.1007/s11894-004-0059-5. PMID 15341719. S2CID 27281556.
- ^ Sutton DH, Harrell SP, Wo JM (febrero de 2006). "Diagnosis y gestión de pacientes adultos con pseudoobstrucción intestinal crónica". Nutrición en la práctica clínica. 21 (1): 16–22. doi:10.1177/011542650602100116. PMID 16439766.
- ^ Iida, Hiroshi; Ohkubo, Hidenori; Inamori, Masahiko; Nakajima, Atsushi; Sato, Hajime (2013). "Epidemiología y experiencia clínica de pseudo-obstrucción intestinal crónica en Japón: una encuesta epidemiológica nacional". Journal of Epidemiology. 23 (4): 288–294. doi:10.2188/jea.je20120173. ISSN 1349-9092. PMC 3709546. PMID 23831693.
- ^ a b c d e Zenzeri, Letizia; Tambucci, Renato; Quitadamo, Paolo; Giorgio, Valentina; De Giorgio, Roberto; Di Nardo, Giovanni (mayo 2020). "Actualizar sobre pseudo-obstrucción intestinal crónica". Opinión actual en Gastroenterología. 36 (3): 230–237. doi:10.1097/MOG.0000000000630. ISSN 1531-7056. PMID 32073506. S2CID 211193582.
- ^ Downes, Thomas J.; Cheruvu, Manikandar S.; Karunaratne, Tennekoon B.; De Giorgio, Roberto; Farmer, Adam D. (Julio 2018). "Pathophysiology, Diagnosis, and Management of Chronic Intestinal Pseudo-Obstruction". Journal of Clinical Gastroenterology. 52 (6): 477–489. doi:10.1097/MCG.0000000001047. ISSN 1539-2031. PMID 29877952. S2CID 46960493.
- ^ a b Antonucci A, Fronzoni L, Cogliandro L, et al. (mayo de 2008). "Seudo-obstrucción intestinal crónica". World Journal of Gastroenterology. 14 (19): 2953–61. doi:10.3748/wjg.14.2953. PMC 2712158. PMID 18494042.
- ^ Cucchiara, Salvatore; Borrelli, Osvaldo (abril de 2009). "Reto histórico en pseudo-obstrucción: el puente entre la motilidad y la nutrición". Journal of Pediatric Gastroenterology and Nutrition. 48 (Supl 2): S83–85. doi:10.1097/MPG.0b013e3181a15bfe. hdl:11573/406753. ISSN 1536-4801. S2CID 11393186.
- ^ "Pediatric Intestinal Failure". National para niños. Retrieved 8 de noviembre 2021.
- ^ a b "Falta intestinal". Top Doctors Reino Unido. Retrieved 8 de noviembre 2021.
- ^ a b c d Gabbard SL, Lacy BE (junio de 2013). "Seudo-obstrucción intestinal crónica". Nutrición en la práctica clínica. 28 (3): 307–16. doi:10.1177/0884533613485904. PMID 23612903. S2CID 8288714.
- ^ Guzé CD, Hyman PE, Payne VJ (enero de 1999). "Estudios familiares de miopatía visceral infantil: un síndrome de pseudo-obstrucción miopática congénita". American Journal of Medical Genetics. 82 (2): 114–22. doi:10.1002/(SICI)1096-8628(19990115)82:2 armonizado114::AID-AJMG3 confianza3.0.CO;2-H. PMID 9934973.
- ^ Auricchio A, Brancolini V, Casari G, et al. (abril de 1996). "El locus para una nueva forma sindromática de mapas de pseudoobstrucción intestinal neuronal a Xq28". American Journal of Human Genetics. 58 (4): 743-8. PMC 1914695. PMID 8644737.
- ^ "Hirschsprung disease". GARD: Centro de Información sobre Enfermedades Genéticas y Raras. 4 de septiembre de 2017. Archivado desde el original el 24 de noviembre de 2018. Retrieved 8 de noviembre 2021.
- ^ Akikusa JD, Laxer RM, Friedman JN (mayo de 2004). "Seudoobstrucción intestinal en la enfermedad de Kawasaki". Pediatría. 113 (5): e504–6. doi:10.1542/pedes.113.5.e504. PMID 15121996.
- ^ Colomba, Claudia; La Placa, Simona; Saporito, Laura; Corsello, Giovanni; Ciccia, Francesco; Medaglia, Alice; Romanin, Benedetta; Serra, Nicola; Di Carlo, Paola; Cascio, Antonio (noviembre 2018). "Involución intestinal en la enfermedad de Kawasaki". The Journal of Pediatrics. 202: 186-193. doi:10.1016/j.jpeds.2018.06.034. hdl:10447/350574. ISSN 1097-6833. PMID 30029859. S2CID 51704336.
- ^ Salari, Mehri; Fayyazi, Emad; Mirmosayyeb, Omid (2016). "Disfunción gastrointestinal en Parkinsonismo idiopático: Una revisión narrativa". Journal of Research in Medical Sciences. 21: 126. doi:10.4103/1735-1995.196608ISSN 1735-1995. PMC 5348835. PMID 28331512. (Retracted, see doi:10.4103/1735-1995.212042)
- ^ Takahashi, Hiroki; Ohara, Mikiko; Imai, Kohzoh (junio de 2004). "[Las enfermedades del colágeno con manifestaciones gastrointestinales]". Nihon Rinsho Men'eki Gakkai Kaishi = Japanese Journal of Clinical Immunology. 27 (3): 145–155. doi:10.2177/jsci.27.145. ISSN 0911-4300. PMID 15291251.
- ^ Finsterer, Josef; Frank, Marlies (enero de 2017). "Manifestaciones gastrointestinales de trastornos mitocondriales: una revisión sistemática". Avances terapéuticos en Gastroenterología. 10 (1): 142–154. doi:10.1177/1756283X16666806. ISSN 1756-283X. PMC 5330602. PMID 28286566.
- ^ Cagir, Burt (2018-07-23). "Pseudo-obstrucción intestinal: fondo, anatomía, fisiopatología". Referencia de Medscape. Retrieved 2024-04-15.
- ^ Briejer MR, Prins NH, Schuurkes JA (octubre de 2001). "Efectos del prucaloprido enterokinético (R093877) sobre la motilidad colon en perros ayunos". Neurogastroenterología y Motilidad. 13 (5): 465–72. doi:10.1046/j.1365-2982.2001.00280.x. PMID 11696108. S2CID 13610558.
- ^ Oustamanolakis P, Tack J (febrero de 2012). "Prucalopride para pseudo-obstrucción intestinal crónica". Farmacología Alimentaria. 35 (3): 398-9. doi:10.1111/j.1365-2036.2011.04947.x. PMID 22221087.
- ^ Sharma S, Ghoshal UC, Bhat G, Choudhuri G (noviembre de 2006). "Adenocarcinoma gástrico presentando con pseudoobstrucción intestinal, tratada con éxito con octreotida". Indian Journal of Medical Sciences. 60 11): 467-70. doi:10.4103/0019-5359.27974. PMID 17090868.
- ^ Sørhaug S, Steinshamn SL, Waldum HL (abril de 2005). "Tratamiento octreotide para la pseudo-obstrucción intestinal paraneoplásica complicando SCLC". Lung Cancer. 48 (1): 137–40. doi:10.1016/j.lungcan.2004.09.008. PMID 15777981.
- ^ a b Heneyke S, Smith VV, Spitz L, Milla PJ (julio de 1999). "Seudoobstrucción crónica intestinal: tratamiento y seguimiento a largo plazo de 44 pacientes". Archivos de Enfermedad en la Infancia. 81 (1): 21–7. doi:10.1136/adc.81.1.21. PMC 1717974. PMID 10373127.
- ^ Mousa, Hayat; Hyman, Paul E.; Cocjin, José; Flores, Alejandro F.; Di Lorenzo, Carlo (octubre de 2002). "Desenlace a largo plazo de pseudoobstrucción intestinal congénita". Enfermedades y Ciencias Digestivas. 47 (10): 2298–2305. doi:10.1023/a:1020199614102. ISSN 0163-2116. PMID 12395903. S2CID 25029477.
- ^ Bond, Geoffrey J.; Reyes, Jorge D. (noviembre de 2004). "Transplantación intestinal para aganglionosis total/cerca-total y pseudo-obstrucción intestinal". Seminarios en Cirugía Pediátrica. 13 (4): 286–292. doi:10.1053/j.sempedsurg.2004.10.016. ISSN 1055-8586. PMID 15660322.
- ^ Discovery Channel – trasplante multiorgánico
- ^ Westfal, Maggie L.; Goldstein, Allan M. (junio de 2017). " Neuropatías ventriculares: diagnóstico y gestión actual". Opinión actual en Pediatría. 29 (3): 347-353. doi:10.1097/MOP.0000000000486. ISSN 1531-698X. PMC 5475271. PMID 28319561.
- ^ Halter, Joerg P.; Michael, W.; Schüpbach, M.; Mandel, Hanna; Casali, Carlo; Orchard, Kim; Collin, Matthew; Valcarcel, David; Rovelli, Attilio; Filosto, Massimiliano; Dotti, Maria T. (octubre de 2015). "Transplante de células madre haematopoyéticas para la encefalomyopatía neurogastrointestinal mitocondrial". Cerebro: Revista de Neurología. 138 (Pt 10): 2847–2858. doi:10.1093/brain/awv226. ISSN 1460-2156. PMC 4836400. PMID 26264513.
- ^ Lin XH, Wang YQ, Wang HC, Ren XQ, Li YY (agosto de 2013). "Role of endogenous cannabinoid system in the gut" (PDF). Sheng Li Xue Bao. 65 (4): 451–60. PMID 23963077.
Enlaces externos
- 00530 en CHORUS
