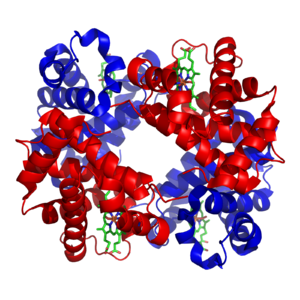
Proteína globular
En bioquímica, las proteínas globulares o esferoproteínas son proteínas esféricas ("globulares") y son uno de los tipos de proteínas comunes (los otros siendo proteínas fibrosas, desordenadas y de membrana). Las proteínas globulares son algo solubles en agua (forman coloides en agua), a diferencia de las proteínas fibrosas o de membrana. Hay múltiples clases de pliegues de proteínas globulares, ya que hay muchas arquitecturas diferentes que pueden plegarse en una forma más o menos esférica.
El término globina puede referirse más específicamente a proteínas, incluido el pliegue de globina.
Estructura globular y solubilidad
El término proteína globular es bastante antiguo (probablemente data del siglo XIX) y ahora es algo arcaico debido a los cientos de miles de proteínas y al vocabulario de motivos estructurales más elegante y descriptivo. La naturaleza globular de estas proteínas se puede determinar sin los medios de las técnicas modernas, pero solo mediante el uso de ultracentrífugas o técnicas de dispersión dinámica de la luz.
La estructura esférica es inducida por la estructura terciaria de la proteína. Los aminoácidos apolares (hidrofóbicos) de la molécula están unidos hacia el interior de la molécula, mientras que los aminoácidos polares (hidrofílicos) están unidos hacia el exterior, lo que permite interacciones dipolo-dipolo con el solvente, lo que explica la solubilidad.
Las proteínas globulares son solo marginalmente estables porque la energía libre liberada cuando la proteína se pliega en su conformación nativa es relativamente pequeña. Esto se debe a que el plegamiento de proteínas requiere un costo entrópico. Como una secuencia primaria de una cadena polipeptídica puede formar numerosas conformaciones, la estructura globular nativa restringe su conformación a solo unas pocas. Da como resultado una disminución de la aleatoriedad, aunque las interacciones no covalentes, como las interacciones hidrofóbicas, estabilizan la estructura.
Plegado de proteínas
Aunque todavía se desconoce cómo se pliegan las proteínas de forma natural, nueva evidencia ha ayudado a avanzar en la comprensión. Parte del problema del plegamiento de proteínas es que se forman varias interacciones débiles no covalentes, como enlaces de hidrógeno e interacciones de Van der Waals. A través de varias técnicas, actualmente se está estudiando el mecanismo de plegamiento de proteínas. Incluso en el estado desnaturalizado de la proteína, se puede plegar en la estructura correcta.
Las proteínas globulares parecen tener dos mecanismos para el plegamiento de proteínas, ya sea el modelo de colisión de difusión o el modelo de condensación de nucleación, aunque hallazgos recientes han mostrado proteínas globulares, como PTP-BL PDZ2, que se pliegan con rasgos característicos de ambos modelos. Estos nuevos hallazgos han demostrado que los estados de transición de las proteínas pueden afectar la forma en que se pliegan. El plegamiento de proteínas globulares también se ha relacionado recientemente con el tratamiento de enfermedades, y se han desarrollado ligandos anticancerígenos que se unen a la proteína plegada pero no a la natural. Estos estudios han demostrado que el plegamiento de las proteínas globulares afecta su función.
Según la segunda ley de la termodinámica, la diferencia de energía libre entre los estados plegado y desplegado se debe a los cambios de entalpía y entropía. Como la diferencia de energía libre en una proteína globular que resulta del plegamiento en su conformación nativa es pequeña, es marginalmente estable, lo que proporciona una tasa de renovación rápida y un control efectivo de la degradación y síntesis de proteínas.
Rol
A diferencia de las proteínas fibrosas que solo cumplen una función estructural, las proteínas globulares pueden actuar como:
- Enzimas, al catalizar reacciones orgánicas que tienen lugar en el organismo en condiciones leves y con una gran especificidad. Las diferentes esterases cumplen este papel.
- Mensajeros, transmitiendo mensajes para regular los procesos biológicos. Esta función es hecha por hormonas, es decir, insulina, etc.
- Transportadores de otras moléculas a través de membranas
- Existencias de aminoácidos.
- Los roles reguladores también son realizados por proteínas globulares en lugar de proteínas fibrosas.
- Proteínas estructurales, por ejemplo, actina y tubulina, que son globulares y solubles como monómeros, pero polímeros para formar fibras largas y rígidas
Miembros
Entre las proteínas globulares más conocidas se encuentra la hemoglobina, un miembro de la familia de proteínas globina. Otras proteínas globulares son las globulinas alfa, beta y gamma (IgA, IgD, IgE, IgG e IgM). Consulte electroforesis de proteínas para obtener más información sobre las diferentes globulinas. Casi todas las enzimas con funciones metabólicas importantes tienen forma globular, así como muchas proteínas de transducción de señales.
Las albúminas también son proteínas globulares, aunque, a diferencia de todas las demás proteínas globulares, son completamente solubles en agua. No son solubles en aceite.
Contenido relacionado
Orgánulo
Estreptococo
Indríidos