Proteína de membrana periférica
Se ha demostrado que la unión reversible de proteínas a las membranas biológicas regula la señalización celular y muchos otros eventos celulares importantes, a través de una variedad de mecanismos. Por ejemplo, la estrecha asociación entre muchas enzimas y membranas biológicas puede acercarlas mucho a su(s) sustrato(s) lipídico(s). La unión de membrana también puede promover la reorganización, la disociación o los cambios conformacionales dentro de muchos dominios estructurales de proteínas, lo que resulta en una activación de su actividad biológica. Además, el posicionamiento de muchas proteínas se localiza en las superficies internas o externas o en las láminas de su membrana residente. Esto facilita el ensamblaje de complejos multiproteicos al aumentar la probabilidad de cualquier interacción proteína-proteína apropiada.

Unión a la bicapa lipídica
Las proteínas de membrana periférica pueden interactuar con otras proteínas o directamente con la bicapa lipídica. En este último caso, se las conoce como proteínas anfitrópicas. Algunas proteínas, como las proteínas G y ciertas proteínas quinasas, interactúan con las proteínas transmembrana y la bicapa lipídica simultáneamente. Algunas hormonas polipeptídicas, péptidos antimicrobianos y neurotoxinas se acumulan en la superficie de la membrana antes de ubicarse e interactuar con sus objetivos receptores de la superficie celular, que pueden ser proteínas de la membrana periférica.
La bicapa de fosfolípidos que forma la membrana de la superficie celular consta de una región central interna hidrofóbica intercalada entre dos regiones de hidrofilia, una en la superficie interna y otra en la superficie externa de la membrana celular (consulte el artículo sobre bicapa lipídica para obtener información más detallada). descripción estructural de la membrana celular). Se ha demostrado que las superficies interna y externa, o regiones interfaciales, de las bicapas de fosfolípidos modelo tienen un grosor de alrededor de 8 a 10 Å, aunque esto puede ser más ancho en las membranas biológicas que incluyen grandes cantidades de gangliósidos o lipopolisacáridos. La región del núcleo interno hidrofóbico de las membranas biológicas típicas puede tener un grosor de alrededor de 27 a 32 Å, según lo estimado por la dispersión de rayos X de ángulo pequeño (SAXS). La región límite entre el núcleo interno hidrofóbico y las regiones interfaciales hidrofílicas es muy estrecha, alrededor de 3 Å (consulte el artículo sobre bicapa lipídica para obtener una descripción de los grupos químicos que lo componen). Al alejarse de la región del núcleo hidrofóbico y hacia la región hidrofílica interfacial, la concentración efectiva de agua cambia rápidamente a través de esta capa límite, desde casi cero hasta una concentración de alrededor de 2 M. Los grupos fosfato dentro de las bicapas de fosfolípidos están completamente hidratados o saturados con agua y están situados alrededor de 5 Å fuera del límite de la región del núcleo hidrofóbico.
Algunas proteínas solubles en agua se asocian con las bicapas lipídicas de forma irreversible y pueden formar canales alfa-helicoidales o beta-barril transmembrana. Tales transformaciones ocurren en toxinas formadoras de poros como la colicina A, la alfa-hemolisina y otras. También pueden ocurrir en la proteína similar a BcL-2 en algunos péptidos antimicrobianos anfifílicos y en ciertas anexinas. Estas proteínas generalmente se describen como periféricas, ya que uno de sus estados conformacionales es soluble en agua o solo está débilmente asociado con una membrana.
Mecanismos de unión de membrana
La asociación de una proteína con una bicapa lipídica puede implicar cambios significativos dentro de la estructura terciaria de una proteína. Estos pueden incluir el plegamiento de regiones de la estructura de la proteína que se desplegaron previamente o una reorganización en el plegamiento o un replegamiento de la parte de las proteínas asociada a la membrana. También puede implicar la formación o disociación de estructuras cuaternarias de proteínas o complejos oligoméricos y la unión específica de iones, ligandos o lípidos reguladores.
Las proteínas anfitrópicas típicas deben interactuar fuertemente con la bicapa lipídica para poder realizar sus funciones biológicas. Estos incluyen el procesamiento enzimático de lípidos y otras sustancias hidrofóbicas, el anclaje a la membrana y la unión y transferencia de pequeños compuestos no polares entre diferentes membranas celulares. Estas proteínas pueden anclarse a la bicapa como resultado de interacciones hidrofóbicas entre la bicapa y los residuos no polares expuestos en la superficie de una proteína, mediante interacciones de unión no covalente específicas con lípidos reguladores o mediante su unión a anclajes de lípidos unidos covalentemente.
Se ha demostrado que las afinidades de unión a la membrana de muchas proteínas periféricas dependen de la composición lipídica específica de la membrana con la que están asociadas.
Asociación hidrofóbica no específica
Las proteínas anfitrópicas se asocian con las bicapas lipídicas a través de varias estructuras de anclaje hidrofóbicas. Tales como hélices α anfifílicas, bucles no polares expuestos, residuos de aminoácidos lipidados o acilados postraduccionalmente, o cadenas de acilo de lípidos reguladores unidos específicamente, como fosfatos de fosfatidilinositol. Se ha demostrado que las interacciones hidrofóbicas son importantes incluso para péptidos y proteínas altamente catiónicos, como el dominio polibásico de la proteína MARCKS o la histactofilina, cuando están presentes sus anclajes hidrofóbicos naturales.
Anclajes lipídicos unidos covalentemente
Las proteínas ancladas en lípidos se unen covalentemente a diferentes cadenas de acilo de ácidos grasos en el lado citoplásmico de la membrana celular mediante palmitoilación, miristoilación o prenilación. En la cara exoplásmica de la membrana celular, las proteínas ancladas en lípidos están unidas covalentemente a los lípidos glicosilfosfatidilinositol (GPI) y colesterol. La asociación de proteínas con las membranas mediante el uso de residuos acilados es un proceso reversible, ya que la cadena de acilo puede quedar enterrada en el bolsillo de unión hidrofóbico de una proteína después de la disociación de la membrana. Este proceso ocurre dentro de las subunidades beta de las proteínas G. Quizás debido a esta necesidad adicional de flexibilidad estructural, los anclajes de lípidos generalmente se unen a los segmentos altamente flexibles de la estructura terciaria de las proteínas que no se resuelven bien mediante estudios cristalográficos de proteínas.
Unión específica proteína-lípido
Algunas proteínas citosólicas se reclutan en diferentes membranas celulares al reconocer ciertos tipos de lípidos que se encuentran dentro de una membrana determinada. La unión de una proteína a un lípido específico se produce a través de dominios estructurales dirigidos a la membrana específicos que se encuentran dentro de la proteína y tienen bolsillos de unión específicos para los grupos de cabeza de lípidos de los lípidos a los que se unen. Esta es una interacción proteína-ligando bioquímica típica y se estabiliza mediante la formación de enlaces de hidrógeno intermoleculares, interacciones de van der Waals e interacciones hidrofóbicas entre la proteína y el ligando lipídico. Dichos complejos también se estabilizan mediante la formación de puentes iónicos entre los residuos de aspartato o glutamato de la proteína y los fosfatos de lípidos mediante la intervención de iones de calcio (Ca2+). Dichos puentes iónicos pueden ocurrir y son estables cuando los iones (como Ca2+) ya están unidos a una proteína en solución, antes de la unión a los lípidos. La formación de puentes iónicos se observa en la interacción proteína-lípido entre los dominios de tipo proteína C2 y las anexinas.
Interacciones electrostáticas entre proteínas y lípidos
Cualquier proteína cargada positivamente será atraída a una membrana cargada negativamente por interacciones electrostáticas inespecíficas. Sin embargo, no todos los péptidos y proteínas periféricos son catiónicos, y solo ciertos lados de la membrana tienen carga negativa. Estos incluyen el lado citoplásmico de las membranas plasmáticas, la hoja externa de las membranas bacterianas externas y las membranas mitocondriales. Por lo tanto, las interacciones electrostáticas desempeñan un papel importante en la dirección de la membrana de los transportadores de electrones, como el citocromo c, las toxinas catiónicas, como la caribdotoxina, y los dominios específicos de la membrana, como algunos dominios PH, dominios C1 y dominios C2.
Las interacciones electrostáticas dependen en gran medida de la fuerza iónica de la solución. Estas interacciones son relativamente débiles a la fuerza iónica fisiológica (NaCl 0,14 M): ~3 a 4 kcal/mol para proteínas catiónicas pequeñas, como el citocromo c, la caribdotoxina o la hisactofilina.
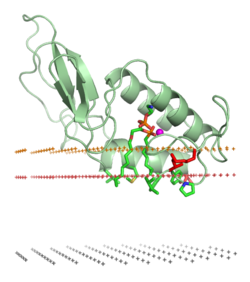
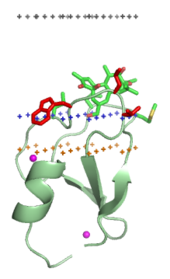
Posición espacial en la membrana
Las orientaciones y las profundidades de penetración de muchas proteínas y péptidos anfitrópicos en las membranas se estudian mediante el etiquetado de espín dirigido al sitio, el etiquetado químico, la medición de las afinidades de unión a la membrana de proteínas mutantes, la espectroscopia de fluorescencia, la solución o la espectroscopia de RMN de estado sólido, Espectroscopía ATR FTIR, difracción de rayos X o de neutrones y métodos computacionales.
Se han identificado dos modos distintos de asociación de membrana de proteínas. Las proteínas solubles en agua típicas no tienen residuos no polares expuestos ni ningún otro anclaje hidrofóbico. Por lo tanto, permanecen completamente en solución acuosa y no penetran en la bicapa lipídica, lo que sería energéticamente costoso. Dichas proteínas interactúan con las bicapas solo electrostáticamente, por ejemplo, la ribonucleasa y la polilisina interactúan con las membranas de este modo. Sin embargo, las proteínas anfitrópicas típicas tienen varios anclajes hidrofóbicos que penetran en la región interfacial y alcanzan el interior hidrocarbonado de la membrana. Tales proteínas "deforman" bicapa lipídica, disminuyendo la temperatura de transición fluido-gel lipídica. La unión suele ser una reacción fuertemente exotérmica. La asociación de hélices α anfifílicas con membranas ocurre de manera similar. Los péptidos intrínsecamente no estructurados o desplegados con residuos no polares o anclajes lipídicos también pueden penetrar en la región interfacial de la membrana y alcanzar el núcleo hidrocarbonado, especialmente cuando dichos péptidos son catiónicos e interactúan con membranas cargadas negativamente.
Categorías
Enzimas
Las enzimas periféricas participan en el metabolismo de diferentes componentes de la membrana, como los lípidos (fosfolipasas y colesterol oxidasas), los oligosacáridos de la pared celular (glucosiltransferasa y transglucosidasas) o las proteínas (peptidasa señal y palmitoilproteína tioesterasa). Las lipasas también pueden digerir lípidos que forman micelas o gotitas no polares en agua.
| Clase | Función | Fisiología | Estructura |
|---|---|---|---|
| Pliegue hidrolase alfa/beta | Cataliza la hidrolisis de los vínculos químicos. | Incluye lipas bacterianas, fúngicas, gástricas y pancreáticas, proteína de palmitoil tioesterasas, cutinasa y collinesterasas | |
| Phospholipase A2 (secretario y citosolico) | Hidrolisis de la unión de ácidos grasos sn-2 de fosfolípidos. | Digestión Lipid, trastorno de membrana y señalización de lípidos. | |
| Phospholipase C | Hydrolyzes PIP2, un fosfatidylinositol, en dos segundos mensajes, inositol triphosphate y diacylglycerol. | Lipid signaling | |
| oxidaciones del colesterol | Oxidiza e isomeriza el colesterol para cholest-4-en-3-uno. | Degrada las membranas celulares del colesterol, utilizadas en la patogénesis bacteriana. | |
| Oxigenopatía carotenoidea | Los carotenoides. | Los carotenoides funcionan tanto en plantas como en animales como hormonas (incluye vitamina A en humanos), pigmentos, sabores, aromas florales y compuestos de defensa. | |
| Lipoxigenas | Enzimas que contienen hierro que catalizan la dioxigenación de ácidos grasos poliinsaturados. | En animales los lipoxigenases están involucrados en la síntesis de mediadores inflamatorios conocidos como leucotrienes. | |
| Toxinas alfa | Fosfolípidos inteligentes en la membrana celular, similar a la fosfolipasa C. | Patogénesis bacteriana, particularmente por Clostridium perfringens. | |
| Sphingomyelinase C | Una fosfodiesterasa, oculta enlaces de fósforo. | Procesamiento de lípidos como esphingomyelin. | |
| Glycosyltransferases: MurG y Transglycosidases | Cataliza la transferencia de moieties de azúcar de moléculas de donante activadas a moléculas de aceptor específicas, formando bonos glicosidicos. | Biosíntesis de disacáridos, oligosacáridos y polisacáridos (glycoconjugados), MurG participa en la biosíntesis bacteriana peptidoglycan. | |
| Ferrochelatase | Convierte protoporfirina IX en heme. | Involucrada en metabolismo de la porfirina, las protoporfirinas se utilizan para fortalecer las cáscaras de huevo. | |
| Familia de proteína relacionada con la mioubularina | Fosfatasa de Lipid que desfosforila PtdIns3P y PtdIns(3,5)P2. | Se requiere para la diferenciación de células musculares. | |
| Dihydroorotate dehydrogenases | Oxidación de dihidroorotate (DHO) a orotate. | Biosíntesis de nucleótidos de pirimidina en células procariotas y eucariotas. | |
| Glycolate oxidase | Cataliza la oxidación de ácidos α-hidroxicarboxílicos a los correspondientes α-ketoácidos. | En plantas verdes, la enzima participa en la fotorespiración. En animales, la enzima participa en la producción de oxalato. |
Dominios dirigidos a la membrana ("pinzas de lípidos")
Los dominios dirigidos a la membrana se asocian específicamente con grupos de cabeza de sus ligandos lipídicos incrustados en la membrana. Estos ligandos lipídicos están presentes en diferentes concentraciones en distintos tipos de membranas biológicas (por ejemplo, PtdIns3P se puede encontrar principalmente en membranas de endosomas tempranos, PtdIns(3,5)P2 en endosomas tardíos y PtdIns4P en Golgi). Por lo tanto, cada dominio está dirigido a una membrana específica.
- Dominios C1 [1] unen el diacylglycerol y esteres de phorbol.
- Dominios C2 [2] bind phosphatidylserine, phosphatidylcholine o PtdIns(3,4)P2 o PtdIns(4,5)P2.
- Pleckstrin homology domains [3], PX domains [4] y Tubby domains [5] unen diferentes fosphoinositides
- dominios FYVE [6] son más específicos para PtdIns3P.
- Dominios ENTH [7] bind PtdIns(3,4)P2 o PtdIns(4,5)P2.
- dominio ANTH [8] binds PtdIns(4,5)P2.
- Proteínas de la familia ERM (ezrin/radixin/moesin) [9] bind PtdIns(4,5)P2.
- Otras proteínas de unión de fosfoinositida incluyen el dominio de unión de fosfotilrosina [10] y ciertos dominios de PDZ. Ataron a PtdIns(4,5)P2.
- Dominios de discoidina de factores de coagulación sanguínea [11]
- dominios ENTH, VHS y ANTH [12]
Dominios estructurales
Los dominios estructurales median la unión de otras proteínas a las membranas. Su unión a las membranas puede estar mediada por iones de calcio (Ca2+) que forman puentes entre los residuos de proteínas ácidas y los grupos fosfato de los lípidos, como en las anexinas o los dominios GLA.
| Clase | Función | Fisiología | Estructura |
|---|---|---|---|
| Anexos | Calcio-dependiente de membrana intracelular / unión fosfolípido. | Las funciones incluyen tráfico de vesículas, fusión de membrana y formación de canales de iones. | |
| Sinapsin I | Coats vesicles sinápticos y se une a varios elementos citoesqueléticos. | Funciones en la regulación de la liberación del neurotransmisor. | |
| Sinnucleina | Función celular desconocida. | Pensado en desempeñar un papel en la regulación de la estabilidad y/o la rotación de la membrana plasmática. Asociada con la enfermedad de Parkinson y la enfermedad de Alzheimer. | |
| GLA-dominios del sistema de coagulación | Los dominios Gamma-carboxyglutamate (GLA) son responsables de la unión de alta afinidad de iones de calcio. | Involucró en función de factores de coagulación en la cascada de coagulación sanguínea. | |
| Espectrina y α-actinina-2 | Encontradas en varias proteínas citosceletal y microfilament. | Mantenimiento de la integridad de la membrana plasmática y la estructura citoesquelética. |
Transportadores de pequeñas moléculas hidrofóbicas
Estas proteínas periféricas funcionan como transportadores de compuestos no polares entre diferentes tipos de membranas celulares o entre membranas y complejos proteicos citosólicos. Las sustancias transportadas son fosfatidilinositol, tocoferol, gangliósidos, glicolípidos, derivados de esteroles, retinol, ácidos grasos, agua, macromoléculas, glóbulos rojos, fosfolípidos y nucleótidos.
- Proteínas de transferencia de glucolipides
- Lipocalinas incluyendo proteínas de unión retinol y proteínas de unión de ácidos grasos
- Proteína de unión poliisoprenoide, como el dominio de proteína YceI
- Proteínas activadoras Ganglioside GM2
- CRAL-TRIO dominio (α-Tocopherol y fosfatidylinositol sec14p proteínas de transferencia)
- Proteínas portadoras de esterol
- Proteínas de transferencia de fosfatidylinositol y dominios STAR
- Proteína de unión de oxígeno
Transportadores de electrones
Estas proteínas están involucradas en las cadenas de transporte de electrones. Incluyen citocromo c, cupredoxinas, proteína de hierro de alto potencial, adrenodoxina reductasa, algunas flavoproteínas y otras.
Hormonas polipeptídicas, toxinas y péptidos antimicrobianos
Muchas hormonas, toxinas, inhibidores o péptidos antimicrobianos interactúan específicamente con los complejos de proteínas transmembrana. También pueden acumularse en la superficie de la bicapa lipídica, antes de unirse a sus proteínas objetivo. Dichos ligandos polipeptídicos a menudo tienen carga positiva e interactúan electrostáticamente con las membranas aniónicas.
Algunas proteínas y péptidos solubles en agua también pueden formar canales transmembrana. Por lo general, experimentan oligomerización, cambios conformacionales significativos y se asocian con las membranas de manera irreversible. Se ha determinado la estructura 3D de uno de estos canales transmembrana, la α-hemolisina. En otros casos, la estructura experimental representa una conformación soluble en agua que interactúa con la bicapa lipídica periféricamente, aunque algunos de los péptidos formadores de canales son más bien hidrófobos y, por lo tanto, se estudiaron mediante espectroscopía de RMN en disolventes orgánicos o en presencia de micelas.
| Clase | Proteínas | Fisiología |
|---|---|---|
| Venom toxins |
| Los tipos bien conocidos de biotoxinas incluyen neurotoxinas, citotoxinas, hemotoxinas y necrotoxinas. Las biotoxinas tienen dos funciones principales: predación (snake, escorpión y toxinas de caracol) y defensa (honeybee y ant toxinas). |
| Toxinas de anémona marina |
| La inhibición de canales de sodio y potasio y la formación de poro de membrana son las acciones primarias de más de 40 toxinas de anémona marina conocidas. Las anémonas marinas son animales carnívoros y usan toxinas en la predación y defensa; la toxina anémona es de toxicidad similar como los agentes de guerra química organofosfata más tóxicos. |
| Toxinas bacterianas |
| Las toxinas microbianas son los principales factores de virulencia para una variedad de bacterias patógenas. Algunas toxinas, son poro formando toxinas que lisas membranas celulares. Otras toxinas inhiben la síntesis de proteínas o activan segundas vías de mensajero causando alteraciones dramáticas a las vías de transducción de señal crítica para mantener una variedad de funciones celulares. Varias toxinas bacterianas pueden actuar directamente en el sistema inmunitario, actuando como superantigenos y provocando la proliferación masiva de células T, que supera el sistema inmunitario. La toxina botulínica es una neurotoxina que evita que las vesículas neuro-secretorias atraquen/fuercen con la membrana de plasma sinapsis nerviosa, inhibiendo la liberación del neurotransmisor. |
| Toxinas fúngicas |
| Estos péptidos se caracterizan por la presencia de un aminoácido inusual, ácido α-aminoisobutírico, y exhiben propiedades antibióticas y antifúngicas debido a sus actividades de formación de canales de membrana. |
| Péptidos antimicrobianos |
| Los modos de acción por los cuales los péptidos antimicrobianos matan bacterias son variados e incluyen membranas perturbadoras, interfiriendo con el metabolismo y apuntando componentes citoplasmáticos. En contraste con muchos antibióticos convencionales estos péptidos parecen ser bacteriocidas en lugar de bacteriostáticos. |
| Defensinas |
| Las defensinas son un tipo de péptidos antimicrobianos; y son un componente importante de prácticamente todas las defensas anfitrionas innatas contra la invasión microbiana. Las defensinas penetran las membranas microbianas a través de la atracción eléctrica, y forman un poro en la membrana que permite el eflujo, que en última instancia conduce a la lisis de microorganismos. |
| Péptidos neuronales |
| Estas proteínas excitan neuronas, evocan respuestas conductuales, son vasodilatadores potentes, y son responsables de la contracción en muchos tipos de músculo liso. |
| Reguladores de apoptosis |
| Los miembros de la familia Bcl-2 gobiernan la permeabilidad de la membrana exterior mitocondrial. Bcl-2 suprime la apoptosis en una variedad de tipos de células incluyendo linfocitos y células neuronales. |
Referencias generales
- Lukas K. Tamm, ed. (2005). Interacciones Protein-Lipid: Desde Dominios Membrane a Redes Celulares. Chichester: John Wiley & Hijos. ISBN 3-527-31151-3.
- Cho, W. ' Stahelin, R.V. (junio de 2005). "Interacciones de membrana-proteína en señalización celular y tráfico de membrana". Annual Review of Biophysics and Biomolecular Structure. 34 (1): 119–151. doi:10.1146/annurev.biophys.33.110502.133337. PMID 15869386.
- Goni F.M. (2002). "Proteínas no permanentes en las membranas: cuando las proteínas vienen como visitantes" (PDF). Mol. Biol. 19 (4): 237–245. doi:10.1080/0968768021000035078. PMID 12512770. S2CID 20892603.
- Johnson J, Cornell R (1999). "Proteínas anfitrópicas: regulación por interacciones reversibles de membrana (revisión)" (PDF). Mol Membr Biol. 16 (3): 217–235. doi:10.1080/096876899294544. PMID 10503244.
- Seaton B.A. y Roberts M.F. Proteínas de membrana periférica. pp. 355–403. In Membranas biológicas (Eds. K. Mertz y B.Roux), Birkhauser Boston, 1996.
- Benga G. Protein-lipid interactions in biological membranas, pp. 159–188. In Estructura y propiedades de las memorias biológicas, vol. 1 (Ed. G. Benga) Boca Raton CRC Prensa, 1985.
- Kessel A. and Ben-Tal N. 2002. Determinantes de energía libre de asociación de péptidos con lípidos. In Temas actuales en Membranes 52: 205–253.
- Malmberg N, Falke J (2005). "Uso de la saturación de energía EPR para analizar las geometrías de las membranas de las proteínas periféricas: aplicaciones a los dominios C2". Annu Rev Biophys Biomol Struct. 34 (1): 71–90. doi:10.1146/annurev.biophys.34.040204.144534. PMC3637887. PMID 15869384.
- McIntosh T, Simon S (2006). "Roles de propiedades materiales de bicapa en función y distribución de proteínas de membrana". Annu Rev Biophys Biomol Struct. 35 (1): 177–198. doi:10.1146/annurev.biophys.35.040405.102022. PMID 16689633.
Contenido relacionado
Rosáceas
Naranja china
Ácido beta hidroxi